Trophic niche analysis of Collichthys lucidus in Pearl River Estuary
-
摘要:
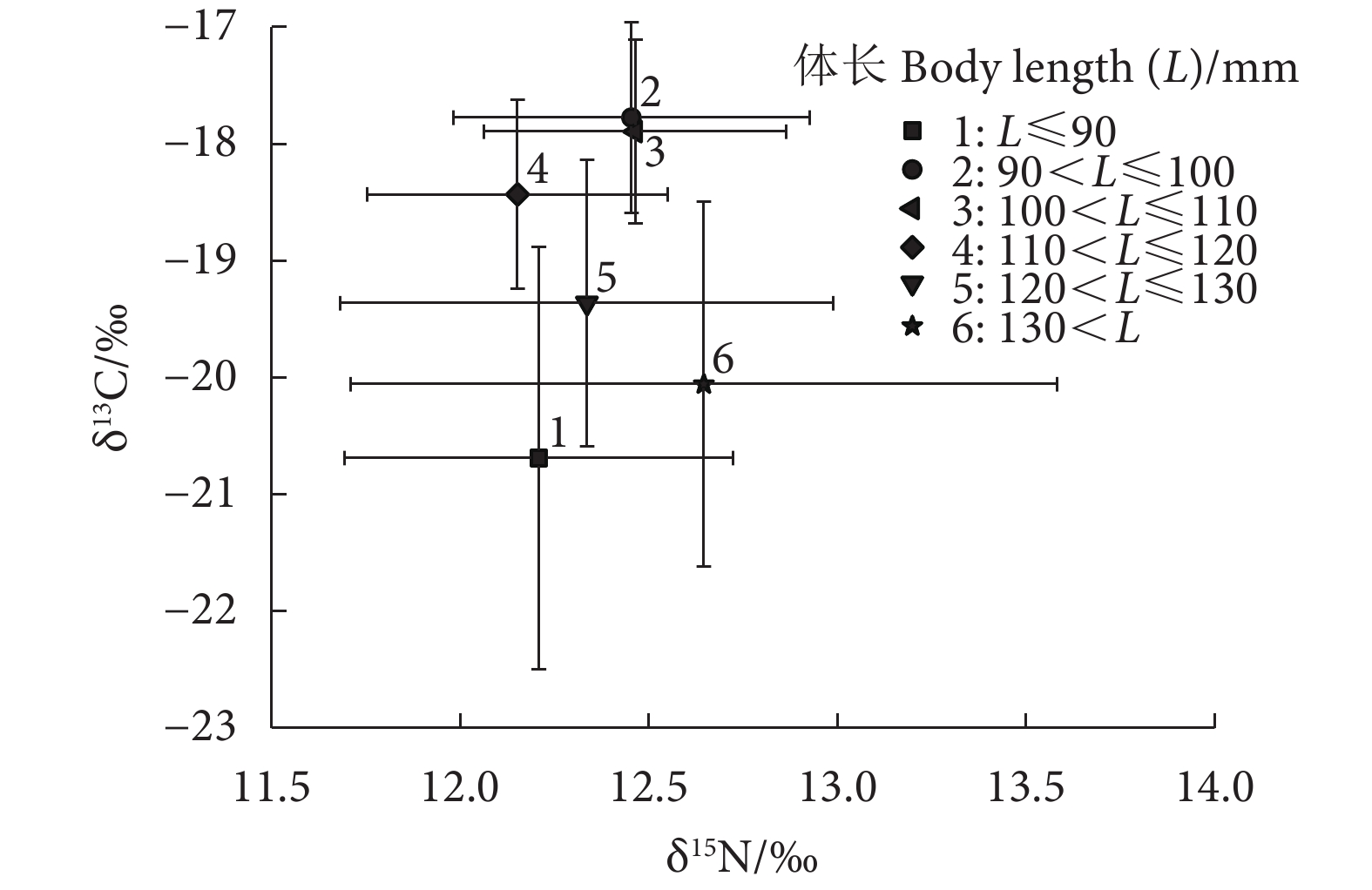
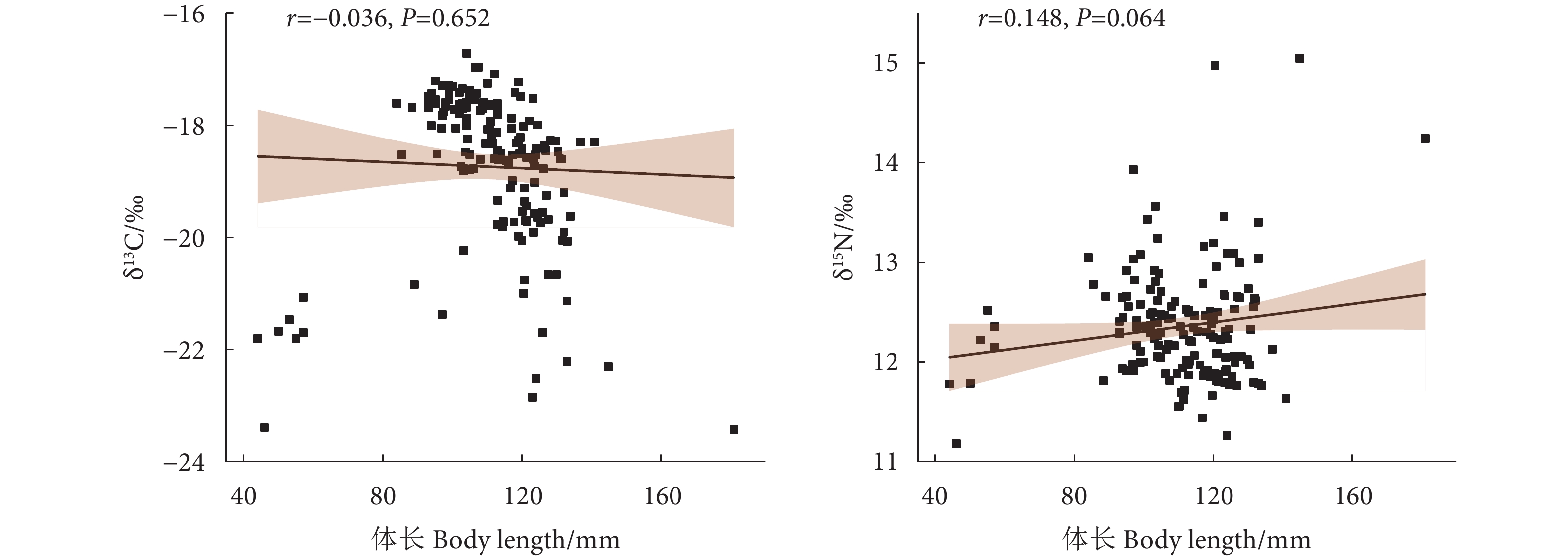
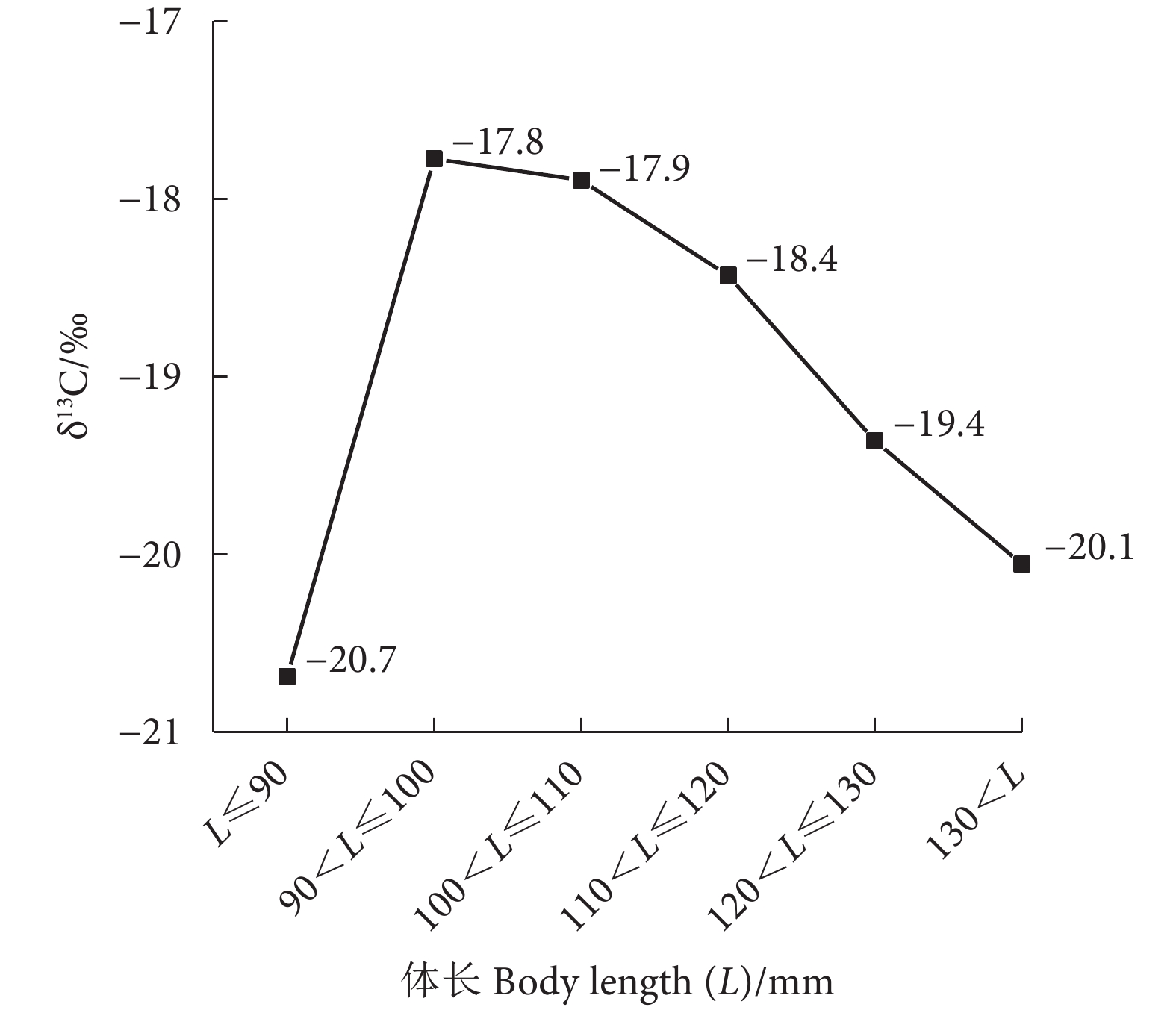
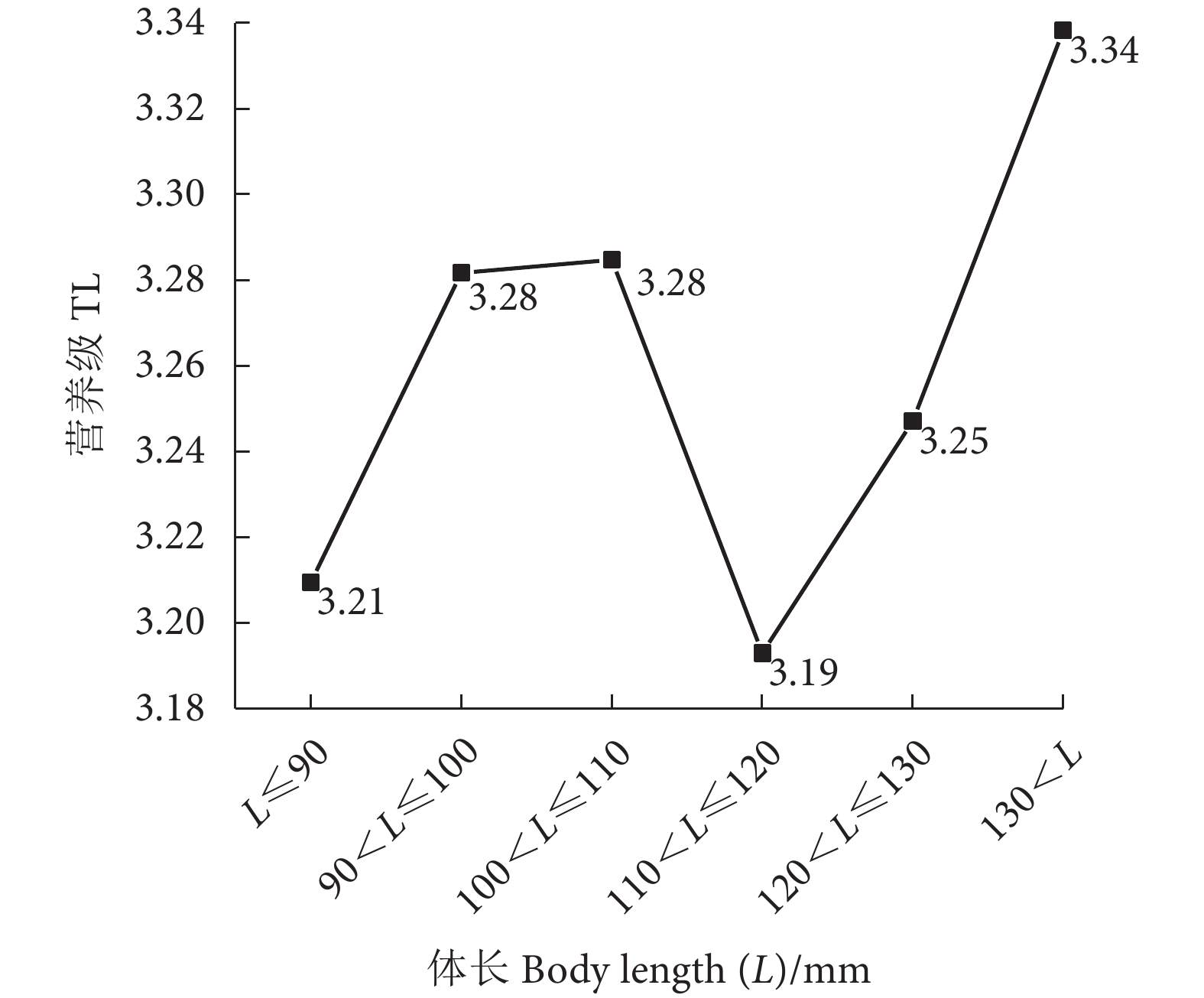
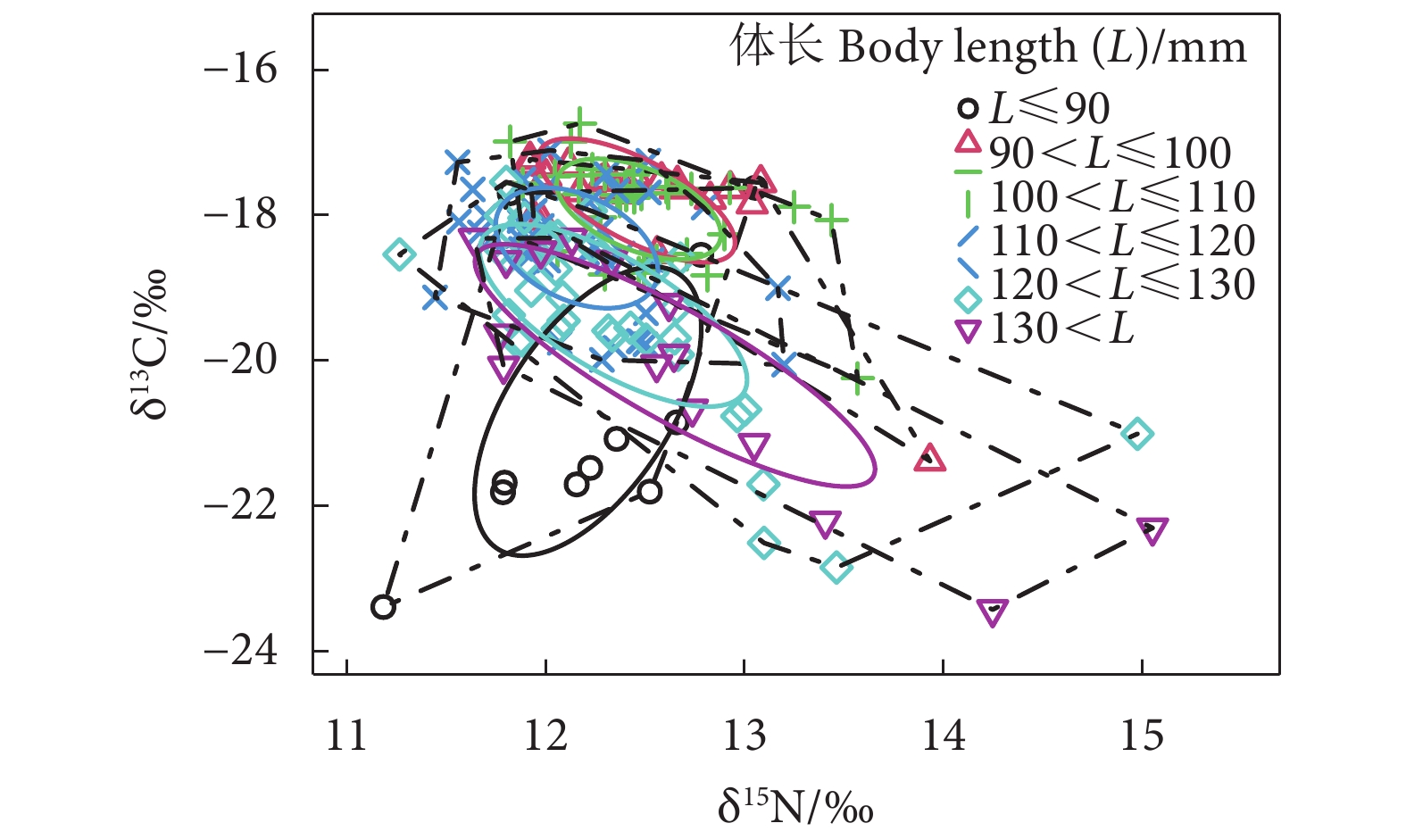
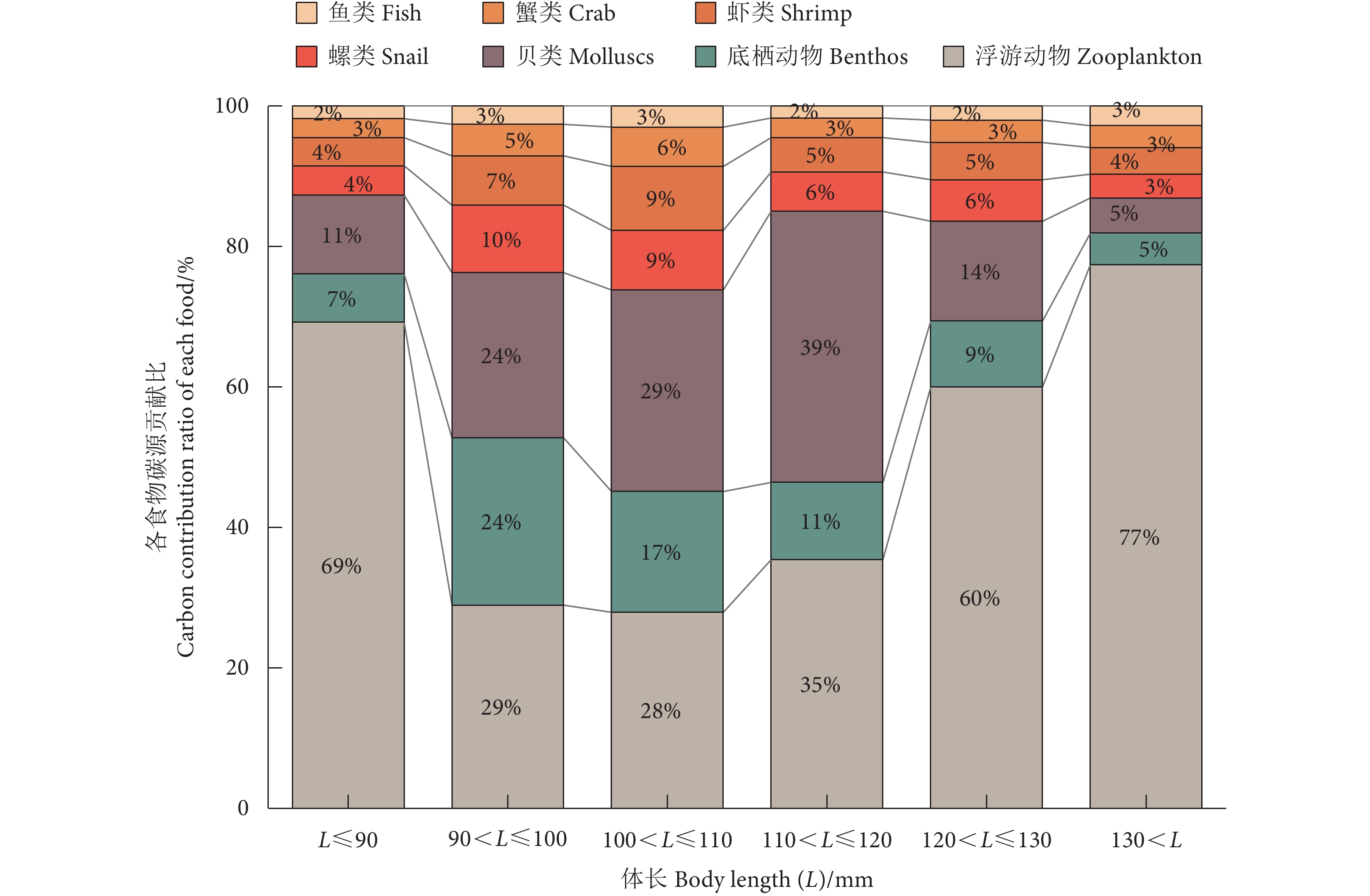
棘头梅童鱼 (Collichthys lucidus) 是重要的小型经济鱼类,为了解其营养结构和食性等特征,于2021和2022年在珠江口水域采集样本,并基于碳、氮稳定同位素 (δ13C、δ15N) 技术从营养生态位、营养结构指标、食性等角度对其进行研究。结果表明:棘头梅童鱼δ13C为 (−18.74±1.41)‰,δ15N为 (12.35±0.57)‰,营养级为 (3.25±0.17)‰。δ13C在体长小于100.00 mm时随体长增加逐渐上升,之后随体长增加而下降;δ15N在体长 <110.00 mm时随体长增加而上升,在110.00~120.00 mm时出现骤降拐点,δ15N最小,之后随体长增加而上升。在体长 <100.00 mm和 >120.00 mm两阶段的营养多样性较高,营养生态位宽幅较大;在体长100.00~120.00 mm阶段,种群冗余度与均匀度较高,群落内营养生态位分布均匀,拥有相似营养特征的个体占比高。贝叶斯混合模型溯源表明,浮游动物对棘头梅童鱼的食物贡献比例最高。研究结果可为棘头梅童鱼的资源保护与开发提供理论依据。
Abstract:Collichthys lucidus is an important small economic fish, and in order to understand its nutritional structure and dietary characteristics, we collected samples from the waters of the Pearl River Estuary in 2021 and 2022, and studied them from the perspectives of trophic niche, trophic structure index and feeding habit by on stable isotope technology. The results indicate that the δ13C and δ15N values of C. lucidus were (−18.74±1.41)‰ and (12.35±0.57)‰, respectively, with a trophic level of (3.25±0.17)‰. The δ13C value gradually increased when the body length was less than 100.00 mm, then decreased with the increase of body length. The δ15N value increased with the increase of body length when the body length was less than 110.00 mm, and the inflection point occurred at body length of 110.00–120.00 mm. The δ15N value was the lowest, and then increased with the increase of body length. When the body length was less than 100.00 mm and more than 120.00 mm, the trophic diversity was high, and the trophic niche width was large. When the body length was 100.00–120.00 mm, the redundancy and evenness were high, and the trophic niche distribution was uniform in the community, and the individuals with similar trophic characteristics accounted for the majority. Bayesian mixing model tracing reveals that the highest food contribution proportion for C. lucidus was from zooplankton. The research provides a theoretical basis for the resource conservation and management of C. lucidus.
-
Keywords:
- Collichthys lucidus /
- Stable isotope /
- Niche /
- Trophic level /
- Pearl River Estuary
-
克氏原螯虾(Procambarus clarkii)俗称小龙虾,2017年我国克氏原螯虾的产量达到112.97×104 t[1],连续两年成为甲壳类淡水养殖第一品种。苗种运输是克氏原螯虾养殖生产过程中的重要环节,实际养殖生产中克氏原螯虾以干法运输为主[2]。干法运输即无水运输,它利用了克氏原螯虾抗缺水能力较强的特点。
在干法运输过程中,克氏原螯虾离开水体处于干露状态,随着时间的延长会对机体造成干露胁迫。目前已有对三疣梭子蟹(Portunus trituberculatus)、日本囊对虾(Penaeus japonicus)、脊尾白虾(Exopalaemon carinicauda)等甲壳动物干露方面的研究[3-5],而关于克氏原螯虾干露方面的研究尚未见报道。研究表明干露条件下,低氧、盐度、pH、失水等环境胁迫因子的联合作用引发了水产动物强烈的应激反应[4]。Omori等[6]认为蟹类的干露耐受能力由鳃的保水能力所决定,姜令绪等[3]研究表明三疣梭子蟹干露耐受性取决于温、湿度条件和幼体的发育阶段。在运输过程中,水生动物会通过调节血糖升高以适应各种胁迫[7],随着干露时间的延长,无氧代谢参与其中导致体内乳酸浓度上升[8]。姜娜等[4]发现干露胁迫下,三疣梭子蟹肝胰腺的总抗氧化能力(T-AOC)和机体胁迫程度有显著相关性;段亚飞等[9]认为谷胱甘肽过氧化物酶(GPx)、过氧化氢酶(CAT)、超氧化物歧化酶(SOD)和丙二醛(MDA)可作为日本囊对虾干露胁迫下的免疫监测指标。本文主要研究了不同干露时间胁迫和再入水过程中,克氏原螯虾血糖、肌肉乳酸、SOD、CAT、T-AOC、MDA和死亡率的变化,旨在选出与克氏原螯虾干露耐受性相关的健康指标,为干法运输改良和养殖监测提供理论参考。
1. 材料与方法
1.1 实验材料
克氏原螯虾幼虾取自上海海洋大学崇明基地,体质量为(8.7±0.4) g。幼虾暂养于循环水族缸(180 cm×180 cm×80 cm)中,时间为1周。养殖水温为(20±1) ℃、pH为7.6±0.3、光暗周期为14 h∶10 h、持续充氧,每天投喂配合饲料(浙江欣欣饲料有限公司)。干露容器为450 mL的PP塑料盒(8.8 cm×6.3 cm×12.0 cm)。
1.2 实验设计
克氏原螯虾幼虾干露实验在室内进行,配备了空调和抽湿机,温度为(20±1) ℃,相对湿度(relative humidity, RH)为(50±5)%。根据预实验的结果设4个干露时间组(6 h、12 h、18 h和24 h)和1个对照组(无干露处理),每组80尾幼虾,干露结束后记录各组成活率并在存活个体中随机抽取6尾用于酶活等指标测定,再将各组剩余的幼虾进行再入水处理,分别在第1、第6和第12小时随机抽取6尾幼虾用于酶活等指标测定并记录各组成活率。
1.3 实验方法
克氏原螯虾置于解剖盘上,用吸水纸擦干体表,将1 mL的注射器针头插入幼虾的附肢关节膜,抽取血液于2 mL的离心管中。剪开头胸甲和腹部取出肝胰腺和肌肉,用2 mL的离心管分装完后立即放入液氮里冻存,最后均保存于−80 ℃冰箱中待测。
肌肉和肝胰腺粗酶液的制备:取肝胰腺或肌肉样品称质量,移液枪取9倍于组织块的预冷匀浆介质,用电动匀浆器冰浴匀浆,充分匀浆后用4 ℃低温离心机8 000 r·min−1离心10 min,取上清液即为粗酶液,之后放入−80 ℃冰箱保存备用,用于组织酶活力的测定。
血清的制备:取出冻存的血淋巴样品,待样品融化后,用电动匀浆器冰浴匀浆,充分匀浆后用4 ℃低温离心机10 000 r·min−1离心10 min,取上清液即为血清待测液。
1.4 指标测定
T-AOC、SOD、CAT和MDA均采用苏州科铭生物技术有限公司试剂盒进行测定。T-AOC的单位定义为37 ℃条件下,样品组织使反应体系的吸光度(OD)每增加0.066时,为1个总抗氧化能力单位(U·g−1)。SOD活力测定采用NBT法,单位定义为在反应体系中抑制百分率为50%时,反应体系中的SOD酶活力定义为1个酶活力单位(U·g−1)。CAT酶活的单位定义为每克组织每分钟催化1 mol的H2O2降解定义为1个酶活力单位。MDA质量摩尔浓度(nmol·g−1)采用硫代巴比妥酸(TAB)法测定。血糖(μmol·mL−1)和乳酸(μmol·g−1)采用苏州科铭生物技术有限公司的试剂盒进行测定,具体方法按照试剂盒说明书进行。
1.5 数据分析
实验数据均以“平均值±标准差(
$\overline X \pm {\rm{SD}}$ )”表示,结果用SPSS 17.0软件进行单因素方差分析(One-Way ANOVA)和Duncan检验进行多重比较,P<0.05表示有显著性差异。2. 结果
2.1 干露胁迫和再入水对死亡率的影响
不同干露时间胁迫下克氏原螯虾累积成活率见图1。干露6 h和12 h组的幼虾成活率均为100%,干露过程中大部分时间表现为静止状态,身体蜷缩,用镊子触碰后立即张开螯足,作防御姿态,活力正常。18 h组的幼虾无个体死亡,但在干露过程中会有间歇性“躁动”现象:尝试从容器中爬出,触碰后反应迟钝。24 h组幼虾开始出现死亡(成活率为53.3%),表现为第二触角的顶端会明显卷曲,咀嚼器附近分泌出许多泡沫。
4个干露时间组的幼虾再入水成活率均为100%,其中12 h、18 h和24 h组的幼虾入水时会漂浮于水面,约2 min后再完全沉入水体。
2.2 干露胁迫和再入水对血糖浓度的影响
克氏原螯虾血糖浓度随着干露时间的延长逐渐升高(图2-a)。干露第6小时血糖浓度显著上升(P<0.05),之后持续升高,在第24 小时达到最高值(4.08 μmol·mL−1),是对照组(0.54 μmol·mL−1)的7.5倍,而且各处理组之间差异显著(P<0.05)。
再入水阶段(图2-b),干露6 h组入水第1小时血糖浓度显著上升(P<0.05),第6小时略有下降,入水第12小时达到峰值(1.15 μmol·mL−1)。干露12 h组的血糖浓度呈下降趋势,第12小时达到最低值(0.94 μmol·mL−1),但仍显著高于对照组(P<0.05)。干露18 h组的血糖浓度呈下降趋势,入水1 h后显著高于对照组,入水第6小时开始降低,但仍显著高于对照组,入水第12小时又有所回升。干露24 h组入水第1小时血糖浓度显著高于对照组水平,入水第6小时达到峰值(1.05 μmol·mL−1),入水第12小时又有所下降。
2.3 干露胁迫和再入水对肌肉乳酸浓度的影响
克氏原螯虾干露后肌肉乳酸浓度见图3-a。与对照组(1.67 μmol·mL−1)相比,干露第6小时幼虾乳酸浓度(4.75 μmol·mL−1)显著升高(P<0.05)。在干露第12和第18小时,乳酸浓度一直维持在较高水平,和对照组有显著性差异。干露第24 小时达到最高(5.2 μmol·mL−1),但各组之间没有显著差异(P>0.05)。
干露6 h组和12 h组入水第1小时乳酸浓度即降低到对照组水平(图3-b),在入水第6和第12小时略有升高,但与对照组相比无显著差异(P>0.05)。干露18 h和24 h组的乳酸浓度呈逐渐下降的趋势,入水第1小时显著高于对照组(P<0.05),入水第6和第12小时略有下降,但仍显著高于对照组(P<0.05)。
2.4 干露胁迫和再入水对CAT活力的影响
克氏原螯虾肝胰腺中CAT活力随着干露时间的延长逐渐升高(图4-a)。CAT活力从干露第12小时开始显著高于对照组(P<0.05),之后维持此水平至第18小时。干露第24小时CAT活力达到最高[190 nmol·(min·g)−1],是对照组[37 nmol·(min·g)−1]的5倍,且CAT活力显著高于其他3个处理组(P<0.05)。
克氏原螯虾干露后入水阶段肝胰腺CAT活力见图4-b。干露6 h组入水后CAT活力一直维持较高水平,显著高于对照组(P<0.05)。干露12 h组在入水第6小时CAT活力达到最大值,在入水第12小时恢复至对照组水平。干露18 h组CAT活力逐渐下降,在入水第12小时恢复到对照组水平。干露24 h组CAT活力随着入水时间的延长逐渐升高,在入水第12小时达到最大值。
2.5 干露胁迫和再入水对SOD活力的影响
克氏原螯虾肝胰腺SOD活力的变化见图5-a。与对照组相比,干露第6小时SOD活力显著下降(P<0.05),之后一直维持较低水平,在干露第24小时有明显上升,但仍显著低于对照组水平。
干露6 h组在入水第1小时SOD活力显著低于对照组(P<0.05),入水第12小时酶活力达到最高(243 U·g−1),但仍显著低于对照组水平。12 h组再入水阶段SOD活力显著低于对照组水平(P<0.05),呈逐渐下降的趋势。干露18 h组入水第1小时SOD活力显著低于对照组,入水第6小时略有下降,在第12小时明显升高,酶活力达到峰值(371 U·g−1),但仍显著低于对照组水平(466 U·g−1)。干露24 h组SOD活力在入水第6小时(389 U·g−1)升高到对照组水平,之后在第12小时又明显降低,显著低于对照组(图5-b)。
2.6 干露胁迫和再入水对T-AOC水平的影响
与对照组相比,克氏原螯虾肝胰腺中T-AOC水平随着干露时间的延长无显著性变化(P>0.05),而且各组之间也无显著性差异(图6-a)。
干露6 h组T-AOC水平在入水阶段有逐渐上升的趋势(图6-b),入水第6小时开始显著高于对照组(85 U·g−1),在第12小时达到最高值(132 U·g−1)。干露12 h组T-AOC水平呈先下降再升高的趋势,在入水第1小时显著高于对照组,第6小时又下降到对照组水平,之后在第12小时又显著上升(P<0.05)到最大值(127 U·g−1)。干露18 h组T-AOC水平在入水第1小时显著高于对照组(P<0.05),之后一直维持较高水平,在入水第12小时达到最大值(137 U·g−1)。干露24 h组T-AOC水平入水第1小时显著升高(P<0.05),随后开始下降,在入水第12 小时降至对照组水平。
2.7 干露胁迫和再入水对MDA质量摩尔浓度的影响
干露胁迫对克氏原螯虾肝胰腺MDA质量摩尔浓度的影响见图7-a。MDA质量摩尔浓度随着干露时间的延长整体呈上升趋势。与对照组相比,前3个处理组的MDA质量摩尔浓度均无显著性差异(P>0.05)。干露第24小时达到最大值(31 nmol·g−1),且显著高于对照组(18 nmol·g−1)。
干露6 h组MDA质量摩尔浓度在再入水阶段呈先升高再下降的趋势(图7-b),入水第6 小时达到最大值(25 nmol·g−1),但与对照组之间无显著差异(P>0.05)。干露12 h和18 h组入水后MDA质量摩尔浓度逐渐上升,但与对照组相比无显著性差异。干露24 h组MDA质量摩尔浓度呈逐渐下降的趋势,入水第1小时显著升高(P<0.05),并达到最大值(30 nmol·g−1),入水第6小时略有下降,但仍显著高于对照组,入水第12小时降低到对照组水平。
3. 讨论
3.1 干露胁迫和再入水对克氏原螯虾成活率的影响
在本实验的温、湿度(20 ℃,50% RH)条件下,克氏原螯虾干露18 h的成活率为100%,干露24 h成活率降为53.3%。说明克氏原螯虾幼虾具有一定的干露耐受能力,但干露时间不宜超过18 h。实验中观察到,当幼虾的第二触角开始卷曲,咀嚼器附近有泡沫液体分泌时,幼虾会在短时间内死亡,这可能是幼虾遭受严重胁迫的信号。有研究认为蟹类干露后再入水过程中会排出体内代谢物,重新建立酸碱平衡,鳃小节体液再灌注,恢复至正常水平[10]。但是当再入水阶段发生氧化应激,一些重要的血淋巴物质超过了机体耐受,就会造成机体死亡[11-12]。值得注意的是,本实验中即使干露24 h组的幼虾死亡率已接近50%,入水成活率仍达到100%。说明克氏原螯虾对于干露再入水时的氧化应激有较强的抵抗能力。
3.2 干露胁迫和再入水对克氏原螯虾抗氧化能力的影响
动物机体的抗氧化水平,一定程度上反映了机体的健康状况。氧自由基(ROS)是机体代谢过程中排出外源物质和抗应激反应时的产物[13],包括超氧离子自由基(
$ {\rm{O}}_2^ {-} $ )、羟自由基(•OH)和过氧化氢(H2O2)。当机体内的抗氧化酶系统不能及时清除过量的ROS,就会造成氧化损伤[14]。肝胰腺作为甲壳动物氧化代谢的主要场所,抗氧化酶的水平较高,也是产生大量ROS的器官[15]。因此,本实验主要通过肝胰腺抗氧化酶活的变化来评估幼虾干露胁迫和再入水阶段的健康状况。总抗氧化能力(T-AOC)主要包括机体内的抗氧化酶体系和抗氧化物质体系,也是衡量机体抗氧化系统功能状况的综合性指标[16]。SOD是
$ {\rm{O}}_2^ {-}$ 主要的清除剂,可以与$ {\rm{O}}_2^ {-}$ 发生歧化反应,生成H2O2和O2,CAT再将H2O2分解生成H2O和O2,2种酶之间相互协同,抑制细胞膜脂氧化,减少氧化损伤[13]。本实验发现,SOD活力在干露阶段始终维持较低水平,分析可能是干露引起幼虾机体内产生了过量的ROS,SOD被用来还原$ {\rm{O}}_2^ {-}$ 导致SOD急剧减少[17-18]。CAT活力随着干露时间的延长逐渐上升,说明机体由于胁迫生成的H2O2引起了CAT酶活的显著升高,机体需要提高抗氧化酶活来适应这种胁迫环境。而T-AOC一直维持对照组水平,表明在干露阶段幼虾总的抗氧化能力没有明显下降。MDA是细胞脂类过氧化作用的产物,其浓度反映了细胞的受损伤程度[14]。干露第24小时MDA开始显著升高,说明此时幼虾体内的ROS不能被及时清除,过量的ROS对机体造成了氧化损伤甚至导致死亡(46.7%),同时CAT活力在干露第24小时达到了峰值,2种指标表现出较好的相关性。干露再入水阶段,各处理组的SOD活力始终低于对照组,CAT活力则明显高于对照组,说明机体在入水阶段内发生了氧化应激反应,产生了大量的ROS。干露18 h和24 h组的SOD活力在入水第6和第12小时明显升高,可能是因为干露时间更长,需要更多的SOD来清除体内的ROS。再入水过程中各处理组的CAT活力呈现波动性变化,没有明显的规律,这可能是机体应激反应中的“应激适应”和“应激损伤”造成的[19]。各处理组的T-AOC整体在对照组水平之上,而抗氧化酶体系中的主要组成SOD一直处于较低水平,表明再入水阶段机体内的抗氧化酶被大量消耗,当机体不能提供足够的抗氧化酶时,需要更多的抗氧化物质来抵抗氧化应激,维持ROS的平衡。干露24 h组的MDA质量摩尔浓度在入水第12小时能够降低到对照组水平,入水成活率同样也保持在100%,说明克氏原螯虾有较强的抗氧化应激和再入水恢复能力。
3.3 干露胁迫和再入水对克氏原螯虾血糖和乳酸浓度的影响
有报道称“高血糖”是甲壳动物典型的应激反应标志[20]。本实验中,血糖浓度在干露后呈阶梯式上升,显著高于对照组。这是由于在干露胁迫下机体需要消耗大量的能量,葡萄糖是水生动物血液中的主要糖类,糖原被迅速降解释放大量的ATP来供能[7, 21],导致血糖在短时间内大量增加。同时干露胁迫会导致鳃功能受损,进一步造成缺氧或低氧[22],无氧代谢加强,乳酸浓度随之升高[23]。本研究显示,干露后肌肉乳酸浓度显著升高,表明此阶段幼虾进行了无氧代谢,机体处于缺氧状态。而在干露6 h后肌肉乳酸浓度并没有持续增加,推测是肌肉中的乳酸及时释放到了血液里[24]。而释放到血液中的乳酸也可以作为糖异生原料合成葡萄糖[25],从而导致机体内的血糖升高。
干露再入水阶段,各处理组的血糖浓度明显高于对照组,说明干露后再入水过程中幼虾长时间处于胁迫应激状态,需要更多的能量来抵抗这种应激。干露6 h和12 h组的幼虾入水后,肌肉乳酸被迅速清除体外,恢复到对照组水平。而18 h和24 h组的幼虾干露时间更长,乳酸浓度也明显高于对照组,说明干露时间越短,肌肉乳酸的清除速率越快。整个再入水阶段,受乳酸转化葡萄糖维持酸碱平衡及葡萄糖供应的影响[26],只有干露6 h和12 h组的乳酸浓度恢复到了对照组水平,表明血糖比乳酸的恢复速率慢。
综上所述,干露胁迫时间对克氏原螯虾幼虾抗氧化系统有显著影响,幼虾的干法运输时间不宜超过18 h。抗氧化能力指标中,CAT和SOD对干露胁迫的反应更敏感,干露胁迫对血糖、肌肉乳酸也有显著影响,其中血糖的变化表现出明显的时间效应,可作为干露阶段幼虾健康状况的参考指标。MDA、血糖和肌肉乳酸浓度的变化能够更灵敏地反映出机体再入水阶段的健康状况。
-
表 1 棘头梅童鱼体长组划分及其稳定同位素特征
Table 1 Classification of body length groups and stable isotope characteristics of C. lucidus
体长
Body length (L)/mm样本数
Number of samples/尾平均体长
Average length/mm营养级
Trophic levelδ15N/‰ δ13C/‰ L≤90 11 64.43±17.31 3.21±0.15 12.21±0.52ab −20.69±1.81a 90<L≤100 23 96.36±2.19 3.28±0.14 12.45±0.47a −17.78±0.82d 100<L≤110 34 104.71±2.34 3.28±0.12 12.46±0.40a −17.89±0.79d 110<L≤120 40 114.97±3.17 3.19±0.12 12.15±0.40a −18.43±0.81c 120<L≤130 35 123.84±2.51 3.25±0.19 12.34±0.65ab −19.36±1.23b 130<L 15 137.04±12.39 3.34±0.28 12.65±0.94a −20.06±1.56a 注:同列不同字母表示组间差异显著 (P<0.05)。 Note: Values with different letters within the same column are significantly different (P<0.05). 表 2 棘头梅童鱼各体长组的营养结构指标
Table 2 Trophic structure indexes of each body length group of C. lucidus
体长
Body length (L)/mmδ13C差值
CRδ15N差值
NR平均离心距离
CD平均最邻近距离
MNND平均最邻近距离标准差
SDNND多边形总面积
TA矫正后的标准椭圆面积
SEAcL≤90 5.79 1.87 1.59 0.61 0.52 5.93 2.92 90<L≤100 4.17 2.01 0.60 0.27 0.65 2.86 0.97 100<L≤110 3.53 1.75 0.65 0.20 0.27 3.18 0.78 110<L≤120 2.96 1.76 0.77 0.21 0.18 3.84 0.99 120<L≤130 5.33 3.71 1.09 0.26 0.35 8.35 1.88 130<L 5.13 3.41 1.52 0.55 0.42 6.45 2.73 Note: CR. δ13C range; NR. δ15N range; CD. Mean distance to centroid; MNND. Mean nearest neighbor distance; SDNND. Standard deviation of nearest neighbor distance; TA. Total area; SEAc. Corrected standard ellipse area. 表 3 棘头梅童鱼各体长组营养生态位椭圆重叠面积比率
Table 3 Ratio of overlap area of trophic niche ellipses in each body length group of C. lucidus
体长
Body length (L)/mmL≤90 90<L≤100 100<L≤110 110<L≤120 120<L≤130 130<L L≤90 2.92 0.00% 0.00% 4.76% 32.30% 34.23% 90<L≤100 0.00% 0.97 75.24% 13.21% 0.00% 0.00% 100<L≤110 0.00% 93.24% 0.78 22.54% 0.00% 0.00% 110<L≤120 14.09% 12.94% 17.82% 0.99 58.44% 33.56% 120<L≤130 50.12% 0.00% 0.00% 30.66% 1.88 83.42% 130<L 36.58% 0.00% 0.00% 12.13% 57.46% 2.73 注:加粗字表示该体长组标准椭圆面积(SEAc),右上角数据和左下角数据均表示两个体长组SEAc占左列体长组SEAc的百分比。 Note: Bold represents the standard elliptical area (SEAc) of the body length group. The data in the upper right corner and lower left corner both represent the percentage of the two body length groups' SEAc to the left column body length group's SEAc. -
[1] ZHANG S, LI M, ZHU J F, et al. An integrated approach to determine the stock structure of spinyhead croaker Collichthys lucidus (Sciaenidae) in Chinese coastal waters[J]. Front Mar Sci, 2021, 8: 693954. doi: 10.3389/fmars.2021.693954
[2] 熊朋莉, 陈作志, 侯刚, 等. 珠江河口棘头梅童鱼生物学特征的年代际变化[J]. 南方水产科学, 2021, 17(6): 31-38. [3] 区又君, 廖锐, 李加儿, 等. 利用耳石日轮研究珠江口棘头梅童鱼的产卵期及生长[J]. 台湾海峡, 2012, 31(1): 85-88. [4] SONG N, YIN L N, SUN D R, et al. Fine-scale population structure of Collichtys lucidus populations inferred from microsatellite markers[J]. J Appl Ichthyol, 2019, 35(3): 709-718. doi: 10.1111/jai.13902
[5] 黄良敏, 谢仰杰, 李军, 等. 闽江口及附近海域棘头梅童鱼的生物学特征[J]. 集美大学学报(自然科学版), 2010, 15(4): 8-13. [6] 农业农村部渔业渔政管理局, 全国水产技术推广总站, 中国水产学会. 2022中国渔业统计年鉴[M]. 北京: 中国农业出版社, 2022: 59-64. [7] 农业部渔业渔政管理局. 2014中国渔业统计年鉴[M]. 北京: 中国农业出版社, 2014: 59-63. [8] WANG Y Y, ZHANG H A, CHEN Y W, et al. Trophic niche width and overlap of three benthic living fish species in Poyang Lake: a stable isotope approach[J]. Wetlands, 2019, 39(1): 17-23. doi: 10.1007/s13157-018-1028-3
[9] WANG J, JIANG R J, XIAO Y, et al. Trophic niche partitioning of five Sciaenidae species sampled in Zhoushan Archipelago waters via stable isotope analysis[J]. Front Mar Sci, 2022, 9: 880123. doi: 10.3389/fmars.2022.880123
[10] WANG S Q, WANG X F, XU L X, et al. Feeding habits and trophic niche of rainbow runner Elagatis bipinnulata in the western and central Pacific Ocean[J]. Environ Biol Fishes, 2022, 105(1): 139-149. doi: 10.1007/s10641-021-01200-w
[11] KVAAVIK C, OSKARSSON G J, PÉTURSDÓTTIR H, et al. New insight into trophic niche partitioning and diet of mackerel (Scomber scombrus) and herring (Clupea harengus) in Icelandic waters[J]. ICES J Mar Sci, 2021, 78(4): 1485-1499. doi: 10.1093/icesjms/fsaa100
[12] CHENG J, MA G Q, MIAO Z Q, et al. Complete mitochondrial genome sequence of the spinyhead croaker Collichthys lucidus (Perciformes, Sciaenidae) with phylogenetic considerations[J]. Mol Biol Rep, 2012, 39(4): 4249-4259. doi: 10.1007/s11033-011-1211-6
[13] MA Q Y, TIAN S Q, HAN D Y, et al. Growth and maturity heterogeneity of three croaker species in the East China Sea[J]. Reg Stud Mar Sci, 2021, 41: 101483.
[14] LIU H B, JIANG T, HUANG H H, et al. Estuarine dependency in Collichthys lucidus of the Yangtze River Estuary as revealed by the environmental signature of otolith strontium and calcium[J]. Environ Biol Fish, 2015, 98(1): 165-172. doi: 10.1007/s10641-014-0246-7
[15] 高世科, 黄金玲, 于雯雯, 等. 吕泗渔场两种石首鱼科鱼类营养生态学特征: 来自稳定同位素的证据[J]. 应用海洋学学报, 2021, 40(3): 413-420. [16] 贺舟挺, 薛利建, 金海卫. 东海北部近海棘头梅童鱼食性及营养级的探讨[J]. 海洋渔业, 2011, 33(3): 265-273. [17] 王建锋, 赵峰, 宋超, 等. 长江口棘头梅童鱼食物组成和摄食习性的季节变化[J]. 应用生态学报, 2016, 27(1): 291-298. [18] 杨纪明. 渤海鱼类的食性和营养级研究[J]. 现代渔业信息, 2001(10): 10-19. [19] 宋业晖, 薛莹, 徐宾铎, 等. 海州湾3种石首鱼的食物组成和生态位重叠[J]. 水产学报, 2020, 44(12): 2017-2027. [20] 王军, 苏永全, 柳建英, 等. 罗源湾五种石首鱼类的食性研究[J]. 厦门水产学院学报, 1994(2): 34-39. [21] 王静. 舟山群岛海域四种经济鱼类的摄食生态研究[D]. 舟山: 浙江海洋大学, 2022: 25-39. [22] POST D M. Using stable isotopes to estimate trophic position: models, methods, and assumptions[J]. Ecology, 2002, 83(3): 703-718. doi: 10.1890/0012-9658(2002)083[0703:USITET]2.0.CO;2
[23] LAYMAN C A, ARRINGTON D A, MONTAA C G, et al. Can stable isotope ratios provide for community-wide measures of trophic structure?[J]. Ecology, 2007, 88(1): 42-48. doi: 10.1890/0012-9658(2007)88[42:CSIRPF]2.0.CO;2
[24] JACKSON A L, INGER R, PARNELL A C, et al. Comparing isotopic niche widths among and within communities: SIBER-Stable Isotope Bayesian Ellipses in R[J]. J Anim Ecol, 2011, 80(3): 595-602. doi: 10.1111/j.1365-2656.2011.01806.x
[25] 石焱. 基于碳氮稳定同位素的闽江口常见鱼类营养生态位季节性变化[D]. 厦门: 集美大学, 2018: 26-33. [26] 叶学瑶, 任泷, 匡箴, 等. 基于稳定同位素技术的阳澄湖鱼类群落营养结构研究[J]. 中国水产科学, 2021, 28(6): 703-714. [27] 赖丽华, 张申增, 陆丽仪, 等. 2017—2020年珠江口棘头梅童鱼的种群特征[J]. 应用生态学报, 2022, 33(5): 1413-1419. [28] PAULY D, PALOMARES M L. Fishing down marine food web: it is far more pervasive than we thought[J]. Bull Mar Sci, 2005, 76(2): 197-211.
[29] JENNINGS S, GREENSTREET S P R, HILL L, et al. Long-term trends in the trophic structure of the North Sea fish community: evidence from stable-isotope analysis, size-spectra and community metrics[J]. Mar Biol, 2002, 141(6): 1085-1097. doi: 10.1007/s00227-002-0905-7
[30] 郑德锋, 赵金良, 周文玉, 等. 我国沿海棘头梅童鱼(Collichthys lucidus)群体遗传结构的AFLP分析[J]. 海洋与湖沼, 2011, 42(3): 443-447. [31] QUILLFELDT P, EKSCHMITT K, BRICKLE P, et al. Variability of higher trophic level stable isotope data in space and time: a case study in a marine ecosystem[J]. Rapid Commun Mass Spectrom, 2015, 29(7): 667-674. doi: 10.1002/rcm.7145
[32] 廖建基, 郑新庆, 杜建国, 等. 基于氮稳定同位素的九龙江口鱼类营养级研究[J]. 海洋学报, 2015, 37(2): 93-103. [33] 高春霞, 戴小杰, 田思泉, 等. 基于稳定同位素技术的浙江南部近海主要渔业生物营养级[J]. 中国水产科学, 2020, 27(4): 438-453. [34] 何雄波, 李波, 王锦溪, 等. 不同时期北部湾日本带鱼营养生态位差异[J]. 应用生态学报, 2021, 32(2): 683-690. [35] 银利强, 孔业富, 吴忠鑫, 等. 南海中西部海域春季三种金枪鱼类的营养生态位比较[J]. 生态学杂志, 2020, 39(12): 4121-4130. [36] 闫光松, 张涛, 赵峰, 等. 基于稳定同位素技术对长江口主要渔业生物营养级的研究[J]. 生态学杂志, 2016, 35(11): 3131-3136. [37] 王淼, 徐开达, 梁君. 杭州湾北部棘头梅童鱼繁殖群体生物学特征初步分析[J]. 上海海洋大学学报, 2018, 27(5): 781-788. [38] GUL G, DEMIREL N. Ontogenetic shift in diet and trophic role of Raja clavata inferred by stable isotopes and stomach content analysis in the Sea of Marmara[J]. J Fish Biol, 2022, 101(3): 560-572. doi: 10.1111/jfb.15123
[39] 操亮亮, 刘必林, 李建华. 基于稳定同位素技术的东南太平洋公海茎柔鱼摄食生态分析[J]. 大连海洋大学学报, 2022, 37(1): 120-128. [40] ZHOU F, WU H P, JIA S S, et al. Ontogenetic variation of trophic habitat for sympatric benthic octopods in East China Sea derived from isotopic analysis on beaks[J]. Fish Res, 2021, 238: 105902. doi: 10.1016/j.fishres.2021.105902
[41] 郭家彤, 王腾, 陈得仿, 等. 大亚湾黑棘鲷的摄食习性[J]. 中国水产科学, 2021, 28(8): 1041-1050. [42] BARNES C L, BEAUDREAU A H, YAMADA R N. The role of size in trophic niche separation between two groundfish predators in Alaskan waters[J]. Mar Coast Fish, 2021, 13(1): 69-84. doi: 10.1002/mcf2.10141
[43] PARK H J, KWAK J H, LEE Y J, et al. Trophic structures of two contrasting estuarine ecosystems with and without a dike on the temperate coast of Korea as determined by stable isotopes[J]. Estuar Coast, 2020, 43(3): 560-577. doi: 10.1007/s12237-019-00522-4
[44] 杨蕊, 韩东燕, 高春霞, 等. 浙江南部近海前肛鳗营养生态位变化研究: 基于稳定同位素技术[J]. 生态学报, 2022, 42(23): 9796-9807. [45] 黄佳兴, 龚玉艳, 徐姗楠, 等. 南海中西部海域鸢乌贼中型群和微型群的营养生态位[J]. 应用生态学报, 2019, 30(8): 2822-2828. [46] 殷宝法, 淮虎银, 张镱锂, 等. 可可西里地区藏羚羊、藏原羚和藏野驴的营养生态位[J]. 应用生态学报, 2007, 18(4): 766-770. doi: 10.3321/j.issn:1001-9332.2007.04.010 [47] 徐超, 王思凯, 赵峰, 等. 长江口水生动物食物网营养结构及其变化[J]. 水生生物学报, 2019, 43(1): 155-164. [48] 曾艳艺, 赖子尼, 杨婉玲, 等. 珠江河口渔业生物稳定同位素营养级分析[J]. 生态学杂志, 2018, 37(1): 194-202. [49] ZHANG Y L, ZHANG C L, XU B D, et al. Impacts of trophic interactions on the prediction of spatio-temporal distribution of mid-trophic level fishes[J]. Ecol Indic, 2022, 138(2/3): 108826.
[50] AYELEN T, FRANCO C, ANÍBAL G N, et al. Trophic niche partitioning of five skate species of genus Bathyraja in northern and central Patagonia, Argentina[J]. J Fish Biol, 2020, 97(3): 656-667. doi: 10.1111/jfb.14416
[51] 李振华, 徐开达, 蒋日进, 等. 东海中北部小眼绿鳍鱼的食物组成及摄食习性的体长变化[J]. 中国水产科学, 2011, 18(1): 185-193. -
期刊类型引用(14)
1. 田海军,任胜杰,杨治国,顾夕章. 复方中草药制剂对克氏原螯虾抗白斑综合征感染研究. 水产科学. 2024(01): 129-135 .  百度学术
百度学术
2. 黄月,陈荔,钟传艳,陈果,龙晓文. 干露胁迫对中华绒螯蟹成体呼吸和能量代谢及抗氧化能力的影响. 水产学杂志. 2024(02): 61-69 .  百度学术
百度学术
3. 邹宇凡,吴玮杰,白志毅,冯建彬,吴敏,蒋军,李家乐. 5个群体克氏原螯虾生长和养殖生态适应性比较分析. 水产科学. 2024(03): 420-428 .  百度学术
百度学术
4. 王小燕,周胜杰,汪迎港,孙永跃,李铭浩,马振华. 海水酸化对黄鳍金枪鱼幼鱼抗氧化和免疫能力的影响. 南方水产科学. 2024(03): 85-91 .  本站查看
本站查看
5. 苏禹,王力玄,孟泳岐,马源潮,鲁耀鹏,张泽龙,郑佩华,李军涛,冼健安,刘存歧,王冬梅. 环境因素对克氏原螯虾生长与繁育的影响. 中国饲料. 2024(21): 74-82 .  百度学术
百度学术
6. 李晨露,李京昊,成永旭,涂纹,吴乐,奚业文,朱传忠,李嘉尧. 不同饵料对克氏原螯虾仔虾养殖水质、生长、消化酶和非特异性免疫酶的影响. 上海海洋大学学报. 2022(04): 883-892 .  百度学术
百度学术
7. 郭子宇,鲁耀鹏. 克氏原螯虾活体运输技术研究进展. 河北渔业. 2022(09): 38-40+46 .  百度学术
百度学术
8. 罗小莹,李雪红,李述刚,褚上,石柳,吴文锦,丁安子,熊光权,汪兰. 虾类活体贮运中应激诱发因素及其影响研究进展. 食品工业科技. 2022(24): 423-432 .  百度学术
百度学术
9. 邓高威,段健诚,王玉,王林华,欧阳乐飞,高焕,赖晓芳,张庆起,阎斌伦. 干露胁迫对脊尾白虾存活率及氧化应激反应的影响. 水产科学. 2021(02): 244-249 .  百度学术
百度学术
10. 米少辉,尹欣茹,李军涛,张泽龙,冼健安,王冬梅. 免疫增强剂对克氏原螯虾热带引种影响的研究进展. 河北渔业. 2021(06): 38-42 .  百度学术
百度学术
11. 王源源,成永旭,李晨露,刘明明,奚业文,朱传忠,李嘉尧. 干露对克氏原螯虾成虾存活、相关代谢酶及组织结构的影响. 南方水产科学. 2021(05): 34-44 .  本站查看
本站查看
12. 郝晨光,李军涛,张泽龙,张秀霞,冼健安,王冬梅. 模拟空运过程中克氏原螯虾生理生化指标的变化规律. 南方农业学报. 2021(10): 2896-2903 .  百度学术
百度学术
13. 黄志峰,倪国彬. 外力挤压和保存方式对不同规格克氏原螯虾苗种运输成活率的影响. 水产科技情报. 2020(04): 230-233 .  百度学术
百度学术
14. 王文豪,董宏标,孙彩云,段亚飞,李华,刘青松,张家松,曾祥兵. 石菖蒲挥发油和水溶性氮酮对鱼用麻醉剂的促皮渗透效果研究. 南方水产科学. 2020(04): 62-68 .  本站查看
本站查看
其他类型引用(11)





 下载:
下载:










 粤公网安备 44010502001741号
粤公网安备 44010502001741号
