Effect of dietary angelica polysaccharide (AP) on growth performance, antioxidant capacity, serum immune and serum biochemical indices of juvenile golden pompano (Trachinotus ovatus)
-
摘要: 研究了当归多糖对卵形鲳鲹 (Trachinotus ovatus)幼鱼生长性能、肝脏抗氧化能力、血清免疫指标和血清生化指标的影响。配制6种饲料,当归多糖的质量分数分别为0 (对照组)、0.05%、0.10%、0.20%、0.40%和0.80%。挑选体质量为(4.99±0.08) g的卵形鲳鲹幼鱼随机分为6组,每组3个平行,每个平行20尾,放于池塘网箱中喂养,每天饱食投喂2次,为期8周。结果显示,各组末质量、增重率和特定生长率差异不显著(P>0.05)。0.10%组肝脏超氧化物歧化酶活性和总抗氧化能力显著高于0.80%组和对照组(P<0.05);0.10%组和0.20%组血清补体3、补体4含量显著高于对照组(P<0.05);0.10%组血清溶菌酶活性显著高于对照组(P<0.05);0.10%组血清胆固醇、甘油三酯含量和谷草转氨酶活性显著低于0.40%组、0.80%组和对照组(P<0.05)。以上结果表明,当归多糖能显著提高卵形鲳鲹幼鱼的抗氧化能力,增强机体免疫力,但促生长的作用不显著。卵形鲳鲹幼鱼饲料中当归多糖的适宜添加量为0.10%。Abstract: To study the effects of dietary angelica polysaccharide (AP) on the growth performance, hepatic antioxidant capacity, serum immune and serum biochemical indices of juvenile golden pompano (Trachinotus ovatus), we designd six diets with addition of 0 (control group), 0.05%, 0.10%, 0.20%, 0.40% and 0.80% AP, respectively. The fish [(4.99±0.08) g] were assigned randomly into six groups with three replicates per group and 20 fish per replicate. They were cultured in cages and fed twice daily for eight weeks. The results show that the final mass, weight gain rate and specific growth rate were not significantly affected by AP level (P>0.05). The superoxide dismutase activity and total antioxidant capacity of the fish fed with 0.10% AP diet were significant higher than those of 0.80% AP group and the control group (P<0.05). The contents of Complement 3 and Complement 4 of 0.10% and 0.20% AP groups were significant higher than those of the control group (P<0.05). The fish fed with 0.10% AP diet showed higher lysozyme activity than those in the control group (P<0.05), but with lower transaminase activity, cholesterol and triglycerides than the fish of 0.40%, 0.80% AP groups and the control group (P<0.05). In conclusion, dietary AP can improve the antioxidant capacity and immunity of juvenile golden pompano but not the growth. Suitable AP supplementation level in diet of juvenile golden pompano is 0.10%.
-
植物多糖,又称植物多聚糖,是一类功效多、副作用小、来源广泛的天然活性物质[1]。研究表明,植物多糖具有促生长[2-4]、抗氧化[5-11]、免疫调节[12-13]、降糖调脂[14-16]和保肝护肝[17-19]等作用。当归(Angelica sinensis)是伞形科多年生草本植物当归的干燥根,主要产自甘肃东南部,其次为云南、四川、陕西、湖北等地。当归多糖是当归的主要活性物质,因具有助造血、抗辐射、抗肿瘤、抗氧化、增强免疫力[17]等功能而受到广泛关注。王庆奎[20]研究发现,在饲料中添加当归多糖可以有效提高点带石斑鱼(Epinephelus coioides)的非特异性免疫力和抗病力,而对其生长没有显著性影响。也有研究表明,当归多糖可以提高鸡(Gallus domesticus)[21]和小鼠(Mus musculus)[18,22]的抗氧化能力,调节小鼠的免疫功能[23],且具有一定的保肝作用[18-19]。目前,当归多糖对水产动物影响的研究报道较少见到,有待进一步加强。
卵形鲳鲹 (Trachinotus ovatus),俗称金鲳,隶属硬骨鱼纲、鲈形目、鲹科,主要分布于太平洋、印度洋和大西洋的温热带海域[24]。卵形鲳鲹的肉质细嫩,味道鲜美,是名贵的食用鱼类。目前,在中国的福建、广东、广西和海南等地已经形成规模化养殖。但近两年灾害频发,已严重影响了卵形鲳鲹养殖业的可持续发展。本研究拟通过探讨当归多糖对卵形鲳鲹幼鱼生长性能、肝脏抗氧化能力、血清免疫指标和血清生化指标的影响,为卵形鲳鲹的健康养殖提供参考。
1. 材料与方法
1.1 实验饲料的制备
按照卵形鲳鲹的营养需求以鱼粉、豆粕、大豆浓缩蛋白、花生麸和啤酒酵母为蛋白源,以鱼油和大豆卵磷脂为脂肪源,通过梯度添加当归多糖配制等氮等脂的6种饲料。饲料中当归多糖的质量分数分别为0 (对照组)、0.05%、0.10%、0.20%、0.40%和0.80%。饲料配方组成成分详见表1。将鱼粉、豆粕、花生麸等原料用粉碎机粉碎并过40目筛网。按照饲料配方准确称量每种饲料原料,先把常量组分混合搅拌均匀,再把微量组分通过逐级扩大混匀的方法加入,初步混匀后放入搅拌机(SZ250,广州旭众食品有限公司)搅拌10 min后取出。按比例加入鱼油和大豆卵磷脂,人工搓碎混匀并过40目筛网后倒入搅拌机搅拌10 min。加入适量的水(约40%)搅拌10 min后取出,用双螺杆挤条机(F-26,广州华南理工大学)挤压成直径2.0 mm和2.5 mm的条形物,经造粒机(G-500,广州华南理工大学)制成颗粒后放在18 ℃空调房中抽干,然后用封口袋密封并做好标签,于 – 20 ℃保存备用。
表 1 实验饲料配方及营养组成 (干质量)Table 1. Formulation and nutrient composition of basal diet (dry mass)% 原料
ingredient组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 鱼粉 fish meal 27 27 27 27 27 27 豆粕 soybean meal 16 16 16 16 16 16 大豆浓缩蛋白 soy protein concentrate 12 12 12 12 12 12 花生粕 peanut meal 12 12 12 12 12 12 啤酒酵母 brewer's yeast 5 5 5 5 5 5 面粉 wheat flour 15.6 15.6 15.6 15.6 15.6 15.6 鱼油 fish oil 6 6 6 6 6 6 大豆卵磷脂 soy lecithin 1.5 1.5 1.5 1.5 1.5 1.5 维生素1 vitamin premix 1 1 1 1 1 1 矿物质2 mineral premix 1 1 1 1 1 1 氯化胆碱 (50%) choline chloride 0.5 0.5 0.5 0.5 0.5 0.5 磷酸二氢钙 monocalcium phosphate 0.5 0.5 0.5 0.5 0.5 0.5 维生素C (95%) vitamin C 0.5 0.5 0.5 0.5 0.5 0.5 甜菜碱 betaine 0.5 0.5 0.5 0.5 0.5 0.5 乙氧基喹啉 ethoxyquin 0.1 0.1 0.1 0.1 0.1 0.1 微晶纤维素 microcrystalline cellulose 0.80 0.75 0.70 0.60 0.40 0 当归多糖 (60%)3 angelica polysaccharide 0 0.05 0.10 0.20 0.40 0.80 总和 total 100 100 100 100 100 100 营养成分 proximate composition 水分 moisture 7.78 7.81 7.77 7.76 7.77 7.82 粗蛋白 crude protein 43.40 43.39 43.34 43.40 43.34 43.37 粗脂肪 crude fat 10.75 10.84 10.80 10.72 10.84 10.83 灰分 ash 9.43 9.52 9.46 9.48 9.44 9.47 注:1. 维生素预混料为每千克饲料提供维生素A 1.2 g,维生素T3 450 mg,维生素E 30 g,维生素K3 30 g,维生素B1 8 g,维生素B2 15 g,维生素B6 12 g,维生素B12 90 mg,烟酸 90 g,肌醇 80 g,D-泛酸钙 50 g,叶酸 1.2 g,D-生物素 40 mg;2. 矿物质预混料为每千克饲料添加氟化钠 4 mg,碘化钾 1.6 mg,氯化钴 (1%) 100 mg,硫酸铜 20 mg,硫酸铁 160 mg,硫酸锌 100 mg,硫酸锰 120 mg,硫酸镁 2.4 g,磷酸二氢钙 6.0 g,氯化钠 200 mg,沸石粉30.90 g;3. 购自陕西森弗天然制品有限公司,当归多糖的有效含量为60% Note: 1. Vitamin premix provids the following per kg of diet: VA 1.2 g, ${\rm V}_{{\rm T}_{3}} $ 450 mg, VE 30 g, ${\rm V}_{{\rm K}_{3}} $ 30 g, ${\rm V}_{{\rm B}_{1}} $ 8 g, ${\rm V}_{{\rm B}_{2}} $ 15 g, ${\rm V}_{{\rm B}_{6}} $ 12 g, ${\rm V}_{{\rm B}_{12}} $ 90 mg, nicotinic acid 90 g, inositol 80 g, D-calcium d-pantothenate 50 g, folic acid 1.2 g, D-biotin 40 mg; 2. Mineral premix provides the following per kg of diet: NaF 4 mg, KI 1.6 mg, CoCl2·6H2O (1%) 100 mg, CuSO4·5H2O 20 mg, FeSO4·H2O 160 mg, ZnSO4·H2O 100 mg, MnSO4·H2O 120 mg, MgSO4·7H2O 2.4 g, Ca(H2PO4)2·H2O 6.0 g, NaCl 200 mg, zelote power 30.90 g; 3. It was purchased from Shanxi Sciphar Natural Products Co., Ltd., and the effective content of angelica polysaccharide was 60%. 1.2 实验设计与实验管理
养殖实验在中国水产科学研究院南海水产研究所深圳试验基地室外池塘网箱中进行。实验开始前,将卵形鲳鲹饥饿24 h,用丁香酚(成都艾科达化学试剂有限公司)麻醉,随机挑选360尾大小均匀、健康的幼鱼 [平均体质量(4.99±0.08) g] 放于18个网箱(96 cm×96 cm×135 cm)中,每个网箱20尾。随机分配饲喂6种饲料,每种饲料设置3个重复。实验开始前用商品料饱食驯化1周。实验开始后每天早上7:30和下午5:30各饱食投喂1次,连续充气,为期8周。实验期间详细记录每个网箱的采食量,实验鱼如有死亡,立即捞取称其体质量并做好记录。整个养殖过程中池塘水温为29.1~31.8 ℃,溶解氧为4.8~7.2 mg·L–1,盐度为15~18。
1.3 样品采集
养殖实验结束后饥饿24 h,依次将网箱里的鱼全部捞出,麻醉后计数并称鱼体总质量。从中随机取4尾鱼测其体长、体质量并记录,测量完成后,用2.5 mL的注射器(1%的肝素钠润洗)尾静脉取血,注入1.5 mL的离心管中。4 ℃静置0.5 h后离心(3 000 r·min–1,10 min,4 ℃),收集上清液并分装于0.5 mL的离心管中,于 – 80 ℃保存备用。采血后,按顺序解剖称量内脏和肝脏质量并记录,肝脏分装于2 mL离心管中,于 – 20 ℃保存备用。再将解剖后的鱼去皮取背部肌肉,于 – 20 ℃保存备用。另取3尾全鱼 – 20 ℃保存备用。
1.4 指标测定
增重率 (WGR)=(终末均质量–初始均质量)/初始均质量×100%
特定生长率 (SGR)=(ln终末均质量–ln初始均质量)/实验天数×100%
成活率 (SR)=终末尾数/初始尾数×100%
饲料系数 (FCR)=投喂饲料质量/鱼体增加质量
肝体比 (HSI)=肝脏质量/鱼体质量×100%
脏体比 (VSI)=内脏质量/鱼体质量×100%
肥满度 (CF, g·cm–3)=体质量/体长3
全鱼和肌肉中水分、粗蛋白、粗脂肪、灰分含量参照杜强[25]所描述的方法进行测定。
肝脏和血清相关酶活指标均采用试剂盒(南京建成生物工程研究所)进行测定。血清生化指标委托广州新海医院检验中心进行测定。
1.5 数据的处理分析
实验数据采用Excel 2007软件进行处理,通过SPSS 18.0软件进行统计分析,所得数据以“平均值±标准差(
$\overline X \pm {\rm SD}$ )”表示,P<0.05表示差异显著。2. 结果
2.1 对卵形鲳鲹幼鱼生长性能的影响
随着饲料中当归多糖百分含量的增加,末质量、增重率和特定生长率先升高后降低,各组间末质量、增重率和特定生长率差异不显著(P>0.05);0.40%组和0.80%组的饲料系数显著高于其余组(P<0.05);肝体比先降低后升高,处理组显著低于对照组(P<0.05);各组间成活率、脏体比和肥满度差异不显著(P>0.05,表2)。
表 2 饲料中添加当归多糖对卵形鲳鲹幼鱼生长性能的影响Table 2. Effect of dietary AP level on growth performance of juvenile golden pompano项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 初质量/g initial mass 5.02±0.09 4.96±0.08 4.92±0.05 5.02±0.11 5.05±0.09 4.96±0.05 末质量/g final mass 68.99±1.51 69.59±2.58 71.83±3.35 70.66±1.93 70.20±5.86 68.65±3.57 增重率/% weight gain rate 1 273.54±52.26 1 302.29±72.41 1 358.57±74.79 1 307.57±68.82 1 290.46±98.50 1 284.25±80.27 特定生长率/% SGR 4.16±0.06 4.19±0.08 4.25±0.08 4.20±0.08 4.18±0.11 4.17±0.09 饲料系数 FCR 1.21±0.03a 1.21±0.06a 1.22±0.02a 1.23±0.02a 1.28±0.04b 1.30±0.02b 成活率/% survival rate 98.33±2.89 98.33±2.89 96.67±5.77 95.00±8.66 93.33±5.77 95.00±5.00 肝体比/% HSI 0.89±0.04b 0.79±0.01a 0.73±0.04a 0.74±0.01a 0.74±0.01a 0.75±0.05a 脏体比/% VSI 5.53±0.06 5.57±0.10 5.92±0.43 5.89±0.10 5.62±0.25 5.46±0.22 肥满度/g·cm–3 CF 3.30±0.01 3.34±0.02 3.43±0.05 3.48±0.01 3.34±0.17 3.30±0.05 注:同行数据上标字母不同表示差异显著 (P<0.05),后表同此 Note: The values with different superscript letters within the same row indicate significant difference (P<0.05). The same case in the following tables. 2.2 对卵形鲳鲹幼鱼全鱼和肌肉成分的影响
0.10%组的全鱼粗蛋白显著低于0.40%组和0.80%组(P<0.05);0.10%组和0.20%组全鱼粗脂肪含量显著高于0.40%组和0.80%组(P<0.05);0.10%组和0.20%组全鱼灰分含量显著高于0.80%组和对照组(P<0.05);各组间全鱼水分含量无显著性差异(P>0.05,表3)。肌肉中脂肪含量先降低后升高,0.10%组、0.20%组和0.40%组显著低于0.80%组和对照组(P<0.05);各组间肌肉水分、蛋白和灰分含量无显著性差异(P>0.05)。
表 3 饲料中添加当归多糖对卵形鲳鲹幼鱼全鱼和肌肉成分的影响Table 3. Effect of dietary AP level on whole body and muscle proximate composition of juvenile golden pompano% 项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 全鱼 whole body 水分 moisture 69.43±1.25 69.77±1.37 69.34±1.18 69.40±1.31 69.33±1.19 70.03±1.15 粗蛋白 crude protein 53.16±1.02abc 52.72±0.22ab 50.88±0.34a 50.98±1.19ab 53.52±0.42bc 54.77±0.16c 粗脂肪 crude lipid 29.38±0.89ab 30.32±0.49ab 32.53±0.52b 32.36±0.96b 28.71±0.61a 27.64±0.45a 灰分 ash 12.76±0.17ab 13.34±0.29bc 13.49±0.24c 13.57±0.26c 13.22±0.33bc 12.58±0.28a 肌肉 muscle 水分 moisture 76.72±0.83 77.54±0.13 76.60±0.29 76.82±0.58 76.58±0.26 76.46±0.83 蛋白 crude protein 72.93±0.89 73.13±0.18 73.59±0.48 73.35±0.15 72.75±0.17 72.14±0.56 脂肪 crude lipid 18.39±0.73b 17.74±0.56ab 16.62±0.28a 16.58±0.56a 16.82±0.20a 18.13±0.12b 灰分 ash 8.16±0.16 7.62±0.33 8.04±0.30 8.06±0.12 7.82±0.55 7.78±0.12 2.3 对卵形鲳鲹幼鱼肝脏抗氧化能力的影响
0.10%组的超氧化物歧化酶活性显著高于0.05%组、0.80%组和对照组(P<0.05);0.10%组、0.20%组和0.40%组丙二醛含量显著低于0.80%组和对照组(P<0.05);0.10%组总抗氧化能力显著高于0.40%组、0.80%组和对照组(P<0.05);0.20%组谷胱甘肽过氧化物酶活性显著高于对照组(P<0.05,表4)。
表 4 饲料中添加当归多糖对卵形鲳鲹幼鱼肝脏抗氧化能力的影响Table 4. Effect of dietary AP level on hepatic antioxidative ability of juvenile golden pompano项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 超氧化物歧化酶/U·g–1 SOD 594.03±15.34a 635.38±13.71a 894.33±15.59c 817.18±12.51bc 813.71±14.86bc 745.23±13.39b 丙二醛/nmol·g–1 MDA 107.74±3.18d 82.88±2.09bc 63.26±2.16b 38.13±2.14a 80.95±2.25b 104.47±4.64cd 总抗氧化能力/U·g–1 T-AOC 212.55±6.85a 277.94±5.02ab 324.15±4.09b 285.77±3.84ab 223.38±4.16a 229.75±2.06a 谷胱甘肽过氧化物酶/U·g–1 GSH-Px 1.20±0.02a 1.23±0.03ab 1.36±0.01ab 1.39±0.02b 1.32±0.05ab 1.26±0.03ab 2.4 对卵形鲳鲹幼鱼血清免疫指标的影响
0.10%组和0.20%组补体3含量显著高于对照组(P<0.05);0.10%组和0.20%组补体4含量显著高于其余各组(P<0.05);随饲料中当归多糖百分含量的增加,溶菌酶活性先升高后降低,0.10%组显著高于对照组(P<0.05);各组间碱性磷酸酶活性无显著性差异(P>0.05,表5)。
表 5 饲料中添加当归多糖对卵形鲳鲹幼鱼血清免疫指标的影响Table 5. Effect of dietary AP level on plasma immune parameters of juvenile golden pompano项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 补体3/μg·mL–1 C3 95.80±0.14a 97.25±1.48ab 98.62±0.60bc 99.98±1.94c 98.44±0.08abc 98.32±0.39abc 补体4/μg·mL–1 C4 182.75±0.07a 183.80±1.56a 205.30±1.84b 208.55±3.18b 184.05±2.62a 183.00±1.09a 溶菌酶/U·mL–1 LZM 2.83±0.16a 4.89±0.60ab 5.93±0.45b 5.39±0.34ab 5.12±0.48ab 4.26±0.28ab 碱性磷酸酶/U·L–1 AKP 42.50±0.78 44.00±0.00 47.00±0.00 46.00±1.41 45.50±0.71 43.00±1.07 2.5 对卵形鲳鲹幼鱼血清生化指标的影响
0.10%组的血清胆固醇和甘油三酯含量显著低于0.05%组、0.40%组、0.80%组和对照组(P<0.05);0.10%组血清谷草转氨酶活性显著低于0.40%组、0.80%组和对照组(P<0.05);各组间总蛋白、白蛋白、血糖含量和谷丙转氨酶活性无显著性差异(P>0.05,表6)。
表 6 饲料中添加当归多糖对卵形鲳鲹幼鱼血清生化指标的影响Table 6. Effect of dietary AP level on plasma biochemical indices of juvenile golden pompano项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 总蛋白/g·L–1 TP 27.65±1.06 28.15±0.64 29.70±1.41 29.00±0.14 27.20±1.24 27.45±0.92 白蛋白/g·L–1 ALB 7.23±0.50 7.17±0.17 9.50±0.56 8.95±0.62 6.95±0.07 7.87±0.55 血糖/mmol·L–1 GLU 8.53±0.61 7.33±0.60 6.22±0.42 4.99±0.11 5.49±0.66 6.40±0.16 胆固醇/mmol·L–1 CHO 4.42±0.11c 4.13±0.08bc 3.72±0.18a 3.91±0.07ab 4.18±0.16bc 4.32±0.06c 甘油三酯/mmol·L–1 TG 0.98±0.06b 0.88±0.12b 0.68±0.01a 0.82±0.07ab 0.86±0.04b 0.96±0.01b 谷丙转氨酶/U·L–1 ALT 5.00±0.00 5.00±0.00 3.50±0.71 3.50±0.71 3.50±0.71 4.50±0.71 谷草转氨酶/U·L–1 AST 39.50±0.71b 35.00±1.41ab 27.00±1.24a 33.00±0.71ab 37.50±0.71b 37.00±0.00b 3. 讨论
植物多糖作为一类大分子活性物质,广泛存在于植物体内[26],目前在水产养殖中通常被用作生长促进剂和免疫增强剂[27]。植物多糖对水产动物的促生长作用国内外已有相关报道,如饲料中添加一定量的黄芪多糖可以显著提高鲫(Carassius auratus)[2]、尼罗罗非鱼(Oreochromis niloticus)[3]的生长性能。吴旋[4]研究发现,枸杞多糖的添加量为1 200 mg·kg–1时,黄颡鱼(Pelteobagrus fulvidraco)的增重率显著提高。本研究中当归多糖对卵形鲳鲹的增重率和特定生长率显示出一定的促进作用,但差异不显著,相似的结果也出现在点带石斑鱼[20]的报道中。0.40%组和0.80%组的饲料系数显著高于其余组,这在一定程度上说明了植物多糖的两面性,适量添加有益,而过量添加则不利[27]。添加当归多糖明显降低了卵形鲳鲹的肝体比,这与程玉冰等[28]的报道一致。
研究表明,黄芪多糖可以增加鲫的脂肪含量[2],枸杞多糖可以提高黄颡鱼肌肉的粗蛋白含量[4]。而胡兵等[29]发现黄芪多糖可以显著增加异育银鲫(C. auratus gibelio)肌肉中粗脂肪的含量,但是粗蛋白含量无显著性差异。本研究表明,当归多糖显著影响了卵形鲳鲹全鱼的粗蛋白和粗脂肪含量,高添加量组肌肉中的脂肪含量要显著低于对照组,肌肉粗蛋白含量无显著性差异。从以上研究结果可以看出,植物多糖对水产动物体成分的影响因多糖种类、作用对象的不同而呈现出很大的差异。当归多糖影响营养物质在水产动物体内积累的机制目前还不甚明了,因此未来有必要在相关方面做进一步的研究。
多糖类可以提高抗氧化类物质的活性,消除自由基并抑制脂质过氧化[17]。刘丽花[22]以小鼠为实验对象得出结论,当归多糖可以显著提高D-半乳糖致衰老模型小鼠血清中超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶的活性,并降低血浆、肝匀浆和脑匀浆中过氧化脂质的水平。超氧化物歧化酶可以通过清除超氧离子自由基来保护细胞免受损伤[30];丙二醛是脂质过氧化反应的最终产物,其含量反映了组织中脂质过氧化程度及自由基的含量[31]。本研究结果显示,高添加量组肝脏超氧化物歧化酶的活性均显著高于对照组,而0.10%组、0.20%组和0.40%组丙二醛含量显著低于对照组,说明当归多糖可以消除肝脏中的自由基并抑制脂质过氧化,提高肝脏的抗氧化能力。总抗氧化能力是指通过消除机体内过多的自由基和活性氧类物质达到的抗氧化作用;谷胱甘肽过氧化物酶可以通过催化谷胱甘肽对过氧化氢的还原反应来阻止肝脏的损伤,总抗氧化能力和谷胱甘肽过氧化物酶直接反映了肝脏的抗氧化能力[32]。本研究中0.10%组总抗氧化能力显著高于对照组,0.20%组谷胱甘肽过氧化物酶活性显著高于对照组,说明当归多糖可以清除活性氧自由基[33],显著提高卵形鲳鲹肝脏的抗氧化能力。
鱼类既有非特异性免疫系统又有特异性免疫系统,但是与高等脊椎动物相比,鱼类的特异性免疫系统尚不完善。因此,鱼类主要还是依赖非特异性免疫系统来应对外部环境刺激和病原入侵[34]。补体系统作为一种蛋白质反应系统,主要负责破坏或清除病原微生物,是机体非特异性免疫的重要组成部分[35]。本研究中,0.10%组和0.20%组补体3、补体4含量均显著高于对照组,说明当归多糖可以激活卵形鲳鲹的补体系统,这与马红樱等[36]、尹卫平[37]的报道相互印证。研究表明,植物多糖是通过替代途径或者经典途径来激活补体系统的[26]。溶菌酶作为一种碱性蛋白,是吞噬细胞杀菌的物质基础,对机体防御起着重要作用[38]。碱性磷酸酶是一种磷酸单酯酶,是机体内重要的解毒体系,也作为溶酶体酶的重要组成部分在免疫系统中发挥重要作用[39]。从结果中可看出,溶菌酶的活性先升高后降低,当归多糖添加量为0.10%时活性最高且显著高于对照组,而各组间碱性磷酸酶活性无显著性差异。王庆奎[20]研究发现,当归多糖可以提高点带石斑鱼血液中白细胞的吞噬率和血清溶酶体酶活性。以上结果说明,当归多糖可以调节水产动物的免疫系统,提高机体非特异性免疫力[40]。
血清生化指标反映了机体的生理状态、健康状况及营养水平[41]。血清中总蛋白、白蛋白的含量反映了机体蛋白质的吸收、合成和分解状况,也与机体的免疫力有关[42]。血清胆固醇和甘油三酯含量一定程度上反映了机体内的脂肪代谢状况[43]。本研究中,各组血清总蛋白和白蛋白没有显著性差异,0.10%组胆固醇和甘油三酯含量显著低于0.40%组、0.80%组和对照组。而枸杞多糖可以提高黄颡鱼血清总蛋白和白蛋白含量, 并降低胆固醇和甘油三酯的含量[4]。以上结果都说明了植物多糖具有降血脂的作用[44]。正常情况下鱼体的血糖处于动态平衡中,但是容易受到外部刺激而发生波动,一般活动性强的鱼体血糖会偏高[45]。本研究中,血糖无显著性差异,说明各组卵形鲳鲹状态良好且没有受到外部环境的威胁。谷丙转氨酶和谷草转氨酶在机体蛋白代谢中起重要作用,其活性能反映肝细胞是否受损伤[46]。本研究结果表明,适量的当归多糖可以降低卵形鲳鲹血清中的谷草转氨酶含量,但是过量添加又会导致谷草转氨酶含量升高,说明过量的当归多糖对肝脏造成了一定的损伤,这也印证了植物多糖的两面性[27]。
4. 结论
饲料中添加适量的当归多糖能显著提高卵形鲳鲹幼鱼肝脏抗氧化能力、增强机体免疫力,但促生长的作用不显著。卵形鲳鲹幼鱼饲料中当归多糖的适宜添加量为0.10%。
-
表 1 实验饲料配方及营养组成 (干质量)
Table 1 Formulation and nutrient composition of basal diet (dry mass)
% 原料
ingredient组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 鱼粉 fish meal 27 27 27 27 27 27 豆粕 soybean meal 16 16 16 16 16 16 大豆浓缩蛋白 soy protein concentrate 12 12 12 12 12 12 花生粕 peanut meal 12 12 12 12 12 12 啤酒酵母 brewer's yeast 5 5 5 5 5 5 面粉 wheat flour 15.6 15.6 15.6 15.6 15.6 15.6 鱼油 fish oil 6 6 6 6 6 6 大豆卵磷脂 soy lecithin 1.5 1.5 1.5 1.5 1.5 1.5 维生素1 vitamin premix 1 1 1 1 1 1 矿物质2 mineral premix 1 1 1 1 1 1 氯化胆碱 (50%) choline chloride 0.5 0.5 0.5 0.5 0.5 0.5 磷酸二氢钙 monocalcium phosphate 0.5 0.5 0.5 0.5 0.5 0.5 维生素C (95%) vitamin C 0.5 0.5 0.5 0.5 0.5 0.5 甜菜碱 betaine 0.5 0.5 0.5 0.5 0.5 0.5 乙氧基喹啉 ethoxyquin 0.1 0.1 0.1 0.1 0.1 0.1 微晶纤维素 microcrystalline cellulose 0.80 0.75 0.70 0.60 0.40 0 当归多糖 (60%)3 angelica polysaccharide 0 0.05 0.10 0.20 0.40 0.80 总和 total 100 100 100 100 100 100 营养成分 proximate composition 水分 moisture 7.78 7.81 7.77 7.76 7.77 7.82 粗蛋白 crude protein 43.40 43.39 43.34 43.40 43.34 43.37 粗脂肪 crude fat 10.75 10.84 10.80 10.72 10.84 10.83 灰分 ash 9.43 9.52 9.46 9.48 9.44 9.47 注:1. 维生素预混料为每千克饲料提供维生素A 1.2 g,维生素T3 450 mg,维生素E 30 g,维生素K3 30 g,维生素B1 8 g,维生素B2 15 g,维生素B6 12 g,维生素B12 90 mg,烟酸 90 g,肌醇 80 g,D-泛酸钙 50 g,叶酸 1.2 g,D-生物素 40 mg;2. 矿物质预混料为每千克饲料添加氟化钠 4 mg,碘化钾 1.6 mg,氯化钴 (1%) 100 mg,硫酸铜 20 mg,硫酸铁 160 mg,硫酸锌 100 mg,硫酸锰 120 mg,硫酸镁 2.4 g,磷酸二氢钙 6.0 g,氯化钠 200 mg,沸石粉30.90 g;3. 购自陕西森弗天然制品有限公司,当归多糖的有效含量为60% Note: 1. Vitamin premix provids the following per kg of diet: VA 1.2 g, ${\rm V}_{{\rm T}_{3}} $ 450 mg, VE 30 g, ${\rm V}_{{\rm K}_{3}} $ 30 g, ${\rm V}_{{\rm B}_{1}} $ 8 g, ${\rm V}_{{\rm B}_{2}} $ 15 g, ${\rm V}_{{\rm B}_{6}} $ 12 g, ${\rm V}_{{\rm B}_{12}} $ 90 mg, nicotinic acid 90 g, inositol 80 g, D-calcium d-pantothenate 50 g, folic acid 1.2 g, D-biotin 40 mg; 2. Mineral premix provides the following per kg of diet: NaF 4 mg, KI 1.6 mg, CoCl2·6H2O (1%) 100 mg, CuSO4·5H2O 20 mg, FeSO4·H2O 160 mg, ZnSO4·H2O 100 mg, MnSO4·H2O 120 mg, MgSO4·7H2O 2.4 g, Ca(H2PO4)2·H2O 6.0 g, NaCl 200 mg, zelote power 30.90 g; 3. It was purchased from Shanxi Sciphar Natural Products Co., Ltd., and the effective content of angelica polysaccharide was 60%. 表 2 饲料中添加当归多糖对卵形鲳鲹幼鱼生长性能的影响
Table 2 Effect of dietary AP level on growth performance of juvenile golden pompano
项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 初质量/g initial mass 5.02±0.09 4.96±0.08 4.92±0.05 5.02±0.11 5.05±0.09 4.96±0.05 末质量/g final mass 68.99±1.51 69.59±2.58 71.83±3.35 70.66±1.93 70.20±5.86 68.65±3.57 增重率/% weight gain rate 1 273.54±52.26 1 302.29±72.41 1 358.57±74.79 1 307.57±68.82 1 290.46±98.50 1 284.25±80.27 特定生长率/% SGR 4.16±0.06 4.19±0.08 4.25±0.08 4.20±0.08 4.18±0.11 4.17±0.09 饲料系数 FCR 1.21±0.03a 1.21±0.06a 1.22±0.02a 1.23±0.02a 1.28±0.04b 1.30±0.02b 成活率/% survival rate 98.33±2.89 98.33±2.89 96.67±5.77 95.00±8.66 93.33±5.77 95.00±5.00 肝体比/% HSI 0.89±0.04b 0.79±0.01a 0.73±0.04a 0.74±0.01a 0.74±0.01a 0.75±0.05a 脏体比/% VSI 5.53±0.06 5.57±0.10 5.92±0.43 5.89±0.10 5.62±0.25 5.46±0.22 肥满度/g·cm–3 CF 3.30±0.01 3.34±0.02 3.43±0.05 3.48±0.01 3.34±0.17 3.30±0.05 注:同行数据上标字母不同表示差异显著 (P<0.05),后表同此 Note: The values with different superscript letters within the same row indicate significant difference (P<0.05). The same case in the following tables. 表 3 饲料中添加当归多糖对卵形鲳鲹幼鱼全鱼和肌肉成分的影响
Table 3 Effect of dietary AP level on whole body and muscle proximate composition of juvenile golden pompano
% 项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 全鱼 whole body 水分 moisture 69.43±1.25 69.77±1.37 69.34±1.18 69.40±1.31 69.33±1.19 70.03±1.15 粗蛋白 crude protein 53.16±1.02abc 52.72±0.22ab 50.88±0.34a 50.98±1.19ab 53.52±0.42bc 54.77±0.16c 粗脂肪 crude lipid 29.38±0.89ab 30.32±0.49ab 32.53±0.52b 32.36±0.96b 28.71±0.61a 27.64±0.45a 灰分 ash 12.76±0.17ab 13.34±0.29bc 13.49±0.24c 13.57±0.26c 13.22±0.33bc 12.58±0.28a 肌肉 muscle 水分 moisture 76.72±0.83 77.54±0.13 76.60±0.29 76.82±0.58 76.58±0.26 76.46±0.83 蛋白 crude protein 72.93±0.89 73.13±0.18 73.59±0.48 73.35±0.15 72.75±0.17 72.14±0.56 脂肪 crude lipid 18.39±0.73b 17.74±0.56ab 16.62±0.28a 16.58±0.56a 16.82±0.20a 18.13±0.12b 灰分 ash 8.16±0.16 7.62±0.33 8.04±0.30 8.06±0.12 7.82±0.55 7.78±0.12 表 4 饲料中添加当归多糖对卵形鲳鲹幼鱼肝脏抗氧化能力的影响
Table 4 Effect of dietary AP level on hepatic antioxidative ability of juvenile golden pompano
项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 超氧化物歧化酶/U·g–1 SOD 594.03±15.34a 635.38±13.71a 894.33±15.59c 817.18±12.51bc 813.71±14.86bc 745.23±13.39b 丙二醛/nmol·g–1 MDA 107.74±3.18d 82.88±2.09bc 63.26±2.16b 38.13±2.14a 80.95±2.25b 104.47±4.64cd 总抗氧化能力/U·g–1 T-AOC 212.55±6.85a 277.94±5.02ab 324.15±4.09b 285.77±3.84ab 223.38±4.16a 229.75±2.06a 谷胱甘肽过氧化物酶/U·g–1 GSH-Px 1.20±0.02a 1.23±0.03ab 1.36±0.01ab 1.39±0.02b 1.32±0.05ab 1.26±0.03ab 表 5 饲料中添加当归多糖对卵形鲳鲹幼鱼血清免疫指标的影响
Table 5 Effect of dietary AP level on plasma immune parameters of juvenile golden pompano
项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 补体3/μg·mL–1 C3 95.80±0.14a 97.25±1.48ab 98.62±0.60bc 99.98±1.94c 98.44±0.08abc 98.32±0.39abc 补体4/μg·mL–1 C4 182.75±0.07a 183.80±1.56a 205.30±1.84b 208.55±3.18b 184.05±2.62a 183.00±1.09a 溶菌酶/U·mL–1 LZM 2.83±0.16a 4.89±0.60ab 5.93±0.45b 5.39±0.34ab 5.12±0.48ab 4.26±0.28ab 碱性磷酸酶/U·L–1 AKP 42.50±0.78 44.00±0.00 47.00±0.00 46.00±1.41 45.50±0.71 43.00±1.07 表 6 饲料中添加当归多糖对卵形鲳鲹幼鱼血清生化指标的影响
Table 6 Effect of dietary AP level on plasma biochemical indices of juvenile golden pompano
项目 item 组别 group 对照
control0.05% 0.10% 0.20% 0.40% 0.80% 总蛋白/g·L–1 TP 27.65±1.06 28.15±0.64 29.70±1.41 29.00±0.14 27.20±1.24 27.45±0.92 白蛋白/g·L–1 ALB 7.23±0.50 7.17±0.17 9.50±0.56 8.95±0.62 6.95±0.07 7.87±0.55 血糖/mmol·L–1 GLU 8.53±0.61 7.33±0.60 6.22±0.42 4.99±0.11 5.49±0.66 6.40±0.16 胆固醇/mmol·L–1 CHO 4.42±0.11c 4.13±0.08bc 3.72±0.18a 3.91±0.07ab 4.18±0.16bc 4.32±0.06c 甘油三酯/mmol·L–1 TG 0.98±0.06b 0.88±0.12b 0.68±0.01a 0.82±0.07ab 0.86±0.04b 0.96±0.01b 谷丙转氨酶/U·L–1 ALT 5.00±0.00 5.00±0.00 3.50±0.71 3.50±0.71 3.50±0.71 4.50±0.71 谷草转氨酶/U·L–1 AST 39.50±0.71b 35.00±1.41ab 27.00±1.24a 33.00±0.71ab 37.50±0.71b 37.00±0.00b -
[1] 桑野, 李晓光, 张昌浩, 等. 国内植物多糖的研究及发展趋势[J]. 吉林医药学院学报, 2017, 38(6): 455-457. [2] 张银花, 刘畅, 曹永春, 等. 黄芪多糖对鲫鱼生长性能及营养物质沉积的影响[J]. 饲料研究, 2013(6): 65-68. [3] ZAHRAN E, RISHA E, ABDELHAMID F, et al. Effects of dietary Astragalus polysaccharides (APS) on growth performance, immunological parameters, digestive enzymes, and intestinal morphology of Nile tilapia (Oreochromis niloticus)[J]. Fish Shellfish Immunol, 2014, 38(1): 149-157.
[4] 吴旋. 四种中草药多糖对黄颡鱼生长、体成分及部分生理生化指标的影响[D]. 天津: 天津农学院, 2011: 13-41. [5] TIAN S Y, HAO C C, XU G K, et al. Optimization conditions for extracting polysaccharide from Angelica sinensis and its antioxidant activities[J]. J Food Drug Anal, 2017, 25(4): 766-775.
[6] CUI G, ZHANG W, ZHANG A, et al. Variation in antioxidant activities of polysaccharides from Fructus jujubae in South Xinjiang area[J]. Int J Biol Macromol, 2013, 57(6): 278-284.
[7] WU H, MIN T, LI X, et al. Physicochemical properties and antioxidant activities of acidic polysaccharides from wampee seeds[J]. Int J Biol Macromol, 2013, 59(4): 90-95.
[8] ZHAO B, ZHANG J, YAO J, et al. Selenylation modification can enhance antioxidant activity of Potentilla anserina L. polysaccharide[J]. Int J Biol Macromol, 2013, 58(2): 320-328.
[9] TANG Z, GAO H, WANG S, et al. Hypolipidemic and antioxidant properties of a polysaccharide fraction from Enteromorpha prolifera[J]. Int J Biol Macromol, 2013, 58(7): 186-189.
[10] YU C H, DAI X Y, CHEN Q, et al. Hypolipidemic and antioxidant activities of polysaccharides from Rosae Laevigatae Fructus in rats[J]. Carbohydr Polym, 2013, 94(1): 56-62.
[11] YU F, LI H, MENG Y, et al. Extraction optimization of Angelica sinensis polysaccharides and its antioxidant activity in vivo[J]. Carbohydr Polym, 2013, 94(1): 114-119.
[12] INNGJERDINGEN K T, LANGERUD B K, RASMUSSEN H, et al. Pectic polysaccharides isolated from Malian medicinal plants protect against Streptococcus pneumoniae in a mouse pneumococcal infection model[J]. Scand J Immunol, 2013, 77(5): 372-388.
[13] WU Y, WANG X, SHEN B, et al. Extraction, structure and bioactivities of the polysaccharides from Fructus corni[J]. Recent Pat Food Nutr Agric, 2013, 5(1): 57-61.
[14] HONG T, ZHAO J, DONG M, et al. Composition and bioactivity of polysaccharides from Inula britannica flower[J]. Int J Biol Macromol, 2012, 51(4): 550-554.
[15] HUANG Y L, CHOW C J, TSAI Y H. Composition, characteristics, and in-vitro physiological effects of the water-soluble polysaccharides from Cassia seed[J]. Food Chem, 2012, 134(4): 1967-1972.
[16] AMAGASE H, SUN B, BOREK C. Lycium barbarum (goji) juice improves in vivo antioxidant biomarkers in serum of healthy adults[J]. Nutr Res, 2009, 29(1): 19-25.
[17] 王利华, 王菲菲, 刘悦, 等. 当归多糖的研究进展[J]. 天津药学, 2017, 29(3): 67-70. [18] GAO Z, ZHANG C, TIAN W, et al. The antioxidative and hepatoprotective effects comparison of Chinese angelica polysaccharide (CAP) and selenizing CAP (sCAP) in CCl4 induced hepatic injury mice[J]. Int J Biol Macromol, 2017, 97: 46-54.
[19] WANG K P, SONG Z Z, WANG H J, et al. Angelica sinensis polysaccharide attenuates concanavalin A-induced liver injury in mice[J]. Int Immunopharmacol, 2016, 31: 140-148.
[20] 王庆奎. 当归多糖对点带石斑鱼非特异性免疫力的影响[D]. 青岛: 中国海洋大学, 2012: 44-71. [21] 靳录洋, 徐小芳, 谷新利. 当归多糖对鸡抗氧化功能的影响[J]. 中国兽医杂志, 2017, 53(6): 76-79. [22] 刘丽花. 当归多糖抗氧化作用的研究[J]. 当代医药论丛, 2014, 12(3): 284-285. [23] 杨铁虹, 贾敏, 梅其炳. 当归多糖对小鼠免疫功能的调节作用[J]. 中成药, 2005, 27(5): 563-565. [24] 刘楚斌, 陈锤. 卵形鲳鲹的生物学与养殖技术[J]. 齐鲁渔业, 2009, 26(6): 32-33. [25] 杜强. 卵形鲳鲹赖氨酸和蛋氨酸需求量及饲料中鱼粉替代的研究[D]. 上海: 上海海洋大学, 2012: 12 [26] 尚庆辉, 解玉怀, 张桂国, 等. 植物多糖的免疫调节作用及其机制研究进展[J]. 动物营养学报, 2015, 27(1): 49-58. [27] 魏帮鸿, 杨志刚, 郭瑞瑞. 植物多糖在水产养殖中的应用[J]. 饲料研究, 2016(14): 39-42. [28] 程玉冰, 潘庭双, 侯冠军, 等. 不同中草药添加剂对草鱼生长及肝胆综合症的影响[J]. 安徽农学通报, 2008, 14(23): 146, 155. [29] 胡兵, 刘军, 侯永清, 等. 黄芪多糖对异育银鲫肌肉组成成分的影响[J]. 中国饲料, 2008(11): 37-38, 44. [30] 罗燕, 谷新利, 徐小芳, 等. 当归多糖对杂交肉鸡血清中SOD、MDA、GSH-Px的影响[J]. 黑龙江畜牧兽医, 2009(7): 104-106. [31] BRAUGHLER J M, HALL E D. Central nervous systems trauma and stroke: I. Biochemical considerations for oxygen radical formation and lipid peroxidation[J]. Free Radical Biol Med, 1989, 6(3): 289-301.
[32] 俞诗源, 孟茹, 李重阳, 等. 当归多糖对麻黄素小鼠肝组织抗氧化酶活性和NF-κB、TNF-α表达的影响[J]. 西北师范大学学报(自然科学版), 2015(1): 75-81. [33] 李贵荣, 吕昌银, 杨胜圆. 当归多糖清除活性氧自由基作用的研究[J]. 南华大学学报(理工版), 2002, 16(3): 18-20. [34] 艾庆辉, 麦康森. 鱼类营养免疫研究进展[J]. 水生生物学报, 2007, 31(3): 425-430. [35] 余英才, 张纯, 夏循礼, 等. 补体系统的进化[J]. 生命科学, 2012, 24(4): 362-367. [36] 马红樱, 张德禄, 胡春香, 等. 植物活性多糖的研究进展[J]. 西北师范大学学报(自然科学版), 2004, 40(3): 112-117. [37] 尹卫平. 抗癌天然药物研究进展[M]. 北京: 科学出版社, 2009: 107-108. [38] 刘云, 孔伟丽, 姜国良, 等. 2种免疫多糖对刺参组织主要免疫酶活性的影响[J]. 中国水产科学, 2008, 15(5): 787-793. [39] 孙静秋, 许燕, 张慧绮, 等. 凡纳对虾体内ACP、AKP酶的细胞化学定位[J]. 复旦学报(自然科学版), 2007, 46(6): 947-951. [40] 杨铁虹, 卢保华, 贾敏, 等. 当归多糖对小鼠免疫功能的影响[J]. 中国药理学通报, 2003, 19(4): 448-451. [41] 韩娜娜, 史成银. 血液指标在鱼类学研究中的应用[J]. 安徽农业科学, 2010, 38(33): 18877-18878, 18880. [42] 刘红柏, 宿斌, 王荻. 三种中草药方剂对鲫部分生化指标的影响[J]. 水产学杂志, 2012, 25(4): 24-28. [43] 田允波, 周家容, 李琦华, 等. 白术多糖对仔猪生长性能和血清生化参数的影响[J]. 中国畜牧杂志, 2009, 45(9): 45-48. [44] 罗祖友, 胡筱波, 吴谋成. 植物多糖的降血糖与降血脂作用[J]. 食品科学, 2007, 28(10): 596-600. [45] 杜强, 林黑着, 王芸, 等. 华南沿海5种海水鱼类血液生化指标的比较研究[J]. 饲料工业, 2014, 35(21): 74-76. [46] 陈玉春, 顾雪飞, 刘敏. 5种中草药对鲤血清谷丙转氨酶、谷草转氨酶及红细胞过氧化氢酶活性的影响[J]. 淡水渔业, 2007, 37(5): 11-13. -
期刊类型引用(26)
1. 黄晓兰,王苗苗,刘海静,杨奇慧,张会兰,陈厚宏,黎杰,徐静,陈岗富,李华涛. 当归副产物对颗粒饲料的保护作用及其对鲫生长和缺氧应激的影响. 动物营养学报. 2025(02): 1173-1187 .  百度学术
百度学术
2. 朱文婷,李文嘉,宣雄智,赵娟. 渔用中草药种类、作用机理及应用效果研究进展. 中国饲料. 2024(05): 94-100 .  百度学术
百度学术
3. 杨鹏,李锐,查红刚,叶志祥,史庆超,张志勇. 复合植物多糖对澳洲淡水龙虾血清生化指标的影响. 现代畜牧兽医. 2023(06): 36-39 .  百度学术
百度学术
4. 李蕾,蒋昕彧,朱雷,孔祥会. 多糖类免疫增强剂在鱼类养殖中的应用研究进展. 水产学杂志. 2023(06): 127-135+145 .  百度学术
百度学术
5. 刘辉,鹿瑶,辛运腾,董乐,董福霖,林基亮,于朝磊,张黎黎. 饲料中添加植物乳杆菌对花鲈生长性能、血清生化指标及抗哈维弧菌感染的影响. 饲料研究. 2023(23): 49-55 .  百度学术
百度学术
6. 曹雪,孙佳,杨质楠,梁爽,李月红. 中草药在水产动物养殖中的研究进展. 饲料研究. 2023(24): 133-137 .  百度学术
百度学术
7. 刘永,闫世雄,杜彦丽,何洋,施红梅,王坤,豆腾飞,刘丽仙,申志超,贾俊静,葛长荣. 植物多糖在鱼类养殖中的应用研究进展. 山西农业科学. 2022(02): 272-280 .  百度学术
百度学术
8. 肖芳,陈涛,伍振煌,王俊龙. 植物多糖的提取工艺、生物学功能及其在动物生产中的研究进展. 饲料研究. 2022(14): 125-128 .  百度学术
百度学术
9. 韦宏杰,李雪鹤,吴远彩,易远名,朱东文君,杨奇慧,谭北平. 月桂酸单甘油酯对凡纳滨对虾生长、肌肉氨基酸、非特异性免疫及肠道菌群的影响. 水产学报. 2022(10): 1912-1926 .  百度学术
百度学术
10. 卫明亮,张志伟,张志勇,林志杰,祝斐,贾超峰,孟乾,徐大凤,张曹进. 冷应激对黑鲷组织损伤及细胞凋亡基因表达的影响. 南方水产科学. 2022(05): 110-117 .  本站查看
本站查看
11. 杨欣仪,类延菊,阳佩蓉,蔡佳玲,杨品红,杨春英. 植物多糖的生物学功能及其对鱼类健康的影响. 饲料研究. 2022(20): 130-136 .  百度学术
百度学术
12. 贾慧凝,侍苗苗,卞永乐,侍崇敬,刘恒蔚,宋学宏,秦粉菊. 纳米硒对低氧胁迫下中华绒螯蟹免疫保护和抗氧化能力的影响. 南方水产科学. 2022(06): 100-109 .  本站查看
本站查看
13. 袁仲瑾,岑剑伟,李来好,杨贤庆,黄卉,魏涯,郝淑贤,赵永强,王悦齐,林织. 低温暂养对珍珠龙胆石斑鱼存活、非特异性免疫及抗氧化指标的影响. 南方水产科学. 2022(06): 118-126 .  本站查看
本站查看
14. 李忠琴,张新艳,杨求华,林茂,江兴龙,翟少伟. 五种中草药复方体外激活花鳗鲡(Anguilla marmorata)外周血白细胞活性的评价. 海洋与湖沼. 2022(06): 1487-1493 .  百度学术
百度学术
15. 孙彩云,董宏标,王文豪,李勇,古群红,段亚飞,张家松,许晓东. 月桂酸单甘油酯对花鲈脂质代谢的影响. 南方水产科学. 2021(01): 67-75 .  本站查看
本站查看
16. 虞为,杨育凯,林黑着,黄小林,黄忠,李涛,周传朋,马振华,荀鹏伟,杨长平. 牛磺酸对花鲈生长性能、消化酶活性、抗氧化能力及免疫指标的影响. 南方水产科学. 2021(02): 78-86 .  本站查看
本站查看
17. 杨蕊,周胜杰,方伟,马振华. 营养强化对卵形鲳鲹仔、稚鱼骨骼发育基因表达的影响. 水产科技情报. 2021(03): 126-131 .  百度学术
百度学术
18. 曾祥兵,董宏标,韦政坤,段亚飞,陈健,张慧,孙彩云,许晓东,张家松. 鸡内金多糖对尖吻鲈幼鱼生长、消化、肠道抗氧化能力和血清生化指标的影响. 南方水产科学. 2021(04): 49-57 .  本站查看
本站查看
19. 韩梦瑶,王晓梅,王占旗,叶金云,张忠山. 天然活性多糖在水产动物养殖中的应用. 水产学杂志. 2021(04): 85-92 .  百度学术
百度学术
20. 李正花,周建虹,陈土艳. 八珍汤加味治疗气滞血瘀证月经不调患者的疗效及作用机制探析. 世界中西医结合杂志. 2021(09): 1719-1723 .  百度学术
百度学术
21. 杨大俏,王锦旭,李来好,杨贤庆,马海霞,胡晓. 近江牡蛎膜分离联产制备多糖多肽及其功能特性研究. 大连海洋大学学报. 2020(01): 126-133 .  百度学术
百度学术
22. 杨大俏,王锦旭,李来好,杨贤庆,马海霞,岑剑伟,王悦齐. 近江牡蛎多糖的结构鉴定及免疫调节能力分析. 食品科学. 2020(10): 38-46 .  百度学术
百度学术
23. 李琛琛,何建,纪鹏,魏彦明,刘胜利,袁子文,张晓松,文艳巧,张亚辉,华永丽,姚万玲. 当归多糖对头孢噻呋钠联合LPS致鸡肝损伤的防治效果. 动物医学进展. 2020(06): 74-80 .  百度学术
百度学术
24. 杨玲,胡睿智,夏嗣廷,贺建华. 植物多糖的功能性研究进展及其在动物生产中的应用. 动物营养学报. 2019(06): 2534-2543 .  百度学术
百度学术
25. 虞为,杨育凯,陈智彬,林黑着,黄小林,周传朋,杨铿,曹煜成,黄忠,马振华,李涛,王珺,王芸,荀鹏伟,黄倩倩,于万峰. 饲料中添加螺旋藻对花鲈生长性能、消化酶活性、血液学指标及抗氧化能力的影响. 南方水产科学. 2019(03): 57-67 .  本站查看
本站查看
26. 赵香菊,刘秀玲,王中华. 大蒜多糖对肉鸡血清生化指标及抗氧化能力的影响. 中国家禽. 2019(20): 52-54 .  百度学术
百度学术
其他类型引用(9)
计量
- 文章访问数: 3391
- HTML全文浏览量: 1160
- PDF下载量: 166
- 被引次数: 35



 下载:
下载:
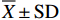
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
