Effects of cold stress on black porgy tissue injury and apoptosis gene expression
-
摘要: 为探究黑鲷 (Acanthopagrus schlegelii) 在低温下的生理适应机制,设计了3个温度梯度 (15、10和5 ℃),以15 ℃为对照,低温胁迫24 h,分别研究了冷应激前后黑鲷的组织结构变化、生理生化反应及凋亡基因的表达。结果显示,随着温度的降低,黑鲷呈现出肝脏空泡化、腮小片收缩、肌纤维断裂等组织损伤现象;肝脏中的甘油三酯 (TG) 含量显著降低 (P<0.05),谷草转氨酶 (AST)、谷丙转氨酶 (ALT) 活性和总胆固醇 (T-CHO) 含量显著升高 (P<0.05),表明黑鲷遭受冷应激,肝脏功能紊乱、结构遭到破坏。q-PCR结果显示,10 ℃时黑鲷通过降低apaf-1、bax、caspase-1基因表达量,促进caspase-3、diablo基因表达,从而减少肝脏细胞丢失来降低冷应激的损伤;胁迫至5 ℃时,温度超过黑鲷自身生理调节阈值,肝脏细胞受损程度加重,黑鲷促进apaf-1、bcl-2和diablo基因表达,抑制caspase-3基因表达,最大限度维持了肝脏细胞的稳态。结果表明,随着温度的降低,黑鲷的肝脏、腮、肌肉损伤加重,其中肝脏通过调节AST、ALT、T-CHO、TG以及凋亡基因表达,以减少组织损伤带来的危害。Abstract: In order to explore the physiological adaptation mechanism of black porgy (Acanthopagrus schlegelii) under low temperature stress, we designed three temperature gradient groups (15, 10 and 5 ℃). Taking 15 ℃ as the control group and with a low temperature stress for 24 h, we studied the tissue structure changes, physiological, biochemical reactions and the expression of apoptosis genes before and after the cold stress. The results show that with the intensification of low temperature stress, the tissue damage such as liver vacuolation, gill lamellae contraction and breakage and muscle fiber breakage were aggravated. The content of triglyceride (TG) in the liver decreased significantly, while the activities of aspartate aminotransferase (AST) and alanine aminotransferase (ALT) as well as the content of total cholesterol (T-CHO) increased significantly, indicating that A. schlegelii had suffered from liver dysfunction and structural damage under cold stress condition. At 10 ℃, the liver reduced the damage of cold stress by decreasing expression levels of apaf-1, bax and caspase-1 genes, increasing expression of caspase-3 and diablo genes so as to reduce the loss of liver cells. When the temperature reached 5 ℃, the temperature exceeded A. schlegelii's physiological regulation threshold, so the degree of liver cell damage was aggravated. The expression of apaf-1, bcl-2 and diablo genes were promoted, while the caspase-3 gene expression was inhibited in order to maintain the homeostasis of liver cells to the greatest extent. It is showed that as the temperature decreased, the liver, gills and muscle damages of A. schlegelii increased. The liver regulated the expression of AST, ALT, T-CHO, TG and apoptotic pathway related genes to reduce the damage caused by tissue damage.
-
Keywords:
- Acanthopagrus schlegelii /
- Cold stress /
- Tissue section /
- Apoptosis
-
水温作为环境中的应激源之一,会直接或间接影响鱼类的生理和行为[1]。水温降低时,鱼类为适应低温会通过多种调节方式使机体内环境再次平衡[2]。一旦鱼类的调节系统无法满足其基本需求时,低温将造成鱼类致死性损伤[3]。研究表明,冷应激可能会对鱼类产生组织学损伤并影响其正常的生理功能,这种组织学损伤是机体对外部应激源的重要反应[4-6]。为了抵御低温,鱼类肝脏中富含的谷草转氨酶 (AST)、谷丙转氨酶 (ALT)、甘油三酯 (TG) 及总胆固醇 (T-CHO) 等物质维持了生物体稳态平衡[7-12]。因此,通过检测这些生理生化指标,可指示鱼类肝脏在急性低温胁迫下是否产生损伤[13-14]。同时,冷应激也会引起多细胞生物体产生细胞凋亡现象,将不需要的或受损的细胞进行调控移除,这种现象是由生物体为适应环境而自主进行的调控[15]。目前,细胞凋亡途径中内在的线粒体途径是国内外一条较为精确的研究途径,此途径由线粒体中细胞色素c (Cyto-c) 的释放引发。在此途径中,apoptotic protease activating factor-1基因 (apaf-1基因) 是凋亡酶激活因子,可以激活细胞凋亡相关酶;促凋亡bcl-associated x基因 (bax基因) 与抗凋亡b-cell lymphoma-2基因 (bcl-2基因) 可以调控线粒体中Cyto-c等凋亡因子的释放参与凋亡途径[16-21]。Smac/Diablo蛋白定位于线粒体,与连锁凋亡抑制蛋白家族结合后,抑制抗凋亡活性从而实现增强凋亡;cysteinyl aspartate specific proteinase-3基因 (caspase-3基因) 是在线粒体凋亡途径中执行最后步骤的凋亡基因[22-23]。cysteinyl aspartate specific proteinase-1基因 (caspase-1基因) 是介导炎症反应的主要基因,通过招募凋亡相关斑点样蛋白与caspase-1前体蛋白结合,形成炎性体复合物进而激活细胞炎症反应[15]。这些基因均是参与细胞凋亡途径的重要基因,其表达水平的动态变化可以说明机体是否发生细胞凋亡。
黑鲷 (Acanthopagrus schlegelii) 隶属鲈形目、鲷科、棘鲷属,因其具有广温、广盐等特性,在我国沿海地区均有分布,是我国沿海重要的经济鱼类[24-25]。黑鲷适宜的生长水温为15~25 ℃,当水温低于5 ℃则无法长期生存[26]。因此在江苏地区养殖黑鲷无法进行室外自然越冬。为解决这一问题,通常采取室内越冬或者锅炉升温等方式,但这些方法会增加养殖成本,并限制黑鲷相关养殖产业的发展。因此选育耐低温品种已逐渐成为黑鲷养殖业的重点研究方向,而黑鲷低温适应相关机制研究是重中之重[27-28]。本研究评估了冷应激下黑鲷不同组织 (肝脏、腮、肌肉) 的结构变化,肝脏的生理生化指标 (AST、ALT、TG、T-CHO) 变化以及肝脏中细胞凋亡相关基因 (apaf-1、bax、bcl-2、caspase-1、caspase-3、diablo) 的表达水平变化,以为解析黑鲷低温适应机制提供理论支持,并为海洋鱼类耐低温性状选育提供更多的基础数据,以提高选育精确性。
1. 材料与方法
1.1 实验材料
选取300尾规格相近、健康无伤的黑鲷幼鱼,体长为 (11.3±1.7) cm、体质量为 (39.6±5.3) g,实验用鱼均取自江苏省海洋水产研究所繁育的苗种。幼鱼暂养在实验用的长条水泥池中,水温为15 ℃,溶解氧质量浓度≥6 mg·L−1,24 h连续充氧,定期换水,每日固定时间投喂1次。暂养2周后,随机挑选健康黑鲷幼鱼270尾,进行正式实验;正式实验开始前禁食1 d。
1.2 降温处理
前期预实验中,将水温从15 ℃快速降至4 ℃时,短时间内黑鲷幼鱼出现死亡现象。因此,挑选3个长3.9 m×宽2.6 m×高0.9 m的长条水泥池,分别设置为15 ℃对照组、10 ℃处理组、5 ℃处理组。每个水泥池中各放入3个同等规格的网箱,即每个温度梯度设置3个平行组,每个网箱中放入30尾黑鲷。利用冷循环系统进行降温,10与5 ℃处理组采用逐级降温的方式。从15 ℃开始降温 (2 ℃·h−1),降至11 ℃后,以1 ℃·h−1的速度降至各处理组预设温度。在15、10和5 ℃各个温度点保持24 h后进行取样。取样前先用MS-222将黑鲷快速麻醉后解剖,每个温度点取3尾鱼的腮、肌肉、肝脏固定于4%多聚甲醛中,另取6尾鱼的肝脏置于1.5 mL离心管中,液氮快速冷冻后于−85 ℃保存。实验期间,水温的温差维持在 ±0.5 ℃,24 h连续充氧。
1.3 石蜡组织切片观察
流水冲洗多聚甲醛固定的肝脏、肌肉和鳃,用70%~95%的乙醇依次进行脱水处理。经二甲苯透明,石蜡包埋、脱蜡处理等步骤后,用苏木精-伊红染色法进行染色以及切片机进行连续切片,切片厚度为5~6 μm,中性树脂封片,显微镜下观察并拍照记录。
1.4 肝脏生理生化指标的测定
采用南京建成生物工程研究所的试剂盒对黑鲷肝脏中的AST、ALT、T-CHO及TG进行检测。
1.5 肝脏组织RNA的提取与cDNA的合成
肝脏组织RNA的提取采用柱式动物组织总RNA抽提试剂盒 (上海生物工程有限公司,B518651),将提取的RNA用1%琼脂糖凝胶电泳检测质量 (电压180 V,时间25 min),用Nanodrop仪器检测纯度 (OD260/280) 和浓度。根据MightyScript第一链cDNA合成试剂盒(上海生物工程有限公司,B639251) 的说明书进行第一链cDNA反转录。
1.6 荧光定量PCR
利用本实验室前期测序获得的黑鲷全基因组数据[29],获取黑鲷的apaf-1、bax、bcl-2、caspase-1、caspase-3、diablo基因CDS序列,用Oligo 7软件设计用于荧光定量PCR检测的上、下游引物,并由上海生物工程有限公司合成。以β-actin作为内参基因,引物序列见表1。荧光定量试剂采用SuperReal PreMix Plus (SYBR Green) 试剂盒 (TIANGEN公司),用ABI 7300 plus荧光定量PCR仪扩增。反应体系:1 μL cDNA模板 (5 ng·μL−1),0.6 μL上、下游引物 (10 μmol·L−1),17.8 μL SuperReal PreMix Plus (SYBR Green) 试剂盒。三步法反应程序:预变性1个循环的条件为95 ℃,15 min;PCR反应40个循环的条件为变性95 ℃,10 s;退火50~60 ℃,20 s;延伸72 ℃,31 s,且在此阶段进行荧光信号采集。每个样品重复测定3次。
表 1 引物信息Table 1. Primer information引物
Primer引物序列 (5'—3')
Primer sequence (5'–3')产物长度
Length of product/bp退火温度
Annealing temperature/℃β-actin-F CGACGGTCAGGTCATCAC 91 β-actin-R GCCAGCAGACTCCATTCC apaf-1-F AGACTACGAAGCTGCACACGTCCT 135 59 apaf-1-R ATCCCGTCCTGCCATCACGTACC bax-F AAGGCGCTGACCACCAACC 150 58 bax-R GGCTACTGTCCTCCACCGAGA bcl-2-F ACCATCGTCACCTCCGACTCC 115 56 bcl-2-R ACTTTGGGCGAGTTCTTTGTCGT caspase-1-F GAGACAGCCCGATCCACTCCCAC 150 58 caspase-1-R AGCAGAGACCCTTTGACCGAGTGT caspase-3-F ATGGACTACCCCAGCCTCGGAAC 101 57 caspase-3-R GCAGCATCAACATCCGTCCCGTT diablo-F CAATGCTGTCAACCTGTG 146 55 diablo-R TCTTATCTGCGTCTGCTG 1.7 数据统计与分析
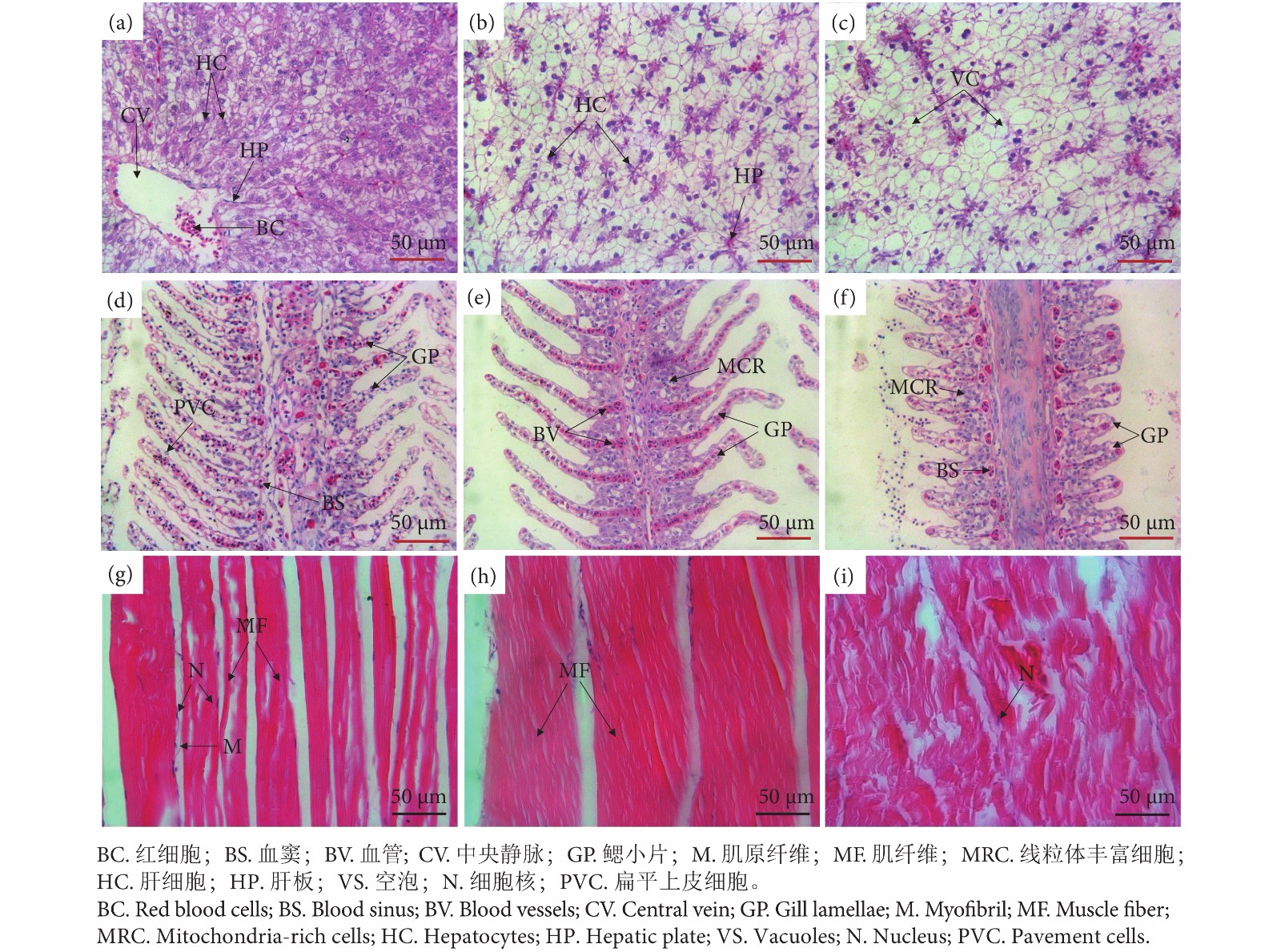
采用2−△△Ct法计算实时荧光定量PCR分析后目的基因的相对表达量。各个实验所得的数据均用“平均值±标准差 (
$\overline { X}\pm { \rm {SD}} $ )”表示,利用单因素方差分析 (One-way ANOVA)对同一时间不同温度组间进行数据处理和检验分析,所有实验数据均用Origin 2019软件进行统计分析以及绘图。2. 结果
2.1 冷应激对黑鲷肝脏组织结构的影响
15 ℃对照组的肝细胞形状类似卵圆形或四边形,细胞间连接的方式清晰可见,体积较大,细胞核呈圆球形且位于中央或边缘 (图1-a)。10 ℃时细胞为不规则的几何形状,细胞紧密连接方式可见,部分区域的肝细胞空泡化、细胞核位于细胞内一侧并出现固缩现象;肝细胞整体染色变浅 (图1-b)。5 ℃时肝细胞为不规则的几何形状,部分细胞核消失不见或呈现收缩状,细胞结构破碎,空泡化现象加重 (图1-c)。
![]() 图 1 冷应激对黑鲷肝脏、腮、肌肉组织结构的影响 (10×40 倍)注:a. 肝脏,15 ℃ 对照组;b. 肝脏,10 ℃ 处理组;c. 肝脏,5 ℃ 处理组;d. 腮,15 ℃ 对照组;e. 腮,10 ℃ 处理组;f. 腮,5 ℃ 处理组;g. 肌肉,15 ℃ 对照组;h. 肌肉,10 ℃ 处理组;i. 肌肉,5 ℃ 处理组。Figure 1. Effects of cold stress on tissue structure of liver, gill and muscle of A. schlegelii (10×40 times)Note: a. Liver, 15 ℃ control group; b. Liver, 10 ℃ treatment group; c. Liver, 5 ℃ treatment group; d. Gill, 15 ℃ control group; e. Gill, 10 ℃ treatment group; f. Gill, 10 ℃ treatment group; g. Muscle, 15 ℃ control group; h. Muscle, 10 ℃ treatment group; i. Muscle, 5 ℃treatment group.
图 1 冷应激对黑鲷肝脏、腮、肌肉组织结构的影响 (10×40 倍)注:a. 肝脏,15 ℃ 对照组;b. 肝脏,10 ℃ 处理组;c. 肝脏,5 ℃ 处理组;d. 腮,15 ℃ 对照组;e. 腮,10 ℃ 处理组;f. 腮,5 ℃ 处理组;g. 肌肉,15 ℃ 对照组;h. 肌肉,10 ℃ 处理组;i. 肌肉,5 ℃ 处理组。Figure 1. Effects of cold stress on tissue structure of liver, gill and muscle of A. schlegelii (10×40 times)Note: a. Liver, 15 ℃ control group; b. Liver, 10 ℃ treatment group; c. Liver, 5 ℃ treatment group; d. Gill, 15 ℃ control group; e. Gill, 10 ℃ treatment group; f. Gill, 10 ℃ treatment group; g. Muscle, 15 ℃ control group; h. Muscle, 10 ℃ treatment group; i. Muscle, 5 ℃treatment group.2.2 冷应激对黑鲷鳃组织结构的影响
15 ℃对照组中鳃丝的中间血管清晰可见,鳃小片分布在鳃丝两侧 (图1-d)。鳃小片中间分布着微血管即为鳃血窦,线粒体丰富细胞主要分布在鳃小片基部,扁平上皮细胞在鳃小片表面清晰可见。与15 ℃对照组相比,10 ℃处理组的线粒体丰富细胞的数量增多,鳃小片收缩变细,毛细血管出现充血现象 (图1-e)。5 ℃处理组的血窦间隙增大,部分扁平上皮细胞脱落,线粒体丰富细胞减少,鳃小片断裂、萎缩严重,毛细血管充血现象严重 (图1-f)。
2.3 冷应激对黑鲷肌肉组织结构的影响
15 ℃对照组的肌纤维呈长柱型 (图1-g)。与对照组相比,10 ℃处理组的肌纤维间隙增大,肌原纤维之间产生空隙 (图1-h)。5 ℃处理组大部分肌纤维断裂,并出现纵向开裂、肌原纤维散乱现象,部分肌纤维溶解并暴露出细胞核 (图1-i)。
2.4 低温胁迫对黑鲷肝脏中AST、ALT、TG、T-CHO的影响
在不同的低温环境下,黑鲷的AST、ALT、TG、T-CHO随着温度的降低变化趋势各不相同。AST活性在10、5 ℃时均显著升高 (P<0.05),在10 ℃时达到最大值 (P<0.05,图2-a)。ALT活性在10 ℃时无显著变化 (P>0.05),但5 ℃时显著升高 (P<0.05,图2-b)。10、5 ℃组肝脏中TG浓度显著降低 (P<0.05);肝脏中T-CHO浓度在10 ℃时无显著变化 (P>0.05),5 ℃时显著升高 (P<0.05,图2-c、图2-d)。
![]() 图 2 冷应激对黑鲷肝脏组织的谷草转氨酶、谷丙转氨酶、甘油三酯和总胆固醇的影响注:方柱上相同字母表示组间差异不显著 ( P>0.05),不同字母表示组间差异显著 (P<0.05);图3同此。Figure 2. Effects of cold stress on AST, ALT, TG and T-CHO in liver tissue of A. schlegeliiNote: The same letters above the column indicate no significant difference between groups (P>0.05), while different letters indicate significant difference between groups (P<0.05). The same case in Fig. 3.
图 2 冷应激对黑鲷肝脏组织的谷草转氨酶、谷丙转氨酶、甘油三酯和总胆固醇的影响注:方柱上相同字母表示组间差异不显著 ( P>0.05),不同字母表示组间差异显著 (P<0.05);图3同此。Figure 2. Effects of cold stress on AST, ALT, TG and T-CHO in liver tissue of A. schlegeliiNote: The same letters above the column indicate no significant difference between groups (P>0.05), while different letters indicate significant difference between groups (P<0.05). The same case in Fig. 3.2.5 冷应激对黑鲷肝脏组织凋亡相关基因表达的影响
采用实时荧光定量PCR方法测定不同温度下黑鲷肝脏中apaf-1、bax、bcl-2、caspase-1、caspase-3及diablo的mRNA表达量,与对照组相比,apaf-1基因的mRNA相对表达量随着温度的降低呈现出先降低后升高的趋势,10 ℃时最低 (P<0.05),5 ℃时最高 (P<0.05,图3)。bax、caspase-1基因表达量在降温过程中显著降低 (P<0.05)。bcl-2基因表达量在5 ℃时显著升高 (P<0.05)。caspase-3基因表达量在10 ℃时最高 (P<0.05),5 ℃时降至最低 (P<0.05)。diablo基因表达量在10与5 ℃均显著升高 (P<0.05),在10 ℃时达到最大值 (P<0.05)。
3. 讨论
鱼类作为变温动物,水温时刻影响其呼吸与循环系统并与其生理生化指标产生相关性[30]。因此,病理学研究和生理生化指标常被用于评估鱼类在低温环境下的适应能力[31]。
3.1 冷应激对黑鲷组织结构的影响
肝脏是鱼类机体中参与多种物质合成、贮存、代谢、转化和分解的重要器官[32]。本研究结果显示,黑鲷幼鱼的肝脏细胞在低温下发生显著变化,5 ℃处理组出现肝细胞排列无序、细胞核固缩或碎裂、组织空泡化等现象。结合区又君等[33]对低温胁迫下四指马鲅 (Eleutheronema tetradactylum) 的肝脏结构变化分析,推测冷应激下黑鲷为维持机体基本生命活动需大量能量,肝糖原或脂肪被大量氧化分解,肝脏失去自我调节能力,从而造成肝细胞出现空泡化,细胞核萎缩或破碎,最后导致肝脏损伤。
鳃是鱼类的主要呼吸器官,同时也具有排泄代谢废物、调节渗透压等功能[34-35]。对赤鲷 (Pagrus pagrus) 的研究表明腮损伤会随着水温的降低而逐渐加重,并伴随着渗透压调节失衡现象[36]。与对照组相比,5 ℃下黑鲷的鳃小片同样出现了断裂与水肿的趋势,扁平上皮细胞逐渐脱落,损伤程度加深,无法进行正常呼吸。这种现象与青鳉 (Oryzias latipes)、尼罗罗非鱼 (Oreochromis niloticus) 的鳃部组织结构在低温下的变化相似[37-38]。推测当水温低于黑鲷的耐受阈值时,其鳃出现小片充血或断裂、渗透压调节功能失常以及呼吸功能紊乱的现象,从而导致机体缺氧或死亡。
肌肉不仅是鱼类的蛋白源,还是鱼类在水中游动的主要参与者[33]。黑鲷在面对低温时产生应激反应,易受惊且游动迅速,频繁的游动会对肌肉组织造成一定损伤。与对照组相比,10 ℃ 下的肌纤维出现间隙增大、弯曲等现象,表明温度骤降会影响黑鲷的肌肉结构。当水温降至5 ℃ 并胁迫24 h后,肌肉出现肌纤维断裂、溶解、细胞核暴露现象,致使黑鲷无法游动。相关研究表明,低温下细胞膜的流动性会降低且其脂质会发生过氧化损伤,此时剧烈的运动将导致细胞膜破损[39-40]。因此在降温过程中,黑鲷频繁游动可能会导致部分肌细胞的细胞膜遭到破坏甚至露出细胞核。
3.2 冷应激对黑鲷肝脏相关指标的影响
AST和ALT在糖、脂肪和蛋白质三大物质代谢过程中起到重要作用,主要存在于细胞中,在各组织器官中,心脏和肝脏中的活性最高[10-13]。本研究中,黑鲷肝脏的AST活性随着温度的降低先升高后下降;ALT活性在10 ℃时无明显变化,在5 ℃时显著升高。表明当黑鲷在10 ℃处理后肝脏出现了损伤,当温度持续降低至5 ℃并保持24 h后,肝脏损伤加剧,部分肝细胞受损后AST可能被释放进入机体中导致活性降低。这与低温胁迫下条纹锯鮨 (Centropristis striata) 血清中的ALT、AST活性的变化趋势相似[41]。结合10、5 ℃下的黑鲷肝脏组织切片(图1-b、图1-c),表明黑鲷肝脏的损伤程度随温度的降低而加重。
TG和T-CHO是机体内重要的能源物质,它们主要通过肝、肠进行合成和分泌,能够反映合成以及摄取蛋白质的能力[11]。本研究中的10、5 ℃处理组的TG浓度均显著低于对照组,说明作为能源物质的TG在降温实验中被大量消耗。同时,陈旭等[13]发现低温胁迫会导致鱼体的代谢能力下降,各种代谢酶的活性受到抑制,TG的合成减缓。因此,10 ℃处理组黑鲷肝脏的TG浓度与5 ℃处理组相比无显著变化。T-CHO浓度在5 ℃时显著高于对照组和10 ℃处理组,这与温度骤降时吉富罗非鱼 (GIFT O. niloticus) 血清中T-CHO浓度变化趋势相似[42]。推测黑鲷肝脏内T-CHO浓度上升促进了机体内相关生理活性物质的产生,以抵御急性低温胁迫所带来的损伤。
3.3 冷应激对黑鲷肝脏中细胞凋亡相关基因表达的影响
细胞凋亡的形态学表现为细胞内DNA降解,细胞核固缩、碎裂,凋亡小体形成,但细胞膜保持完整,不会引起继发炎性反应[15]。郭晓丽等[43]在研究热应激对大菱鲆 (Scophthalmus maximus) 心脏的影响时发现,其心脏细胞在高温下会发生凋亡并伴随着线粒体空泡化现象,电镜下显示细胞结构遭到破坏。从图1-b、图1-c中可以观察到,冷应激下黑鲷肝脏细胞形态的变化符合细胞凋亡形态学的表现,但电镜下细胞结构变化未知。因此推测黑鲷在10、5 ℃条件下,肝脏会出现细胞凋亡的现象。
荧光定量PCR结果表明,冷应激对黑鲷肝脏中的apaf-1、bax、bcl-2、caspase-1、caspase-3以及diablo基因的表达量均产生显著影响。在对Apaf-1-caspase-9通路进行研究时,Bratton等[21]发现Apaf-1基因可以激活caspase级联反应,产生细胞凋亡现象。因此,冷应激可能会诱导黑鲷肝脏中apaf-1基因表达量发生变化,进而激活细胞凋亡途径。秦华平等[44]通过研究深低温情况下大鼠 (Rattus norvegicus) 脑部的细胞凋亡现象,发现大鼠会抑制Bax基因表达,减少神经细胞Cyto-C释放,阻止细胞凋亡。由此推测黑鲷处于冷应激状态时,会通过调控抗凋亡基因bcl-2与促凋亡基因bax的表达,抑制或促进肝脏细胞Cyto-C的释放,进而影响细胞凋亡。本研究发现,10 ℃下黑鲷肝脏的促凋亡基因diablo、凋亡启动基因caspase-3会同时发挥作用,抑制抗凋亡蛋白并执行细胞凋亡程序,导致线粒体出现损伤[22-23]。当线粒体损伤后,细胞会将超出耐受阈值的氧化应激给予负面的生理反馈[43]。陈自强等[28]发现急性低温胁迫会对黑鲷肝脏抗氧化指标产生显著影响。对线粒体Smac/Diablo-XIAP-Caspase-9/3凋亡途径研究发现,微小RNA-24可能通过抑制此途径,抑制H2O2诱导的HLE-B3细胞凋亡[45]。5 ℃处理组的黑鲷可能通过同样的方式,调控肝脏中促凋亡基因diablo以及凋亡启动caspase-3基因的表达,以此抑制细胞凋亡,维持肝脏细胞的基本功能。而与低温下青鳉 (Oryzias latipes)[37]腮部的细胞凋亡研究结果不同的是,黑鲷肝脏中caspase-1基因在降温过程中始终被抑制。推测黑鲷的肝脏细胞在骤降的低温环境中,抑制了细胞炎症反应,保证凋亡时细胞无炎症发生。
4. 结论
综上所述,冷应激下黑鲷的肝脏、腮以及肌肉的生理结构遭受破坏,随着温度的降低损伤加重;冷应激对黑鲷肝脏中AST、ALT、TG、T-CHO均产生了显著的影响并诱导肝脏细胞产生细胞凋亡现象。当水温低于黑鲷机体的耐受阈值时,肝脏中apaf-1、diablo基因的表达上调激活其凋亡通路,去除坏死细胞;降低bax、caspase-3、caspase-1基因的表达量并促进bcl-2基因的表达,抑制细胞凋亡及炎症反应,尽量保证肝细胞的完整性与数量、维持肝脏的功能和稳态。
-
图 1 冷应激对黑鲷肝脏、腮、肌肉组织结构的影响 (10×40 倍)
注:a. 肝脏,15 ℃ 对照组;b. 肝脏,10 ℃ 处理组;c. 肝脏,5 ℃ 处理组;d. 腮,15 ℃ 对照组;e. 腮,10 ℃ 处理组;f. 腮,5 ℃ 处理组;g. 肌肉,15 ℃ 对照组;h. 肌肉,10 ℃ 处理组;i. 肌肉,5 ℃ 处理组。
Figure 1. Effects of cold stress on tissue structure of liver, gill and muscle of A. schlegelii (10×40 times)
Note: a. Liver, 15 ℃ control group; b. Liver, 10 ℃ treatment group; c. Liver, 5 ℃ treatment group; d. Gill, 15 ℃ control group; e. Gill, 10 ℃ treatment group; f. Gill, 10 ℃ treatment group; g. Muscle, 15 ℃ control group; h. Muscle, 10 ℃ treatment group; i. Muscle, 5 ℃treatment group.
图 2 冷应激对黑鲷肝脏组织的谷草转氨酶、谷丙转氨酶、甘油三酯和总胆固醇的影响
注:方柱上相同字母表示组间差异不显著 ( P>0.05),不同字母表示组间差异显著 (P<0.05);图3同此。
Figure 2. Effects of cold stress on AST, ALT, TG and T-CHO in liver tissue of A. schlegelii
Note: The same letters above the column indicate no significant difference between groups (P>0.05), while different letters indicate significant difference between groups (P<0.05). The same case in Fig. 3.
表 1 引物信息
Table 1 Primer information
引物
Primer引物序列 (5'—3')
Primer sequence (5'–3')产物长度
Length of product/bp退火温度
Annealing temperature/℃β-actin-F CGACGGTCAGGTCATCAC 91 β-actin-R GCCAGCAGACTCCATTCC apaf-1-F AGACTACGAAGCTGCACACGTCCT 135 59 apaf-1-R ATCCCGTCCTGCCATCACGTACC bax-F AAGGCGCTGACCACCAACC 150 58 bax-R GGCTACTGTCCTCCACCGAGA bcl-2-F ACCATCGTCACCTCCGACTCC 115 56 bcl-2-R ACTTTGGGCGAGTTCTTTGTCGT caspase-1-F GAGACAGCCCGATCCACTCCCAC 150 58 caspase-1-R AGCAGAGACCCTTTGACCGAGTGT caspase-3-F ATGGACTACCCCAGCCTCGGAAC 101 57 caspase-3-R GCAGCATCAACATCCGTCCCGTT diablo-F CAATGCTGTCAACCTGTG 146 55 diablo-R TCTTATCTGCGTCTGCTG -
[1] JI L Q, JIANG K Y, LIU M, et al. Low temperature stress on the hematological parameters and HSP gene expression in the turbot Scophthalmus maximus[J]. Chin J Oceanol Limnol, 2016, 34(3): 430-440. doi: 10.1007/s00343-016-4367-z
[2] 刘丽丽, 朱华, 闫艳春, 等. 鱼类低温耐受机制与功能基因研究进展[J]. 生物技术通报, 2018, 34(8): 50-57. [3] BEN S R, TOMMY N, WILLIAM R D. The benefit of being still: energy savings during winter dormancy in fish come from inactivity and the cold, not from metabolic rate depression[J]. Proc Roy Soc B, 2018, 285(1886): 1-10.
[4] 王晓煜, 胡春兰, 程鹏丽, 等. 低温驯化对斑马鱼ZF4细胞凋亡和ROS的影响[J]. 基因组学与应用生物学, 2020, 39(10): 4475-4480. [5] SUNG C H, DO H M, LEE M K, et al. Histopathological observation of liver in cultured black rock fish Sebastes schlegeli in low temperature season[J]. J Fish Pathol, 2011, 24(3): 225-236. doi: 10.7847/jfp.2011.24.3.225
[6] 蔡润佳, 张静, 黄建盛, 等. 低温胁迫对军曹鱼幼鱼脂代谢相关生理生化的影响[J]. 广东海洋大学学报, 2021, 41(3): 123-130. doi: 10.3969/j.issn.1673-9159.2021.03.016 [7] 邵彦翔, 陈超, 李炎璐, 等. 低温胁迫对云纹石斑鱼(♀)×鞍带石斑鱼(♂)杂交后代血清生化指标的影响[J]. 渔业科学进展, 2017, 38(2): 70-76. doi: 10.11758/yykxjz.20160103001 [8] 施兆鸿, 谢明媚, 彭士明, 等. 温度胁迫对银鲳 (Pampus argenteus) 幼鱼消化酶活性及血清生化指标的影响[J]. 渔业科学进展, 2016, 37(5): 30-37. [9] 管敏, 张厚本, 王龙, 等. 急性低温胁迫对史氏鲟幼鱼抗氧化和免疫指标的影响[J]. 淡水渔业, 2018, 48(6): 17-22. doi: 10.3969/j.issn.1000-6907.2018.06.003 [10] 谭连杰, 林黑着, 黄忠, 等. 当归多糖对卵形鲳鲹生长性能、抗氧化能力、血清免疫和血清生化指标的影响[J]. 南方水产科学, 2018, 14(4): 72-79. doi: 10.3969/j.issn.2095-0780.2018.04.009 [11] 李向. 小肽和维生素D3对大口黑鲈 (Micropterus salmoides) 生长、肝脏代谢和肠道微生物的影响[D]. 上海: 上海海洋大学, 2020: 21-34. [12] 李丹丹, 陈丕茂, 朱爱意, 等. 黑鲷幼鱼力竭运动后代谢酶活性的恢复水平[J]. 南方水产科学, 2018, 14(6): 59-65. doi: 10.12131/20180064 [13] 陈旭, 王一福, 周胜杰, 等. 低温胁迫下甘草对尖吻鲈幼鱼血清和肝脏免疫酶及鳃Na+-K+-ATP酶活性的影响[J]. 中国渔业质量与标准, 2020, 10(5): 18-24. doi: 10.3969/j.issn.2095-1833.2020.05.004 [14] 陈智. 低温胁迫对荷那龙罗非鱼血液生理生化指标的影响[D]. 湛江: 广东海洋大学, 2011: 10-32. [15] 郭双, 邢栋, 吕勃. 细胞凋亡及细胞程序性坏死和细胞焦亡的研究进展[J]. 中华实用诊断与治疗杂志, 2021, 35(3): 321-324. [16] ZHANG Y Y, CHEN X, CYRIL G, et al. Plasma membrane changes during programmed cell deaths[J]. Cell Res, 2018, 28(1): 9-21. doi: 10.1038/cr.2017.133
[17] 杨静, 许明君, 王钇力, 等. 千金藤碱通过MAPK/ERK信号通路对鼻咽癌大鼠的防治作用及对Survivin、XIAP、Bcl-2表达的影响[J]. 西安交通大学学报(医学版), 2021, 42(4): 633-638. [18] JORDAN L M, GERMAIN G, JULIEN P, et al. Bcl-2 family of proteins in the control of mitochondrial calcium signalling: an old chap with new roles[J]. Int J Mol Sci, 2021, 22(7): 3730. doi: 10.3390/ijms22073730
[19] 张彐宁, 高维娟, 周晓红, 等. 沉默Apaf-1基因对氧糖剥夺/复氧复糖PC12细胞线粒体凋亡通路的影响[J]. 中国免疫学杂志, 2021, 37(1): 21-25, 30. doi: 10.3969/j.issn.1000-484X.2021.01.003 [20] 胡善明, 王亚楠, 许正茂, 等. Bcl-2家族分子在细胞凋亡中的作用研究进展[J]. 动物医学进展, 2021, 42(10): 85-89. doi: 10.3969/j.issn.1007-5038.2021.10.016 [21] BRATTON S B, SALVESEN G S. Regulation of the Apaf-1-caspase-9 apoptosome[J]. J Cell Sci, 2010, 123(19): 3209-3214. doi: 10.1242/jcs.073643
[22] 王建卫. XIA P、Apaf-1和Caspase-3在膀胱尿路上皮癌中的表达及临床意义[D]. 石家庄: 河北医科大学, 2019: 32-35. [23] ADRAIN C, CREAGH E M, MARTIN S J. Apoptosis-associated release of Smac/DIABLO from mitochondria requires active caspases and is blocked by Bcl-2[J]. EMBO J, 2001, 20(23): 6627-6636. doi: 10.1093/emboj/20.23.6627
[24] LIN Z J, ZHANG Z Y, SOLBERG M F, et al. Comparative transcriptome analysis of mixed tissues of black porgy (Acanthopagrus schlegelii) with differing growth rates[J]. Aquac Res, 2021, 52(11): 5800-5813. doi: 10.1111/are.15455
[25] 王裕玉, 徐跑, 张志伟, 等. 不同养殖模式对黑鲷生长、血清生化指标及抗氧化性能的影响[J]. 江苏农业科学, 2020, 48(23): 155-160. [26] 李涛, 吕国敏, 黄小林, 等. 温度和盐度骤变对黑鲷仔鱼存活率的影响[J]. 江苏农业科学, 2014, 42(4): 181-182. doi: 10.3969/j.issn.1002-1302.2014.04.069 [27] 陈得仿, 王腾, 刘永, 等. 大亚湾黑鲷繁殖特征的生物学研究[J]. 南方水产科学, 2019, 15(5): 41-47. doi: 10.12131/20190051 [28] 陈自强, 张志勇, 祝斐, 等. 急性低温对黑鲷抗氧化酶活性和热休克蛋白含量的影响[J]. 动物学杂志, 2020, 55(6): 784-792. [29] ZHANG Z Y, ZHANG K, CHEN S Y, et al. A draft genome of the Chinese black porgy, Acanthopagrus schlegelii[J]. GigaScience, 2018, 7(4): 1-7.
[30] 张先炳, 胡亚萍, 杨威, 等. 水温对淡水温水性鱼类生命活动的影响[J]. 水生态学杂志, 2021, 42(4): 117-122. [31] 龙勇, 葛国栋, 李西西, 等. 鱼类低温应激反应的调控机制[J]. 水生生物学报, 2021, 45(6): 1405-1414. [32] 陆健, 张佳佳, 周国勤, 等. 急性高温胁迫对大口黑鲈“优鲈3号”肝脏凋亡相关酶活性和基因表达的影响[J]. 淡水渔业, 2021, 51(2): 81-86. doi: 10.3969/j.issn.1000-6907.2021.02.010 [33] 区又君, 刘奇奇, 温久福, 等. 急性低温胁迫对四指马鲅幼鱼肝脏、肌肉以及鳃组织结构的影响[J]. 生态科学, 2018, 37(5): 53-59. [34] 余焱方, 刘鉴毅, 冯广朋, 等. 盐度骤变对金钱鱼幼鱼鳃线粒体丰富细胞形态结构的影响[J]. 南方水产科学, 2021, 17(2): 60-69. doi: 10.12131/20200214 [35] 丁炜东, 曹丽萍, 曹哲明, 等. 氨氮胁迫对翘嘴鳜幼鱼鳃、消化道酶活力的影响[J]. 南方水产科学, 2020, 16(3): 31-37. doi: 10.12131/20190188 [36] OSTROWSKI A D, WATANABE W O, MONTGOMERY F P, et al. Effects of salinity and temperature on the growth, survival, whole body osmolality, and expression of Na+/K+ ATPase mRNA in red porgy (Pagrus pagrus) larvae[J]. Aquaculture, 2011, 314(1): 193-201.
[37] 胡玲红, 王映, 王化敏, 等. 不同温度胁迫对青鳉鳃凋亡的影响[J]. 大连海洋大学学报, 2021, 36(6): 929-936. [38] 宾石玉, 林勇, 曾兰, 等. 低温胁迫对埃及尼罗罗非鱼肝、脾和鳃细胞形态的影响[J]. 广西师范大学学报(自然科学版), 2015, 33(3): 123-128. [39] 张琦, 杨昭杰, 赵汝丽, 等. 多不饱和脂肪酸与深黄被孢霉低温适应性的关系(英文)[J]. 昆明理工大学学报(自然科学版), 2015, 40(1): 67-73. [40] MOURENTE G, DIAZ-SALVAGO E, BELL J G, et al. Increased activities of hepatic antioxidant defence enzymes in juvenile gilthead sea bream (Sparus aurata L. ) fed dietary oxidised oil: attenuation by dietary vitamin E[J]. Aquaculture, 2002, 214(1/2/3/4): 343-361.
[41] 油九菊, 李伟业, 殷小龙, 等. 急性低温胁迫对条纹锯鮨血清生化指标的影响[J]. 安徽农业科学, 2019, 47(8): 109-113. doi: 10.3969/j.issn.0517-6611.2019.08.028 [42] 刘波, 王美垚, 谢骏, 等. 低温应激对吉富罗非鱼血清生化指标及肝脏HSP70基因表达的影响[J]. 生态学报, 2011, 31(17): 4866-4873. [43] 郭晓丽, 黄智慧, 马爱军, 等. 热应激对大菱鲆心肌损伤及细胞凋亡的影响[J]. 水产学报, 2022, 46(6): 1074-1084. [44] 秦华平, 杨常春, 王强, 等. 深低温对全脑缺血大鼠海马Bax表达的影响及其与细胞凋亡的关系[J]. 中华神经医学杂志, 2017, 16(12): 1286-1289. doi: 10.3760/cma.j.issn.1671-8925.2017.12.019 [45] 闫利霞, 黄晓, 张鑫, 等. miR-24对过氧化氢诱导的HLE-B3细胞凋亡的影响及其与线粒体Smac/Diablo-XIAP-caspase-9/3凋亡途径的关系[J]. 眼科新进展, 2021, 41(5): 417-421. -
期刊类型引用(0)
其他类型引用(3)



 下载:
下载:
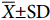


 粤公网安备 44010502001741号
粤公网安备 44010502001741号
