Feasibility of flow cytometry experiments based on fin
-
摘要:
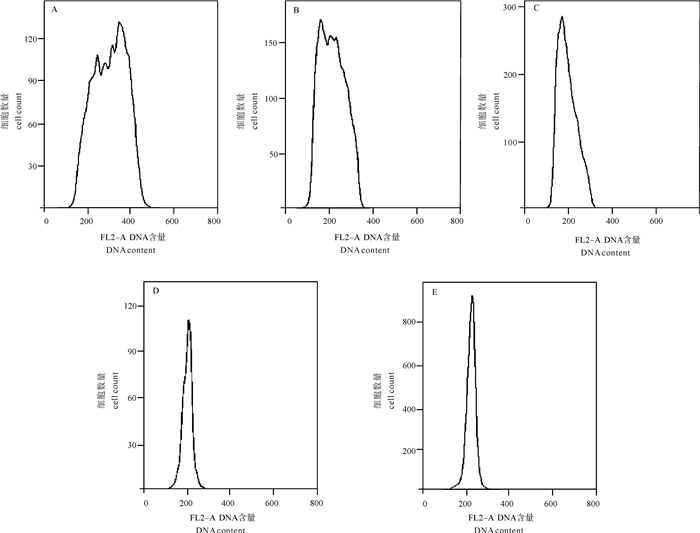
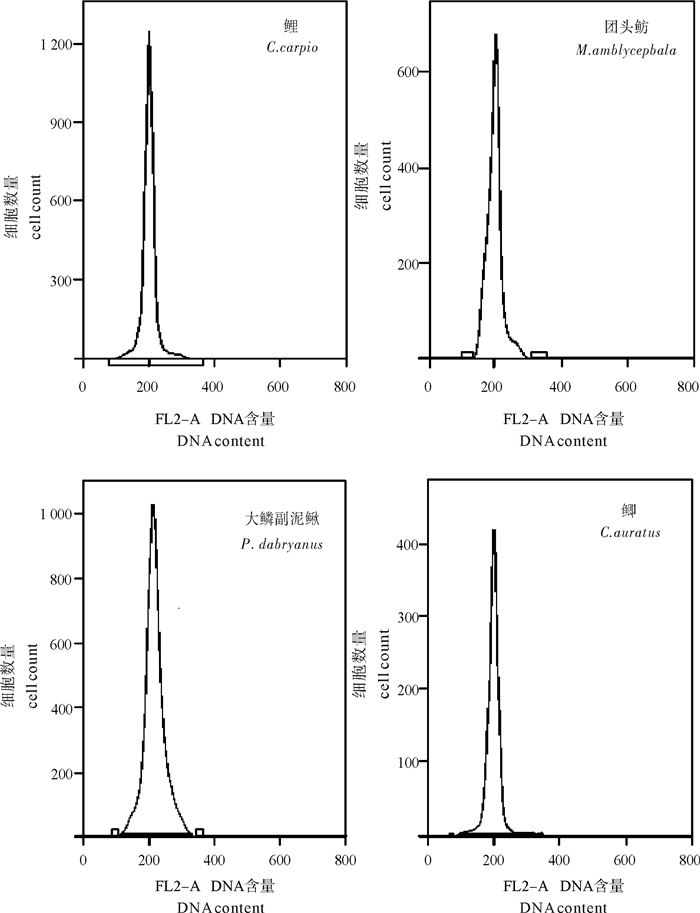
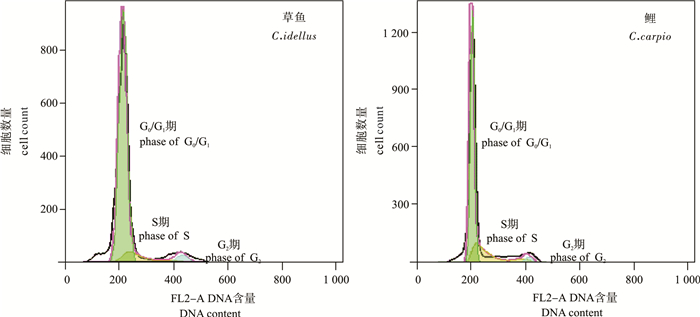
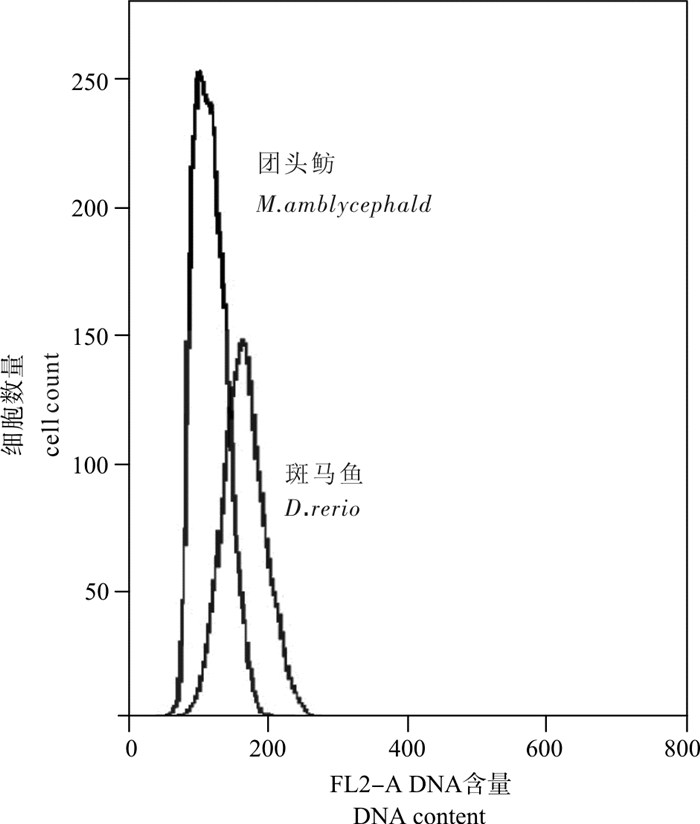
流式细胞术能快速检测生物细胞的DNA含量和细胞周期,在鱼类遗传育种方面已得到广泛运用。目前的研究多基于鱼类血液和生殖细胞开展实验,存在周期性和操作难度的限制。该研究利用草鱼(Ctenopharyngodon idellus)不同组织进行流式分析,在鳍条组织中得到了明显的峰图,并在4种鱼类的重复实验中得到了稳定结果,且不同鱼类的鳍条组织均存在细胞周期,大部分细胞停留在G0/G1期。利用斑马鱼(Danio rerio)作为内标测定出团头鲂(Megalobrama amblycephala)鳍条组织的相对DNA含量(C值)为(1.25 ±0.07)pg,与相关研究结果基本吻合,认为利用鳍条组织作为血液和生殖细胞的替代材料进行流式细胞实验是科学可行的。
Abstract:Flow cytometry, which is widely used in fish breeding, can detect cell cycle and DNA content of living organisms rapidly. However, the current studies mainly focus on experiments based on fish blood and germ cells, which have limitation in periodicity and operation. We used different tissues of Ctenopharyngodon idellus by flow cytometry to obtain a desired and stable histogram showing DNA content of the fin tissues from four different fishes. All fin tissues exhibited cell cycle phenomenon, and low ratio appeared at time phase of G0/G1. Besides, Danio rerio was used as internal calibration to detect the DNA content (C value) of Megalobrama amblycephala (1.25±0.07) pg, and the result has no significant difference with the results of other studies. Therefore, it is concluded that use of fin as alternative for blood and germ cells for flow cytometry research is scientific and feasible.
-
Keywords:
- flow cytometry /
- fin /
- DNA content /
- cell cycle
-
多氯联苯 (Polychlorinated biphenyls, PCBs) 具有优良的阻燃性、热稳定性、惰性和介电能力,曾被广泛用于工业生产中[1],但其对生物具有致癌、致畸、致突变等毒害作用[2],故被《斯德哥尔摩公约》列为首批禁止的持久性有机污染物之一。目前各国政府已颁布禁令,严禁PCBs的生产及使用,1979年PCBs被美国环境保护署 (EPA) 列入优先检测物黑名单,全美禁用[3];我国也于20世纪80年代起全面禁用PCBs。由于PCBs具有难降解性及可长距离迁移等特点,因此尽管已被禁用多年,仍广泛存在于自然环境中[4-6]。而残留在环境中的PCBs,因其具有亲脂性可在生物体内积累并在食物链中传递产生生物放大效应,代谢产物在水生生物体内会产生与内分泌相关的毒性作用,继而导致水产品质量安全问题,至今仍备受国际社会的高度关注。
牡蛎是广东省的特色水产品,2018年广东牡蛎产量位居全国第二[7],是广东省乃至全国海洋经济重要产业和高值海产品,远销国内外。但广东省沿海地区加工业、电子电器制造业等发达,而这些正是环境中PCBs的主要来源,近年来广东沿岸海域环境介质中常有PCBs检出[8-10]的报道,而牡蛎固着性的生活方式使其对环境中的污染物具有更强的吸收和累积能力[11],可通过食物链传递从而威胁到其他水生生物和人体健康,因此广东省养殖牡蛎质量安全可能存在着风险隐患。膳食摄入是人体暴露于环境污染物的最重要途径,有研究表明人体暴露的PCBs 97%来源于食物摄入[12]。2011年香港食物安全中心也指出鱼类等海产品是市民从膳食摄入二噁英和类二噁英多氯联苯的主要来源[13]。而牡蛎等双壳类动物可较准确地反映背景水体污染物质的含量,也被广泛应用于海洋环境中痕量污染物的监测。因此为维护中国养殖牡蛎的质量安全,开展广东省养殖牡蛎中PCBs含量的摸底调查尤为重要。
目前鲜有广东省牡蛎中PCBs残留和人体健康风险的报道,甘居利等[14-15]、Gan等[16]和王清云等[17]曾分别报道了2003—2007年及2008—2012年广东沿海牡蛎中的PCBs残留水平,指出广东沿海牡蛎体内普遍存在PCBs的污染,但由于环境污染监测具有时效性,且上述报道重点是针对生态环境状况评价,非养殖区牡蛎的质量安全风险评估,可能存在采样点设置针对性不强的问题,因此无法全面评估当前广东沿海牡蛎中PCBs残留的风险隐患。基于此,本研究于2016—2017年对广东省主要养殖区牡蛎体内的PCBs含量进行了全面摸查,分析了广东省养殖牡蛎中PCBs的残留水平、分布特征及组成模式,并对其食用安全性进行评估,旨在为我国养殖牡蛎质量安全评估与管理提供重要参考依据。
1. 材料与方法
1.1 样品的采集与预处理
2016年8月至2017年5月于广东汕头、汕尾、深圳、珠海、江门、阳江及湛江的牡蛎养殖重要产区 (图1)不同的牡蛎养殖场,共采集牡蛎样品208份,每份生物个体数量30个。样品现场开壳取其软体组织部分,装入密封袋后置于冷冻冰箱内运回实验室,经匀浆处理冷冻干燥后于−18 ℃保存至分析。
1.2 仪器与试剂
气相色谱质谱联用仪 (7890A-5975C,配电子电离源,美国Agilent公司);凝胶渗透色谱仪器 (美国普立泰科公司);加速溶剂萃取仪 (美国戴安公司);冷冻干燥仪 (北京博医康实验仪器有限公司);旋转蒸发仪 (日本Eyela公司);正已烷、环已烷、乙酸乙酯、二氯甲烷、异丙醇 (色谱纯,美国Honeywell公司);浓硫酸 (分析纯,广州市化学试剂厂);CNW Si硅胶柱 (德国Technologies GmbH公司);弗罗里硅土 (美国Sigma-Aldrich公司)。
30种多氯联苯标准品有PCB1、PCB8、PCB18、PCB28、PCB44、PCB52、PCB66、PCB77、PCB81、PCB87、PCB101、PCB105、PCB114、PCB118、PCB123、PCB126、PCB128、PCB138、PCB153、PCB156、PCB157、PCB167、PCB169、PCB170、PCB180、PCB187、PCB189、PCB195、PCB206,上述标准品均购自美国AccuStandars公司;PCB209购自美国O2SI公司。
多氯联苯定量内标为13C LABELED PCB MIXTURE PCBS-77/101/141/178标准品,购自美国AccuStandars公司。
多氯联苯回收内标为PCB 202-13C12标准品,购自美国AccuStandars公司。
1.3 样品前处理
使用分析天平称取牡蛎软组织干样4 g,加入适量硅藻土和定量内标充分混匀,用100 mL的正己烷和二氯甲院 (1∶1) 加速溶剂萃取。将提取液旋转蒸发至干,再用正己烷进行复溶,加入佛罗里硅土除脂,将除脂后的上层清液旋干,用环己烷和乙酸乙酯 (1∶1) 复溶,浓缩转移至GPC进一步净化、旋干,用正己烷复溶,加入硫酸除脂至上清液无色,取上清液过硅胶柱,收集液加入回收内标后,氮气吹干,加入100 μL异丙醇定容,待上机测定。
1.4 仪器条件
色谱柱为HP-5MS毛细管柱 (30 m×0.25 mm×0.25 μm);载气为高纯氮气;进样口和检测器温度分别为280 和300 ℃。升温程序为初始柱温60 ℃保持2 min,再以10 ℃·min−1升至180 ℃保持4 min,以5 ℃·min−1升至190 ℃保持8 min,以10 ℃·min−1升至200 ℃保持10 min,以3 ℃·min−1升至250 ℃保持10 min,以30 ℃·min−1升至280 ℃保持10 min。样品进样量均为1 μL,无分流进样。
1.5 质量控制与保证措施
质量控制和保证措施包括方法空白、加标空白、基质加标、平行样等测定。每10个样品分析一个程序空白,所有程序空白中未检测出目标化合物,表明分析过程中未引入人为的有机污染。在分析前所有样品添加回收率指示物,并以3倍信噪比作为方法的检出限。在所有样品中,PCBs方法检出限为0.10~0.13 ng·g−1 (干质量),回收率介于78.5%~115.8%,相对标准偏差 (RSD) 介于0.32%~12.8%。
1.6 评价方法
每日摄入量 (Estimated daily intake, EDI) 常被用来评估居民通过饮食摄入对污染物的暴露风险,其计算公式为:
$${\rm{EDI}} = C \times M$$ 式中EDI是每日摄入量 (ng·g−1),C为牡蛎中PCBs的平均质量分数 (ng·g−1,湿质量),M为广州居民对贝类的日摄入量 (g·d−1),参考已发表文献[18]中的调研值。
危险指数 (Hazard quotient, HQ) 被用来评估人体通过饮食对污染物的暴露非致癌风险,具体计算方法为:
$${\rm{HQ}} = \frac{{{\rm{EDI}}}}{{{\rm{BW}} \times {\rm{RfD}}}}$$ 式中EDI是每日摄入量 (ng·g−1),BW是体质量 (kg),不同年龄段的体质量数据采用王宗爽等[19]总结的我国居民体质量数据。RfD是化合物的每日摄入参考剂量[Reference dose, ng·(kg·d)−1],参照世界卫生组织和美国环保局 (United States Environmental Protection Agency, EPA) 推荐的PCBs每日耐受剂量20 ng·(kg·d)−1。HQ>1表明膳食暴露存在潜在的非致癌健康风险。
致癌风险 (Carcinogen risk, CR) 是指个体长期暴露潜在致癌物质中而增加患癌的概率,其计算公式为:
$${\rm{CR}} = \frac{{{\rm{EDI}} \times {\rm{CSF}}}}{{{\rm{BW}}}}$$ 式中EDI为每日摄入量 (ng·g−1),CSF为致癌斜率因子,取1.56 mg·(kg·d)−1,BW为体质量 (kg),不同年龄段的体质量数据采用王宗爽等[19]总结的我国居民体质量数据。
牡蛎样品中PCBs质量分数以湿质量表示(ng·g−1,湿质量) ,显著性水平以P<0.05表示。
2. 结果与分析
2.1 广东养殖牡蛎中PCBs的残留水平
经调查广东省沿海养殖牡蛎体内普遍存在PCBs残留,PCBs检出率为97.6% (表1),在所有牡蛎样品中,PCBs的质量分数范围在nd~8.62 ng·g−1 (湿质量,下同),平均值为 (0.57±1.23) ng·g−1,中值为0.28 ng·g−1,远低于我国《食品安全国家标准 食品中污染物限量》 (GB 2762-2017) 中双壳类软体动物PCBs限量要求 (≤0.5 mg·kg−1) 和我国农业行业标准《无公害食品 水产品中有毒有害物质限量》 (NY 5073-2006) 中海产品PCBs残留量 (≤2.0 mg·kg−1),同时低于《欧盟食品污染物限量标准》 (EC No 1881/2006) 中水产品PCBs最大限量12 ng·g−1,表明广东养殖牡蛎受PCBs污染程度较低,符合中国和欧盟国家贝类卫生标准,能满足食品安全要求。
表 1 广东沿海养殖牡蛎多氯联苯的残留水平及检出率Table 1. Concentration and occurrence rates of PCBs in farmed oysters along Guangdong coast采样点
Sampling site多氯联苯
w (PCBs)/(ng·g−1, wet mass)检出率
Detection rate/%范围
Range平均值
Mean汕头 Shantou 0.16~0.67 0.34 100 汕尾 Shanwei nd~0.87 0.21 90.6 深圳 Shenzhen nd~8.62 3.90 100 珠海 Zhuhai 0.06~1.60 0.63 100 江门 Jiangmen nd~1.00 0.30 95.8 阳江 Yangjiang 0.12~0.82 0.33 100 湛江 Zhanjiang nd~0.80 0.22 97.1 注:nd. 未检出;后表同此 Note: nd. Undetected; the same case in the following table. 与国内外其他海域中贝类相比 (表2),广东省养殖牡蛎中PCBs含量低于青岛、舟山渔场、海口、厦门、尼加拉瓜海岸、加利西亚海岸、萨克森瓦登海岸、孟加拉国沿海、巴塔哥尼亚沿海,与山东沿海双壳贝类中PCBs含量相当,略高于宁波、地中海海岸等区域。可见广东省养殖牡蛎的PCBs含量处于中低水平。本研究所得结论与苏杨等[20]一致,后者研究发现南海海域香港周边海域野生鱼体中PCBs质量分数 (0.028~6.3 ng·g−1,湿质量) 处于中低水平。
表 2 国内外不同地区双壳贝类多氯联苯质量分数比较Table 2. Comparison of PCBs concentration in oysters from different sampling sites in the world采样地点
Sampling site采样时间
Sampling time多氯联苯
w(PCBs)/(ng·g−1)文献
Reference广东沿海 (中国) Guangdong coast (China) 2016—2017 nd~36.07a, nd~8.62b, nd~319.26c, 0.57±1.23b 本研究 舟山渔场 (中国) Zhoushan fishery areas (China) 2010 18.0~95.9a [24] 宁波 (中国) Ningbo (China) 2009 nd~0.32b [25] 青岛 (中国) Qingdao (China) 2018 nd~168.66a [26] 海口 (中国) Haikou (China) 2017 17.51~47.43a [27] 厦门 (中国) Xiamen (China) 2014 3.4±4.3b [28] 山东沿海 (中国) Shandong coast (China) 2017 nd~36.8b [29] 萨克森瓦登海岸 (德国) Sachsenwadden coast (Germany) 2007 475.75~937.39c [30] 尼加拉瓜海岸 (尼加拉瓜) Nicaraguan coast (Nicaraguan) 2012—2013 230a [31] 孟加拉国沿海 (孟加拉) Bangladesh coast (Bangladesh) 2015 3.8~37.7b [32] 加利西亚海岸 (西班牙) Galicia coast (Spain) 2011—2014 5.58~179.49a [33] 地中海海岸 (西班牙) Mediterranean coast (Spain) 2000—2013 0.1~5.8a [34] 巴塔哥尼亚 (阿根廷) Patagonia (Argentina) 2010 48~61a [35] 注:a. 以组织干质量计;b. 以组织湿质量计;c. 以组织脂质量计 Note: a, b and c indicate PCBs concentrations calculated based on dry tissue mass, wet tissue mass and lipid tissue mass, respectively. 与历史数据相比,本研究结果远低于2003—2007年广东近江牡蛎PCBs质量分数 (30~2 040 ng·g−1,干质量)[16],低于2008—2012年的调查结果 (8.11~29.10 ng·g−1,湿质量)[17],接近于1989—1991年的调查结果 (0.35~1.43 ng·g−1,干质量) [16],表明广东省沿海牡蛎PCBs含量自20世纪90年代升高后一直呈下降趋势。这可能与广东省工业发展的历史及当地政府的政策导向有关。PCB是典型的工业污染物,广东省非老工业区,因此90年代初广东省牡蛎体内PCBs含量较低。20世纪90年代改革开放后,广东省城市建设和经济快速发展,电子科技、电器制造、五金电镀等企业的工业废水及生活污水的大量排放,致使其毗邻海域环境受到严重破坏,导致20世纪初广东省牡蛎体内PCBs含量剧增。但2004年后广东省政府相继颁布《广东省环境保护条例》 《广东省固体废物污染环境防治条例》 《实施十项民心工程推进城市污水和垃圾处理工作方案》等条例加强环境污染治理,同时开展重点污染源的排查工作,查封了一系列违规排废的电镀、印染、造纸、线路板等企业,故自2000年后牡蛎中PCBs含量呈下降趋势,处于较低水平。而近年来的文献报道也显示广东海域环境及海洋生物体内PCBs含量呈较低水平[8-10]。这一分析也可以从广东省牡蛎体内重金属污染的变化趋势得到佐证,即牡蛎体内重金属水平也呈现类似变化规律[21-23],20世纪90年代牡蛎体内重金属含量较高,而到2000年后回落至较低水平。
2.2 广东养殖牡蛎PCBs的空间分布
广东沿海不同区域养殖牡蛎的PCBs质量分数分布见表1,其中以深圳最高(3.90 ng·g−1),其次为珠海 (0.63 ng·g−1),而汕头 (0.34 ng·g−1)、阳江 (0.33 ng·g−1)、江门 (0.30 ng·g−1)、湛江 (0.22 ng·g−1) 和汕尾 (0.21 ng·g−1) 较低。单因素方差分析发现不同海区的养殖牡蛎PCBs含量分布呈显著差异,表明PCBs污染具有明显的地域差异。Tanabe等[36]指出PCBs的区域分布情况与当地工业化发展水平紧密相关,珠江三角洲人口密集,是全球电子工业品的最大出口基地之一,也是我国四大工业基地之一;深圳牡蛎养殖区主要位于珠江口小铲岛附近,因此深圳养殖区受珠江河流污染及城市生活污水和工业排放废水的影响较大。珠海牡蛎养殖区主要分布于高栏岛附近海域,地处珠江口外海区域,受珠江河流污染的影响小于深圳,因此珠海牡蛎体内的PCBs残留量比深圳低。汕头牡蛎养殖区分布在榕江、濠江以及沿海区域,而汕头市贵屿镇曾是世界著名的电子垃圾处理地,电子垃圾不恰当处理会使大量的持久性有机污染物 (如PCBs等) 进入环境,因此汕头周边的养殖牡蛎仍有一定量的PCBs生物累积。相比较而言,江门、湛江、阳江和汕尾等地的养殖牡蛎受区域环境污染影响相对较小,故其体内PCBs含量也较低,与养殖海域环境污染状况相一致。
2.3 广东沿海养殖牡蛎PCBs组成特征
本研究测定了广东养殖牡蛎体内含1~10个氯原子的30种PCBs同系物,得出牡蛎中PCBs同系物指纹图谱 (图2)。结果显示,不同地区牡蛎中PCBs组成特征类似,均以五氯、六氯代PCBs为主,其次是四氯、七氯代PCBs,三氯代PCBs比例最低,其余氯代PCBs未检出 (图3)。广东省牡蛎养殖区相似的同分异构体组成在一定程度上反映了目前广东海域PCBs污染的同源性。而上述PCBs的组成模式:1) 可能与我国历史上PCBs的生产、使用及其环境残留有关,中国历史上生产的PCBs:中国1号 (1#PCBs) 和中国2号 (2#PCBs),分别以三氯联苯和五氯联苯为主的同系物组成[37],而低氯代PCBs具有更强的降解性和挥发性,弱降解性的高氯代PCBs在环境中滞留时间更长,因此海洋环境中PCBs以5或6个氯原子同系物的比率较高[38]。2) 也可能与牡蛎对不同氯代PCBs的生物富集能力及其在体内的代谢速率有关,有关资料显示PCBs在水生生物体内富集程度与其氯原子个数呈抛物线关系,即中等氯原子取代的同系物在生物体内的富集因子高于低氯、高氯原子取代的PCBs同系物[39],因此中氯代PCBs在广东省养殖牡蛎体内的富集量高于低氯代和高氯代的PCBs,类似的PCBs组成特征在珠江口海域的翡翠贻贝 (Perna virdis)[40]、鱼类[41]和广东大鹏湾海域糙齿海豚 (Steno bredanensis)[42]等生物体内也得到了证实,即均以中氯代的PCBs为主。
2.4 广东养殖牡蛎PCBs的风险隐患评估
膳食摄入是人体暴露于环境污染物的重要途径之一,本研究用日摄入量评估人体通过摄食牡蛎对PCBs的饮食暴露风险 (表3),得出人体对牡蛎中残留PCBs的日摄入量为1.57~154.57 ng·d−1,其中不同人群对PCBs的日摄入量的大小顺序为青少年 (6~18岁) >成人 (>18岁) >儿童 (2~5岁),男性>女性,显示出不同年龄、性别对牡蛎中PCBs的日摄入量存在差异。
表 3 广东养殖牡蛎多氯联苯的人体健康风险评价Table 3. Human health risk assessment for PCBs in farmed oysters along Guangdong coast采样点
Sampling site评价参数
Evaluation parameter儿童 (2~5岁)
Child (2−5 years)青少年 (6~18岁)
Teenager (6−18 years)成人 (>18岁)
Adult (>18 years)男
Boy女
Girl男
Boy女
Girl男
Male女
Female汕头 Shantou 日摄入量 EDI/(ng·d−1) 4.22 2.54 13.58 8.40 8.40 7.96 致癌风险 CR 1.3×10−9 8.5×10−10 6.8×10−10 4.7×10−10 1.7×10−10 2.1×10−10 危害商数 HQ 0.01 0.01 0.02 0.01 0.01 0.01 汕尾 Shanwei 日摄入量 EDI/(ng·d−1) 2.61 1.57 8.39 5.19 5.19 4.92 致癌风险 CR 7.9×10−10 5.2×10−10 4.2×10−10 2.9×10−10 1.1×10−10 1.3×10−10 危害商数 HQ 0.01 0.01 0.01 0.01 0.00 0.00 深圳 Shenzhen 日摄入量 EDI/(ng·d−1) 48.01 28.88 154.57 95.63 95.63 90.56 致癌风险 CR 1.5×10−8 9.6×10−9 7.7×10−9 5.3×10−9 1.9×10−9 2.4×10−9 危害商数 HQ 0.15 0.09 0.20 0.13 0.08 0.08 珠海 Zhuhai 日摄入量 EDI/(ng·d−1) 7.69 4.63 24.77 15.33 15.33 14.51 致癌风险 CR 2.3×10−9 1.5×10−9 1.2×10−9 8.5×10−10 3.1×10−10 3.9×10−10 危害商数 HQ 0.02 0.02 0.03 0.02 0.01 0.01 江门 Jiangmen 日摄入量 EDI/(ng·d−1) 3.68 2.22 11.86 7.34 7.34 6.95 致癌风险 CR 1.1×10−9 7.4×10−10 5.9×10−10 4.1×10−10 1.5×10−10 1.9×10−10 危害商数 HQ 0.01 0.01 0.02 0.01 0.01 0.01 阳江 Yangjiang 日摄入量 EDI/(ng·d−1) 4.08 2.45 13.14 8.13 8.13 7.70 致癌风险 CR 1.2×10−9 8.2×10−10 6.6×10−10 4.5×10−10 1.6×10−10 2.1×10−10 危害商数 HQ 0.01 0.01 0.02 0.01 0.01 0.01 湛江 Zhanjiang 日摄入量 EDI/(ng·d−1) 2.65 1.60 8.54 5.28 5.28 5.00 致癌风险 CR 8.1×10−10 5.3×10−10 4.3×10−10 2.9×10−10 1.1×10−10 1.4×10−10 危害商数 HQ 0.01 0.01 0.01 0.01 0.00 0.00 为进一步评价上述PCBs暴露水平对人体健康的潜在影响,本研究对癌症及非癌症效应采用量化风险分析法进行了评估。类二噁英多氯联苯 (dl-PCBs) 具有二噁英相似的毒性性质,其毒性比非类二噁英多氯联苯更强。本研究在广东养殖牡蛎体内仅检出2种类二噁英多氯联苯,分别为PCB105和PCB118,两者占总PCBs的6.3%,表明广东省养殖牡蛎受dl-PCBs的影响较小。根据《食品中二噁英及其类似物毒性当量的测定》 (GB 5009.205-2013)公布的PCBs毒性当量因子 (TEFs),计算广东省养殖牡蛎的毒性当量 (TEQ),得出通过摄食广东养殖牡蛎对dl-PCBs的日暴露量为0~5.56×10−3 pg·(kg·d)−1,远低于世界卫生组织 (WHO) 发布的dl-PCBs每日可耐受摄入量[1~4 pg·(kg·d)−1],以及美国疾病预防控制中心的有毒物质与疾病登记处 (ATSDR) 制定的PCBs日均允许摄入量[20 ng·(kg·d)−1][43]。中国居民通过食用养殖牡蛎而导致癌症和非癌症疾病的风险评估结果见表3,研究发现广东省养殖牡蛎的CR值均低于10−6,表明人体食用广东养殖牡蛎而暴露dl-PCBs致癌物质产生的致癌几率<10−6,可见对人类健康产生的负面影响极小。本次调查的广东沿海养殖牡蛎的HQ均小于1,说明人体发生非癌症疾病的可能性较小。表明消费者在正常食用水平下仅通过食用广东海域养殖的牡蛎摄入PCBs的量较低,不会对人体带来潜在危害。
3. 结论
通过对广东省养殖牡蛎中PCBs含量测定及其对消费者健康的风险评价,得出以下结论:
1) PCBs在广东沿岸海区养殖的牡蛎体内普遍存在,其中深圳的含量最高,其次为珠海,而汕头、阳江、江门、湛江和汕尾的较低,牡蛎中PCBs含量分布差异主要受到区域环境污染的影响。牡蛎中PCBs的组成模式以五氯代和六氯代的PCBs为主,广东省牡蛎的PCBs残留水平低于中国和欧盟国家的贝类卫生标准,不影响消费者的食用安全。
2) 儿童、成人、老年人通过广东养殖牡蛎摄入途径暴露PCBs的致癌风险及危害商数均小于EPA推荐的可接受风险水平,表明广东养殖牡蛎中PCBs对消费者的致癌风险处于可接受水平。本研究只分析了PCBs这类污染物,而考虑到牡蛎体内的污染物种类很多且共同存在,是否可能影响到人体的饮食暴露风险尚未可知,因此今后还需加强对多种污染物的监测研究。
-
表 1 基于不同材料和方法测得的团头鲂DNA含量结果比较
Table 1 Comparison of DNA content detected by different methods and tissues
标定物种
calibration species实验材料
experiment tissueDNA含量(C值)/pg
DNA content(C value)测定方法
method与该研究相比
comparison with this study研究者
researcher斑马鱼(Danio rerio) 鳍条 1.25±0.07 FCM - 该研究 鸡(Gallus domesticus) 血液 1.33±0.03 FCM +0.08 范兆廷等[33] 人(Homo sapiens) 血液 1.17 FD -0.08 周暾[34] 人 血液 1.2 FD -0.05 李渝成等[35] 鸡 血液 1.33±0.01 FCM +0.07 吴成宾等[36] 鸡 血液 1.32±0.03 FCM +0.08 尹洪滨等[37] 注:FCM.流式细胞术;FD.显微荧光光度法
Note:FCM. flow cytometry;FD. feulgen densitometry -
[1] 赵书涛, 武晓东, 王策, 等.流式细胞仪的原理、应用及最新进展[J].现代生物医学进展, 2011, 11(22):4378-4381. http://www.docin.com/p-942805691.html [2] 贾永蕊.流式细胞术在检测中的应用[J].中国医学装备, 2010, 7(4):4-6. http://med.wanfangdata.com.cn/Paper/Detail/PeriodicalPaper... [3] 杜立颖, 冯仁青.流式细胞术[M]. 2版.北京:北京大学出版社, 2014:22. [4] 贾永蕊.流式细胞术[M].北京:化学工业出版社, 2009:4. [5] ZHOU Q, CHEN W, ZHANG H Y, et al. A flow cytometer based protocol for quantitative analysis of bloom-forming cyanobacteria (Microcystis) in lake sediments[J]. J Environ Sci, 2012, 24(9):1709-1716. doi: 10.1016/S1001-0742(11)60993-5
[6] YANG Y C, TSAI M H, CHENG H F. Determine the potency of BCG vaccines by flow cytometer[J]. Biotechnol Biotec EQ, 2011, 25(2):2394-2398. doi: 10.5504/BBEQ.2011.0048
[7] 董晓琳, 李志萍, 高玮村, 等.基于适配体的金黄色葡萄球菌流式细胞术检测方法[J].吉林农业科学, 2016, 41(3):81-86. http://www.cnki.com.cn/Article/CJFDTotal-JLNK201603017.htm [8] 程群英, 邹春标.流式细胞术检测红细胞渗透脆性有效性分析[J].中国免疫学杂志, 2016, 32(8):1179-1182. http://d.g.wanfangdata.com.cn/Periodical_zgsyxyxzz201601043.aspx [9] 程玉萍. 急性髓系白血病干细胞新靶点3A4抗原的生物学特性研究[D]. 杭州: 浙江大学, 2015: 6. http://cdmd.cnki.com.cn/Article/CDMD-10335-1015608937.htm [10] 张广鑫. 抗肺癌小分子药物的筛选及其作用机制的研究[D]. 长春: 吉林大学, 2015: 28. http://cdmd.cnki.com.cn/Article/CDMD-10183-1015597265.htm [11] RIBALTA F M, CROSER J S, OCHATT S J. Flow cytometry enables identification of sporophytic eliciting stress treatments in gametic cells[J]. J Plant Physiol, 2012, 169(1):104-110. doi: 10.1016/j.jplph.2011.08.013
[12] VECSLER M, LAZAR I, TZUR A. Using standard optical flow cytometry for synchronizing proliferating cells in the G1 phase[J]. PLoS ONE, 2013, 8(12):1-8. https://www.researchgate.net/profile/Manuela_Vecsler/publication...
[13] REWERS M, JEDRZEJCZYK I. Genetic characterization of Ocimum genus using flow cytometry and inter-simple sequence repeat markers [J]. Ind Crops Prod, 2016, 91:142-151. doi: 10.1016/j.indcrop.2016.07.006
[14] 韦云芳, 张跃骏, 唐树生, 等.流式细胞仪分离工作犬精子的研究[J].安徽农业科学, 2015, 43(9):95-98. [15] 邓灯, 吴晓春, 程顺峰, 等.鱼肠道弧菌单克隆抗体流式细胞术检测技术的研究[J].水产科学, 2015, 34(2):113-117. http://www.cqvip.com/QK/93386X/201502/663743460.html [16] 范兆廷, 尹洪滨, 宋苏祥, 等.十三种淡水养殖鱼类的DNA含量[J].水产学报, 1995, 19(4):322-326. http://www.cnki.com.cn/Article/CJFDTOTAL-SCKX504.006.htm [17] 杨坤, 王子健, 祝东梅, 等.麦穗鱼的组型分析和含量测定[J].华中农业大学学报, 2012, 31(3):371-375. http://www.irgrid.ac.cn/handle/1471x/916366?mode=full [18] 徐康, 段巍, 肖军, 等.鱼类遗传育种中生物学方法的应用及研究进展[J].中国科学:生命科学, 2014, 44(12):1272-1288. http://life.scichina.com:8082/sciC/CN/abstract/abstract516334.shtml [19] 安苗, 周棋春, 王金娜, 等.草海鲫含量与倍性[J].淡水渔业, 2013, 43(4):3-7. http://www.cnki.com.cn/Article/CJFDTOTAL-DSYY201304002.htm [20] ANBUMANI S, MOHANKUMAR M N. Gamma radiation induced cell cycle perturbations and DNA damage in Catla catla as measured by flow cytometry [J]. Ecotoxicol Environ Saf, 2015, 113:18-22. doi: 10.1016/j.ecoenv.2014.11.011
[21] 方礼豹, 周小云, 崔蕾, 等.二倍体、四倍体泥鳅与大鳞副泥鳅杂交子代相对含量与染色体组型的比较[J].华中农业大学学报, 2011, 30(4):500-505. http://d.wanfangdata.com.cn/periodical_hznydx201104021.aspx [22] REYES-BECERRIL M, ALAMILLO E, SANCHEZ-TORRES L A, et al. Leukocyte susceptibility and immune response against Vibrio parahaemolyticus in Totoaba macdonaldi [J]. Dev Comp Immunol, 2016, 65:258-267. doi: 10.1016/j.dci.2016.07.016
[23] WANG Y P, LU Y, ZHANG Y, et al. The draft genome of the grass carp (Ctenopharyngodon idellus) provides insights into its evolution and vegetarian adaptation [J]. Nat Genet, 2015, 47(6):625-631. doi: 10.1038/ng.3280
[24] XU P, ZHANG X F, WANG X M, et al. Genome sequence and genetic diversity of the common carp, Cyprinus carpio [J]. Nat Genet, 2014, 46 (11):1212-1219. doi: 10.1038/ng.3098
[25] WU C W, ZHANG D, KAN M Y, et al. The draft genome of the large yellow croaker reveals well-developed innate immunity [J]. Nat Com, 2014, 5:5227. doi: 10.1038/ncomms6227
[26] CHEN S L, ZHANG G J, SHAO C W, et al. Whole-genome sequence of a flatfish provides insights into ZW sex chromosome evolution and adaptation to a benthic lifestyle [J]. Nat Genet, 2014, 46 (3):253-260. doi: 10.1038/ng.2890
[27] 刘少军, 赵如榕, 刘锦辉, 等.不同倍性鱼的血细胞和精子含量比较[J].动物学报, 2005, 51(2):360-364. http://www.cqvip.com/QK/94056X/200502/15576544.html [28] 徐钢春, 殷文健, 顾若波, 等.龙池鲫含量、倍性分析及其形态学特征研究[J].淡水渔业, 2015, 45(3):9-13. http://www.cnki.com.cn/Article/CJFDTOTAL-DSYY201503002.htm [29] 王敏君. 肝细胞的衰老特征及衰老逆转的研究[D]. 上海: 第二军医大学, 2014: 12-13. http://cdmd.cnki.com.cn/Article/CDMD-90030-1015518728.htm [30] 魏熙胤, 牛瑞芳.流式细胞仪的发展历史及其原理和应用进展[J].现代仪器, 2006, 1(4):8-11. http://www.bioon.com.cn/sub/showarticle.asp?sub_id=1022&newsid=6328 [31] VINOGRADOV A E. Genome size and GC-percent in vertebrates as determined by flow cytometry:the triangular relationship[J]. Cytometry, 1998, 31(2):100-109. doi: 10.1002/(ISSN)1097-0320
[32] 杨坤, 祝东梅, 张新辉, 等.麦穗鱼不同组织含量及细胞周期的分析研究[J].中国农学通报, 2012, 28(32):113-118. doi: 10.3969/j.issn.1000-6850.2012.32.022 [33] 范兆廷, 尹洪滨, 宋苏祥, 等.四种鱼类外周血红细胞细胞周期及DNA含量[J].动物学报, 1995, 41(4):370-374. http://www.cnki.com.cn/Article/CJFDTOTAL-BEAR199504004.htm [34] 周暾.鱼类染色体研究[J].动物学研究, 1984, 5(1):38-52. http://www.cnki.com.cn/Article/CJFDTOTAL-DWXY1984S1007.htm [35] 李渝成, 李康, 周暾.十四种淡水鱼的DNA含量[J].遗传学报, 1983, 10(5):384-389. http://www.cnki.com.cn/Article/CJFDTOTAL-YCXB198305008.htm [36] 吴成宾, 李福贵, 陈杰, 等.鳊鲂鱼类的染色体核型及含量分析[J].上海海洋大学学报, 2015, 24(6):801-809. doi: 10.12024/jsou.20150301367 [37] 尹洪滨, 范兆廷, 孙中武, 等.团头鲂核型与含量分析研究[J].水产学杂志, 1995, 8(1):22-26. http://www.cqvip.com/QK/85010A/199501/5549061.html -
期刊类型引用(7)
1. 张潇潇,杨少森,邹翠云,张勇,黄锦雄,甘松永,秦真东,黄玮坪,陈永南,吴锦辉,林蠡. 蓝圆鲹的胚胎及胚后发育特征观察. 水产学报. 2025(01): 105-115 .  百度学术
百度学术
2. 高彩霞,赖素群,曾进. 诸氏鲻虾虎鱼胚胎及早期仔鱼发育研究. 水产科技情报. 2024(01): 1-7 .  百度学术
百度学术
3. 王岳松,徐林,杨洋,程睿,王崇,何大江,黎国樑,马海涛,毕建启,陈锋,万正平,张志明. 长鳍光唇鱼(Acrossocheilus longipinnis)人工繁殖和早期发育研究. 南方水产科学. 2024(02): 63-72 .  本站查看
本站查看
4. 谭泽宇,李涛,姜敬哲,黄小林,杨育凯. 喷点雪印小丑鱼的胚胎及仔、稚、幼鱼形态发育观察. 南方水产科学. 2024(02): 73-82 .  本站查看
本站查看
5. 韩豪祥,廉杰,金洪宇,马波. 额尔齐斯河黑鲫胚胎及早期仔鱼发育特征. 中国水产科学. 2024(06): 684-692 .  百度学术
百度学术
6. 欧阳焱,潘瑾岷,冼霖,刘宝锁,郭华阳,朱腾飞,张楠,朱克诚,张殿昌. 尖翅燕鱼染色体水平基因组与特征分析. 南方水产科学. 2024(06): 31-42 .  本站查看
本站查看
7. 陈思奇,朱永久,吴兴兵,杨德国,李晓莉. 大鳍鳠胚胎及仔稚鱼发育观察. 南方水产科学. 2023(06): 60-70 .  本站查看
本站查看
其他类型引用(2)




 下载:
下载:





 粤公网安备 44010502001741号
粤公网安备 44010502001741号
