Trace elements in statoliths of Sthenoteuthis oualaniensis in the South China Sea
-
摘要:
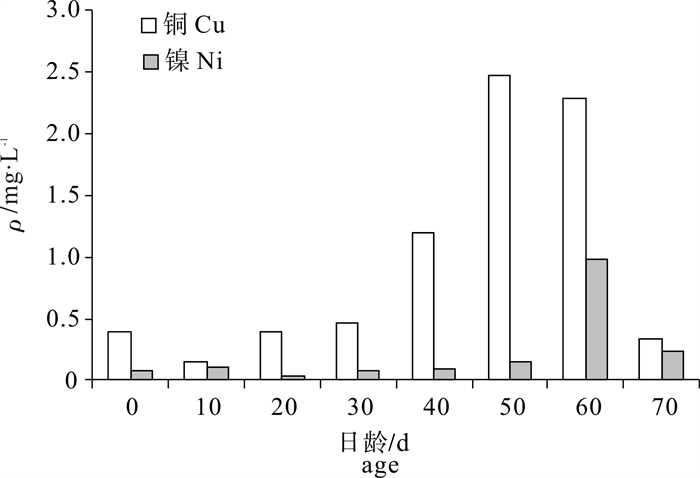
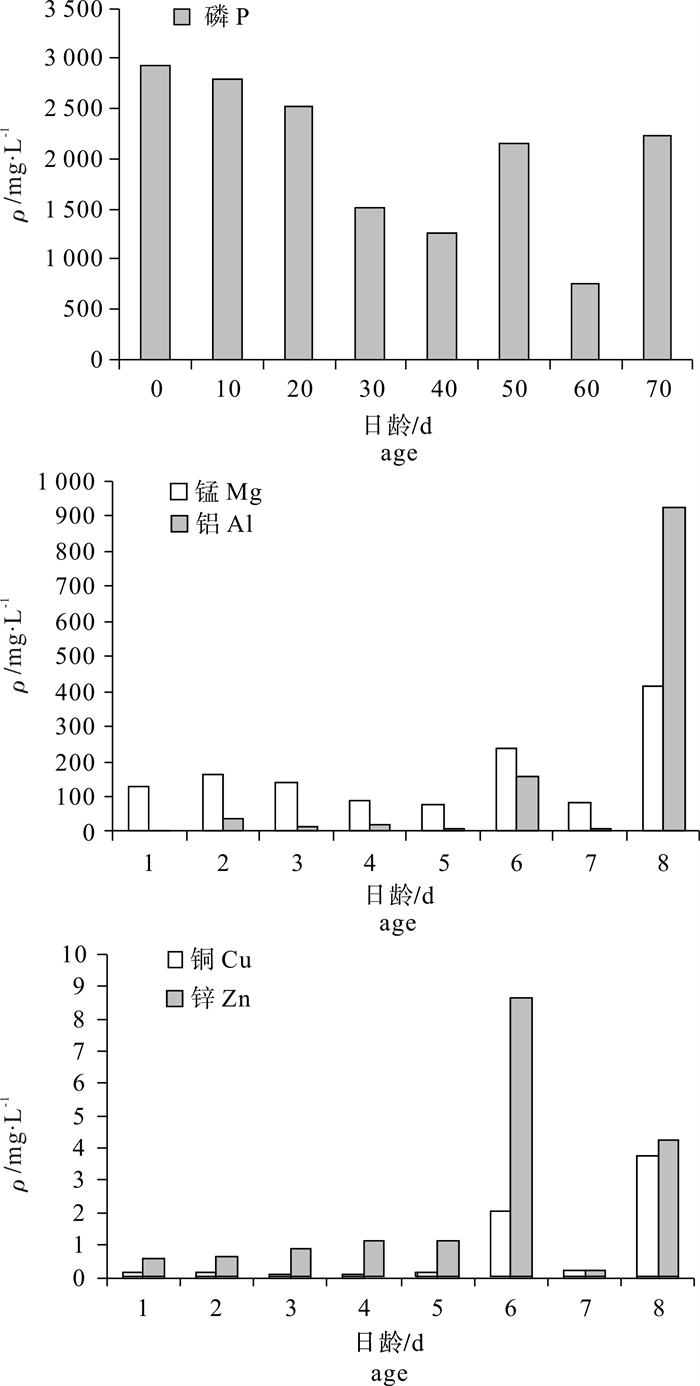
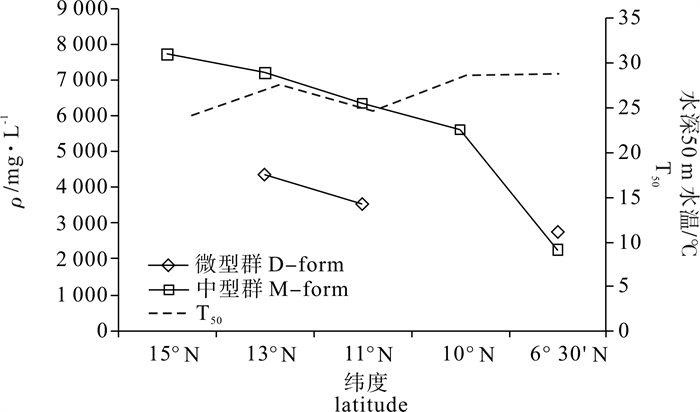
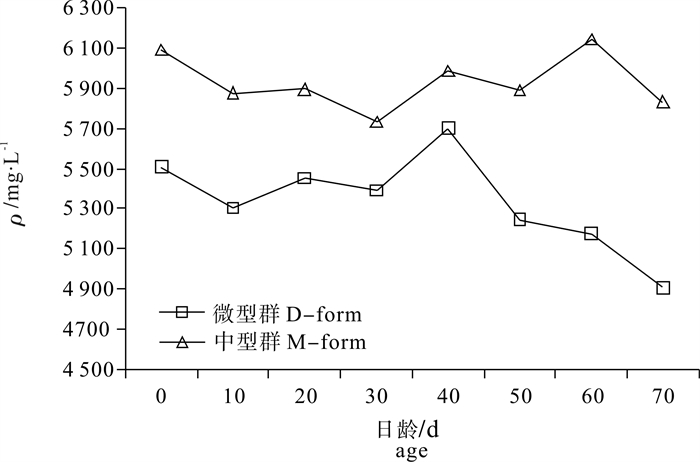
根据2012年9月~10月于南海采集的鸢乌贼(Sthenoteuthis oualaniensis)样本,利用激光剥蚀电感等离子质谱法(laser ablation inductively coupled plasma mass spectrometry,LA-ICP-MS)分析鸢乌贼耳石微量元素组成及分布。结果显示,南海鸢乌贼耳石含量前10位的元素依次为钙(Ca)、锶(Sr)、钠(Na)、磷(P)、钾(K)、镁(Mg)、锌(Zn)、铝(Al)、铜(Cu)和镍(Ni)。P方差分析发现,鸢乌贼耳石微量元素Ca(P=0.017)、Sr(P=0.016)、Na(P=0.042)种群差异显著(P < 0.05);中型群Ca(P=0.026)、Sr(P=0.021)、Na(P=0.025)性别差异显著(P < 0.05),微型群性别差异不显著(P>0.05);中型群Cu(P=0.002)、Ni(P=0.001)日龄差异显著(P < 0.05),微型群P(P=0.000)、Mg(P=0.002)、Zn(P=0.023)、Al(P=0.000)、Cu(P=0.003)日龄差异显著(P < 0.05)。南海鸢乌贼Sr含量随纬度的降低而减少,且0日龄高于10日龄。
Abstract:The trace elements of Sthenoteuthis oualaniensis collected from the South China Sea during September to October, 2012 were analyzed by laser ablation inductively coupled plasma mass spectrometry (LA-ICP-MS). The top 10 abundant elements are calcium (Ca), strontium (Sr), sodium (Na), phosphorus (P), potassium (K), magnesium (Mg), zinc (Zn), aluminum (Al), copper (Cu) and nickel (Ni). The analysis of variance (ANOVA) reveals significant difference in Ca (P=0.017), Sr (P=0.016) and Na (P=0.042) between middle-form (M-form) and dwarf-form (D-form) of S.oualaniensis (P < 0.05);significant difference of M-form existed in Ca (P=0.026), Sr (P=0.021) and Na(P=0.042) in sex (P < 0.05), but no significant difference of D-form existed in sex (P>0.05);significant difference of M-form existed in Cu (P=0.002), Ni (P=0.001) at different ages (P < 0.05), and significant difference of D-form existed in P (P=0.000), Mg (P=0.002), Zn (P=0.023), Al (P=0.000) and Cu (P=0.003) at different ages (P < 0.05). Sr in statolith declined as latitude decreased, and the concentration of 0 dah was higher than that of 10 dah.
-
Keywords:
- Sthenoteuthis oualaniensis /
- statolith /
- trace element /
- the South China Sea
-
pH调节法提取蛋白质早期应用于鱼白肉和碎鱼肉中提取、分离鱼蛋白。20世纪末,美国学者就报道了一种提取动物蛋白的新方法,即pH调节法或称酸碱法、等电点溶解/沉淀法[1]。该法是根据蛋白质在不同酸碱度中溶解度的异同,利用蛋白质在等电点附近溶解度最低的原理将蛋白质沉淀并回收。整个提取过程具有操作温度低、蛋白质变性程度小、功能特性保持较完全等优点。此后,采用等电点法提取分离动物蛋白的报道逐渐增多。UNDELAND等[2]报道了利用等电点法从鲱(Clupea harengus)鱼肉中提取的分离蛋白具有更好的色泽和优良的凝胶强度。CHOI和PARK[3]对酸处理(pH 5.0)回收太平洋鳕(Gadus macrocephalus)蛋白的研究表明,与传统水洗法相比,酸处理法回收蛋白的得率高、组织蛋白酶的活性强,但部分蛋白,如肌球蛋白和肌动蛋白在提取过程中发生了降解。等电点法主要应用于以鱼白肉、碎鱼肉和鱼下脚料为原料的鱼蛋白提取[4-7]。GIGLIOTTI等[8]采用了等电点法从南极磷虾(Euphaususa superba)中分离提取蛋白,并对其营养价值和安全性进行了分析。其蛋白质含量为78%(干基),安全性与酪蛋白无明显差异。
在甲壳动物中,绝大多数类胡萝卜素都以类胡萝卜蛋白(类胡萝卜素结合高密度脂蛋白)的形式存在[9]。该蛋白被认为有2种作用,改善色素的水溶性和提供颜色。甲壳动物的类胡萝卜素蛋白分为3种[10-11]:1)类胡萝卜脂蛋白。主要分布在甲壳动物的卵和卵巢中,但在血液和表皮中也有少量存在。它们使组织呈现蓝色、绿色和紫色;2)从甲壳动物外壳中发现的几丁质类胡萝卜素。它们由几丁质和类胡萝卜素通过Schiff碱键结合而成或是由几丁质的氮端和类胡萝卜素上的酮环结合而成;3)类胡萝卜结合蛋白。主要是虾青素结合脱辅基蛋白而生成的虾青蛋白,它们主要存在于甲壳动物的体表结构中,为其提供保护色。
虾壳在虾熟制过程中会发生红变现象,这是由于虾青蛋白受热变性,释放了与其共价结合的类胡萝卜素而引起的[12]。虾壳的色泽不仅会左右人们的购买,而且也在一定程度上反映了整虾的新鲜程度[13]。传统方法提取虾青蛋白主要是经硫酸铵分级沉淀后,采用高效液相色谱进一步纯化[14]。不仅试验试剂消耗大、目标蛋白得率低,并且温度对目标蛋白的提取影响大。该试验采用pH调节法对比传统硫铵盐析法从凡纳滨对虾壳中提取β虾青蛋白,并对所得蛋白在回收率、纯度和光谱性质等方面进行比较,旨在对pH调节法提取虾青蛋白的可行性进行分析讨论,为有效提取、利用甲壳动物甲壳中的虾青蛋白提供参考。
1. 材料与方法
1.1 材料
凡纳滨对虾(Litopenaeus vannamei)虾壳(亚洲水产,湛江产),运回实验室后立即用冰水洗净、4 ℃下干燥、粉碎、称质量。
1.2 仪器与试剂
UV-1800紫外可见分光光度计(日本岛津出品),CR22GⅡ型高速冷冻离心机(日本日立出品),LC-20AD高效液相色谱仪(日本岛津出品),AE-7300型电泳仪(日本帝国理化出品),Jasco-725型圆二色光谱仪(日本Jasco出品),Alpha 2-4型真空冷冻干燥机(德国Martin Christ出品),Ettan IPGphorⅡ型等电聚焦仪(美国GE Healthcare出品),F-52型pH计(日本崛场出品),Immobiline DryStrip pH 3-10 NL、13 cm型胶条(美国GE Healthcare出品)。试验用水为超纯水,磷酸氢二钠、磷酸二氢钠、EDTA和CHAPS等试剂均为国产分析纯。
1.3 方法
1.3.1 盐析法提取β虾青蛋白
参考ZAGALSKY[14]。将虾壳用预冷却的质量分数为10%的EDTA溶液浸泡[m(虾壳,g):V(EDTA, mL)=25:1 000]10 h(4 ℃)。过滤后向滤液中加入55%饱和度的硫酸铵,4 ℃静置10 h。离心(10 000 g,4 ℃,20 min)后,用100 mL、50 mmol·L-1磷酸盐缓冲液(pH 7.0)溶解沉淀并加入20 %饱和度的硫酸铵,4 ℃静置10 h。二次离心后弃沉淀并向清液中加入50%饱和度的硫酸铵,4 ℃静置10 h后离心所得沉淀即为粗蛋白。将多次提取的粗蛋白收集后,通过真空冷冻干燥浓缩、保存。
在使用高效液相色谱纯化前,需用保存液(50 mmol·L-1,pH 7.0磷酸盐缓冲液)透析数次,以尽量减少硫酸铵对纯化的影响。试验选用的是离子交换柱(5 mm×50 mm Mono Q阴离子交换柱)。流动相:溶剂A为50 mmol·L-1磷酸盐缓冲液(pH 7.0),溶剂B为含1.0 mol·L-1氯化钠的50 mmol·L-1磷酸盐缓冲液(pH 7.0)。梯度洗脱程序为10~80 min内溶剂B的体积从0上升至70%,90 min时增加至100%并维持10 min,115 min时降为0;流速为0.5 mL·min-1,进样量1 mL。
1.3.2 pH调节法提取β虾青蛋白
将预处理后的凡纳滨对虾虾壳用预冷却的质量分数为10%的EDTA溶液浸泡10 h、过滤。提取液pH设置为3.0~11.0,以1.0为pH变化梯度。将滤液分为2份,分别用2 mol·L-1的盐酸(HCl)调节至3.0(酸处理)和2 mol·L-1的氢氧化钠(NaOH)调节pH至11.0(碱处理)。4 ℃、10 000 g离心17 min,得到不同pH下的溶出物和未溶物。
用2 mol·L-1的HCl或NaOH将溶出物的pH调节至等电点后4 ℃、10 000 g离心17 min,得到目标蛋白和未回收的溶出物。
蛋白质溶解度和回收率计算公式为[15]:
$$ 蛋白质溶解度 (\%)=\frac{A}{C} \times 100 $$ $$ 蛋白质回收率 (\%)=\frac{A-A_1}{C} \times 100 $$ 其中A为不同pH处理后离心所得清液中虾青蛋白质量(mg)=清液中蛋白质质量浓度(mg·mL-1)×清液体积(mL);A1为等电点沉淀后,离心所得清液中的虾青蛋白质量(mg);C为总虾青蛋白质量(mg),C=EDTA脱钙后滤液中虾青蛋白质量浓度(mg·mL-1)×滤液体积(mL)。每组试验重复3次取平均值。
1.3.3 β虾青蛋白的基本性质分析
1) 等电聚焦电泳。将经盐析、离子交换色谱纯化后的蛋白质溶于50 mmol·L-1磷酸盐缓冲液中(pH 7.0),透析数次,以消除盐对试验结果的影响。向洁净、干燥的胶条槽(13 cm)内加入含1.0 mL β虾青蛋白纯品(170.14 mg)的再水化液250 mL,将撕去保护膜的IPG胶条置于胶条槽内(酸性端位于正极),尽量避免气泡的形成。最后加入IPG覆盖液以防止蛋白质样品的蒸发和尿素结晶的形成。等电聚焦电泳参数设定为500 V,60 min;1 000 V梯度,60 min;8 000 V梯度,150 min;8 000 V,25 min。电泳完成后经固定、染色、脱色后拍照、保存。2)SDS-PAGE电泳。预制胶浓度为5%~20%(Atto,日本产),Marker范围为10~250 kDa(Bio-Rad,美国产)。电泳完成后经考马斯亮蓝R250染色,脱色。3)凝胶过滤层析。对经过2种方法纯化后的蛋白质选用HiPrep 16/60 Sephacryl S-100 HR和S-300 HR预装柱(GE Healthcare,美国产)进一步确认其分子量。洗脱液为50 mmol·L-1、pH 7.0的磷酸盐缓冲液,流速为15 mL·h-1,标准品分子量为1.35~670 kDa(Bio-Rad,美国产)。4)蛋白质纯度测定。利用凯氏定氮法(GB/T 5009.5-2003)进行测定。每组试验重复3次取平均值。5)最大吸收波长的测定。利用紫外可见光谱仪对蛋白质的最大吸收波长进行测定。6)β虾青蛋白二级结构的测定。在Jasco-725型圆二色光谱仪上进行圆二色光谱测量,光源系统用氮气保护(流量为15 L·min-1),试验均采用2 mm光程石英样品池。测量参数:扫描波长范围200~240 nm,扫描时间50 nm·min-1,分辨率0.1 nm,响应时间1 s,累积次数3次,在室温下进行测定[16]。CD谱用平均残基摩尔椭圆度表示,单位deg·cm2·dmol-1。利用圆二色光谱仪附带的杨氏法二级结构分析软件对二级结构含量进行计算[17]。
2. 结果与分析
2.1 pH调节法分离蛋白质的回收率、溶解度和纯度
pH处理对蛋白质溶解度的影响呈现先下降后上升的趋势(图 1)。当pH为3.0~5.0时溶解度呈逐渐下降趋势;pH为5.0~11.0时溶解度呈上升趋势;5.0~9.0时上升较为缓慢。酸性溶液中蛋白质溶解度在pH 3.0时最大为60.5%,碱性溶液中蛋白质溶解度在pH 11.0时最大为55.7%;pH为5.0时溶解度最小为15.4%。
pH调节法对蛋白质回收率的影响趋势与溶解度一致。最大回收率为pH 3.0时的47.5%,高于传统硫铵盐析的24.3%。同时,pH调节法所得β虾青蛋白的纯度经凯氏定氮法测得为78.23%,也高于盐析法的74.06%。
2.2 β虾青蛋白的光谱性质
盐析法所得虾青蛋白粗品经高效液相分离纯化,按洗脱先后顺序共有3个峰:1)在20% B液条件下洗脱出,在520 nm处有最大吸收,被定义为α虾青蛋白;2)在40% B液条件洗脱出,在580 nm处有最大吸收,被定义为β虾青蛋白;3)在100% B液条件下被洗脱出,在500 nm处有最大吸收,被定义为虾青蛋白的变性产物(图 2)。这与ZAGALSKY [14]的研究一致,α虾青蛋白在0.25 mol·L-1浓度下被洗脱。而TIMME等 [18]对南非龙虾(Jasus lalandii)的研究认为α与β虾青蛋白的洗脱浓度分别为0.4 mol·L-1和0.2 mol·L-1 B液浓度,且最大吸收峰分别为525 nm和560 nm。产生洗脱差异的原因仍需进一步研究,初步推断是组成蛋白质的氨基酸序列和数量的不同所引起。
图 3为不同提取方法获得的β虾青蛋白的紫外可见光谱图。可见2种方法获得的目标蛋白在最大吸收波长上无差异,均为580 nm。TIMME等[18]发现南非龙虾壳中提取的β虾青蛋白的最大吸收波长为560 nm;ZAGALSKY[14]在对无脊椎动物中提取的类胡萝卜蛋白研究后指出,美国龙虾壳中提取的β虾青蛋白的最大吸收波长为580~590 nm;CHAYEN等[19]研究发现欧洲龙虾(Homarus gammarus)壳中提取的β虾青蛋白的最大吸收波长为585 nm。不同地区虾壳中提取的β虾青蛋白最大吸收波长差异的原因仍需进一步研究。
标准蛋白质二级结构的圆二色光谱为:α螺旋在222 nm和208 nm处呈现负峰,在192 nm附近显示一个正峰;β折叠在215 nm处呈负峰,在198 nm附近有一正峰;无规则卷曲则在198 nm有一负峰,在220 nm附近有一正峰。试验得到的圆二色光谱可以看作一定百分比的α螺旋、β折叠和无规则卷曲的线性迭加图谱[20]。通过对比标准二级结构的远紫外圆二色光谱图,试验结果显示β虾青蛋白二级结构主要是α螺旋(盐析法),含量为65%~70% (25 ℃)(图 4)。pH调节法所得β虾青蛋白与传统盐析法提取的β虾青蛋白在二级结构含量上无明显差异,分别为70.1%和67%。
2.3 β虾青蛋白的等电点与分子量
盐析法所得β虾青蛋白等电聚焦电泳仅显示1条条带(图 5),证明凯氏定氮中盐析法所得蛋白质纯度为74.06%是可靠的。以标准蛋白质等电点为对照计算得知β虾青蛋白等点电为5.6,这也符合pH 5.0~6.0时蛋白质溶解度最低。
凝胶色谱结果显示,在20% B液下收集的520 nm处有最大吸收峰,被定义为α虾青蛋白的物质,分子量为380 kDa;在40% B液下收集的580 nm处有最大吸收峰,被定义为β虾青蛋白的物质,分子量为45 kDa,这与TIMME等[18]的研究结果较为一致。
聚丙烯酰胺凝胶电泳粗蛋白显示3个特征条带区(图 6),分布在相对分子量为350 kDa、75 kDa和37 kDa处。β虾青蛋白是由2个分子量约为20 kDa的亚基组成的二聚物[14, 19],因此推断37 kDa附近的条带为β虾青蛋白。而α虾青蛋白是由8个β型组合而成的一个八面体结构[14, 19],因此350 kDa的条带推断为α虾青蛋白。75 kDa的条带仍需进一步研究,推测为α型的降解产物[19]或是纯化过程中得到的其他蛋白质亚基[14]。2种方法纯化后的蛋白质在37 kDa附近的条带均被稀释,说明SDS-PAGE不适合用来鉴定β虾青蛋白分子量。
3. 讨论
蛋白质的溶解度对优化酸碱法回收蛋白质有决定性作用。在酸性或碱性条件时,蛋白质由于携带不同电荷会发生沉淀或溶解的现象[21]。极端pH条件下,由于强烈的排斥作用蛋白质很难发生沉淀(尽管此时已有蛋白质发生变性),它会与水分子结合而使溶解度升高。当溶液pH处于蛋白质等电点附近时,蛋白质净电荷为零而产生聚合现象使溶解度降低[19]。溶解度高有利于将目标蛋白从杂质中分离出来,而等电点时的低溶解度则有利于提高目标蛋白的回收率[22]。从凡纳滨对虾壳中提取的β虾青蛋白溶解度曲线呈U型,这与尼罗罗非鱼(Oreochromis niloticus)[23]和南极磷虾[15]肌肉中回收的蛋白质溶解度曲线一致。随着pH的降低,溶解度逐渐增加的原因是蛋白质在酸度系数2.5~7.0时比7.0~11.0含有更多的离子化基团[2]。
β虾青蛋白通过萃取和沉淀从凡纳滨对虾壳中获得,在pH 3.0和11.0时其回收率约为40%~47%。PALAFOX等[22]使用pH调节法从巨型鱿鱼(Dosidicus gigas)中提取肌肉蛋白的回收率约为75%;KRISTINSSON等[24]采用pH调节法从石首鱼(Micropogonias undulates)中提取肌肉蛋白的回收率约为65%~78%。β虾青蛋白回收率较低的原因是虾壳主要由虾青素和几丁质构成,蛋白质含量相对较低[25]; CHEN和JACZYNSKI[26]报道了pH调节法提取蛋白质的回收率与溶液离子强度有关。类胡萝卜素在结合载脂蛋白后会增强其水溶性[10, 12],同时蛋白质在pH 3.0和11.0时的高溶解度会进一步提高β虾青蛋白的回收率。
pH调节法在目标蛋白的纯度和产量上均优于传统盐析法。这主要是由于pH调节法可以减少提取步骤从而降低杂蛋白的产量和不利影响。同时,蛋白质具有酸碱基团的特性也有利于增加产量、提高目标蛋白纯度。
虾青蛋白对虾壳熟制过程中的颜色变化发挥着重要作用,因此提高蛋白质的提取率对深入了解和利用虾青蛋白具有重要意义。pH调节法提取β虾青蛋白在蛋白质回收率、纯度上均优于传统盐析法,蛋白质分子量、二级结构也无明显差异。虽然等电点的确认需要通过传统盐析法得到纯品,而且在等电点法提取时酸碱会在一定程度上引起蛋白质变性,但该法简单、快捷,蛋白质产量和纯度均优于传统方法, 同时试剂消耗少,试验条件要求低。因此,pH调节法可以作为从虾壳中提取β虾青蛋白的参考方法。
-
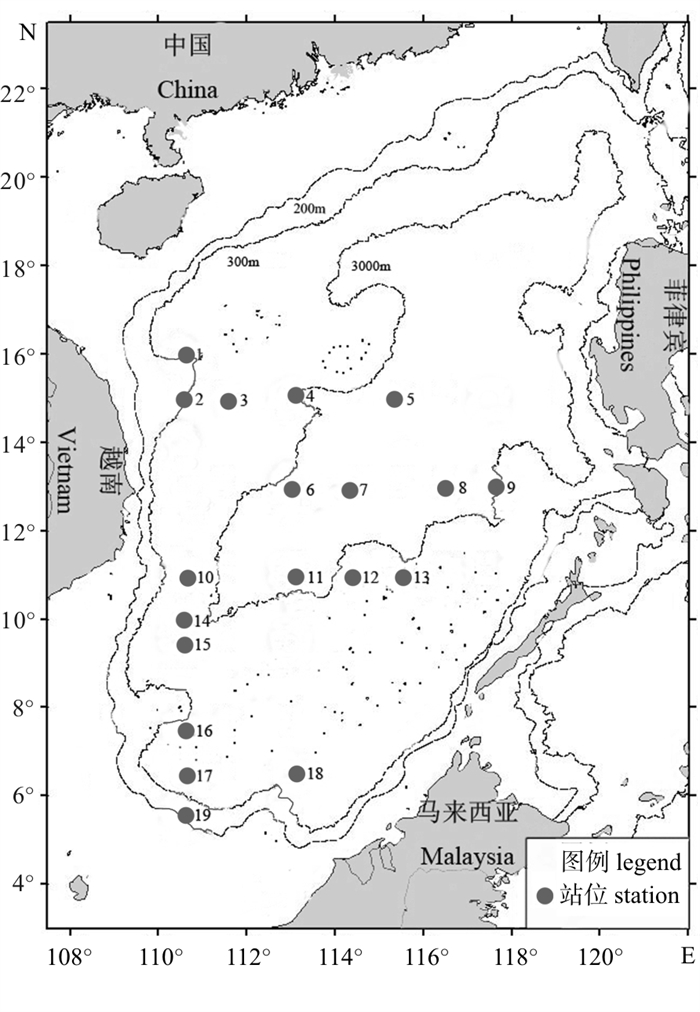
表 1 耳石微量元素分析样本
Table 1 Statolith samples tested by statolith microchemistry analysis
编号
No.站位
station纬度类别
latitude category50 m水温/℃
T50胴体长/mm
ML体质量/g
BW性别
sex性腺成熟度
maturity stage种群
form1 1 15° 27.07 153 184.55 F Ⅱ M 2 2 15° 19.67 85 20.61 M Ⅱ D 3 2 15° 19.67 109 47.70 F Ⅲ D 4 3 15° 22.10 168 257.74 F Ⅱ M 5 4 15° 23.40 80 16.09 M Ⅱ D 6 4 15° 23.40 99 35.52 F Ⅳ D 7 5 15° 28.61 111 42.70 M Ⅰ M 8 6 13° 28.61 94 28.37 F Ⅲ D 9 7 13° 24.61 103 31.61 F Ⅲ D 10 7 13° 24.61 116 68.07 M Ⅱ M 11 7 13° 24.61 186 314.93 F Ⅲ M 12 7 13° 24.61 176 242.23 F Ⅳ M 13 8 13° 28.31 106 42.32 M Ⅰ M 14 8 13° 28.31 133 135.59 F Ⅱ M 15 8 13° 28.31 122 78.12 M Ⅲ D 16 9 13° 28.65 157 203.44 F Ⅲ M 17 9 13° 28.65 118 94.13 M Ⅳ M 18 10 11° 25.53 88 20.91 M Ⅲ D 19 11 11° 21.31 73 13.58 M Ⅱ D 20 11 11° 21.31 69 9.82 F Ⅱ D 21 11 11° 21.31 129 92.62 F Ⅱ M 22 12 11° 27.47 96 32.88 F Ⅲ D 23 13 11° 27.87 61 9.43 F Ⅰ D 24 14 10° 28.64 114 57.40 F Ⅳ D 25 14 10° 28.64 88 25.84 M Ⅰ M 26 14 10° 28.64 130 102.80 F Ⅱ M 27 14 10° 28.64 119 82.01 M Ⅲ M 28 14 10° 28.64 124 99.45 M Ⅳ M 29 15 10° 28.47 95 27.55 F Ⅰ M 30 16 6°30′ 28.37 98 42.17 F Ⅰ M 31 16 6°30′ 28.37 130 110.32 M Ⅲ M 32 17 6°30′ 28.70 78 15.16 M Ⅱ D 33 18 6°30′ 28.47 116 80.97 M Ⅳ M 34 18 6°30′ 28.47 69 10.96 M Ⅰ D 35 19 6°30′ 29.31 59 7.17 F Ⅰ D 注:D. 微型群;M. 中型群;T50. 水深50 m水层温度
Note:D. dwarf form;M. middle form;T50.sea temperature at 50 m water depth表 2 南海鸢乌贼耳石微量元素的质量浓度及其与Ca的比值
Table 2 Element concentration in whole statoliths of S.oualaniensis using solution-based ICP-MS in the South China Sea
元素
element质量浓度/mg·L-1
concentration元素/钙
element/Ca锶 Sr 1 600.72~11 100.76(6 137.26±2 687.36) 1.386 0~1.650 7(1.476 4±0.074 4) 钠 Na 1 627.33~6 528.52(3 961.20±1 376.05) 0.880 3~1.317 2(1.014 4±0.222 4) 磷 P 398.21~3387.55(1 908.31±767.82) 0.220 4~1.262 1(0.498 5±0.218 5) 钾 K 88.17~639.71(337.02±145.64) 0.045 8~0.139 1(0.085 8±0.027 4) 镁 Mg 87.33~543.51(230.52±97.08) 0.025 5~0.122 1(0.061 9±0.025 2) 锌 Zn 45.94~379.03(153.84±88.71) 0.021 6~0.182 5(0.046 6±0.043 3) 铝 Al 1.12~64.22(12.97±16.77) 0.000 2~0.035 5(0.004 5±0.008 5) 铜 Cu 1.64~17.46(8.99±5.29) 0.000 4~0.009 9(0.002 3±0.001 6) 镍 Ni 3.48~17.76(7.66±3.46) 0.000 9~0.004 5(0.002 3±0.001 6) 表 3 头足类耳石微量元素含量前10位的元素比较
Table 3 Comparison of top 10 trace elements in statoliths between S.oualaniensis, Dosidicus gigas, O.bartramii and I.argentisnus
鸢乌贼
S.oualaniensis茎柔鱼
D.gigas柔鱼
O.bartramii阿根廷滑柔鱼
I.argentisnus钙 Ca 钙 Ca 钙 Ca 钙 Ca 锶 Sr 锶 Sr 锶 Sr 锶 Sr 钠 Na 钠 Na 钠 Na 钠 Na 磷 P 硅 Si 磷 P 磷 P 钾 K 钾 K 钾 K 钾 K 镁 Mg 镁 Mg 硅 Si 铁 Fe 锌 Zn 钡 Ba 镁 Mg 镁 Mg 铝 Al 锌 Zn 硼 B 钡 Ba 铜 Cu 锰 Mn 铁 Fe 硼 B 镍 Ni 锂 Li 钡 Ba 镓 Ga -
[1] ROPER C E, SWEENY M J, NAUEN C E. An annotated and illustrated catalogue of species of interest to fisheries[J]. FAO Fish Synop, 1984, 125(3): 157-181.
[2] 刘必林. 利用耳石微结构研究印度洋西北海域鸢乌贼的年龄和生长[D]. 上海: 上海水产大学, 2006: 1-70. [3] 张鹏, 杨吝, 张旭丰, 等. 南海金枪鱼和鸢乌贼资源开发现状及前景[J]. 南方水产, 2010, 6(1): 68-74. doi: 10.3969/j.issn.1673-2227.2010.01.012 [4] 张俊, 陈作志, 陈国宝, 等. 南海鸢乌贼水声学测量和评估相关技术研究[J]. 南方水产科学, 2014, 10(6): 1-11. doi: 10.3969/j.issn.2095-0780.2014.06.001 [5] 肖述, 郑小东, 王如才, 等. 头足类耳石轮纹研究进展[J]. 中国水产科学, 2003, 10(1): 73-78. doi: 10.3321/j.issn:1005-8737.2003.01.016 [6] CHEN X J, LIU B L, TIAN S Q, et al. Fishery biology of purpleback squid, Sthenoteuthis oualaniensis, in the northwest Indian Ocean[J]. Fish Res, 2007, 83(1): 98-104. doi: 10.1016/j.fishres.2006.09.005
[7] 刘必林, 陈新军, 马金, 等. 头足类耳石的微化学研究进展[J]. 水产学报, 2010, 34(2): 315-321. [8] BASIR S. Biological feature of an oceanic squid, Sthenoteuthis oualaniensis in the South China Sea, Area Ⅲ: western Philippines[C]//Proceedings of SEAFDEC Seminar on Fishery Resources in the South China Sea. Western Philippines. Malaysia, 2000: 135-147.
[9] 颜云榕, 冯波, 卢伙胜, 等. 南沙群岛北部海域鸢乌贼(Sthenoteuthis oualaniensis)夏季渔业生物学研究[J]. 海洋与湖沼, 2012, 43(6): 1177-1186. [10] 江艳娥, 陈作志, 林昭进, 等. 南海中部海域鸢乌贼耳石形态特征分析[J]. 南方水产科学, 2014, 10(4): 85-90. doi: 10.3969/j.issn.2095-0780.2014.04.014 [11] 江艳娥, 张鹏, 林昭进, 等. 南海外海鸢乌贼耳石形态特征分析[J]. 南方水产科学, 2015, 11(5): 27-37. doi: 10.3969/j.issn.2095-0780.2015.05.004 [12] 陈新军, 刘金立. 利用形态学方法分析印度洋西北部海域鸢乌贼种群结构[J]. 上海水产大学学报, 2007, 16(2): 174-179. [13] CHEMBIAN A J, MATHEW S. Population structure of the purpleback squid Sthenoteuthis oualaniensis (Lesson, 1830) along the south-west coast of India[J]. Ind J Fish, 2014, 61(3): 20-28.
[14] 田思泉, 钱卫国, 陈新军. 印度洋西北部海域鸢乌贼渔获量、渔获率和脱钩率的初步研究[J]. 上海水产大学学报, 2004, 13(3): 224-229. [15] LIPINSKI M R, UNDERHILL L G. Sexual maturation in squid: quantum or continuum[J]. S Afr J Mar Sci, 1995, 15: 207-223. doi: 10.2989/02577619509504844
[16] 刘必林, 陈新军, 钟俊生. 采用耳石研究印度洋西北海域鸢乌贼的年龄、生长和种群结构[J]. 大连水产学院学报, 2009, 24(3): 206-212. [17] 涂湘林, 张红, 邓文峰, 等. RESOlution激光剥蚀系统在微量元素原位微区分析中的应用[J]. 地球化学, 2011, 40(1): 83-98. [18] HU Z C, GAO S, LIU Y S, et al. Signal enhancement in laser ablation ICP-MS by addition of nitrogen in the central channel gas[J]. J Anal At Spectrom, 2008, 23(8): 1093-1101. doi: 10.1039/b804760j
[19] 陆化杰, 刘必林, 陈新军, 等. 智利外海茎柔鱼耳石微量元素研究[J]. 海洋渔业, 2013, 35(3): 269-277. doi: 10.3969/j.issn.1004-2490.2013.03.003 [20] LIU B L, CHEN X J, FANG Z, et al. A preliminary analysis of trace-elemental signatures in statoliths of different spawning cohorts for Dosidicus gigas off EEZ waters of Chile[J]. J Ocean Univ China, 2015, 14(6): 1059-1067. doi: 10.1007/s11802-015-2620-2
[21] LIU B L, CHEN X J, CHEN Y, et al. Geographic variation in statolith trace elements of the Humboldt squid, Dosidicus gigas, in high seas of Eastern Pacific Ocean[J]. Mar Biol, 2013, 160(11): 2853-2862. doi: 10.1007/s00227-013-2276-7
[22] NESIS K N. Distribution of recent cephalopod and implications for plio-pleistocene events[M]//WARNKE K, KEUPP H, BOLETZKY S V. Coleoid cephalopods throngh time. Berlin: Alãobiologische Abhandlungen, 2003: 199-224.
[23] JARRE A, CLEKW M R, PAULY D. Re-examination of growth estimates in oceanic squids: the case of Kondakovia longimana (Onychoteuthidae)[J]. ICES J Mar Sci, 1991, 48(2): 195-200. doi: 10.1093/icesjms/48.2.195
[24] 陆化杰, 陈新军, 马金. 西北太平洋柔鱼耳石微量元素[J]. 应用生态学报, 2014, 25(8): 2411-2417. [25] 陆化杰, 陈新军, 方舟. 西南大西洋阿根廷滑柔鱼耳石元素组成[J]. 生态学报, 2015, 35(2): 297-305. [26] IKEDA Y, ARAI N, SAKAMOTO W, et al. Relationship between statoliths and environmental variables in cephalopods[J]. Int J PIXE, 2001, 06(1n02): 339-345.
[27] IKEDA Y, ARAI N, SAKAMOTO W, et al. Comparison on trace elements in squid statoliths of different species′ origin: as available key for taxonomic and phylogenetic study[J]. Int J PIXE, 2011, 7(3n04): 141-146.
[28] IKEDA Y, ARAI N, SAKAMOTO W, et al. Preliminary report on PIXE analysis for trace elements of Octopus dofleini statoliths[J]. Fish Sci, 1999, 65(1): 161-162.
[29] RODHOUSE P K, ROBINSON K, GAJDATSY S B, et al. Gro- wth, age structure and environmental history in cephalopod Martialia hyadesi(Teuthoidea: Ommastrephidae)at the Antarctic Polor Frontal Zone and on the Patagonian Shelf Edge[J]. Antarct Sci, 1994, 6(2): 259-267.
[30] ZUMHOLZ K, HANSTEEN T H, PIATKOWSKI U, et al. Influence of temperature and salinity on the trace element incorporation into statioliths of the common cuttlefish(Sepia officinalis)[J]. Mar Biol, 2007, 151(4): 1321-1330.
[31] LEA D W, SHEN G T, BOYLE E A. Coralline barium records temporal variability in equatorial Pacific upwelling[J]. Nature, 1989, 340(6232): 373-376.
[32] FALLON S J, MCCULLOCH M T, WOESIK R, et al. Corals at their latitudinal limits: laser ablation trace element systematics in Porites from Shirigai Bay, Japan[J]. Earth Planet Sci Lett, 1999, 172(3): 21-238.
[33] RIBERGAARD M H, BUCH E. Oceanographic investigations off West Greenland 2004[R]. NAFO Sci Council Documents, 2004: 5-19.
[34] 刘必林, 陈新军, 陆化杰, 等. 头足类耳石[M]. 北京: 科学出版社, 2011: 161-178. [35] SUKRAMONGKOL N, PROMJINDA S, PROMMAS R. Age and reproduction of Sthenoteuthis oualaniensis in the Bay of Bengal[C]//'The Ecosystem-Based Fishery Management in the Bay of Bengal′, 14 December 2007, Phuket, Thailand. Bangkok, Thailand: Department of Fisheries (DOF), Ministry of Agriculture and Cooperatives, 2007: 195-205.
[36] HURLEY G V, ODENSE P, O′DOR R K, et al. Strontium labeling for verifying daily growth increments in the statoliths of the short-finned squid(Ilex illecebrosus)[J]. Can J Fish Aqua Sci, 1985, 42(2): 380-383.
[37] LIU B L, CHEN X J, CHEN Y, et al. Trace elements in the statoliths of jumbo flying squid off the Exclusive Economic Zones of Chile and Peru[J]. Mar Ecol Prog Ser, 2011, 429: 93-101.
-
期刊类型引用(17)
1. 杨禧越,刘永,李纯厚,唐广隆,张达娟,游奕来,潘淑芳,郑秋实,肖雅元,吴鹏. 珠江口万山群岛黄鳍棘鲷食性随年龄的变化特征. 中国水产科学. 2024(02): 219-231 .  百度学术
百度学术
2. 谢志伟,杨刚,庄平,赵峰,耿智,蒋俊,张涛. 基于鱼类完整性指数(F-IBI)的长江口生态健康状况评价. 海洋渔业. 2024(02): 140-150 .  百度学术
百度学术
3. 马菁菁,陈海刚,张喆,田斐,唐振朝,熊倩,张林宝. 2018—2023年珠江口鱼类群落结构变化及其与环境因子的关系. 南方水产科学. 2024(06): 62-73 .  本站查看
本站查看
4. 张翠萍,袁丽媚,吴妤莘,叶志权,陈晓莹,赖星星,李强,舒琥. 珠江口花鰶的生物学特征研究. 水生生物学报. 2023(04): 637-647 .  百度学术
百度学术
5. 刘文瑜,黄建强,戴国贤,刘国强,雷学铁,周永东,叶永昌. 珠江口伶仃洋春季鱼类群落结构及其与环境因子的RDA分析. 渔业信息与战略. 2023(01): 32-41 .  百度学术
百度学术
6. 唐广隆,刘永,吴鹏,孙典荣,肖雅元,王腾,谢雨芳,李纯然,石娟,钟智辉,李纯厚. 珠江口万山群岛海域春季渔业资源群落结构特征及其与环境因子的关系. 中国水产科学. 2022(08): 1198-1209 .  百度学术
百度学术
7. 李忠义,于小涛,关丽莎,林群,李娇,单秀娟,金显仕. 潮流与布放时间对青岛石雀滩海域海洋牧场刺网CPUE的影响. 中国水产科学. 2021(02): 195-204 .  百度学术
百度学术
8. 周卫国,丁德文,索安宁,何伟宏,田涛. 珠江口海洋牧场渔业资源关键功能群的遴选方法. 水产学报. 2021(03): 433-443 .  百度学术
百度学术
9. 徐鹏,谢木娇,周卫国,孙英婷,丁德文,索安宁. 近30年珠江口海域游泳动物经济物种群落结构变化特征. 应用海洋学学报. 2021(02): 239-250 .  百度学术
百度学术
10. 高天翔,高兵兵,李忠炉,单斌斌,宋娜. 基于线粒体DNA控制区序列的短棘鲾群体遗传学. 水产学报. 2020(05): 715-722 .  百度学术
百度学术
11. 林坤,麦广铭,王力飞,王学锋. 2015—2018年珠江口近岸海域鱼类群落结构及其稳定性. 水产学报. 2020(11): 1841-1850 .  百度学术
百度学术
12. 刘岩,吴忠鑫,杨长平,单斌斌,刘胜男,孙典荣. 基于Ecopath模型的珠江口6种增殖放流种类生态容纳量估算. 南方水产科学. 2019(04): 19-28 .  本站查看
本站查看
13. 应锐,蒋力,尹芳敏,黄建荣,黎祖福,王英永,冯建祥. 基于刺网、地笼的考洲洋游泳动物群落结构和多样性分析. 南方水产科学. 2019(04): 1-10 .  本站查看
本站查看
14. 张亚洲,卢占晖,朱文斌,毕远新. 东海北部桁杆拖虾渔获组成分析. 浙江海洋大学学报(自然科学版). 2019(05): 395-400+441 .  百度学术
百度学术
15. 蔡研聪,徐姗楠,陈作志,许友伟,江艳娥,杨长平. 南海北部近海渔业资源群落结构及其多样性现状. 南方水产科学. 2018(02): 10-18 .  本站查看
本站查看
16. 袁梦,汤勇,徐姗楠,陈作志,杨玉滔,江艳娥. 珠江口南沙海域秋季渔业资源群落结构特征. 南方水产科学. 2017(02): 18-25 .  本站查看
本站查看
17. 王学锋,吕少梁,黄一平,杨锋,李波. 基于流刺网调查的雷州湾游泳生物群落结构分析. 南方水产科学. 2017(03): 1-8 .  本站查看
本站查看
其他类型引用(11)




 下载:
下载:





 粤公网安备 44010502001741号
粤公网安备 44010502001741号
