Comparative and phylogenetic analysis of mitochondrial Cytochrome b gene and control region from natural triploid (Carassius auratus gibelio) in Chuzhou
-
摘要:
采用PCR产物直接测序法测定了14尾滁州鲫(Carassius auratus gibelio in Chuzhou)的线粒体细胞色素b(Cytochrome b,Cyt b)基因和控制区(D-loop)全序列,长度分别为1 141 bp和924 bp,且均无核苷酸变异位点。Cyt b基因的T、C、A和G含量分别为29.2%、27.8%、28.5%和14.5%;D-loop的T、C、A和G含量分别为33.2%、20.1%、32.6%和14.1%。2种序列中A+T含量(57.7%,65.8%)均明显大于G+C含量(42.3%,34.2%),且G含量偏低,显示了与其他水生动物线粒体核苷酸碱基含量相似的特征。通过对滁州鲫的控制区结构进行分析,识别了其终止序列区(ETAS)、中央保守区(CD)和保守序列区(CSB)的关键序列。滁州鲫与其他鲫属鱼类的Cyt b和D-loop序列均具有高度的相似性,分别为93%~100%和94%~99%。基于2种序列的分子系统进化树分析均表明,滁州鲫与方正鲫(C.auratus gibelio in Fangzheng)亲缘关系最近,而与来自日本的鲫类群亲缘关系最远。
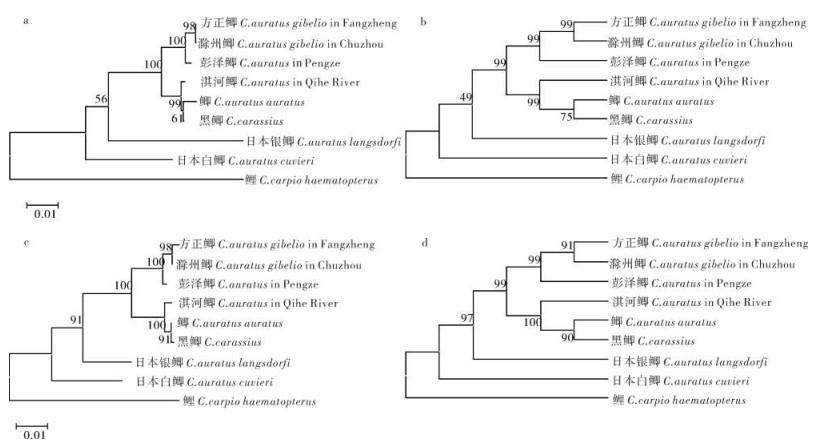
Abstract:The complete sequences of mitochondrial cytochrome b (Cyt b) gene and control region (D-loop) were amplified and sequenced in Carassius auratus gibelio, a natural triploid crucian carp in Chuzhou City of Anhui Province. No nucleotide variation sites were found in all sequences among 14 samples. The 1 141 bp Cyt b gene contained 29.2%, 27.8%, 28.5% and 14.5% of T, C, A and G, respectively; while 924 bp D-loop sequence contained 33.2%, 20.1%, 32.6% and 14.1% of T, C, A and G, respectively. The contents of A+T (57.5%, 65.8%) were significantly greater than those of G+C (42.3%, 34.2%) and G was the lowest among four nucleotides, the similar case as other aquatic animals. The key sequences of extended terminal associated sequences (ETAS), central domains (CSB-D, E and F) and conserved sequence blocks (CSB-1, CSB-2 and CSB-3) were identified. There was high sequence similarity between C.auratus gibelio in Chuzhou and other Carassius species recorded in GenBank based on Cyt b (93%~100%) and D-loop (94%~99%) sequences, respectively. The phylogenetic trees constructed by NJ and MP methods based on the two sequences indicated that the closest phylogenetic relationship was between C.auratus gibelio in Chuzhou and that in Fangzheng, while the farthest one was between C.auratus gibelio in Chuzhou and crucian carps in Japan.
-
Keywords:
- Carassius auratus gibelio in Chuzhou /
- Cyt b /
- control region /
- phylogenetic analysis
-
珠江口水域由于终年受珠江径流和南海陆架水的综合作用,造就了其独特的水环境特征,渔业资源群落结构也较为复杂[1]。珠江口近海渔业资源在南海渔业上具有举足轻重的地位,曾是许多经济鱼、虾、蟹类的产卵和索饵场所,也是多种经济鱼类入海或溯河洄游的通道[2]。近年来,由于过度捕捞及环境变化,造成了珠江口渔业资源的严重破坏,其群落结构也发生了变化。针对这种现状,中国已有很多学者对于珠江口水域低氧[3]、浮游生态及渔业等[4-8]方面进行了相关研究并提出了各自的建议,但未见不同网目尺寸刺网的渔获组成分析,对于单片、双重和三重刺网之间的渔获组成差异及多样性差异也未见报道。因此,有必要针对珠江口海域不同网目尺寸、不同结构的刺网渔业现状开展系统的渔获组成及网目选择性调查,以确定最适合该海域作业的刺网种类,为渔业管理提供科学参考。
该研究根据采集的40 mm、50 mm和60 mm网目尺寸的单片、双重和三重刺网的渔获数据,分析了不同网目尺寸刺网的渔获组成及多样性,并探讨了单片、双重和三重刺网捕捞对渔业资源的影响效应,为该水域渔业资源的保护和合理利用提供科学依据。
1. 材料与方法
1.1 试验时间和海域
试验于2014年9月16日~25日采用订制的单片、双重、三重刺网进行,延续时间为8 d,共完成了7个作业网次,并对试验网的全部渔获进行了测量。
试验捕鱼海域位于珠江口渔场(图 1),经纬度范围为21°49′N~21°56′N,113°53′E~113°55′E,水深30 m。
1.2 试验渔船
试验渔船为“粤阳东渔18208”,木质,船长24.85 m,型宽5.30 m,型深2.70 m,总吨位96.0 GT,净吨位34.0 t,2台主机总功率为324 kW,主机型号为NT855-M300和NH-250,功率分别为203 kW和121 kW。主作业方式为流刺网,船上配备雷达、垂直探鱼仪、避碰仪、GPS导航仪、单边带对讲机等导航助渔设备。
1.3 试验网具
试验的渔具分为单片刺网、双重刺网和三重刺网3种,每种刺网30片,总90片。每种刺网又按照小网目网衣的尺寸规格分为3种,每种10片。小网目网衣的网目尺寸分别为40 mm、50 mm和60 mm。刺网的上纲长度、装配高度、网目尺寸等详细参数见表 1。试验的刺网全部由舟山市乐达特种渔具有限公司统一制作。
表 1 试验刺网的主要参数Table 1. Main parameters of gillnets in this survey名称
name上纲长度/m
head line length装配高度/m
network height内套规格及用量inside norm 外套规格及用量outside norm 网片数量
network number长度/目
length高度/目
height网目/mm
mesh size长度/目
length高度/目
height网目/mm
mesh size单片刺网single wall gillnet 25 3 1 200 75.5 40 10 25 3 1 000 60.5 50 10 25 3 800 50.5 60 10 双重刺网double wall gillnet 25 3 1 200 90.5 40 668 12 120 10 25 3 1 000 73.5 50 668 12 120 10 25 3 800 60.5 60 668 12 120 10 三重刺网trammel gillnet 25 3 1 350 95.5 40 150 10 300 10 25 3 1 200 76.5 50 150 10 300 10 25 3 1 050 63.5 60 150 10 300 10 以上渔具的参数是试验前经课题承担单位、协作单位和渔具制作方共同讨论决定。在试验地点,将网片按照设计好的顺序连接起来,连接方式见图 2。试验时将不同网目尺寸的网片连接起来,考虑到不同网目尺寸刺网对渔获的接触概率,放网时采用“Z”字形进行放网。
1.4 数据处理
在调查过程中,记录渔船作业时的经纬度、作业时间、作业水深等。起网后对渔获物全部进行种类组成鉴定、分类计数、称质量,并对渔获进行生物学测定,体长(胴长、肛长、甲宽)、最大体周等以mm为单位,体质量以g为单位。样品所有个体鉴定到种。
根据南海珊瑚礁水域的生态特征及所获数据的具体情况,该研究采用相对重要性指数(IRI)、Margalef丰富度指数(D)、Shannon-Wiener多样性指数(H′)、Simpson多样性指数(C)、Pielou均匀度指数(J′)对渔获物种多样性进行分析研究[9-13],并采用欧氏距离法(Euclidian distance,ED)[14-16]建立不同网目规格下的相异性矩阵,判定珠江口渔业资源群落结构随网目规格变化的相异性,主要公式为:
1) 运用相对重要性指数IRI来评价渔获种类的优势种,IRI≥1 000为优势种;100≤IRI < 1 000为重要种;10≤IRI < 100为常见种;IRI < 10为少见种。
$$ \text{IRI}=\left(n_i /N+w_i W\right) \times F_i $$ 其中ni和wi分别为第i种渔获的个体数和质量,N和W分别为所有渔获的总数量和总质量,Fi表示出现频率百分比。
2) Margalef丰富度指数的一般模式为
$$ D_i=(S-1)/ \mathrm{ln} N $$ 以生物量为基础计算的Margalef丰富度指数公式为$ D_b=(S-1)/ \operatorname{ln} W$
3) Shannon-Wiener多样性指数:
$$ H_i^{\prime}=-\sum\limits_{i=1}^S\left(n_i /N\right) \ln \left(n_i /N\right) $$ 以生物量代替个体数来估算的Shannon-Wiener多样性指数为$ H_b^{\prime}=-\sum\limits_{i=1}^S\left(w_i /W\right) \ln \left(w_i /W\right)$
4) Simpson多样性指数:
$$ C_i=1-\sum\limits_{i=1}^S\left(n_i/ N\right)^2 $$ 应用生物量代替个体数估算的Simpson多样性指数为$ C_b=1-\sum\limits_{i=1}^s\left(w_i /W\right)^2$
5) Pielou均匀度指数:
$$ J_i^{\prime}=H_{i^{\prime}}^{\prime}/ \text { ln } S $$ 应用生物量代替个体数来估算的Pielou均匀度指数为$ J_b{ }^{\prime}=H_b{ }^{\prime} / \mathrm{ln} S$
6) 欧氏距离法:
$$ \mathrm{ED}=\left[\sum\limits_{i=1}^S\left(\boldsymbol{x}_ij-\boldsymbol{x}_{i k}\right)^2\right]^{1 / 2} $$ 式中xij为j样本中i种类的生物量,xik为k样本中i种类的生物量。
2. 结果
2.1 渔获组成
此次调查单片刺网一共鉴定渔获种类43种,其中鱼类34种,隶属于5目21科31属;虾类4种,隶属于1目1科4属;蟹类2种,隶属于1目1科1属;虾蛄类2种,隶属于1目1科2属。双重刺网一共鉴定渔获种类48种,其中鱼类42种,隶属于6目27科39属;虾类1种,隶属于1目1科1属;蟹类3种,隶属于1目1科2属;虾蛄类2种,隶属于1目1科2属。三重刺网一共鉴定渔获种类57种,其中鱼类45种,隶属于6目28科40属;虾类5种,隶属于1目2科5属;蟹类1种,隶属于1目1科1属;虾蛄类2种,隶属于1目1科2属;头足类1种,隶属于1目1科1属(表 2~表 4)。从目级水平分析,单片、双重、三重刺网都以鲈形目的种类数占绝对优势,分别为68.29%、63.27%和65.52%;从科级水平分析,单片刺网中石首鱼科的种类数最多(6种),其次为鲹科(4种)、虾蛄科(3种)和对虾科(3种);双重刺网中也是石首鱼科的种类数最多(6种),其次为鲹科(5种)、鳀科(3种)和梭子蟹科(3种);三重刺网中石首鱼科、对虾科、鲹科的种类数都为6种。单片、双重、三重刺网在40 mm、50 mm和60 mm网目下所捕获的种类数、尾数和质量见表 5。3种刺网的渔获种类数、尾数和质量都随着网目尺寸的增大而减少,尤其是单片刺网,60 mm网目下的渔获质量只有40 mm网目下的18.6%。且除了60 mm网目外,在40 mm和50 mm网目下,三重刺网的渔获种类数、尾数和质量都是最高的,而在60 mm网目下因渔获急剧减少而并未呈现该种现象。
表 2 单片刺网渔获种类Table 2. Catch composition of single wall gillnet分类
classification种类
species分类
classification种类
species鱼类fish 白姑鱼Argyrosomus argentatus 鱼类fish 丽叶鲹Caranx kalla 刺鲳Psenopsis anomala 六指马鲅Polydactylus sextarius 粗顶美尾 
鹿斑鲾Secutor ruconius 大黄鱼Larimichthys crocea 皮氏叫姑鱼Johnius belengeri 大甲鲹Megalaspis cordyla 乔氏台雅鱼Daya jordani 带鱼Trichiurus lepturus 日本金线鱼Nemipterus japonicus 短带鱼T. brevis 乳香鱼Lactarius lactarius 短尾大眼鲷Priacanthus macracanthus 深水金线鱼N. bathybius 多齿蛇鲻Saurida tumbil 弯 
二长棘鲷Paerargyrops edita Tanaka 羽鳃鲐Rastrelliger kanagurta 海鳗Muraenesox cinereus 中华青鳞鱼Harengula nymphaea 褐斑三线舌鳎Cynoglossus trigrammus 竹荚鱼Trachurus japonicus 红丝 
蟹类crab 红星梭子蟹Portunus sanguinolentus 黄斑篮子鱼Siganus oramin 三疣梭子蟹P. trituberculatus 黄姑鱼Nibea albiflora 虾姑类squillid 棘突猛虾蛄Harpiosquilla raphidea 黄鲫Setipinna taty 断脊口虾蛄Oratosquillina interrupta 截尾白姑鱼Pennahia anea 口虾蛄O. oratoria 孔 
虾类shrimp 长足鹰爪虾Trachypenaeus longipes 
刀额新对虾Metapenaeus ensis 蓝圆鲹Decapterus maruadsi 中国对虾Penaeus chinensis 鳓Ilisha elongata 中华管鞭虾Solenocera crassicornis 李氏  表 3 双重刺网渔获种类Table 3. Catch composition of double wall gillnet
表 3 双重刺网渔获种类Table 3. Catch composition of double wall gillnet分类
classification种类
species分类
classification种类
species鱼类fish 白姑鱼 鱼类fish 
斑鳍天竺鱼Apogonichthys carinatus 蓝圆鲹 赤鼻棱鳀Thryssa kammalensis 鳓 粗毒鲉Synanceia Linnaeus 丽叶鲹 大黄鱼 六指马鲅 大甲鲹 鹿斑鲾 带鱼 皮氏叫姑鱼 短棘鲾Leiognathus equulus 乳香鱼 短尾大眼鲷 少牙斑鲆Pseudorhombus oligodon 二长棘鲷 深水金线鱼 海鳗 
褐斑三线舌鳎 弯 黑尾吻鳗Rhynchoconger ectenurus 印度鲬Platycephalus indicus 红丝 
油 
黄斑篮子鱼 长棘银鲈Gerres filamentosus 黄姑鱼 中颌棱鳀Thryssa mystax 黄鲫 中华青鳞鱼 黄鳍鲷Acanthopagrus latus 棕斑腹刺鲀Gastrophysus spadiceus 黄鳍马面鲀Navodon xanthopterus 蟹类crab 红星梭子蟹 尖吻裸颊鲷Lethrinus olivaceus 三疣梭子蟹 截尾白姑鱼 锈斑鲟Charybdis feriata 金鲳Trachinotus ovatus 虾类shrimp 长足鹰爪虾 金带细鲹Selaroides leptolepis 虾姑类squillid 断脊口虾蛄 孔 
口虾蛄 表 4 三重刺网渔获种类Table 4. Catch composition of trammel gillnet分类
classification种类
species分类
classification种类
species鱼类fish 白姑鱼 鱼类fish 六指马鲅 斑鳍天竺鱼 鹿斑鲾 赤鼻棱鳀 皮氏叫姑鱼 刺鲳 乔氏台雅鱼 大黄鱼 日本 
大甲鲹 乳香鱼 带鱼 深水金线鱼 单角革鲀Aluterus monoceros 弯 
短带鱼 印度鲬 短棘鲾 油 
短尾大眼鲷 羽鳃鲐 二长棘鲷 中颌棱鳀 海鳗 中华青鳞鱼 褐斑三线舌鳎 竹䇲鱼 红丝 
棕斑腹刺鲀 黄斑蓝子鱼 蟹类crab 红星梭子蟹 黄带副绯鲤Parupeneus chrysopleuron 三疣梭子蟹 黄姑鱼 虾类shrimp 墨吉对虾Penaeus merguiensis 黄鳍鲷 日本对虾P. japonicus 尖吻裸颊鲷 中华管鞭虾 截尾白姑鱼 中国对虾 金带细 长足鹰爪虾 孔 
刀额新对虾 
亨氏仿对虾Parapenaeopsis hungerfordi 蓝颊鹦嘴鱼Scarus janthochir 虾姑类squillid 口虾蛄 蓝圆鲹 棘突猛虾蛄 鳓 断脊口虾蛄 丽叶鲹 头足类cephalopods 莱氏拟乌贼Sepioteuthis lessoniana 六带石斑鱼Epinephelus sexfasciatus 表 5 不同网目规格下捕获的种类数、尾数和质量Table 5. Species number, total number and weight of different gillnets40 mm 50 mm 60 mm 种类数
species number尾数
number质量/g
weight种类数
species number尾数
number质量/g
weight种类数
species number尾数
number质量/g
weight单片刺网single wall gillnet 33 367 19 793 26 172 14 745 13 28 3 685 双重刺网double wall gillnet 32 364 23 728 30 237 20 396 21 137 9 600 三重刺网trammel gillnet 42 442 31 540 31 290 26 963 18 83 8 482 表 6 不同网目规格的优势种Table 6. Dominant species of different gillnets40 mm 50 mm 60 mm 种类species IRI 种类species IRI 种类species IRI 单片刺网single walll gillnet 深水金线鱼 4 641.41 深水金线鱼 6 868.63 深水金线鱼 2 953.67 中华青鳞鱼 2 583.07 皮氏叫姑鱼 3 381.54 白姑鱼 2 765.36 蓝圆鲹 2 148.44 白姑鱼 2 067.69 黄姑鱼 1 716.18 皮氏叫姑鱼 2 107.55 褐斑三线舌鳎 1 398.74 红星梭子蟹 1 084.71 白姑鱼 1 503.47 海鳗 1 019.82 褐斑三线舌鳎 1 051.16 双重刺网double walll gillnet 深水金线鱼 6 160.73 深水金线鱼 6 771.52 红星梭子蟹 3 005.69 中华青鳞鱼 1 911.71 褐斑三线舌鳎 1 875.05 深水金线鱼 2 578.53 红星梭子蟹 1 467.75 白姑鱼 1 166.90 棕斑腹刺鲀 2 281.93 皮氏叫姑鱼 1 288.71 皮氏叫姑鱼 1 162.40 白姑鱼 1 938.79 蓝圆鲹 1 181.01 棕斑腹刺鲀 1 027.45 蓝圆鲹 1 641.69 黄姑鱼 1 425.30 三重刺网trammel gillnet 深水金线鱼 6 118.68 深水金线鱼 5 963.76 红星梭子蟹 5 910.40 褐斑三线舌鳎 2 680.59 棕斑腹刺鲀 1 912.04 棕斑腹刺鲀 4 807.47 皮氏叫姑鱼 1 547.72 白姑鱼 1 131.36 白姑鱼 2 554.69 中华青鳞鱼 1 501.97 海鳗 1 021.36 深水金线鱼 1 849.71 海鳗 1 283.31 褐斑三线舌鳎 1 009.39 红星梭子蟹 1 277.63 蓝圆鲹 1 218.05 2.2 优势种
根据珠江口渔获物个体大小悬殊的特点,采用相对重要性指数(IRI)作为优势种的度量指标。表 6列出了不同网目规格下的优势种及其IRI,深水金线鱼(Nemipterus bathybius)是单片、双重和三重刺网不同网目下的共同优势种,这种现象在单片刺网中尤为明显。40 mm网目下,除了深水金线鱼之外,中华青鳞鱼(Harengula nymphaea)、蓝圆鲹(Decapterus maruadsi)、皮氏叫姑鱼(Johnius belengeri)也都是3种刺网的共同优势种,但三重刺网的优势种种类数相对较多,且红星梭子蟹(Portunus sanguinolentus)、褐斑三线舌鳎(Cynoglossus trigrammus)、棕斑腹刺鲀(Gastrophysus spadiceus)等底层鱼类的渔获比例有了明显的增加;50 mm网目下,除了深水金线鱼之外,白姑鱼(Argyrosomus argentatus)、褐斑三线舌鳎也都是3种刺网的共同优势种,与40 mm网目一样,三重刺网的优势种种类数相对较多,且底层鱼类的渔获比例也有所增加;60 mm网目下,除了深水金线鱼之外,白姑鱼、红星梭子蟹也都是3种刺网的共同优势种,与40 mm和50 mm网目一样,三重刺网底层鱼类的渔获比例有了明显增加,且这种现象在60 mm网目下尤为明显,但三重刺网的优势种种类数并不是3种刺网中最多。
2.3 生物多样性指数
2.3.1 Margalef丰富度指数(D)
无论是以个体数还是以生物量计算,单片、双重、三重刺网的D都随着网目尺寸的增大而呈现下降趋势,而单片刺网与双重刺网、三重刺网的D差异不大,三重刺网的物种丰富度相对较大,单片刺网的物种丰富度相对较小(表 7)。
表 7 不同网目规格下的渔获生物多样性指数Table 7. Diversity indices of catch by different gillnets网目尺寸
/mm mesh size种类数
numberMargalef指数
Margalef indexShannon-Wiener指数
Shannon-Wiener indexSimpson指数
Simpson indexPielou均匀度
Pielou evenness indexDi Db Hi′ Hb′ Ci Cb Ji′ Jb′ 单片刺网single wall gillnet 40 33 5.42 3.23 2.56 2.56 0.88 0.89 0.73 0.73 50 26 4.86 2.60 2.45 2.17 0.85 0.80 0.75 0.67 60 13 3.60 1.46 2.33 2.15 0.89 0.86 0.91 0.84 双重刺网double wall gillnet 40 32 5.26 3.08 2.44 2.36 0.86 0.85 0.70 0.68 50 30 5.30 2.92 2.60 2.37 0.87 0.82 0.77 0.70 60 21 4.07 2.18 2.38 2.43 0.88 0.89 0.78 0.80 三重刺网trammel gillnet 40 42 6.73 3.96 2.64 2.45 0.87 0.85 0.71 0.65 50 31 5.29 2.94 2.70 2.45 0.89 0.85 0.79 0.71 60 18 3.85 1.88 2.08 2.06 0.82 0.81 0.72 0.71 2.3.2 Shannon-Wiener多样性指数(H′)
不同网目下,单片、双重、三重刺网的H′差异不大。40 mm网目的Hi′,最高的是三重刺网,最低的是双重刺网,而Hb′最高的是单片刺网,最低的也是双重刺网;50 mm网目无论是以个体数还是生物量计算的H′,都呈现三重刺网>双重刺网>单片刺网的趋势;60 mm网目无论是Hi′还是Hb′,都呈现双重刺网>单片刺网>三重刺网的趋势。
2.3.3 Simpson多样性指数(C)
不同网目单片、双重、三重刺网的C差异也不大。40 mm网目Ci,最高的是单片刺网,最低的是双重刺网,Cb最高的也是单片刺网,最低的却是三重刺网;50 mm网目无论是以个体数还是生物量计算,C都呈现三重刺网>双重刺网>单片刺网的趋势;60 mm网目的Ci,最高的是单片刺网,最低的是三重刺网,而Cb最高的是双重刺网,最低的也是三重刺网。
2.3.4 Pielou均匀度指数(J′)
40 mm网目Ji′最高的是单片刺网,最低的是双重刺网,而Jb′则呈现单片刺网>双重刺网>三重刺网的趋势;50 mm网目无论以个体数还是生物量计算,J′都呈现三重刺网>双重刺网>单片刺网的趋势;60 mm网目无论以个体数还是生物量计算,J′却都呈现单片刺网>双重刺网>三重刺网的趋势。
3. 讨论
3.1 优势种的差异
詹海刚[7]把珠江口鱼类划分为淡水、河口和沿岸3个群落类型,沿岸群落的优势种为丽叶鲹、带鱼、银鲳(Pampus argenteus)等海水鱼类和杜氏棱鳀(Thryssa dussumieri)、赤鼻棱鳀等咸淡水鱼类,而王迪和林昭进[2]将珠江口的鱼类群落结构划分为淡水区、咸淡水区、沿岸区和近海区4个区域,沿岸区优势种为丽叶鲹、杜氏棱鳀、棘头梅童鱼(Collichthys lucidus)、银鲳等,与该研究结果有较大差异。这主要是由于不同的作业方式和作业时间造成的。李永振等[1]所用的数据是1997年~1998年掺缯网和尖尾罟网的周年月度鱼类采样数据,但采样范围只在内伶仃岛周围,其鱼类群落季节变化的分析结果只能代表河口、咸淡水水域,与该研究对比意义不大。
3.2 以个体数和生物量计算的多样性指数比较
物种多样性指数可以作为描述群落物种组成特征的重要参数指标,它与群落的生态恢复功能密切相关[17-18]。为了明确以生物量和个体数分别计算的多样性指数之间的差异,该研究采用了成对数据的t检验,计算的D、H′、C和J′的P分别为5.21E-09、0.01、0.03和0.01,P < 0.05,说明以个体数和生物量计算的多样性指数存在显著差异。郁尧山等[19]用以上2种方法计算的浙江北部岛礁周围海域鱼类的H′,结果无显著相关,与该研究一致。然而陈国宝等[12]用以上2种方法计算的南海主要珊瑚礁水域鱼类的D、H′、C显著相关,费鸿年等[20]计算的南海北部大陆架水域鱼类的H′也是显著相关。这可能是由于浙江北部岛礁水域和珠江口水域捕捞强度和水域污染过大而造成的渔业资源群落结构发生变化,以及研究海域、研究对象不同所导致的。
无论是以个体数还是生物量计算,只有50 mm网目下计算的D、H′、C和J′都呈现相同的变动趋势,即三重刺网>双重刺网>单片刺网(表 4)。这主要是由于40 mm网目更容易因缠绕而捕获幼鱼,60 mm网目下渔获尾数又太少所致,而50 mm网目既能保证一定的渔获量,维持渔民收入,又能减少幼鱼比例。
3.3 群落结构相异性分析
表 8反映了研究群落在不同网目规格下物种生物量组成差异的相异性矩阵,欧氏距离越大表明相对应的渔业资源群落结构的差异性越高。ED最高值为11.84,为M40和M602个样本间的差异性程度,表明三重刺网40 mm网目和60 mm网目下渔业资源群落结构的差异性最高,其次为11.64和11.03,分别是M40和O60、T60间的差异性程度,说明不同网目尺寸下刺网的渔业资源群落结构的差异性较高;ED最小值为2.17,其次为2.46和2.82,都为同一网目下不同网具的差异性程度,表明同一网目下3种刺网的渔业资源群落结构差异性不大。
表 8 不同网目规格下群落结构的欧氏距离矩阵Table 8. Euclidian distance matrix of community structure of different gillnetsO40 O50 O60 T40 T50 T60 M40 M50 M60 O40 O50 4.26 O60 5.83 5.97 T40 5.18 4.34 8.56 T50 5.39 2.82 7.74 3.26 T60 5.56 5.70 2.46 7.75 7.01 M40 7.08 7.15 11.64 4.56 5.65 11.03 M50 6.36 5.61 9.50 5.75 4.19 8.76 5.05 M60 6.63 6.51 3.50 8.65 7.85 2.17 11.84 9.14 注: O40. 40 mm网目下的单片刺网;T40. 40 mm网目下的双重刺网;M40. 40 mm网目下的三重刺网;以此类推
Note: O40.the single wall gillnet with 40 mm mesh size;T40.the double wall gillnet with 40 mm mesh size;M40.the trammell gillnet with 40 mm mesh size,and by this analogy.3.4 刺网渔业资源群落结构的影响因素
渔业资源群落演替是捕捞及多种环境波动变化等多因素共同作用的结果[21-22],而采用刺网进行渔业资源群落研究时,由于刺网采集的种类与网目大小有较大关系,在鱼类群落研究中常常通过使用多层不同规格网目的刺网进行采样[23]。该研究从40 mm、50 mm和60 mm 3种不同网目尺寸下探讨了单片、双重和三重刺网的渔获组成、多样性及群落结构相异性,分析刺网捕捞对渔业资源群落结构的影响效应,具有一定的可行性和准确性。结果表明只有严格控制50 mm网目的刺网网具可捕标准,才能在保证一定渔获量的同时,维持渔业资源群落结构的稳定。但由于条件有限,该研究未能对各项环境因子对渔业资源群落演替过程中所起的作用效果进行相关分析[24],以及对整个生态系统结构功能及其变化机制的研究,具有一定的局限性,有待以后完善。
-
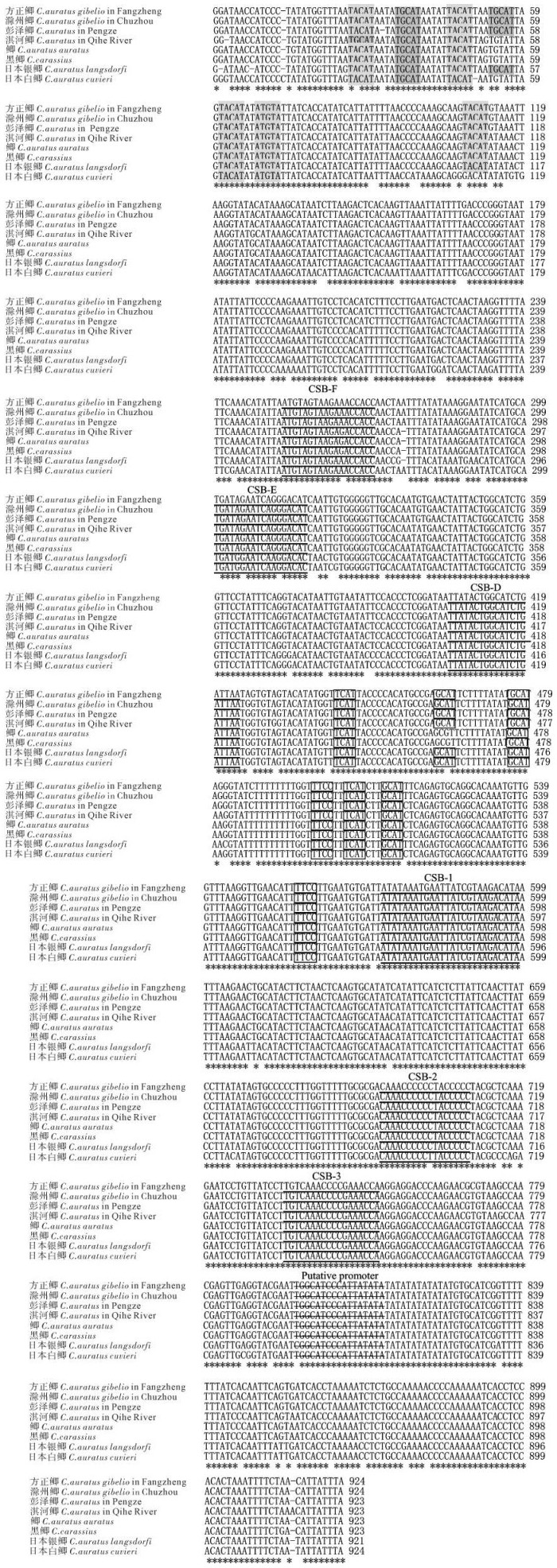
图 1 鲫属鱼类线粒体控制区序列及结构
*. 相同的核苷酸位点;-. 缺失位点;中央保守序列(CSB-F,CSB-E,CSB-D)和保守序列(CSB-1,CSB-2,CSB-3) 用下划线表示;终止相关序列(TAS)和其反向互补序列(ATGTA)用阴影表示;短小重复序列用方框表示;删除线表示启动子序列
Figure 1. Sequence and structure of mitochondrial DNA control region in genus Carassius
*. the same base site; -. gaps required for alignment; the conserved blocks (CSB-F, CSB-E, CSB-D) in central conserved sequence domain and conserved sequence blocks (CSB1, CSB2, CSB3) in conserved sequence blocks domain are underlined; TAS motifs (TACAT) and palindromic motifs (ATGTA) are shadowed; short repeated sequences are framed; promoters are indicated with strikethroughs.
表 1 基于线粒体Cyt b基因和D-loop序列的滁州鲫的碱基组成
Table 1 Base composition of mitochondrial Cyt b and D-loop sequences of C.auratus gibelio in Chuzhou
% 序列
sequence密码子
condon碱基组成 base composition T C A G A+T C+G 细胞色素b Cyt b 第1位first site 23.6 26.2 25.2 24.9 48.8 51.2 第2位second site 41.8 25.0 20.0 13.2 61.8 38.2 第3位third site 2.4 32.1 40.3 5.3 62.7 37.3 总计total 29.3 27.8 28.5 14.5 57.7 43.3 控制区D-loop 总计total 33.2 20.1 32.6 14.1 65.8 34.2 表 2 滁州鲫与其他鱼类间线粒体Cyt b和D-loop区的序列相似率
Table 2 Similarity of nucleotide sequences of mitochondrial Cyt b or D-loop between C.auratus gibelio in Chuzhou and other fishes
% 物种
species细胞色素b
Cyt b控制区
D-loop domain方正鲫 C.auratus gibelio in Fangzheng 100 99 彭泽鲫 C.auratus in Pengze 99 99 淇河鲫 C.aurutus in Qihe River 98 97 鲫 C.auratus auratus 98 97 黑鲫 C.carassius 98 97 日本银鲫 C.auratus langsdorfi 94 96 日本白鲫 C.auratus cuvieri 93 94 鲤 C.carpio haematopterus 88 89 -
[1] 张克俭, 万全, 李公行, 等. 滁州鲫的形态学和血清蛋白电泳谱型[J]. 水产学报, 1996, 20(4): 352-356. https://xueshu.baidu.com/usercenter/paper/show?paperid=be53c9802dddecec1d656391de70e631&site=xueshu_se [2] 张克俭, 万全, 李公行, 等. 滁州鲫染色体组型的研究[J]. 中国水产科学, 1995, 2(4): 8-15. doi: 10.3321/j.issn:1005-8737.1995.04.006 [3] 徐广友, 万全, 袁兆祥, 等. 滁州鲫雌核发育的细胞学研究[J]. 安徽农业大学学报, 2009, 36(4): 533-537. [4] 凌武海, 任信林. 天然滁州鲫氨基酸成分分析与营养价值评价[J]. 水产养殖, 2011, 32(1): 50-52. doi: 10.3969/j.issn.1004-2091.2011.01.013 [5] 姚继花, 楼允东, 江涌. 我国六个地区银鲫种群线粒体DNA多态性研究[J]. 水产学报, 1998, 22(4): 289-295. doi: 10.1017/S0266078400010713 [6] 凌武海, 马明发, 袁兆祥, 等. 滁州鲫、方正银鲫和彭泽鲫分子遗传差异的分析[J]. 安徽农业科学, 2009, 37(28): 13482-13483, 13485. doi: 10.3969/j.issn.0517-6611.2009.28.023 [7] 肖武汉, 张亚平. 鱼类线粒体DNA的遗传与进化[J]. 水生生物学报, 2000, 24(4): 384-391. doi: 10.3321/j.issn:1000-3207.2000.04.014 [8] 郭新红, 刘少军, 刘巧, 等. 鱼类线粒体DNA研究新进展[J]. 遗传学报, 2004, 31(9): 983-1000. https://xueshu.baidu.com/usercenter/paper/show?paperid=25713e1ff4e884760e4e4364b31966b8&site=xueshu_se&hitarticle=1 [9] XIAO Wuhan, ZHANG Yaping, LIU Huanzhang. Molecular systematics of Xenocyprinae (Teleostei: Cyprinidae): taxonomy, biogeography, and coevolution of a special group restricted in East Asia[J]. Mol Phylogenet Evol, 2001, 18(2): 163-173. doi: 10.1006/mpev.2000.0879
[10] PERDICES A, DOADRIO I. The molecular systematics and biogeography of the European cobitids based on mitochondrial DNA sequences[J]. Mol Phylogenet Evol, 2001, 19(3): 468-478. doi: 10.1006/mpev.2000.0900
[11] TANG Qiongying, LIU Huanzhang, MAYDEN R, et al. Comparison of evolutionary rates in the mitochondrial DNA cytochrome b gene and control region and their implications for phylogeny of the Cobitoidea (Teleostei: Cypriniformes)[J]. Mol Phylogenet Evol, 2006, 39(2): 347-357. doi: 10.1016/j.ympev.2005.08.007
[12] YU Meiling, HE Shunping. Phylogenetic relationships and estimation of divergence times among Sisoridae catfishes[J]. Sci China Life Sci, 2012, 55(4): 312-320. doi: 10.1007/s11427-012-4305-z
[13] ANG Jinqun, TANG Wenqiao, LIAO Teyu, et al. Phylogeographical analysis on Squalidus argentatus recapitulates historical landscapes and drainage evolution on the island of Taiwan and mainland China[J]. Int J Mol Sci, 2012, 13(12): 1405-1425. doi: 10.3390/ijms13021405
[14] ZHAO Kai, DUAN Ziyuan, PENG Zuogang, et al. Phylogeography of the endemic Gymnocypris chilianensis (Cyprinidae): sequential westward colonization followed by allopatric evolution in response to cyclical Pleistocene glaciations on the Tibetan Plateau[J]. Mol Phylogenet Evol, 2011, 59(2): 303-310. doi: 10.1016/j.ympev.2011.02.001
[15] AVISE J C. Gene trees and organismal histories: a phylogenetic approach to population biology[J]. Evolution, 1989, 43(6): 1192-1208. doi: 10.2307/2409356
[16] YANG Guang, XIAO Mingsong, YU Yanyan, et al. Genetic variation at mtDNA and microsatellite loci in Chinese longsnout catfish (Leiocassis longirostris)[J]. Mol Biol Rep, 2012, 39(5): 4605-4617. doi: 10.1007/s11033-011-1252-x
[17] ALTER S E, PALUMBI S R. Comparing evolutionary patterns and variability in the mitochondrial control region and Cytochrome b in three species of baleen whales[J]. J Mol Evol, 2009, 68(1): 97-111. doi: 10.1007/s00239-008-9193-2
[18] LUNT D H, WHIPPLE L E, HYMAN B C. Mitochondrial DNA variable number tandem repeats (VNTRs): utility and problems in molecular ecology[J]. Mol Ecol, 1998, 7(11): 1441-1455. doi: 10.1046/j.1365-294x.1998.00495.x
[19] PEREIRA S L, GRAU E T, WAJNTAL A. Molecular architecture and rates of DNA substitutions of the mitochondrial control region of cracid birds[J]. Genome, 2004, 47(3): 535-545. doi: 10.1139/g04-009
[20] LIU Guangxun, ZHOU Jian, ZHOU Dinggang. Mitochondrial DNA reveals low population differentiation in elongate loach, Leptobotia elongata (Bleeker): implications for conservation[J]. Environ Biol Fish, 2012, 93(1): 393-402. doi: 10.1007/s10641-011-9927-7
[21] 李娜, 陈少波, 谢起浪, 等. 闽浙地区香鱼线粒体Cyt b基因和D-loop区序列多态性分析[J]. 遗传, 2008, 30(7): 919-925. doi: 10.3321/j.issn:0253-9772.2008.07.018 [22] 赵亮, 谢本贵, 刘志瑾, 等. 太湖新银鱼线粒体D-loop和Cyt b片段序列结构与进化速率比较[J]. 动物学杂志, 2010, 45(2): 27-38. https://www.doc88.com/p-9971835339647.html [23] GALTIER N, GOUY M, GAUTIER C. Seaview and Phylo_ win: two graphic tools for sequence alignment and molecular phylogeny[J]. Comput Appl Biosci, 1996, 12(6): 543-548. doi: 10.1093/bioinformatics/12.6.543
[24] THOMPSON J D, GIBSON T J, PLEWNIAK F. The Clustal X windows interface: flexible strategies for multiple sequences alignment aided by quality analysis tools[J]. Nucleic Acids Res, 1997, 25(4): 4876-4882. doi: 10.1093/nar/25.24.4876
[25] KUMAR S, DUDLEY J, NEI M, et al. MEGA: a biologist-centric software for evolutionary analysis of DNA and protein sequences[J]. Brief Bioinform, 2008, 9(4): 299-306. doi: 10.1093/bib/bbn017
[26] HOCHACHKA P, MOMMSEN T P. Biochemistry and molecular biology of fish[M]. London: Elsevier Science Publishers, 1993: 1-38. https://www.sciencedirect.com/bookseries/biochemistry-and-molecular-biology-of-fishes
[27] CANTATORE P, ROBERTI M, PESOLE G, et al. Evolutionary analysis of cytochrome b sequences in some perciformes: evidence for a slower rate of evolution than in mammals[J]. J Mol Evol, 1994, 39(6): 589-597. doi: 10.1007/BF00160404
[28] 刘焕章. 鱼类DNA控制区的结构和进化: 以鳑鲏为例[J]. 自然科学进展, 2002, 12(3): 266-270. doi: 10.3321/j.issn:1002-008X.2002.03.008 [29] 唐琼英, 刘焕章, 杨秀平. 沙鳅亚科鱼类线粒体DNA控制区结构分析及系统发育关系的研究[J]. 水生生物学报, 2005, 29(6): 645-653. doi: 10.3321/j.issn:1000-3207.2005.06.008 [30] 刘良国, 杨品红, 王文彬, 等. 洞庭青鲫与其他六个鲫鱼品系线粒体DNA控制区的比较分析[J]. 水生生物学报, 2010, 34(2): 378-387. doi: 10.3724/SP.J.1035.2010.00378 [31] 苏天凤, 江世贵, 马之明, 等. 二长棘犁齿鲷线粒体DNA控制区结构和进化[J]. 南方水产科学, 2012, 8(6): 1-8. doi: 10.3969/j.issn.2095-0780.2012.06.001 [32] 马明发, 张克俭, 凌武海, 等. 三种群银鲫形态特征的比较研究[J]. 河北渔业, 2009(4): 17-19. doi: 10.3969/j.issn.1004-6755.2009.04.005 [33] 程磊, 常玉梅, 鲁翠云, 等. 鲫属鱼类DNA条码及种与亚种划分[J]. 动物学研究, 2012, 33(5): 463-472. doi: 10.3724/SP.J.1141.2012.05463 [34] 王姝妍. 古环境的变化和人工选择对鲫属鱼类遗传结构的影响[D]. 合肥: 中国科学技术大学, 2013. http://www.51papers.com/lw/70/8/wz1915427.htm [35] 乐佩琦. 硬骨鱼纲· 鲤形目· 下卷[M]. 北京: 科学技术出版社, 2000: 427-434. https://www.las.ac.cn/front/book/detail?id=91264d2d652fd346c5ed4c5ceb712232 [36] HOSOYA K. Cyprinidae[M]//NAKABO T. Fishes of Japan with pictorial keys to the species. Tokyo: Tokai University Press, 2002: 253-254.
[37] MURAKAMI M, MATSUBA C, FUJITANI H. The maternal origins of the triploid ginbuna (Carassius auratus langsdorfi): phylogenetic relationships within the C. auratus taxa by partial mitochondrial D-loop sequencing[J]. Genes Genet Syst, 2001, 76(1): 25-32. doi: 10.1266/ggs.76.25
[38] 付小全, 曾柳根, 洪一江, 等. 天然三倍体鲫鱼突变体萍乡肉红鲫线粒体细胞色素b基因序列分析[J]. 动物学杂志, 2009, 44(2): 97-101. http://dwxzz.ioz.ac.cn/dwxb/article/abstract/20090217?st=article_issue -
期刊类型引用(17)
1. 杨禧越,刘永,李纯厚,唐广隆,张达娟,游奕来,潘淑芳,郑秋实,肖雅元,吴鹏. 珠江口万山群岛黄鳍棘鲷食性随年龄的变化特征. 中国水产科学. 2024(02): 219-231 .  百度学术
百度学术
2. 谢志伟,杨刚,庄平,赵峰,耿智,蒋俊,张涛. 基于鱼类完整性指数(F-IBI)的长江口生态健康状况评价. 海洋渔业. 2024(02): 140-150 .  百度学术
百度学术
3. 马菁菁,陈海刚,张喆,田斐,唐振朝,熊倩,张林宝. 2018—2023年珠江口鱼类群落结构变化及其与环境因子的关系. 南方水产科学. 2024(06): 62-73 .  本站查看
本站查看
4. 张翠萍,袁丽媚,吴妤莘,叶志权,陈晓莹,赖星星,李强,舒琥. 珠江口花鰶的生物学特征研究. 水生生物学报. 2023(04): 637-647 .  百度学术
百度学术
5. 刘文瑜,黄建强,戴国贤,刘国强,雷学铁,周永东,叶永昌. 珠江口伶仃洋春季鱼类群落结构及其与环境因子的RDA分析. 渔业信息与战略. 2023(01): 32-41 .  百度学术
百度学术
6. 唐广隆,刘永,吴鹏,孙典荣,肖雅元,王腾,谢雨芳,李纯然,石娟,钟智辉,李纯厚. 珠江口万山群岛海域春季渔业资源群落结构特征及其与环境因子的关系. 中国水产科学. 2022(08): 1198-1209 .  百度学术
百度学术
7. 李忠义,于小涛,关丽莎,林群,李娇,单秀娟,金显仕. 潮流与布放时间对青岛石雀滩海域海洋牧场刺网CPUE的影响. 中国水产科学. 2021(02): 195-204 .  百度学术
百度学术
8. 周卫国,丁德文,索安宁,何伟宏,田涛. 珠江口海洋牧场渔业资源关键功能群的遴选方法. 水产学报. 2021(03): 433-443 .  百度学术
百度学术
9. 徐鹏,谢木娇,周卫国,孙英婷,丁德文,索安宁. 近30年珠江口海域游泳动物经济物种群落结构变化特征. 应用海洋学学报. 2021(02): 239-250 .  百度学术
百度学术
10. 高天翔,高兵兵,李忠炉,单斌斌,宋娜. 基于线粒体DNA控制区序列的短棘鲾群体遗传学. 水产学报. 2020(05): 715-722 .  百度学术
百度学术
11. 林坤,麦广铭,王力飞,王学锋. 2015—2018年珠江口近岸海域鱼类群落结构及其稳定性. 水产学报. 2020(11): 1841-1850 .  百度学术
百度学术
12. 刘岩,吴忠鑫,杨长平,单斌斌,刘胜男,孙典荣. 基于Ecopath模型的珠江口6种增殖放流种类生态容纳量估算. 南方水产科学. 2019(04): 19-28 .  本站查看
本站查看
13. 应锐,蒋力,尹芳敏,黄建荣,黎祖福,王英永,冯建祥. 基于刺网、地笼的考洲洋游泳动物群落结构和多样性分析. 南方水产科学. 2019(04): 1-10 .  本站查看
本站查看
14. 张亚洲,卢占晖,朱文斌,毕远新. 东海北部桁杆拖虾渔获组成分析. 浙江海洋大学学报(自然科学版). 2019(05): 395-400+441 .  百度学术
百度学术
15. 蔡研聪,徐姗楠,陈作志,许友伟,江艳娥,杨长平. 南海北部近海渔业资源群落结构及其多样性现状. 南方水产科学. 2018(02): 10-18 .  本站查看
本站查看
16. 袁梦,汤勇,徐姗楠,陈作志,杨玉滔,江艳娥. 珠江口南沙海域秋季渔业资源群落结构特征. 南方水产科学. 2017(02): 18-25 .  本站查看
本站查看
17. 王学锋,吕少梁,黄一平,杨锋,李波. 基于流刺网调查的雷州湾游泳生物群落结构分析. 南方水产科学. 2017(03): 1-8 .  本站查看
本站查看
其他类型引用(11)




 下载:
下载:

 粤公网安备 44010502001741号
粤公网安备 44010502001741号
