D-loop gene sequence and diversity of Leuciscus waleckii Dybowski in Dali Lake and Ganggeng Lake in Inner Mongolia
-
摘要:
文章对内蒙古达里湖和岗更湖东北雅罗鱼(Leuciscus waleckii Dybowski)的mtDNA D-loop序列进行扩增,获得了896 bp的同源基因序列,得到的同源基因片段中A、T、C和G碱基的平均含量,达里湖群体为32.0%、32.2%、21.3%和14.5%;岗更湖群体为32.0%、32.2%、21.4%和14.5%;达里湖和岗更湖鱼群D-loop基因CG含量相当,未见明显差异。2个群体内和群体间都存在丰富的序列多态性,两湖群体的D-loop基因896个位点中存在可变位点33个,其余位点较为保守;达里湖30尾鱼D-loop基因含有多态性位点/突变位点21个,11个单倍型;岗更湖30尾鱼D-loop基因含有多态性位点/突变体位点31个,17个单倍型;岗更湖鱼群D-loop基因多样性高于达里湖。遗传距离计算显示,岗更湖和达里湖鱼群之间的平均遗传距离为0.007 0;达里湖鱼群之间的平均遗传距离为0.003 6;岗更湖鱼群之间的平均遗传距离为0.007 4。岗更湖鱼群D-loop基因的平均遗传距离大于达里湖鱼,前者群体D-loop基因进化速度大于后者。
Abstract:We amplified the mtDNA D-loop sequence in two stocks of Leuciscus waleckii Dybowski in Dali Lake and Ganggeng Lake in Inner Mongolia, having obtained 896 bp gene sequences; the average contents of T, C, A and G of homological fragments were 32.0%, 32.2%, 21.3%, 14.5% and 32.0%, 32.2%, 21.4%, 14.5% in Dali Lake stock and Ganggeng Lake stock, respectively, with no significant difference. The inter- and intra-population of the two stocks had high degree of sequence polymorphism. There were 33 variable sites in 896 D-loop gene loci in the two stocks, and the rest sites were more conservative. The D-loop genes of 30 fish in Dali Lake contained 21 polymorphisms/mutations and 11 haplotypes; while those in Ganggeng Lake contained 31 polymorphisms /mutations and 17 haplotypes. The diversity of D-loop gene in Ganggeng Lake stock was higher than that in Dali Lake stock. Genetic distance calculation shows that the average genetic distance between Ganggeng Lake and Dali Lake stocks was 0.007 0 (Dali Lake: 0.003 6, Ganggeng Lake: 0.007 4). The genetic distance of the D-loop gene in Ganggeng Lake stock was greater than that in Dali Lake stock, and the evolution speed of the former was faster than that of the latter.
-
Keywords:
- Leuciscus waleckii Dybowski /
- Inner Mongolia /
- D-loop gene /
- diversity /
- genetic distance
-
氨氮是鱼类养殖中非常重要的水质指标,当水体中氨氮浓度超过安全范围后就会对鱼类造成氨氮胁迫。研究表明,氨氮胁迫不仅会影响鱼类的生长、代谢,还会导致鱼体重要组织器官发生病变反应[1],如异育银鲫[2] (Carassius auratus gibelio)、团头鲂[3] (Megalobrama amblycephala) 幼鱼和圆斑星鲽[4] (Verasper variegatus) 幼鱼;还有研究表明,氨氮胁迫会显著抑制鱼体内抗氧化酶相关基因和免疫相关基因的表达,增加炎症细胞因子及细胞凋亡相关基因的表达量[5-8],从而抑制鱼体的抗氧化系统和非特异性免疫系统[4-5],进而导致鱼类死亡。同时,氨氮胁迫易打破养殖系统的平衡性,使养殖水体中的病原微生物迅速繁殖,从而导致养殖鱼类病害频发[9]。由此可见,氨氮胁迫已成为影响鱼类健康养殖的主要因素之一。
史氏鲟 (Acipenser schrenckii) 俗称七粒浮子,因其具有较高的营养价值和经济价值,已成为我国主要的鲟鱼养殖品种之一[10]。为了实现养殖效益最大化,史氏鲟的人工养殖大多采用高密度集约化养殖方式,该养殖模式存在鱼体集中排泄、残饵溶解和水体交换率低等问题,极易导致水体中氨氮浓度的急剧升高,虽然达不到急性致死浓度,但氨氮浓度长期升高会对史氏鲟造成慢性氨氮胁迫。目前,关于氨氮对鲟鱼的胁迫研究主要集中在急性胁迫研究方面,如刘建魁等[11]、杜浩等[12]和袁丁等[13]分别开展了氨氮对史氏鲟幼鱼、中华鲟 (A. sinensis) 和西伯利亚鲟 (A. baerii) 的急性毒性研究,而关于长时间低浓度氨氮胁迫对史氏鲟生长及其肝脏抗氧化、免疫指标的影响研究尚未见报道。本实验在慢性氨氮胁迫条件下,研究了史氏鲟生长及其肝脏抗氧化、免疫指标的变化情况,旨在初步揭示史氏鲟幼鱼对慢性氨氮胁迫的生理响应,从而为深入研究史氏鲟幼鱼应激反应的机理提供理论依据,为优化史氏鲟的增养殖技术提供参考依据。
1. 材料与方法
1.1 实验鱼的选择及暂养
实验鱼为中国长江三峡集团有限公司中华鲟研究所2016年全人工繁殖所得的史氏鲟幼鱼。随机挑选规格一致、体质健康的史氏鲟幼鱼162尾,体质量为 (180.00±15.00) g,体长为 (30.50±1.80) cm,并将其暂养于直径3.00 m的养殖池中,暂养水温16.80 ℃、溶解氧质量浓度 (6.00~7.00) mg·L−1、pH 7.30~7.60、氨氮质量浓度0.01 mg·L−1、亚硝氮质量浓度0.005 mg·L−1,每天饱食投喂1次,7 d后开始实验。
1.2 实验设计
在5个直径3.00 m、水深0.60 m的实验池中进行实验,氨氮质量浓度设置为0.01 mg·L−1 (对照组)、0.50 mg·L−1 (低浓度组)、1.00 mg·L−1 (中浓度组)、2.00 mg·L−1 (中高浓度组) 和4.00 mg·L−1 (高浓度组),每个浓度组30尾鱼。在暂养池中,随机挑选150尾史氏鲟幼鱼用于实验,每个实验池30尾;实验开始前,在每个养殖池设3个挡板,将养殖池分隔成A、B、C 3个相同大小的扇形区域,用120 mg·L−1 MS-222将实验鱼麻醉后称质量、测体长,然后在背鳍上注射T型标记,随机转入A、B、C中的任意一个扇形区域中,每个扇形区域共转入10尾鱼,分别记录3个区域中所有鱼的T标代码,并将T标代码与A、B、C扇形区域一一对应;之后将挡板拆除,把30尾实验鱼混养在一个池中进行实验;实验结束时将养殖池再隔成A、B、C 3个同等大小的扇形区域,并根据T标代码,将池中的实验鱼分别置于与其对应的A、B、C区域中,然后在每个区域中进行随机取样。实验期间,水温16.80~21.50 ℃、溶解氧 6.00~7.00 mg·L−1、pH 7.30~7.60、亚硝酸盐低于0.01 mg·L−1。氨氮质量浓度用10 g·L−1的氯化铵 (NH4Cl) 母液进行调配,实验池水每24 h换1次;每天饱食投喂1次,摄食完成后及时清除残饵,并观察记录鱼的摄食及活动状态,实验持续60 d。
1.3 样品的采集和处理
用120 mg·L−1的MS-222将实验鱼快速麻醉后解剖,取肝脏组织;用预冷的鱼用生理盐水将肝脏冲洗干净,滤纸吸干水分后将其切成小块,并置于2 mL离心管中,经液氮快速冷冻后,−70 ℃保存待测。
1.4 测定指标
1.4.1 生长指标
计算成活率 (SR)、增重率 (WGR)、特定生长率 (SGR)、肝体比 (HSI)、肥满度 (CF) 和脏体比 (VSI),计算公式为:
$$ {{\rm{SR}}} {\rm{ }} = {N_{\rm{f}}}/{N_{\rm{i}}} \times 100\% $$ $$ {{\rm{WGR}}}{\rm{ }} = {\rm{ }}\left( {{W_t} - {W_0}} \right){\rm{ }}/{W_0} \times 100\% $$ $$ {{\rm{SGR}}} {\rm{ }} = {\rm{ }}\left( {{\rm{ln}}{W_t} - {\rm{ln}}{W_0}} \right){\rm{ }}/t \times 100\% $$ $$ {{\rm{HSI}}}{\rm{ }} = {W_{\rm{h}}}/{W_{\rm{b}}} \times 100\% $$ $${{\rm{CF}}}{\rm{ }} = {W_{\rm{b}}}/L \times 100\% $$ $$ {{\rm{VSI}}} {\rm{ }} = {W_{\rm{e}}}/{W_{\rm{b}}} \times 100\% $$ 式中Nf为终末鱼尾数;Ni为初始鱼尾数;Wt为终末体质量 (g);W0为初始体质量 (g);t为实验天数 (d);Wb为每尾鱼体质量 (g);L为每尾鱼体长 (cm);Wh为肝脏质量 (g);We为内脏团质量 (g)。
1.4.2 抗氧化和免疫指标
抗氧化指标包括超氧化物歧化酶 (SOD) 活性、过氧化氢酶 (CAT) 活性、总抗氧化能力 (T-AOC) 活性、谷胱甘肽 (GSH) 含量、丙二醛 (MDA) 含量;免疫指标包括溶菌酶 (LZM) 活性和免疫球蛋白M (lgM) 含量。所有指标的测定采用南京建成生物工程研究所研制的试剂盒,具体方法参见其说明书。
1.5 数据统计
实验数据用SPSS 16.0和Excel 2016软件进行统计分析,利用单因素方差分析 (One-Way ANOVA) 和Duncan's多重比较检验低温胁迫对各项指标影响的显著性,差异的显著性以P<0.05为标准,结果以“平均值±标准差 (
$\overline {{X}} \pm {\rm{SD}}$ ) ”表示。2. 结果
2.1 慢性氨氮胁迫对史氏鲟幼鱼生长性能的影响
慢性氨氮胁迫显著降低了史氏鲟幼鱼增重率和特定生长率 (P<0.05),对照组实验鱼的特定生长率分别是低、中、中高和高浓度组的1.32、1.75、2.41和6.87倍(表1);脏体比和肝体比也随氨氮浓度的增加呈逐渐降低的趋势,高浓度组鱼体脏体比和肝体比显著低于对照组 (P<0.05);各组实验鱼的肥满度从大到小依次为对照组、中浓度组、中高浓度组、高浓度组和低浓度组,但各组之间不存在显著差异 (P>0.05);此外,各实验组史氏鲟幼鱼在实验过程中的成活率均为100%。这表明持续60 d的慢性氨氮胁迫未对史氏鲟的存活产生影响,但对其生长产生了显著的抑制作用。
表 1 慢性氨氮胁迫对史氏鲟幼鱼生长指标的影响Table 1 Effects of chronic ammonia stress on growth indices of juvenile A. schrenckii实验组
Group成活率
SR/%增重率
WGR/%特定生长率
SGR/%·d−1脏体比
VSI/%肝体比
HSI/%肥满度
CF/%对照组 Control group 100.00 77.99±4.71a 0.96±0.27a 4.92±0.27a 2.00±0.19a 0.006 5±0.000 2a 低浓度组 Low concentration group 100.00 58.87±3.56a 0.77±0.27a 4.70±0.27a 1.58±0.20b 0.005 9±0.000 1a 中浓度组 Medium concentration group 100.00 44.52±4.67b 0.61±0.27b 4.76±0.24a 1.48±0.23b 0.006 3±0.000 1a 中高浓度组 Sub-high concentration group 100.00 32.41±3.18b 0.47±0.27b 4.57±0.15a 1.42±0.08b 0.006 1±0.000 2a 高浓度组 High concentration group 100.00 11.35±2.53c 0.18±0.27c 3.89±0.17b 1.31±0.04b 0.005 9±0.000 3a 注:同列不同上标字母表示显著性 (P<0.05)
Note: Different superscript letters in the same column indicate significant difference (P<0.05).2.2 慢性氨氮胁迫对史氏鲟幼鱼肝脏抗氧化、免疫指标的影响
在慢性氨氮胁迫条件下,各实验组史氏鲟幼鱼肝脏SOD活性情况见图1-a。随着氨氮浓度的增大,史氏鲟幼鱼肝脏SOD活性呈逐渐降低的趋势;其中中高、高浓度组肝脏SOD活性显著低于低浓度组和对照组 (P<0.05),其他各组之间不存在显著性差异 (P>0.05)。
随着氨氮浓度的升高,各组史氏鲟幼鱼肝脏CAT活性也呈逐渐降低的趋势 (图1-b),高浓度组史氏鲟幼鱼肝脏CAT活性显著低于对照组 (P<0.05),较对照组降低39.95%,而其他各实验组之间无显著差异 (P>0.05)。
史氏鲟幼鱼肝脏T-AOC活性变化见图1-c。慢性氨氮胁迫显著降低了史氏鲟幼鱼的肝脏T-AOC活性,且氨氮浓度越大,肝脏T-AOC活性下降越明显。低、中、中高和高浓度组肝脏T-AOC活性均显著低于对照组 (P<0.05),较对照组分别下降了20.57%、30.93%、44.57%和74.08%。
在不同氨氮浓度中,各组实验鱼肝脏GSH含量依次表现为对照组>低浓度组>中浓度组>中高浓度组>高浓度组 (图1-d),其中高、中高、中浓度组肝脏GSH质量摩尔浓度显著低于对照组 (P<0.05),但三组之间差异不显著 (P>0.05),低浓度组和对照组也不存在显著性差异 (P>0.05)。
史氏鲟幼鱼肝脏MDA质量摩尔浓度在慢性氨氮胁迫条件下的变化情况见图1-e。各处理组实验鱼肝脏MDA质量摩尔浓度由大到小依次为高浓度组、中高浓度组、中浓度组、低浓度组和对照组,其中高浓度组肝脏MDA质量摩尔浓度显著高于低浓度组 (P<0.05);中、中高和高浓度组肝脏MDA质量摩尔浓度显著高于对照组 (P<0.05),较对照组分别升高25.86%、32.89%和47.33%。
实验结果表明,慢性氨氮胁迫显著降低了史氏鲟幼鱼的肝脏LZM活性 (图1-f)。随着氨氮浓度的升高,史氏鲟幼鱼肝脏LZM活性逐渐降低,其中,中、中高和高浓度组肝脏LZM活性均显著低于对照组 (P<0.05),较对照组分别下降22.22%、27.31%和36.98%;其他各组之间无显著差异 (P>0.05)。
史氏鲟幼鱼肝脏IgM质量分数变化情况见图1-g。氨氮浓度越高,史氏鲟幼鱼肝脏IgM质量分数越低。中高、高浓度组肝脏IgM质量分数显著低于对照组 (P<0.05),较对照组分别下降23.45%和32.62%;与低浓度组相比,高浓度组肝脏IgM质量分数降低31.07%,两者之间存在显著差异 (P<0.05);其他各组之间无显著差异 (P>0.05)。
3. 讨论
3.1 慢性氨氮胁迫对史氏鲟幼鱼生长性能的影响
氨氮是评估养殖水环境好坏的重要指标。大量研究表明,水体中氨氮浓度的升高会显著抑制水生生物的生长。肖炜等[9]发现吉富罗非鱼 (GIFT Oreochromis niloticus) 幼鱼在不同氨氮浓度的水体中胁迫30 d后,3.25、6.51和13.01 mg·L−1组实验鱼的终末体质量、增质量率和特定生长率均低于空白对照组,且对实验鱼生长的抑制作用随氨氮浓度的增加而显著增强;徐杨[14]也发现尼罗罗非鱼 (O. niloticus) 的增重率和特定生长率随氨氮胁迫浓度的升高而下降;Paust等[15]研究指出,大西洋比目鱼 (Hippoglossus hippoglossus) 在NH3质量浓度为0.12、0.17 mg·L−1的水体中养殖62 d后,鱼体的生长速率会受到显著抑制;Peng等[16]得出慢性氨氮胁迫显著降低了虎斑乌贼 (Sepia pharaonis) 的成活率、生长率和摄食量的结论。本研究也得出了相同的结论,慢性氨氮胁迫虽未造成史氏鲟幼鱼的死亡,却显著降低了史氏鲟幼鱼的增重率、特定生长率、肝体比和脏体比,对鱼体的生长产生了显著的抑制作用。这可能是由于氨氮胁迫会导致史氏鲟幼鱼的摄食率和饲料转化率下降,鱼体内大部分能量用于抵御胁迫产生的应激反应,所以导致鱼体的生长速率下降[17]。张晓莹[2]进一步证实了这一结论,指出氨氮胁迫显著提高了鱼体的标准代谢率 (SMR),降低了最大代谢率 (MMR),缩小了有氧代谢范围 (AS),表明鱼体在氨氮胁迫下,鱼体的有氧代谢能力下降,导致游泳能力下降,逃逸、捕食及繁殖等行为均受到限制,鱼体用于修复自身机能并维持基本生理功能所需的能量增加,而可提供的有氧代谢总能量降低,所以鱼体用于生长的能量大大减少了。Xia等[18]、Toni等[19]也得出类似的结论。但黎庆等[20]研究发现,在总氨氮质量浓度为5.65~5.80 mg·L−1的水体中养殖56 d对黄颡鱼 (Pelteobagrus fulvidraco) 的终末体质量、增质量和饵料系数无显著影响,这可能与鱼的种类、规格、抗逆性强弱及氨氮胁迫程度有关。
3.2 慢性氨氮胁迫对史氏鲟幼鱼抗氧化和免疫指标的影响
鱼类长期处于氨氮胁迫中,机体内源性氨的排泄被阻断,外源性氨经鳃和皮肤进入体内并大量积累,产生大量氧自由基 (ROS),从而对鱼体造成损伤[21]。抗氧化酶系统可以催化消除生物体内过多的ROS,是生物体内抗氧化防御体系的重要组成部分,而SOD和CAT则是抗氧化防御体系中非常重要的功能酶[22],两者相互关联,可联合清除活性氧自由基,其活性的下降标志着机体清除活性氧自由基的能力下降[23]。T-AOC是衡量机体抗氧化系统功能的综合性指标,它与鱼体的健康程度密切相关[24]。研究发现经过30 d的氨氮胁迫,3.49、6.99、13.97和27.94 mg·L−1组尼罗罗非鱼的肝脏谷丙转氨酶 (GPT) 和SOD活性均显著下降[14],6.51、13.01 mg·L−1组吉富罗非鱼的血清SOD活性均显著低于对照组[9];黄颡鱼在总氨氮为5.65~5.80 mg·L−1中胁迫56 d后,其SOD、CAT和谷胱甘肽过氧化物酶 (GSH-PX) 显著低于对照组[20],这与本研究所得结论基本一致。本研究中,慢性氨氮胁迫显著降低了史氏鲟幼鱼肝脏SOD、CAT、T-AOC活性,且与氨氮浓度呈显著的负相关性 (P<0.05),这说明持续60 d的慢性氨氮胁迫对史氏鲟幼鱼的肝脏抗氧化酶指标产生了显著的抑制作用,且氨氮浓度越高,抑制作用越明显。在李利红和袁宏利[25] 对福瑞鲤 (Cyprinus carpio)、刘洋[26] 对泥鳅 (Misgurnus anguillicaudatus)、臧元奇等[27]对刺参 (Apostichopus japonicus) 的慢性氨氮胁迫研究中也得出了类似结论,其原因可能是氨氮胁迫降低了鱼体抗氧化相关基因的表达量,抗氧化酶的合成量大大减少,从而降低了抗氧化酶的活性[28]。然而,姜会民[29]、Sun等[30]研究得出不同结论,他们认为抗氧化酶活性随胁迫时间增加呈先升高后下降的趋势;赵海涛[31]研究发现南方鲶 (Silurus meridionalis) 幼鱼SOD活性在低浓度氨氮胁迫时先升高后下降,而在高浓度氨氮胁迫时显著持续下降。这主要是由于鱼体在低氨氮条件下产生了毒物兴奋效应[29],低浓度氨氮胁迫显著增加了免疫相关基因和抗氧化酶相关基因的表达,而高浓度氨氮胁迫显著抑制了免疫相关基因和抗氧化酶相关基因的表达[32]。
GSH是一种低分子活性氧自由基清除剂,是清除ROS非常重要的非酶抗氧化物质[33];而MDA是ROS与脂质发生过氧化反应的产物,它可以反映细胞受活性氧自由基攻击的程度,从而间接反映机体抗氧化能力的强弱及组织细胞受损伤的严重程度[34]。王贞杰等[4]发现圆斑星鲽幼鱼在氨氮处理96 h后,其肝脏MDA含量显著高于对照组,且MDA含量与氨氮浓度呈正相关 (P<0.05);蒋玫等[35]也发现随着氨氮浓度的升高,鲻鱼 (Mugil cephalus) 肝脏、鳃丝的MDA含量逐渐升高,MDA含量与氨氮浓度呈正相关。本研究中,慢性氨氮胁迫显著降低了史氏鲟幼鱼肝脏的GSH含量,而使MDA含量显著增加,这进一步表明持续60 d的慢性氨氮胁迫显著降低了史氏鲟幼鱼的抗氧化能力,加剧了组织细胞膜脂质过氧化程度,使得醛酮类物质在鱼体内不断积累。
溶菌酶 (LZM) 和免疫球蛋白M (IgM) 是鱼体非常重要的免疫因子,前者可以破坏革兰氏阳性菌细胞壁中的肽聚糖,从而瓦解细菌细胞;后者具有强大的抗感染作用[34]。Zhang等[3]研究发现氨氮胁迫显著降低了黄颡鱼的LZM活性和总免疫球蛋白含量;Qin等[36]报道了氨氮胁迫不仅降低了瓦氏黄颡鱼 (P. vachellii) 血清LZM活性和补体C3的含量,还抑制了脾脏、头肾中补体C3和IgM的表达;陈家长等[37]、韩春燕等[38]发现氨氮胁迫显著降低了罗非鱼 (Oreochromis niloticus)、奥尼罗非鱼 (Oreochromis niloticus × O. areus) 的血清溶菌酶的活性;芦光宇等[39]、任海等[40]也发现,长时间的氨氮胁迫会使克氏原螯虾 (Procambarus clarkii) 和脊尾白虾 (Exopalaemon carinicauda) 的免疫酶活性降低;这些研究结果与本实验结果基本一致。本研究中,随着氨氮胁迫浓度的增大,史氏鲟幼鱼肝脏LZM活性及IgM含量均表现为逐渐降低的趋势。这表明慢性氨氮胁迫降低了鱼体LZM活性及IgM的合成,抑制了鱼体的免疫功能,降低了鱼体的免疫力,其原因主要与氨氮胁迫抑制了鱼体LZM、IgM等免疫相关基因的表达有关[32, 36]。
4. 结论
本研究发现,持续60 d的慢性氨氮胁迫导致史氏鲟幼鱼的特定生长率和增重率显著下降,肝脏SOD、CAT、T-AOC、LZM活性及GSH、IgM含量显著下降,MDA含量显著升高,这表明慢性氨氮胁迫对史氏鲟幼鱼的生长、抗氧化能力和免疫能力产生了显著的不利影响。当氨氮质量浓度为0.5 mg·L−1时,史氏鲟幼鱼肝脏SOD、CAT、T-AOC、LZM活性及MDA、IgM含量等指标与对照组相比均未出现显著性变化;而当氨氮质量浓度>0.5 mg·L−1时,肝脏T-AOC、LZM活性及GSH、MDA含量等指标显著低于对照组,这表明当氨氮质量浓度≤0.5 mg·L−1时,氨氮胁迫对史氏鲟幼鱼肝脏抗氧化、免疫指标基本无实质性的影响,但当氨氮质量浓度>0.5 mg·L−1时,氨氮胁迫已对史氏鲟幼鱼的肝脏抗氧化、免疫指标造成了显著的不利影响。因此,在史氏鲟的日常养殖过程中,养殖水体中氨氮质量浓度应至少≤0.5 mg·L−1,以避免其对史氏鲟造成损伤。
-
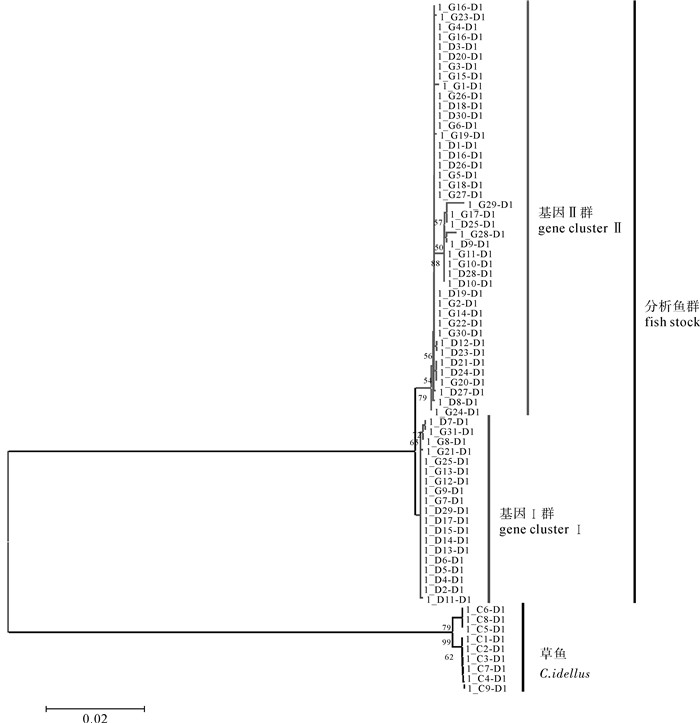
图 2 D-loop序列UPGMA系统树
进化树上名称含义举例说明如下:C7.第7号草鱼的样品;D2.达里湖第2号鱼的样品;G11.岗更湖第11号鱼的样品
Figure 2. UPGMA phylogenetic tree based on D-loop sequences
The codes in the UPGMA phylogenetic tree are illustrated as follows: C7. No.7 grass carp samples; D2. No.2 fish samples in Lake; G11. No.11 fish samples in Ganggeng Lake
表 1 达里湖和岗埂湖东北雅罗鱼群体之间的遗传距离
Table 1 Genetic distance between L.waleckii Dybowski stocks in Dali Lake and Ganggeng Lake
草鱼
C.idellus达里湖东北雅罗鱼
L.waleckiiin Dali Lake岗更湖东北雅罗鱼
L.waleckii in Ganggeng Lake草鱼C.idellus 0.003 6 0.393 0 0.395 0 达里湖东北雅罗鱼L.waleckii in Dali Lake 0.393 0 0.003 6 0.007 0 岗更湖东北雅罗鱼L.waleckii in Ganggeng Lake 0.395 0 0.007 0 0.007 4 -
[1] 安晓萍, 孟和平, 杜昭宏, 等. 达里湖东北雅罗鱼的生长、死亡和生活史类型的研究[J]. 淡水渔业, 2008, 38(6): 3-7. doi: 10.3969/j.issn.1000-6907.2008.06.001 [2] BROWN W M, GEORGE M, WILSON A C. Rapid evolution of animal mitochondrial DNA[J]. Proc Natl Acad Sci USA, 1979, 76 (4): 1967- 1971. doi: 10.1073/pnas.76.4.1967
[3] GILLES A, LECOINTRE G, MIQUELIS A, et al. Partial combination applied to phylogeny of European cyprinids using mitochondrial control region[J]. Mol Phylogenet Evol, 2001, 19(1): 22-33. doi: 10.1006/mpev.2000.0916
[4] 郝君, 杨蔷, 鲍迪, 等. 6种鱼mtDNA D-loop及其邻近区段的序列比较分析[J]. 大连海洋大学学报, 2013, 28(2): 160-165. doi: 10.3969/j.issn.2095-1388.2013.02.009 [5] 周其椿, 林艳红, 彭江涛, 等. 普安银鲫mtDNA D-loop序列多态性分析[J]. 广东农业科学, 2012(22): 173-175. doi: 10.3969/j.issn.1004-874X.2012.22.056 [6] 冉光鑫, 代应贵, 岳晓烔. 稀有白甲鱼西江种群mtDNA D环区的结构及遗传多样性[J]. 上海海洋大学学报, 2012, 21(2): 176-182. [7] 肖永双, 张岩, 高天翔. 基于线粒体DNA部分片段探讨石鲽与星突江鲽的亲缘关系[J]. 中国海洋大学学报: 自然科学版, 2010, 40(6): 69-76. doi: 10.3969/j.issn.1672-5174.2010.06.009 [8] 姚茜, 杨频, 陈立侨, 等. 罗氏沼虾三群体线粒体D-loop基因序列差异的初步研究[J]. 水产学报, 2007, 31(1): 18-22. doi: 10.3321/j.issn:1000-0615.2007.z1.004 [9] 董志国, 李晓英, 王普力, 等. 基于线粒体D-loop基因的中国海三疣梭子蟹遗传多样性与遗传分化研究[J]. 水产学报, 2013, 37(9): 1304-1310. doi: 10.3724/SP.J.1231.2013.38630 [10] 黄雪贞, 钱国英, 李彩燕. 中华鳖3个地理群体线粒体基因D-loop区遗传多样性分析[J]. 水产学报, 2012, 36(1): 17-22. doi: 10.3724/SP.J.1231.2012.27485 [11] 刘金亮, 常玉梅, 徐丽华, 等. 东北雅罗鱼微卫星分子标记的筛选及特征分析[J]. 华北农学报, 2011, 26(1): 87-93. https://max.book118.com/html/2017/0824/129850456.shtm [12] 刘金亮. 东北雅罗鱼微卫星分子标记的筛选及雅罗鱼5个野生群体遗传多样性分析[D]. 上海: 上海海洋大学, 2011. https://www.zhangqiaokeyan.com/academic-degree-domestic_mphd_thesis/020314222443.html [13] 池炳杰, 常玉梅, 闫学春. 瓦氏雅罗鱼达里湖群体和乌苏里江群体的遗传多样性和遗传结构分析[J]. 中国水产科学, 2010, 17(2): 228-235. [14] 黄志坚, 徐晓鹏, 唐晶晶, 等. 鱼类线粒体DNA控制区扩增引物及其设计方法和应用: 中国, 200710028242.1[P]. 2007-05-25. https://xueshu.baidu.com/usercenter/paper/show?paperid=2f7b7b9f121f348658025612d37c2fbe [15] 黄志坚, 徐晓鹏, 唐晶晶等. 淡水鱼类线粒体DNA D-loop基因的引物设计和应用[J]. 中山大学学报: 自然科学版, 2009, 48(4): 84-88. doi: 10.3321/j.issn:0529-6579.2009.04.018 [16] 赵良杰, 何光喜, 周小玉, 等. 千岛湖大眼华鳊形态度量学和D-loop序列分析[J]. 水产学报, 2013, 37(3): 351-357. [17] 郑文娟, 来育洪, 尤昕煜, 等. 舟山小黄鱼线粒体DNA D-loop区序列变异的遗传多样性分析[J]. 动物学研究, 2012, 33(3): 329-336. doi: 10.3724/SP.J.1141.2012.03329 [18] BROUGHTON R E, ROE B A. The complete sequence of the zebra fish (Danio rerio) mitochondrial genome and evolutionary patterns in vertebrate mitochondrial DNA[J]. Genome Res, 2001, 11(11): 1958-1967. doi: 10.1101/gr.156801
[19] KONG Q P, YAO Y G, HUANG S Y. Mitochondrial DNA control region and cytochrome b sequence variation in the genus Mystacoleucus Gunther (Pisces: Cyprindae: Barbinae) from China [J]. Biochem Genet, 2003, 41(9): 305-313. doi: 10.1023/b:bigi.0000006031.20967.08
[20] 彭珊, 代应贵. 濒危鱼类稀有白甲鱼清水江种群mtDNA D-loop序列多态性[J]. 水产学报, 2009, 33(2): 196-200. doi: 10.3724/SP.J.00001 [21] 齐景伟, 安晓萍, 孟和平, 等. 达里湖瓦氏雅罗鱼资源现状及合理利用探讨[J]. 水生态学杂志, 2011, 32(1): 71-76. doi: 10.3969/j.issn.1003-1278.2011.01.013 [22] SHAKLEE J B, TAMARU C S, WAPLES R S. Speciation and evolution of marine fishes studied by electrophoresis analysis of proteins[J]. Pac Sci, 1982, 36(2): 141-157.
-
期刊类型引用(16)
1. 符许娟,黄进强,李永娟,吴深基,赵璐,孙同振. 碱性环境下急性氨氮胁迫对虹鳟抗氧化能力和非特异性免疫的影响. 水生生物学报. 2025(02): 43-53 .  百度学术
百度学术
2. 王恒杰,戴梦杨,王倩,熊信宇,王灿莉,袁向阳. 环境胁迫因子对鱼类健康影响的研究进展. 中国农学通报. 2025(02): 157-164 .  百度学术
百度学术
3. 刘雪娇,李洁,郸彩霞,海强,刘浩,刘哲,朱利瑞,王建福. 氨氮胁迫对虹鳟幼鱼IHNV易感性的影响. 中国水产科学. 2025(02): 246-257 .  百度学术
百度学术
4. 李亚宁,陈敏,刘洋,韩磊,何焱,樊启学,沈志刚. 饲料中小麦胚芽对黄颡鱼雌性亲鱼繁殖性能的影响. 水生生物学报. 2024(02): 264-274 .  百度学术
百度学术
5. 刘品,王文博,李超,严少普,李琪,罗小敏,张硕华,张艺琛,姚林荣. 急性氨氮胁迫下大口黑鲈的肝脏转录组特征分析. 水生生物学报. 2024(05): 713-724 .  百度学术
百度学术
6. 王雪芹,杨晓玲,彭衡阳,戴景辉,阳涛. 氨氮应激对鱼类生命活动影响的研究进展. 水产养殖. 2024(08): 18-24 .  百度学术
百度学术
7. 聂丽玲,杨占虎,张卿,鲍瑞峰,朱传坤,李礼,朱晓鸣,辛未,张磊. 低浓度氨氮预适应后高氨氮暴露对黄颡鱼鳃组织结构、免疫指标及相关基因的影响. 水生生物学报. 2024(11): 1812-1821 .  百度学术
百度学术
8. 吴雷,张学振,王力,刘琪,李建,张殿福,田大才. 饲料中添加酵母硒对史氏鲟幼鱼生长性能、肌肉品质和抗氧化能力的影响. 淡水渔业. 2023(01): 3-11 .  百度学术
百度学术
9. 赵宇曦,刘兴国,周润锋,刘子秋. 光照强度对黄颡鱼生长和生理性能的影响. 水产学报. 2023(07): 77-87 .  百度学术
百度学术
10. 王恒杰,李梦娇,张婷,赵蔚蓝,王灿莉,宋呈文,罗思,袁向阳. 团头鲂Rheb基因分子特征及其对氨氮胁迫的响应. 南方农业学报. 2023(09): 2562-2570 .  百度学术
百度学术
11. 卢军浩,李兰兰,权金强,赵桂研,孙军,林桥荣,刘哲. 纳米硒对热应激虹鳟血清抗氧化指标和免疫指标的影响. 华北农学报. 2022(03): 231-238 .  百度学术
百度学术
12. 孙元琛,徐冰洁,曹艺筹,许颖洁,秦粉菊,袁红霞. 饲料中添加纳米氧化铈对氨氮与嗜水气单胞菌胁迫下中华绒螯蟹的保护效应. 南方水产科学. 2022(03): 94-101 .  本站查看
本站查看
13. 孟骞骞,张雨晴,谭智敏,周针宇,田佳明,谢开英,李萍,沈水宝,王文秀,霍芳,王文娟. 牛至油对慢性氨氮胁迫下幼鲤组织结构的影响. 水生态学杂志. 2022(06): 146-157 .  百度学术
百度学术
14. 贾慧凝,侍苗苗,卞永乐,侍崇敬,刘恒蔚,宋学宏,秦粉菊. 纳米硒对低氧胁迫下中华绒螯蟹免疫保护和抗氧化能力的影响. 南方水产科学. 2022(06): 100-109 .  本站查看
本站查看
15. 孙彩云,董宏标,王文豪,李勇,古群红,段亚飞,张家松,许晓东. 月桂酸单甘油酯对花鲈脂质代谢的影响. 南方水产科学. 2021(01): 67-75 .  本站查看
本站查看
16. 陈旭,左涛,周胜杰,杨蕊,于刚,秦传新,马振华. 尖吻鲈幼鱼运输密度和时长对运输水质及其复苏率和抗氧化能力的影响. 南方水产科学. 2021(02): 122-128 .  本站查看
本站查看
其他类型引用(18)










 下载:
下载:

 粤公网安备 44010502001741号
粤公网安备 44010502001741号
