Influence of water cooking condition on morphology and protein loss of body wall from sea cucumber (Stichopus monotuberculatus)
-
摘要:
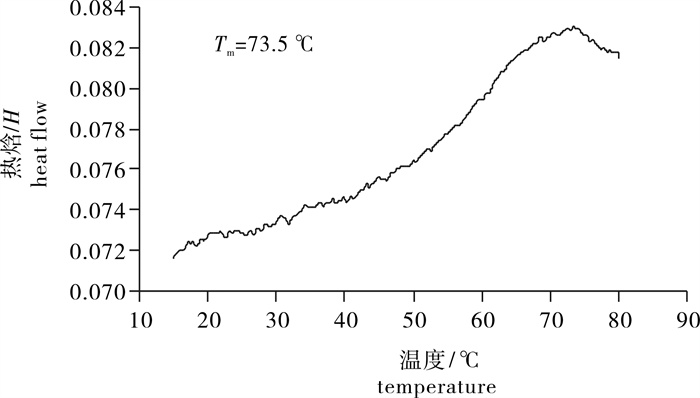
研究了花刺参(Stichopus monotuberculatus)体壁在不同水煮温度(50 ℃、60 ℃、70 ℃、80 ℃和90 ℃)和时间(10 min、20 min和30 min)条件下的失重率、蛋白溶失率、横截面形态结构、新鲜体壁含水量和最大转变温度的变化。结果显示,新鲜花刺参体壁含水量约为93.67%;随着温度和时间的递增,体壁水煮于50~60 ℃开始收缩失重,失重率逐渐升高;从70~80 ℃开始蛋白溶失率逐渐升高;新鲜体壁最大转变温度为73.5 ℃,与海参体壁收缩和蛋白溶失发生温度相一致。采用扫描电子显微镜观察体壁横截面形态结构发现,体壁胶原纤维网络密度从70 ℃开始显著升高,并出现空洞。因此,花刺参的水煮条件应为70 ℃加热20~30 min,或80 ℃加热不超过10 min。
Abstract:We investigated the weight loss, rate of protein loss and cross-sectional morphology of Stichopus monotuberculatus at different temperatures (50 ℃, 60 ℃, 70 ℃, 80 ℃ and 90 ℃) for 10 min, 20 min and 30 min, respectively. Results show that the water content of fresh body wall was about 93.67 %; with the increase of temperature and time, the weight loss beginning at 50~60 ℃ increased gradually; the loss of protein increased steadily, starting from 70~80 ℃. Then the maximum transition temperature of fresh body wall was observed at 73.5 ℃, consistent with the beginning temperatures of weight and protein loss. At last, the cross-sectional morphology of body wall was observed by scanning electron microscope, where the density of collagen fibers network in body wall had increased significantly since 70 ℃ with hollow generating simultaneously. Thus, the cooking condition should be 70 ℃ for 20~30 min, or 80 ℃ within 10 min.
-
Keywords:
- Stichopus monotuberculatus /
- cooking /
- body wall /
- morphology /
- weight loss /
- protein loss
-
浮游植物是海洋生态系统中最基础的一个环节,作为该系统最重要的初级生产者,在海洋生态系统的物质循环和能量流动中起着重要的作用。浮游植物的种类组成和数量变动都将直接或者间接地制约海洋生产力的发展,从而影响海洋生物资源的开发和利用[1-5]。珠江口南沙海域位于广州市最南端,濒珠江出海口伶仃洋,属咸淡水的交汇区域,同时受到地表径流和海洋潮汐的影响,生态环境复杂,形成独特的海洋生物群落。近年来,随着周边地区经济社会的快速发展,以及滩涂围垦、航道疏浚和养殖等人类活动规模不断扩大,使得海水的富营养化加剧,极大地影响了该海区生态群落结构的稳定性,增大了发生赤潮的危险性,珠江口海域已成为中国赤潮的多发区之一[6-7]。
目前,对珠江河口及近海浮游生物的群落特征的研究已有报道[8-12],但是对珠江口内海域研究的比较少,特别是人为扰动最为频繁的珠江口南沙区周围的海域。文章通过对2015年4月(丰水期)和11月(枯水期)珠江口南沙海域生态综合调查采集的浮游植物样品进行鉴定分析,初步研究了该海域海洋浮游植物的种类组成、优势种、细胞丰度的分布及多样性水平,旨在为研究该海域生产力水平、海洋生态系统的群落结构和环境质量状况提供基础数据。
1. 材料与方法
1.1 采样和分析
2015年4月(丰水期)和11月(枯水期)在珠江口南沙区周围的海域(113°29′52″E~113°47′19″E,22°28′10″N~22°51′23″N)进行浮游植物样品采集,丰水期和枯水期都布设了20个调查站位(S1~S20,图 1)。调查站点均位于珠江口南沙海域人类活动扰动频繁海域,覆盖了从近口淡水、咸淡水段到口外海水段的河口典型生境特征。浮游植物样品用浅水Ⅲ型浮游生物网自底至表垂直拖网采集,并当场加入甲醛溶液保存。带回实验室后浓缩至50 mL,于显微镜下进行鉴定与计数,测定分析其种类组成、数量、分布、优势度、多样性指数和均匀度等。
使用YSI便携式温盐深仪现场采集各站位盐度、温度、溶解氧(DO)、pH和水深等物理环境数据;同时现场采集海水样品,带回实验室后分析水体中的溶解性无机氮(TIN)、活性磷酸盐(PO4-P)和叶绿素a(Chl-a)的含量。浮游植物样品的采集和分析均按《海洋监测规范》(GB17378—2007)和《海洋调查规范-海洋生物调查》(GB12763.6—2007)[13-14]中规定的方法进行。
1.2 评价方法
浮游植物优势度(Y)应用以下公式计算:
$ Y = \frac{{{n_i}}}{N} \times {f_i} $
式中ni为第i种的个体数;fi是该种在各站中出现的频率;N为所有站每个种出现的总个体数,以Y>0.02作为优势种。
采用Shannon-Wiener[15]、Pielou[16]测定浮游植物的多样性指数(H′)、均匀度指数(J′),其计算公式分别为:
$ \begin{array}{l} H' =-\sum\limits_{i = 1}^S {{P_i}{\rm{lo}}{{\rm{g}}_2}{P_i}} \\ J' = \frac{{H'}}{{{\rm{lo}}{{\rm{g}}_2}S}} \end{array} $
式中S为样品中的种类总数;Pi为第i种的个体数与总个体数的比值。
浮游植物与环境因子的相关性分析采用SPSS 19.0统计软件分析;典范对应分析(canonical correspondence analysis,CCA)应用CANOCO 4.0软件进行,排序结果用物种-环境因子关系的双序图表示。另外,采用孙军等[17]的浮游植物多样性的评判阈值(表 1)对浮游植物多样性进行等级评价。
表 1 浮游植物多样性指标的评判阈值Table 1. Threshold value evaluation for diversity indices of phytoplankton多样性指标
diversity index很低
very low
(Ⅰ)低
low
(Ⅱ)一般
normal
(Ⅲ)高
high
(Ⅳ)很高
very high
(Ⅴ)种类数species number <15 15~24 25~34 35~44 >45 多样性指数(H′)Shannon-Wiener diversity index <1.5 1.5~2.49 2.5~3.49 3.5~4.5 >4.5 均匀度指数(J′)Pielous evenness index <0.68 0.68~0.73 0.74~0.79 0.80~0.88 >0.88 2. 结果与分析
2.1 浮游植物物种组成
共鉴定出浮游植物44个属76种,隶属于硅藻门、甲藻门、绿藻门、蓝藻门和裸藻门5大门类。其中丰水期共鉴定出浮游植物5门37属68种(包括变种和变形),硅藻门种类最多(24属39种),占总种数的57.35%;其次是绿藻门(7属15种),占总种数的22.06%;甲藻门有2属7种,占总种数的10.29%;裸藻门有3属5种,占总种数的7.35%;蓝藻门有1属2种,占总种数的2.94%。S1站鉴定出的浮游植物种类最多(38种),而S17站鉴定出的浮游植物种类最少(6种),但都是属于硅藻类。各站位中新月筒柱藻(Cylindrotheca closterium)、中肋骨条藻(Skeletonema costatum)、虹彩圆筛藻(Coscinodiscus oculusiridis)在每个站位中都有分布。此外,奇异棍形藻(Bacillaria paradoxa)也分布比较广泛(表 2)。
表 2 珠江口南沙海域浮游植物物种组成Table 2. Species composition of phytoplankton in the Nansha sea area of Pearl River Estuary门类
phylum总种类数
total species number丰水期(5月)
wet season (May)枯水期(11月)
dry season (November)种类
species比例/%
percentage种类
species比例/%
percentage种类
species比例/%
percentage硅藻Bacillariophyta 39 51.32 39 57.35 33 55.00 甲藻Pyrrophyta 15 19.74 7 10.29 14 23.33 绿藻Chlorophyta 15 19.74 15 22.06 8 13.33 蓝藻Cyanophyta 2 2.63 2 2.94 2 3.33 裸藻Euglenophyta 5 6.58 5 7.35 3 5.00 总计total 76 - 68 - 60 - 枯水期共鉴定出浮游植物5门44个属60种(包括变种和变形),其中还是硅藻门种类最多(22属33种),占总种数的55.00%;其次是甲藻门(11属14种),占总种数的23.33%;绿藻门有6属8种,占总种数的13.33%;裸藻门有3属3种,占总种数的5.00%;蓝藻门有2属2种,占总种数的3.33%。中肋骨条藻、虹彩圆筛藻、有棘圆筛藻(C.spinosus)、布氏双尾藻(Ditylum brightwelli)在大部分调查站位中均有分布(表 2)。可见珠江口南沙海域丰水期和枯水期的浮游植物物种组成相似,都是硅藻类占主体。
2.2 浮游植物种类的分布
浮游植物的区域分布具有季节差异,以丰水期较明显。丰水期S1站和S2站分别有38和30种,而S17站只有6种,表现为由河口内向外海递减的特征。枯水期该水域各站位浮游植物种类数比较接近(12~16种),也表现为由河口内向外海递减的特征(图 2)。
2.3 浮游植物细胞丰度的变化及分布
丰水期调查结果表明(图 3),浮游植物细胞丰度为(361.52~2 000.73)×104个· L-1,平均为651.91×104个· L-1,主要集中在万顷沙旁的水道,以S17站最高,其次是S19站(912.59×104个·L-1),S14站最低。细胞丰度组成大部分以硅藻为主,硅藻类平均细胞丰度为636.46×104个· L-1,占该海域浮游植物平均细胞丰度的97.63%,不同站位硅藻细胞丰度占比范围为92.95%~100.00%,其中S14站和S17站均只检出硅藻(图 3)。
枯水期调查结果表明,浮游植物细胞丰度为(4.00~698.40)×104个· L-1,平均为129.21×104个· L-1,也主要集中于万顷沙周围的水道,以S19站最高,其次是S6站(430.13×104个· L-1),S13站最低。细胞丰度组成大部分以硅藻为主,硅藻平均细胞丰度为117.25×104个· L-1,占海域浮游植物平均细胞丰度的90.74%,不同站位硅藻细胞丰度占比为4.88%~100.00%;此外,绿藻在S11站、S13站和S14站都占有较高的比例,裸藻在S17站也同样有较高的比例。
从浮游植物细胞丰度的平均值来看,丰水期的细胞丰度明显高于枯水期。两个时期从各个站位的细胞丰度来看,都是离岸的站位(S6~S9,S18~S20)高于近岸的站位(S1~S5,S10~S13),呈现出近岸向离岸递增的趋势。
2.4 优势种的组成及变化
调查海域浮游植物优势种结果显示,丰水期优势种2种,均为硅藻,新月筒柱藻的优势度最高(0.85);其次是中肋骨条藻,优势度为0.09。枯水期优势种3种,也均为硅藻,其中萎软海链藻(Thalassiosira mala)的优势度最高(0.25);其次是中肋骨条藻(0.20);有棘圆筛藻最低(0.02)。通过对丰水期和枯水期的对比,发现该海域的优势种均为硅藻类,其中中肋骨条藻是两时期的共有优势种,但也表现出季节性的演替现象,丰水期的优势种新月筒柱藻在枯水期更替为萎软海链藻。
2.5 群落多样性
珠江口南沙海域丰水期的H′为0.18~3.32,平均值为1.64;J′为0.07~0.72,平均值为0.40;而该海域枯水期的H′为0.59~2.56,平均值为1.58;J′为0.16~0.64,平均值为0.41(图 4)。丰水期时S4站的H′和J′最高;其次是S5站,分别是2.93和0.68;最低是S17站。枯水期时S1站、S3站、S4站和S10站的H′和J′都较其他站位高;而S9站和S17站则相对较低。
表 3为珠江口南沙海域浮游植物多样性评价结果,表中百分数表示各多样性指标隶属评判阈值的站位数占总站位数的百分比。可见丰水期时种类数、H′和J′都基本处于很低的水平,丰水期的多样性评判结果处于Ⅰ级水平。枯水期时由于H′略高,因此枯水期的多样性评判结果处于Ⅱ级水平。
表 3 珠江口南沙海域浮游植物多样性评价Table 3. Diversity evaluation for phytoplankton in the Nansha sea area of Pearl River Estuary季节
season很低
very low
(Ⅰ)低
low
(Ⅱ)一般
normal
(Ⅲ)高
high
(Ⅳ)很高
very high
(Ⅴ)总评价
general evaluation丰水期wet season 种类数(S)species number 87.50% 12.50% Ⅰ 多样性指数(H′)Shannon-Wiener diversity index 62.50% 37.50% Ⅰ 均匀度指数(J′)Pielous evenness index 100% Ⅰ 枯水期dry season 种类数(S) species number 40% 60% Ⅱ 多样性指数(H′)Shannon-Wiener diversity index 45% 45% 10% Ⅱ 均匀度指数(J′)Pielous evenness index 100% Ⅰ 2.6 浮游植物丰度与环境因子的关系
将浮游植物细胞丰度与水温、盐度进行Pearson相关回归系数分析(表 4),可以看出,丰水期浮游植物细胞丰度与水温呈显著负相关性(P < 0.05);枯水期浮游植物细胞丰度与盐度呈显著正相关性(P < 0.01)。可见温度和盐度对该海域浮游植物的群落结构有较大影响,而其他环境因子与细胞丰度相关性不明显。
表 4 珠江口南沙海域浮游植物细胞丰度与环境因子的相关性Table 4. Correlation between cell density of phytoplankton and environmental factors in the Nansha sea area of Pearl River Estuary季节
season水温
temperature盐度
salinity溶解氧
DO酸碱度
pH丰水期wet season -0.670* -0.209 0.208 0.378 枯水期dry season 0.491 0.597** -0.233 0.133 注:*.P < 0.05;* *.P < 0.01 2.7 典范对应分析
在CCA排序图中(图 5),丰水期与第1排序轴呈正相关的环境因子为盐度(SAL)、温度(TEM)、总氮(DIN)、透明度(SD)和磷酸盐(PO4),相关系数分别为0.978、0.813、0.786、0.567和0.490;与第1排序轴呈负相关的环境因子为溶解氧和pH,相关系数分别为-0.528和-0.018;与第2排序轴呈最大正相关和负相关的环境因子分别为磷酸盐和pH,相关系数分别为0.436和-0.623。枯水期与第1排序轴呈正相关关系的环境因子依次为温度、磷酸盐、盐度、总氮和透明度,相关系数分别为0.846、0.740、0.711、0.702和0.553;与第1排序轴呈负相关的环境因子为pH和溶解氧,相关系数分别为-0.754和-0.439;与第2排序轴呈最大正相关的环境因子为pH,相关系数0.430;透明度与第2排序轴呈最大负相关,相关系数为-0.804。结果表明丰水期和枯水期环境因子对浮游植物群落结构的影响作用存在差异,丰水期环境因子的重要性依次为盐度、温度、总氮、pH、透明度、溶解氧和磷酸盐,枯水期则为温度、透明度、磷酸盐、盐度、总氮、pH和溶解氧。
丰水期浮游植物优势种新月筒柱藻和中肋骨条藻分别位于第三象限和第四象限,新月筒柱藻与温度、总氮和磷酸盐呈负相关,与pH呈正相关;而中肋骨条藻与盐度、温度、总氮、磷酸盐、透明度和pH均呈正相关。枯水期浮游植物优势种萎软海链藻位于第三象限,与pH和透明度呈正相关,与温度和磷酸盐呈负相关;中肋骨条藻位于第四象限,与温度、透明度、磷酸盐、盐度和总氮呈正相关,与pH呈负相关;有棘圆筛藻则位于第一象限,与温度、透明度、pH、磷酸盐、盐度和总氮均呈正相关。
3. 讨论
3.1 浮游植物种类组成
根据珠江口海域浮游植物的特点,可划分为河口类、近岸类、外海类等3大生态类群[8],由于受到珠江水系径流汇入的影响,调查海域的盐度比较低,沿岸带来的营养盐较丰富,因此该海域的浮游植物大量生长和繁殖,种类的组成跨度较大,包括沿岸性种和淡水性种。浮游植物种类组成季节变化明显,丰水期共获得浮游植物37属68种(包括变种和变形),而枯水期共获得浮游植物44属60种(包括变种和变形)。与2008年~2010年在该海域的调查结果相比[10],当前该海域中硅藻类在总种类数中所占比例呈下降趋势,绿藻类所占比例呈现明显上升趋势。
3.2 浮游植物细胞丰度与优势种分布特征
调查发现,该海区浮游植物细胞丰度平面分布在丰水期和枯水期都呈现出由近岸区向离岸区递增的趋势(图 3)。位于龙穴岛东面的S6站、S7站、S8站和S9站以及离岸区的S19站和S20站都是浮游植物平均细胞丰度的高值区,较其他站位平均细胞丰度高,分析发现丰水期离岸高值区站位主要是由硅藻类新月筒柱藻大量繁殖造成的;枯水期离岸高值区站位主要是由硅藻类的萎软海链藻和中肋骨条藻繁殖引起。
优势种在群落中起着主导作用,决定着群落结构中的能量传递和物质循环的途径和方式,支配着群落结构的演替方向[18]。丰水期时的优势种为新月筒柱藻和中肋骨条藻,这2种硅藻都属于广温广盐性藻类,其中新月筒柱藻是一种分布广、高繁殖力的底栖硅藻,也是引发赤潮的一种重要藻类[19],在丰水期其细胞丰度占总细胞丰度的85.15%,特别是S17站,该藻细胞丰度百分比为97.70%;枯水期时的优势种是萎软海链藻、中肋骨条藻和有棘圆筛藻,种类相对较多且优势种发生了更替,由以新月筒柱藻向萎软海链藻和中肋骨条藻优势度并重演替。丰水期时优势种以淡水种和广温广盐种为主,但枯水期时主要是以广温广盐种为主,其中有棘圆筛藻是低温高盐种,这与各个时期由于地表径流引起的水体温度和盐度变化相适应。
丰水期的新月筒柱藻和枯水期的萎软海链藻及中肋骨条藻的细胞丰度分布格局呈现近岸向离岸递增的趋势,这同该海区浮游植物总细胞丰度的分布格局相一致。同时该海域的优势种新月筒柱藻、中肋骨条藻和萎软海链藻都是属于赤潮藻类,说明该海域富营养化严重,有较大的赤潮爆发风险[19]。
3.3 浮游植物群落结构多样性
珠江口南沙海域丰水期和枯水期浮游植物种类数的分布都表现为由河口处向外递减的特征(图 2、图 3),这是由于该海域生长繁殖的主要是以淡水种和广温广盐种为主的藻类[8],盐度的升高反而成为抑制淡水种生长繁殖的因子。藻类平均种类数丰水期略多于枯水期,这是由于丰水期地表径流的增加,导致低盐度的水域扩大,从而使淡水藻类和广温广盐藻类生长繁殖区间扩大,其中丰水期离河口最近的S1站的种类数明显高于同时期的各站位种类数,离河口较远的S19站和S20站的种类数都比较低;而枯水期各站位的种类数较接近(12~16种),这是由于枯水期地表径流的减小,高盐度的海水入侵,导致淡水藻类生长繁殖区间减小,因此以广温广盐类藻类为主。多样性评价结果表明枯水期高于丰水期,但总体而言,两时期的多样性和均匀度都处于较低水平,表明珠江口南沙段海域水质状况一般,水环境受到了一定程度的污染,水域生态系统较为脆弱。
3.4 浮游植物群落结构与水温、盐度的关系
浮游植物群落结构与盐度、水温、营养盐、海流、光照等环境因子存在一定的相关性[20-22],其中水温、盐度是影响浮游植物分布的重要因素[23-25]。广州南沙海域浮游植物群落是以硅藻类为主体的浮游植物群落结构,丰水期和枯水期的细胞丰度都呈现出近岸向离岸递增的趋势。从浮游植物丰度和环境因子的关系,并结合CCA分析可以看出,温度、盐度仍是影响该海区浮游植物的主要环境因子。丰水期细胞丰度与水温、盐度呈负相关性;枯水期细胞丰度则与水温、盐度呈正相关性。由于丰水期浮游植物丰度主要受优势种新月筒柱藻丰度的影响,而新月筒柱藻与温度和盐度呈负相关(图 5-a),这可能是丰水期浮游植物丰度与温度和盐度呈负相关的原因。而枯水期优势种中肋骨条藻和有棘圆筛藻以及浮动弯角藻等多数常见种与温度、盐度呈正相关(图 5-b),而这些种类是枯水期浮游植物丰度的重要组成部分,这可能是浮游植物丰度与温度、盐度呈正相关的主要原因。此外,浮游植物种类不同,其适应的水温和盐度的范围也不同。丰水期时优势种以淡水种和广温广盐种为主,盐度的升高反而抑制了淡水种的生长繁殖,导致细胞丰度的分布格局跟温盐的分布呈现负相关;而枯水期时优势种主要以广温广盐种为主,水温的变化范围为24.7~26.6 ℃,此时细胞丰度与水温呈正相关,表明该水域水温适合大部分藻类的生长,并且随着水温的升高,浮游植物细胞丰度呈增长的趋势,盐度的变化范围为0.14~21.39,适合广温广盐类的藻类生长繁殖,因此枯水期细胞丰度的分布格局与温盐分布格局呈正相关。
4. 小结
1) 调查结果表明,珠江口南沙海域共鉴定浮游植物5门44属76种,种类的组成跨度较大,包括淡水种和广温广盐种,其中硅藻为最主要优势种群。丰水期优势种有2种,分别为新月筒柱藻(0.85)和中肋骨条藻(0.09);枯水期优势种有3种,分别为萎软海链藻(0.25)、中肋骨条藻(0.20)和有棘圆筛藻(0.02)。
2) 丰水期和枯水期浮游植物平均细胞丰度分别为651.91×104个· L-1和129.21×104个· L-1,分别以S17站和S19站最高,而细胞丰度最低的站位位置接近(分别是S14站和S13站)。丰水期和枯水期的细胞丰度分布都表现为近岸向离岸递增的趋势。
3) H′和J′的平均值在丰水期分别为1.64和0.40,而在枯水期分别为1.58和0.41。调查海区的浮游植物群落结构多样性总体处于较低水平,表明珠江口南沙海域水质状况一般,水环境受到了一定程度的污染。
4) 环境因子对珠江口南沙海域浮游植物群落结构有明显影响,丰水期主要影响因子为盐度、温度、总氮和pH;枯水期为温度、透明度、磷酸盐和盐度。
此研究采样频次偏少,今后应加强对其季节演替及动态变化的研究,以更好地理解人类活动干扰下珠江口生态系统的变化过程。
-
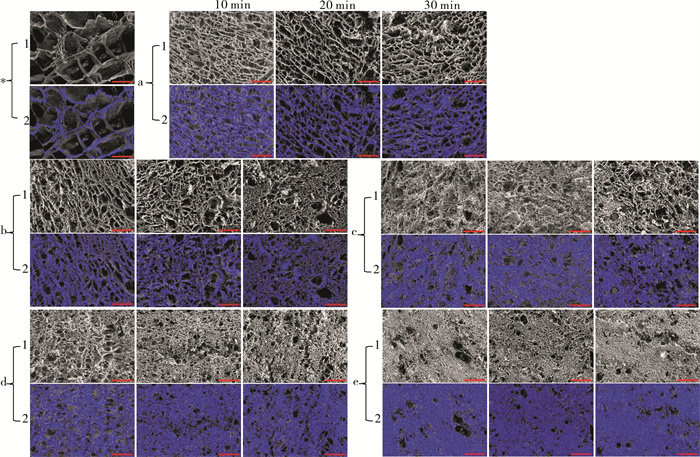
图 2 不同温度和时间下花刺参体壁横截面形态
*.新鲜体壁;a~e.水煮温度分别为50 ℃、60 ℃、70 ℃、80 ℃、90 ℃;行1. SEM原图,放大倍数=100倍,比例尺=250 μm;行2.行1原图中纤维被切割的部分用蓝色替代;列10 min.水煮时间10 min;列20 min. 水煮时间20 min;列30 min. 水煮时间30 min
Figure 2. Cross-section morphology of body wall at different temperatures and time during cooking
*. fresh body wall; a~e. cooking at 50 ℃, 60 ℃, 70 ℃, 80 ℃ and 90 ℃, respectively; Line 1. SEM photographs, magnification: 100, scale bar=250 μm; Line 2. cross-section of fibers in photographs of Line 1 is replaced by blue colors in Line 2;column 10 min. cooking for 10 min; column 20 min.cooking for 20 min; column 30 min. cooking for 30 min
表 1 不同温度和时间下花刺参体壁失重率
Table 1 Weight loss of body wall at different temperatures and time during cooking
温度/℃
temperaturet/min 失重率/%
rate of weight loss50 10 10.25±1.15a 20 12.85±1.72a 30 15.35±2.22a 60 10 27.75±2.22b 20 47.89±2.13c 30 56.91±1.76cd 70 10 66.05±2.70de 20 79.51±2.73f 30 80.40±2.16f 80 10 83.31±2.66f 20 84.60±1.26f 30 87.19±2.60f 90 10 84.37±2.23f 20 86.38±1.36f 30 86.05±2.06f 新鲜体壁fresh body wall 含水量 93.67±0.86g 注:数值由“平均值±标准差”表示,数值右上角不同字母表示差异显著(P<0.05),下表同此
Note:Data are expressed as X±SD of three determinations,and values with different superscript letters are significantly different from one another (P<0.05). The same case in the following tables.表 2 不同温度和时间下花刺参体壁蛋白溶失率
Table 2 Protein loss of body wall at different temperatures and time during cooking
温度/℃
temperaturet/min 蛋白溶失率/% 标准品BSA
rate of protein loss BSA as standard蛋白溶失率/% 标准品PSC
rate of protein loss PSC as standard50 10 0.09±0.03a 0.28±0.03a 20 0.12±0.03a 0.41±0.07a 30 0.14±0.02a 0.47±0.05a 60 10 0.18±0.04ab 1.74±0.12b 20 0.19±0.03ab 2.75±0.08c 30 0.20±0.02ab 2.82±0.08c 70 10 0.33±0.09b 5.65±0.10d 20 0.49±0.08bc 6.89±0.09d 30 0.52±0.07bc 7.15±0.11d 80 10 0.82±0.07d 7.78±0.11d 20 1.95±0.08e 13.10±0.06ef 30 2.51±0.08f 16.67±0.11f 90 10 1.77±0.09e 11.89±0.11e 20 2.56±0.10f 15.91±0.06f 30 2.72±0.08f 17.84±0.09f 表 3 不同温度和时间下花刺参体壁纤维横截面与总横截面积比
Table 3 Ratio of CFCA to WCA at different temperatures and time during cooking
温度/℃
temperaturet/min CFCA/WCA比值/%
ratio of CFCA to WCA新鲜体壁fresh body wall 4.84±0.18a 50 10 12.59±1.34b 20 13.00±1.91b 30 13.05±1.79b 60 10 13.35±1.69b 20 14.96±2.26b 30 16.69±2.35bc 70 10 15.67±2.39bc 20 16.91±1.42bc 30 18.08±1.88c 80 10 17.68±1.32c 20 18.64±1.97c 30 21.76±1.63cd 90 10 19.89±2.42c 20 20.80±1.58cd 30 24.28±2.39d -
[1] TORAL G V, LOVATELLI A, VASCONCELLOS M. Sea cucumbers: a global review of fisheries and trade[M]. Rome: FAO, 2008: 317. https://xueshu.baidu.com/usercenter/paper/show?paperid=bb9174e4680af975470d8aa3c9b20df8&site=xueshu_se
[2] BORDBAR S, ANWAR F, SAARI N. High-value components and bioactives from sea cucumbers for functional foods: a review[J]. Mar Drugs, 2011, 9(10): 1761-1805. doi: 10.3390/md9101761
[3] BOUME M. Food texture and viscosity: concept and measurement[M]. New York: Academic Press, 2002: 1-32. doi: 10.1046/j.1365-2621.2003.00667.x
[4] DHINGRA D, MICHAEL M, RAJPUT H, et al. Dietary fibre in foods: a review[J]. J Food Sci Tech, 2012, 49(3): 255-266. doi: 10.1007/s13197-011-0365-5
[5] SAITO M, KUNISAKI N, URANO N, et al. Collagen as the major edible component of sea cucumber (Stichopus japonicus)[J]. J Food Sci, 2002, 67(4): 1319-1322. doi: 10.1111/j.1365-2621.2002.tb10281.x
[6] 高昕, 刘莲凤, 刘倩, 等. 不同加热温度下刺参肌肉组织与胶原纤维结构的变化[J]. 水产学报, 2012, 36(9): 1465-1472. https://xueshu.baidu.com/usercenter/paper/show?paperid=cbb3d3fc52b3099c5e0bc73e22e2e12b&site=xueshu_se&hitarticle=1 [7] GAO X, ZHANG Z, LIU L, et al. Rheological changes of sea cucumber Stichipus japonicus during different heated times[J]. Int J Fish Aquac, 2011, 2(14): 258-262. https://www.semanticscholar.org/paper/Rheological-changes-of-sea-cucumber-Stichipus-times-Gao-Zhang/bea26db4a0d111747cd9c8dc5dc803a428fbfc7a
[8] LIU L, ZHANG Z, LIU Q, et al. Rheological and structural properties of sea cucumber Stichopus japonicus during different heating temperature[J]. Int J Fish Aquac, 2012, 4(10): 209-216. doi: 10.1007/s11802-005-0041-3
[9] DONG X, ZHU B, SUN L, et al. Changes of collagen in sea cucumber (Stichopus japonicas) during cooking[J]. Food Sci Biotechnol, 2011, 20(4): 1137-1141. doi: 10.1007/s10068-011-0155-x
[10] GAO X, XUE D, ZHANG Z, et al. Rheological and structural properties of sea cucumber Stichopus japonicus during heat treatment[J]. J Ocean Univ China, 2005, 4(3): 244-247. doi: 10.1007/s11802-005-0041-3
[11] 陈言峰, 胡超群, 任春华. 单一或二元的凡纳滨对虾新鲜养殖废物用于花刺参养殖的研究[J]. 南方水产科学, 2014, 10(1): 1-8. doi: 10.3969/j.issn.2095-0780.2014.01.001 [12] 姜松, 王军红, 范嗣刚, 等. 添加光合细菌对糙海参幼苗培育阶段的影响研究[J]. 南方水产科学, 2014, 10(6): 78-82. doi: 10.3969/j.issn.2095-0780.2014.06.011 [13] 李海鹏, 罗鹏, 于宗赫, 等. 热带海参糙刺参野外网箱养殖的初步研究[J]. 南方水产科学, 2013, 9(6): 1-7. doi: 10.3969/j.issn.2095-0780.2013.06.001 [14] BRUCKNER A, JOHNSON K, FIELD J. Conservation strategies for sea cucumbers: can a CITES Appendix Ⅱ listing promote sustainable international trade?[J]. SPC Bêche-de-mer Info Bull, 2003, 18: 24-33. https://www.semanticscholar.org/paper/Conservation-strategies-for-sea-cucumbers-%3A-Can-a-Bruckner-Johnson/aeab3fc0ecdbf5cc9bf5dd7c695771797e46de14
[15] HU C, XU Y, WEN J, et al. Larval development and juvenile growth of the sea cucumber Stichopus sp. (Curry fish)[J]. Aquaculture, 2010, 300(1/2/3/4): 73-79. https://www.semanticscholar.org/paper/Larval-development-and-juvenile-growth-of-the-sea-Hu-Xu/bbd3a9f058d0f7b4ed4c34938c68d9d6523a99b7
[16] KRIEG R C, DONG Y, SCHWAMBORN K, et al. Protein quantification and its tolerance for different interfering reagents using the BCA-method with regard to 2D SDS PAGE[J]. J Biochem Bioph Meth, 2005, 65(1): 13-19. doi: 10.1016/j.jbbm.2005.08.005
[17] MORENO H, MONTERO M, GOMEZ-GUILLEN M, et al. Collagen characteristics of farmed Atlantic salmon with firm and soft fillet texture[J]. Food Chem, 2012, 134(2): 678-685. doi: 10.1016/j.foodchem.2012.02.160
[18] PALKA K, DAUN H. Changes in texture, cooking losses, and myofibrillar structure of bovine M-semitendinosus during heating[J]. Meat Sci, 1999, 51(3): 237-243. doi: 10.1016/S0309-1740(98)00119-3
[19] CHEN J, STOKES J R. Rheology and tribology: two distinctive regimes of food texture sensation[J]. Trends Food Sci Tech, 2012, 25(1): 4-12. doi: 10.1016/j.tifs.2011.11.006
[20] NISHINARI K, KOHYAMA K, KUMAGAI H, et al. Parameters of texture profile analysis[J]. Food Sci Technol Res, 2013, 19(3): 519-521. doi: 10.3136/fstr.19.519
[21] GURDAK E, BOOTH J, ROBERTS C J, et al. Influence of collagen denaturation on the nanoscale organization of adsorbed layers[J]. J Colloid Interf Sci, 2006, 302(2): 475-484. doi: 10.1016/j.jcis.2006.06.064
[22] PURNA SAI K, BABU M. Studies on Rana tigerina skin collagen[J]. Comp Biochem Phys B, 2001, 128(1): 81-90. doi: 10.1016/S1096-4959(00)00301-8
[23] AHMAD M, BENJAKUL S, NALINANON S. Compositional and physicochemical characteristics of acid solubilized collagen extracted from the skin of unicorn leatherjacket (Aluterus monoceros)[J]. Food Hydrocolloid, 2010, 24(6): 588-594. https://www.semanticscholar.org/paper/Compositional-and-physicochemical-characteristics-Ahmad-Benjakul/b97ec1252bf872b4273eb160bcd25f18d070f10e
[24] LIU Z, OLIVEIRA A C, SU Y C. Purification and characterization of pepsin-solubilized collagen from skin and connective tissue of giant red sea cucumber (Parastichopus californicus)[J]. J Agric Food Chem, 2010, 58(2): 1270-1274. doi: 10.1021/jf9032415
[25] YAN M, LI B, ZHAO X, et al. Characterization of acid-soluble collagen from the skin of walleye pollock (Theragra chalcogramma)[J]. Food Chem, 2008, 107(4): 1581-1586. doi: 10.1016/j.foodchem.2007.10.027
[26] SUN W, LI Q, ZHOU F, et al. Surface characterization of oxidized myofibrils using X-ray photoelectron spectroscopy and scanning electron microscopy[J]. J Agric Food Chem, 2014, 62(30): 7507-7514. doi: 10.1021/jf501272p
[27] JOHNSTON I A, ALDERSON R, SANDHAM C, et al. Muscle fibre density in relation to the colour and texture of smoked Atlantic salmon (Salmo salar L. )[J]. Aquaculture, 2000, 189(3/4): 335-349. https://www.semanticscholar.org/paper/Muscle-fibre-density-in-relation-to-the-colour-and-Johnston-Alderson/4b7d67701eef0c08db6deea87f72e9aaf2304666
[28] LEPETIT J, GRAJALES A, FAVIER R. Modelling the effect of sarcomere length on collagen thermal shortening in cooked meat: consequence on meat toughness[J]. Meat Sci, 2000, 54(3): 239-250. doi: 10.1016/S0309-1740(99)00086-8
[29] NISHIMURA T. The role of intramuscular connective tissue in meat texture[J]. Anim Sci J, 2010, 81(1): 21-27. doi: 10.1111/j.1740-0929.2009.00696.x
[30] CIVILLE G V. Food texture-pleasure and pain[J]. Abst Papers Am Chem Soc, 2009, 238(5): 297. https://pubmed.ncbi.nlm.nih.gov/20831247/
-
期刊类型引用(9)
1. 张良奎,林雅君,向晨晖,黄亚东,郑传阳,宋星宇. 粤港澳大湾区近海浮游植物群落结构特征及其驱动因素. 生态科学. 2024(04): 1-10 .  百度学术
百度学术
2. 高广银,李学恒,唐灵刚,李颖颖. 秋冬季浮游植物群落结构特征及其环境因子关系——以珠江口南沙海域为例. 绿色科技. 2024(20): 74-78+84 .  百度学术
百度学术
3. 陈亮东,詹建坡,王庆. 珠江典型河段浮游植物群落结构特征及其对水质的指示作用. 南方水产科学. 2023(06): 1-10 .  本站查看
本站查看
4. 蒋佩文,李敏,张帅,陈作志,徐姗楠. 基于环境DNA宏条码和底拖网的珠江河口鱼类多样性. 水生生物学报. 2022(11): 1701-1711 .  百度学术
百度学术
5. 李桂娇,冯洁娉,叶锦韶. 南沙港海区水质变化与浮游植物群落更替特征. 生态科学. 2021(05): 164-171 .  百度学术
百度学术
6. 姚艳欣,陈楠生. 珠江口及其邻近海域赤潮物种的生物多样性研究进展. 海洋科学. 2021(09): 75-90 .  百度学术
百度学术
7. 陈思,李艺彤,蔡文贵,陈海刚,田斐,张林宝,张喆,郭志勋. 虾蟹混养池塘浮游植物群落结构的变化特征. 南方水产科学. 2020(03): 79-85 .  本站查看
本站查看
8. 李亚军,王先明,程贤松,魏盟智,李江月,朱为菊,邓晓东. 海南岛海尾湾浮游植物群落结构及水质的调查. 热带生物学报. 2020(03): 257-265 .  百度学术
百度学术
9. 李希磊,于潇,卢钰博,杨俊丽,崔龙波. 2015—2017年莱州湾招远海域扇贝养殖区浮游藻类群落变化. 南方水产科学. 2019(04): 11-18 .  本站查看
本站查看
其他类型引用(4)




 下载:
下载:




 粤公网安备 44010502001741号
粤公网安备 44010502001741号
