Effect of pearl culture on N19 and Prismalin-14 genes expression in the pearl oyster Pinctada fucata
-
摘要:
为探讨育珠对壳基质蛋白基因表达的影响,开展了合浦珠母贝(Pinctada fucata)N19和Prismalin-14基因在育珠贝和非育珠贝中的荧光定量表达研究。结果显示,N19和Prismalin-14在育珠贝与非育珠贝的闭壳肌、肝胰脏、性腺、肠、鳃等组织中均无表达,在外套膜均有表达;N19在珍珠囊表达,而Prismalin-14则不表达。N19与Prismalin-14在育珠贝外套膜的表达量均大于非育珠贝,表明育珠可能对某些壳基质蛋白的表达具有一定的促进作用。其中Prismalin-14在育珠贝外套膜的表达量最高(P<0.01),是非育珠贝外套膜Prismalin-14的1.23倍,是育珠贝外套膜N19的25.04倍,是非育珠贝外套膜N19的41.04倍,推测在珍珠贝生长过程中,对Prismalin-14的需求量可能比N19大。N19在育珠贝珍珠囊中表达量最高(P<0.01),是育珠贝N19外套膜的11.58倍,是非育珠贝外套膜的18.97倍,推测在珍珠形成的过程中,对N19的需求量可能比贝壳自身生长对N19的需求量大。
Abstract:To investigate the effect of pearl culture on the expressions of genes encoding shell matrix proteins, the relative expression levels of N19 and Prismalin-14 genes in the pearl-culturing oysters (PC) and non-pearl-culturing oysters (NPC) Pinctada fucata were investigated by using RT-FQ-PCR. The results show that the expressions of both N19 and Prismalin-14 are extremely weak or negative in muscle, liver, gonad, bowel or gill of PC and NPC, but positive in the mantle. The expression of N19 is obviously in pearl sac, while of Prismalin-14 is negative. The expressions of both N19 and Prismalin-14 in PC mantle are higher than that in NPC, which indicate pearl culture may promote expressions of some shell matrix protein genes. The relative expression level of Prismalin-14 is the highest (P < 0.01) in PC mantle, which is 1.23-fold greater than that of NPC mantle, 25.04-fold greater than N19 in PC mantle, 41.04-fold greater than N19 in NPC mantle, suggesting that pearl oysters may demand much more Prismalin-14 than N19 does. Meanwhile, the relative expression level of N19 is the highest in the pearl sac (P < 0.01), being 11.58-fold greater than that of the PC mantle, 18.97-fold greater than that of the NPC mantle, suggesting that pearl growth may demand much more N19 than shell growth does.
-
Keywords:
- shell matrix protein /
- RT-FQ-PCR /
- gene expression /
- pearl culture
-
剩余产量模型因其简单的形式和所需数据较少的特点为渔业资源评估广泛采用[1]。当渔获物的年龄组成无法精确获得时,年龄结构模型(age-structured model)便不能应用,而剩余产量模型只需多年的渔获量和捕捞努力量或单位捕捞努力量渔获量的渔业统计数据。剩余产量模型也可作为年龄结构模型的辅助工具,为渔业动态研究提供不同的思路。这类模型的优点在于其形式简单便于评估和评估结果比较易于理解[2]。通常较难获得现实渔业的相关参数真值,文章主要利用蒙特卡罗(Monte Carlo)模拟方法来检验连续Fox产量模型在几种不同渔业史条件下的模拟渔业中评估结果的有效性,借此来探索能使连续Fox产量模型产生最佳评估效果所需要的渔业条件,为渔业管理部门和渔业种群数量变动的研究人员使用该种模型对真实渔业进行管理和研究时提供参考。
1. 材料与方法
1.1 模型
Fox模型[3]是一个连续的微分方程,假定生长率与生物量的关系为Gompertz分布,方程如下:
$$ d B_t/d t=r B_t \ln \left(K/B_t\right)-C_t $$ (1) 式中Bt表示t时间的生物量,dBt/dt为种群增长率,r为种群内禀生长率,K为种群最大生物量或称环境容纳量,Ct为t时间的捕捞量。
设时间间隔为一年对方程(1)进行积分,得到一个连续的Fox形生物量动态方程:
$$ \begin{aligned} & \ln B_{t+1}=\left(1-\mathrm{e}^{-r}\right) \ln (K)+\mathrm{e}^{-r} \ln \left(B_t\right)-(1- \\ & \left.\mathrm{e}^{-1}\right) r^{-1} F_t \end{aligned} $$ (2) $$ \begin{aligned} &\text { 渔获量: } C_t=\int_t^{t+1} F_t B_t d t=F_t \int_{B_t}^{B_{t+1}} d B_t/[rln (K)\\ &\left.-r \ln \left(B_t\right)-F_t\right] \end{aligned} $$ (3) $$ \begin{aligned} & \quad C_t=F_t B_t\left[\left(1+\mathrm{e}^{-r}/r-r^{-1}\right) \times\left(\ln (K)-\ln \left(B_t\right)\right.\right. \\ & \left.\left.-r^{-1} F_t\right)+1\right] \end{aligned} $$ (4) Ft为t时刻的捕捞死亡系数。Ft=qft,q为可捕系数,ft为t年中的捕捞努力量。
1.2 评估方法
文章所用的评估方法是假设生物量方程(2) 没有误差,误差仅出现在渔获量方程(4)中。因此,此模型估计参数的方法为观测误差估计法,假设渔获量方程存在相乘的误差结构,目标函数表示为:
$$ \min \sum\limits_{t=1}^{\mathrm{T}}\left[\ln \left(C_t\right)-\ln \left(\hat{C}_t\right)\right]^2 $$ 其中t表示年份,Ct表示t年中渔获量的观测值,Ĉt表示t年中渔获量的估计值。应用Excel中的规划求解计算出参数的估计值。直接计算的参数包括B1 (第一年的生物量)、r (种群内禀增长率)、K (环境容纳量)和q (可捕系数)。具体算法如下:
(1) 给出4个参数(B1、r、K、q)的起始估计值。
(2) 利用方程(2)计算出逐年的生物量,再利用方程(4)计算逐年的渔获量估计值。
(3) 最小化目标函数。
(4) 监测目标函数收敛性,如果收敛, 计算结束。否则,调整各个参数起始值后,从步骤2重新做,直至目标函数收敛。
当种群的参数(B1、r、K和q)通过非线性回归方法得出后,相应重要的管理参数可以计算得出fMSY=r/(2q),MSY=rKe-1,其中MSY表示最大可持续产量(maximal stay yield),fMSY表示获得最大可持续产量时的捕捞努力量。
文章通过以下各项指标来比较模型在各个渔业中的评估效果,参数估计值与真值之间的偏差(relative bias of median,RBM%)=|真实值-估计值|×100%/真实值,各个参数的四分位数间距(interquartile range,IQR),相对四分位数间距(relative interquartile range,RIQR%)=四分位数间距×100%/中值。预测误差百分数(percentage prediction error,PPE%)=|CPUE真实值-CPUE估计值|×100%/CPUE真实值[3]。为了计算真实渔业各参数的各项指标,文章采用了非参数化Bootstrap分析法[4],Bootstrap分析过程重复了1 000次,在随机抽取数据过程中,采用的是成对抽取数据。
1.3 模拟渔业
文章采用蒙特卡罗模拟方法产生数据,该方法需要一个操作模型和一个评估模型,采用的操作模型和评估模型都是连续形Fox产量模型。假设不同的渔业史或渔业过程,即给出不同的捕捞努力量变化过程,根据连续形Fox产量模型方程(2)、(4),计算出相应渔业的模拟生物量和渔获量,在此基础上叠加正态分布的随机数[5]作为该渔业的观测值。文章设置了不同的白色噪音水平(变异系数为1%、10%、30%和50%)。种群参数的真值都设为r=0.4,K=1 000,q=0.01,B1的真值随不同的渔业过程而不同。根据相应的计算公式主要的管理参数真值为fMSY=20,MSY=147.15。图 1-a显示的是一种过度捕捞型渔业,以下称为渔业一;该渔业从开始就经历了高的捕捞努力量,并且捕捞努力量逐年增加,生物量逐渐减少。图 1-b显示的是一种恢复型渔业,以下称为渔业二;该渔业由于经历了过度捕捞的缘故,初始阶段生物量较低, 随后采取了保护措施,捕捞努力量一直被限制在较低的水平,生物量随着时间不断增加。图 1-c显示的是一种波动型渔业,也可称为管理良好的渔业,以下称为渔业三;该渔业开始于资源未开发阶段,加入高捕捞努力量生物量下降,然后限制捕捞努力量,生物量逐渐增加,生物量和捕捞努力量随时间上下波动。
1.4 真实渔业
北大西洋剑鱼渔业评估所用数据是ICCAT对该渔业产量和生物量丰度指标——单位捕捞努力渔获量(catch per unit of effort,CPUE)的统计[6],共有1975~1998年24年间的数据,该渔业1988年以前产量逐渐升高,但是CPUE却不断降低,随后产量逐渐降低,CPUE降低趋势趋于平缓(图 2)。
2. 结果
文章对每种渔业在不同白色噪音水平下分别进行了1 000次模拟分析计算,去除部分无效结果(包括参数值< 0、q>=1、B1>K 3种情况)按白色噪音0.01、0.1、0.3、0.5的顺序,各渔业的有效结果次数,渔业一为524、577、639、172;渔业二为496、355、114、22;渔业三为485、445、425、90。取各估计参数的中值为参数的估计值。RBM%、IQR、RIQR%的最终计算结果列于表 1~表 3。
表 1 参数估计值与真实值之间偏差RBM%Table 1. Bias between the estimated and true parameter values白色噪音 white noise 0.01 0.1 0.3 0.5 B1 渔业一 7.1×10-10 2.2×10-4 10.2 21.4 渔业二 1.1×10-6 2.61 0.3 0.3 渔业三 1.9×10-6 0.64 0.9 2.9 r 渔业一 0.001 0.73 2.7 1.8 渔业二 0.03 0.02 1.4 7.8 渔业三 0.01 0.57 0.9 11.5 K 渔业一 1.1×10-8 0.3 2.6×10-4 4.3 渔业二 6.11×0-7 9.3×10-4 0.6 6.0 渔业三 6.3×10-10 0.9 7.5 17.2 q 渔业一 0.2 1.31 0 7.5 渔业二 0.2 0.26 3.4 32.8 渔业三 0.3 2.8 16.7 2.4 最大可持续产量
MSY渔业一 0.01 0.5 3.8 2.0 渔业二 0.02 1.07 0.1 6.9 渔业三 6.5×10-4 0.08 5.8 1.9 最大可持续产量时的捕捞努力量
fMSY渔业一 0.2 1.4 0.4 3.8 渔业二 0.2 0.04 8.6 36.7 渔业三 0.3 3.3 12.0 15.2 表 2 参数估计值的四分位数间距IQRTable 2. Interquartile range of the estimated parameters白色噪音 white noise 0.01 0.1 0.3 0.5 B1 渔业一 2 222 976 1 306 渔业二 3 139 268 325 渔业三 13 136 411 799 r 渔业一 0.001 0.04 0.20 0.26 渔业二 0.002 0.10 0.20 0.20 渔业三 0.002 0.04 0.14 0.20 K 渔业一 0.2 192 878 1 172 渔业二 0.7 565 1 036 828 渔业三 9.0 209 621 1 287 q 渔业一 6.6×10-5 0.002 0.01 0.013 渔业二 9.9×10-5 0.006 0.01 0.012 渔业三 6.4×10-5 0.002 0.006 0.007 最大可持续产量
MSY渔业一 0.5 14 56 83 渔业二 0.6 40 81 66 渔业三 0.6 14 44 81 最大可持续产量时的捕捞努力量
fMSY渔业一 0.1 2.6 11.7 14.5 渔业二 0.3 6.5 12.7 8.6 渔业三 0.09 1.3 3.3 4.8 表 3 参数估计值的相对四分位数间距RIQR%Table 3. Relative IQR(RIQR%)of the estimated parameters白色噪音 white noise 0.01 0.1 0.3 0.5 B1 渔业一 0.3 4.9 110.8 134.5 渔业二 1.4 67.7 133.6 162.2 渔业三 1.6 17.1 51.9 97.1 r 渔业一 0.3 9.8 52.3 65.3 渔业二 0.4 24.2 48.9 44.8 渔业三 0.5 11.2 34.5 51.9 K 渔业一 0.2 19.2 87.8 112.4 渔业二 0.07 56.5 104.2 88.1 渔业三 0.9 20.7 67.1 109.9 q 渔业一 0.7 18.3 101.7 125.3 渔业二 0.9 57.0 137.9 92.6 渔业三 0.6 16.7 53.6 72.1 最大可持续产量
MSY渔业一 0.4 9.6 39.5 55.4 渔业二 0.3 26.8 55.1 48.5 渔业三 0.4 9.6 31.6 54.4 最大可持续产量时的捕捞努力量
fMSY渔业一 0.6 13.2 58.1 75.1 渔业二 1.3 32.5 69.3 68.3 渔业三 0.5 6.9 18.5 28.2 图 3、图 4体现了在白色噪音为10%的情况下3种模拟渔业的观测产量和估计产量的对比关系。
文章还计算了各渔业的预测误差百分数PPE%(图 5)。从总体上看,当白色噪音小于10%的情况下,所有模拟渔业的各个参数估计值接近于真实值。当白色噪音达到30%时,评估结果偏差较大,模型表现不好。从各参数的评估结果来看,渔业起始生物量B1和最大环境容纳量K的评估结果偏差较小,但是RIQR%较大,参数r和q的评估结果比较接近真值。MSY和fMSY的评估结果最为准确,总体RIQR%小于75.1%。从不同渔业来看,用RBM%来衡量,模型在渔业一中的表现为最好,其次为渔业三,各个渔业24个被估参数的偏差平均值,渔业一为2.6%、渔业为二4.6%、渔业三为4.3%;用RIQR%来衡量,模型在渔业三中表现最好,各渔业RIQR%的平均值,渔业一为46.6%、渔业二为55.1%、渔业三为31.6%。
对北大西洋剑鱼渔业的1 000次Bootstrap分析结果列于表 4中。为证明可靠渔业信息对评估结果准确性的影响,文章在白色噪音为0.1的情况下对参数加以约束,假设B1=0.2K,将评估参数减少为3个,对渔业2进行了分析计算,并将计算结果与参数未加约束时作了比较,比较结果见表 5。
表 4 北大西洋剑鱼渔业参数估计值和参数四份位数间距及相对四份位数间距Table 4. Median and IQR, IQR% for the North Atlantic swordfish fishery参数名称
parameter参数中值
median四分位数间距
IQR相对四分位数间距
RIQR%B1 30 773 6 021 19.6 r 0.94 0.05 5.6 K 44 733 2 697 6.0 q 0.013 0.001 9.2 最大可持续产量 MSY 15 678 621 3.9 最大可持续产量时的捕捞努力量 fMSY 37 4.5 12.3 表 5 约束参数与不约束参数评估结果比较Table 5. Comparison of the results with constrained and unconstrained parametersr K q 最大可持续产量
MSY最大可持续产量时的捕捞努力量
fMSY四分位数间距
IQR无约束 0.10 565 0.006 40.0 6.5 约束 0.03 116 0.001 8.9 2.1 相对四分位数间距
RIQR%无约束 24.2 56.5 57.0 26.8 32.5 约束 8.2 11.9 11.2 6.1 10.7 3. 讨论
采用连续Fox模型对渔业初始生物量B1和环境容纳量K的评估结果表明,虽然估计值与真实值之间的偏差较小,但是RIQR%较大,这是因为将中值作为最终参数估计值时个别较大值和较小值对中值影响很小,因此,建议将中值作为最终估计值来平衡个别较大值和较小值对结果的影响。B1和K的RIQR%较大,证明模型对这2个参数的评估结果不够理想,个别渔业甚至出现B1估计值高于环境容纳量K真实值的情况,在最终计算参数时将这样的结果归为无效结果删除,以防止影响结果的准确性,产生这种情况主要是由于白色噪音的影响及该模型对数据较为敏感。但是当B1估计值较大时,K估计值也偏高,B1估计值准确性较差可能主要是由于模型为非线性的,且同时要估计4个参数所导致的,在模拟分析计算时假设B1值与K值呈线性关系;如渔业二中假设B1=0.2K,这样评估参数减少为3个,如表 5所示,添加约束时各参数的IQR和RIQR%仅为未添加约束时的1/3左右,所得结果准确性明显好于同时评估4个参数时的结果。
具体的渔业种群评估中,如果能合理利用渔业信息以确定某个参数,则可以简化计算,并且能提高评估结果的准确性。
模型估计管理参数MSY和fMSY的准确性高于其它参数,这可能由于被估各参数间存在一定的相关性[7],MSY和fMSY的估计值是参数r、K、q以相乘或相除形式结合在一起,这样降低了单个参数估计偏差的影响程度。因此,管理参数MSY和fMSY的估计值更为准确[8]。
当白色噪音大于30%时,参数评估偏差较大,模型表现不好,这可能主要因为较高的白色噪音干扰了种群动态变动的内在规律。例如,噪音较大时曾出现观测产量为负值的不合理情况,使得模型不能捕捉渔业在没有噪音情况下的真实关系。所以,高质量的渔业统计数据对资源评估结果十分重要。
渔业三评估结果好于其它渔业可能因为该渔业经历了过度捕捞和恢复2个渔业阶段,渔业过程较为完整,所含数据信息丰富。而其它2种渔业的信息相对缺乏,导致模型对这2种渔业评估表现较渔业三差。
文章评估北大西洋剑鱼(Xiphias gladius)渔业的MSY为15 678 t,fMSY为37×106钩次·a-1;PRAGER[6]评估该渔业的MSY为14 070和14 510 t;孙利东[8]评估该渔业的MSY为12 493 t,fMSY为53×106钩次·a-1。文章评估的MSY与其它不同模型评估的MSY结果相差不大,证明连续性Fox模型对北大西洋剑鱼渔业的评估结果具有参考价值。该渔业的捕捞努力量从20世纪80年代开始就超过了文章评估的fMSY,这种情况造成了北大西洋剑鱼渔业的衰退,评估结果与图 2反映的情况吻合。从20世纪80年代开始该渔业的CPUE不断降低,为了保护和合理利用该渔业资源,应该将捕捞努力量严格控制到合理水平。
-
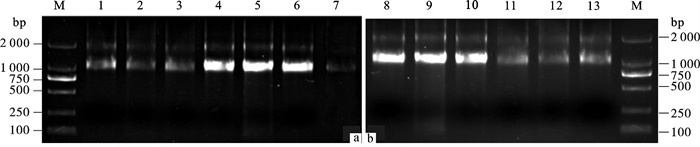
图 1 合浦珠母贝不同组织总RNA
a.育珠贝;b.非育珠贝;M.DNA分子质量标准DL2000;1~7. 鳃、性腺、肠、肝胰脏、外套膜、珍珠囊、闭壳肌;8~13.肝胰脏、外套膜、鳃、闭壳肌、性腺、肠
Figure 1. Total RNA extracted from P.fucata tissues
a. pearl-culturing oyster (PC); b. oyster without pearl-culture (NPC); M. DNA molecular weight marker (DL2000);1~7. gill, gonad, bowel, liver, mantle, pearl sac and muscle; 8~13. liver, bowel, gill, mantle, muscle and gonad
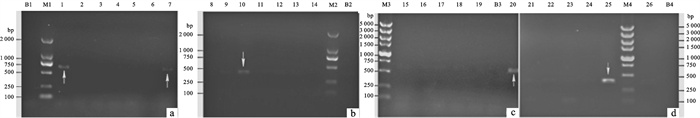
图 2 合浦珠母贝N19、Prismalin-14基因的组织表达谱[育珠贝(a、b)与非育珠贝(c、d)]
M1~M2. DNA分子质量标准DL2000;M3~M4. DNA分子质量标准DL5000;B1~B4.空白对照;1~7(N19).珍珠囊、鳃、性腺、肠、肝胰脏、闭壳肌、外套膜;8~14(Prismalin-14).肝胰脏、肠、外套膜、鳃、珍珠囊、闭壳肌、性腺;15~20(N19).闭壳肌、性腺、鳃、肠、肝胰脏、外套膜;21~26(Prismalin-14).肝胰脏、肠、鳃、闭壳肌、外套膜、性腺
Figure 2. The expression of N19 and Prismalin-14 genes in different tissues of P.fucata [PC(a, b) and NPC(c, d)]
M1~M2. DNA molecular weight marker (DL2000);M3~M4. DNA molecular weight marker (DL5000);B1~B4. blank control group; lane 1~7 (N19): pearl sac, gill, gonad, bowel, liver, muscle and mantle; lane 8~14 (Prismalin-14). liver, bowel, mantle, gill, pearl sac, muscle and gonad; lane 15~20 (N19). muscle, gonad, gill, bowel, liver, and mantle; lane 21~26 (Prismalin-14).liver, bowel, gill, muscle, mantle and gonad
表 1 引物序列
Table 1 Sequences of primers designed in this study
引物primer 引物序列(5′→3′)sequences PCR引物 N19-F CGGAATTCATGGTGTCCCATGCTCACAT primer for PCR N19-R CCCAAGCTTCTACGGCTTACAGCAACGGT Prismalin-14-F CGGAATTCATGCGATCTCTGCTAGTCCT Prismalin-14-R CCCAAGCTTTTAATCATCAAATCCGCCAT Real-Time FQ-PCR引物 N19-F-RT[16-17] TGGCAACAAAGCAGTCATAACCG primer for Real-Time FQ-PCR N19-R-RT[16-17] GGCGTCGTTGTAGCATTGAAGG Prismalin-14-F-RT[17] CAATGCGATCTCTGCTAGTCC Prismalin-14-R-RT[17] ATAGGAGAAACGCGGGAAATA 18S rRNA-F-RT TGTCTGCCCTATCAACTTTC 18S rRNA-R-RT TGTGGTAGCCGTTTCTCA -
[1] 胡曦璇, 石安静. 珍珠囊研究概况[J]. 水生生物学报, 1994, 18(1): 76-81. https://xueshu.baidu.com/usercenter/paper/show?paperid=b269449b51da12d8e9b0c71788c228f3&site=xueshu_se&hitarticle=1 [2] SUZUKI M, SARUWATARI K, KOGURE T, et al. An acidic matrix protein, Pif, is a key macromolecule for nacre formation[J]. Science, 2009, 325(5946): 1388-1390. doi: 10.1126/science.1173793
[3] 尹立鹏, 邓岳文, 杜晓东, 等. 贝龄对马氏珠母贝植核贝生长, 成活率和育珠性状的影响[J]. 中国水产科学, 2012, 19(4): 715-720. doi: 10.3724/SP.J.1118.2012.00715 [4] 金武. 三角帆蚌生长性状与育珠性状的遗传参数估计[D]. 上海: 上海海洋大学, 2012. https://d.wanfangdata.com.cn/thesis/ChhUaGVzaXNOZXdTMjAyNDA5MjAxNTE3MjUSB0QzNjYyNDUaCHR1cnE5c2du [5] 张希, 邢孔武, 喻达辉, 等. 合浦珠母贝不同来源群体小片贝的育珠效果比较[J]. 广东农业科学, 2011, 38(5): 153-154. doi: 10.3969/j.issn.1004-874X.2011.05.053 [6] 邓岳文, 邓陈茂, 杜晓东, 等. 细胞小片处理对马氏珠母贝育珠效果影响[J]. 海洋湖沼通报, 2011 (3): 46-49. doi: 10.3969/j.issn.1003-6482.2011.03.007 [7] YANO M, NAGAI K, MORIMOTO K, et al. A novel nacre protein N19 in the pearl oyster Pinctada fucata[J]. Biochem Biophys Res Commun, 2007, 362(1): 158-163. doi: 10.1016/j.bbrc.2007.07.172
[8] 张立娟, 何毛贤. 生长激素与胰岛素样生长因子-Ⅰ对马氏珠母贝壳生长形成相关基因表达的影响[J]. 热带海洋学报, 2012, 31(2): 96-101. doi: 10.3969/j.issn.1009-5470.2012.02.013 [9] SUZUKI M, MURAYAMA E, INOUE H, et al. Characterization of Prismalin-14, a novel matrix protein from the prismatic layer of the Japanese pearl oyster (Pinctada fucata)[J]. Biochem J, 2004, 382(Pt 1): 205-213.
[10] SUZUKI M, NAGASAWA H. The structure-function relationship analysis of Prismalin-14 from the prismatic layer of the Japanese pearl oyster, Pinctada fucata[J]. FEBS J, 2007, 274(19): 5158-5166. doi: 10.1111/j.1742-4658.2007.06036.x
[11] TAKEUCHI T, ENDO K. Biphasic and dually coordinated expression of the genes encoding major shell matrix proteins in the pearl oyster Pinctada fucata[J]. Mar Biotechnol, 2006, 8(1): 52-61. doi: 10.1007/s10126-005-5037-x
[12] INOUE N, ISHIBASHI R, ISHIKAWA T, et al. Gene expression patterns and pearl formation in the Japanese pearl oyster (Pinctada fucata): a comparison of gene expression patterns between the pearl sac and mantle tissues[J]. Aquaculture, 2010, 308: S68-S74. doi: 10.1016/j.aquaculture.2010.06.036
[13] INOUE N, ISHIBASHI R, ISHIKAWA T, et al. Comparison of expression patterns of shell matrix protein genes in the mantle tissues between high-and low-quality pearl-producing recipients of the pearl oyster, Pinctada fucata[J]. Zool Sci, 2011, 28(1): 32-36. doi: 10.2108/zsj.28.32
[14] YOKO M, TAKUMA N, HIDEO A, et al. Expression of genes responsible for biomineralization of Pinctada fucata during development[J]. Comp Biochem Physiol Part B: Biochem Mol Biol, 2010, 155(3): 241-248. doi: 10.1016/j.cbpb.2009.11.009
[15] 杨桂梅, 鲍宝龙, 任大明. 3-磷酸甘油醛脱氢酶、β-肌动蛋白和18S rRNA作为相对定量的内标在牙鲆发育阶段的稳定性比较[J]. 上海水产大学学报, 2005, 14(1): 84-88. [16] WANG N, KINOSHITA S, RIHO C, et al. Quantitative expression analysis of nacreous shell matrix protein genes in the process of pearl biogenesis[J]. Comp Biochem Physiol Part B: Biochem Mol Biol, 2009, 154(3): 346-350. doi: 10.1016/j.cbpb.2009.07.012
[17] ZHANG L, HE M. Quantitative expression of shell matrix protein genes and their correlations with shell traits in the pearl oyster Pinctada fucata[J]. Aquaculture, 2011, 314(1): 73-79. doi: 10.1016/j.aquaculture.2011.01.039
[18] SATO-OKOSHI W, OKOSHI K. Characteristics of shell microstructure and growth analysis of the Antarctic bivalve Laternula elliptica from Lützow-Holm Bay, Antarctica[J]. Polar Biol, 2008, 31(2): 131-138. doi: 10.1007/s00300-007-0340-9
[19] INOUE N, ISHIBASHI R, ISHIKAWA T, et al. Can the quality of pearls from the Japanese pearl oyster (Pinctada fucata) be explained by the gene expression patterns of the major shell matrix proteins in the pearl sac?[J]. Mar Biotechnol, 2011, 13(1): 48-55. doi: 10.1007/s10126-010-9267-1
[20] INOUE N, ISHIBASHI R, ISHIKAWA T, et al. Gene expression patterns in the outer mantle epithelial cells associated with pearl sac formation[J]. Mar Biotechnol, 2011, 13(3): 474-483. doi: 10.1007/s10126-010-9318-7
[21] 严俊, 邓小琼, 胡丹静, 等. 淡水养殖珍珠棱柱层的微结构形貌特征[J]. 南方水产科学, 2013, 9(1): 48-52. doi: 10.3969/j.issn.2095-0780.2013.01.008 [22] MA H, LI R, YANG L, et al. A modified integrated model of the internal structure of Chinese cultured pearls[J]. J Wuhan Univ Technol: Mater Sci Ed, 2011, 26(3): 510-513. doi: 10.1007/s11595-011-0258-5
[23] MA H, SU A, ZHANG B, et al. Vaterite or aragonite observed in the prismatic layer of freshwater-cultured pearls from South China[J]. Prog Nat Sci, 2009, 19(7): 817-820. doi: 10.1016/j.pnsc.2008.11.005
[24] MA H, ZHANG B, LEE I S, et al. Aragonite observed in the prismatic layer of seawater-cultured pearls[J]. Front Mater Sci China, 2007, 1(3): 326-329. doi: 10.1007/s11706-007-0061-6
-
期刊类型引用(6)
1. 张磊, 王锦旭, 杨贤庆, 魏涯, 杨少玲. 合浦珠母贝糖胺聚糖泡腾片制备工艺优化及其质量分析. 大连海洋大学学报. 2018(05): 644-650 .  百度学术
百度学术
2. 王珍珍, 黄桂菊, 范嗣刚, 刘宝锁, 张博, 苏家齐, 喻达辉. 合浦珠母贝matrilin-1基因的克隆和表达分析. 南方水产科学. 2017(01): 76-84 .  本站查看
本站查看
3. 谭才钢, 刘宝锁, 张东玲, 牛志凯, 张博, 陈明强, 范嗣刚, 姜松, 黄桂菊, 李有宁, 陈素文, 喻达辉. 合浦珠母贝主要形态性状与体质量的灰色关联分析. 南方水产科学. 2015(02): 35-40 .  本站查看
本站查看
4. 邹柯姝, 张殿昌, 郭华阳, 张楠, 江世贵. 4种壳色合浦珠母贝贝壳棱柱层和珍珠质层7种金属元素质量分数的比较分析. 南方水产科学. 2015(03): 74-79 .  本站查看
本站查看
5. 毕晓敏, 黄桂菊, 范嗣刚, 朱文杰, 喻达辉. 合浦珠母贝矿化基因Pearlin重组蛋白的表达条件优化. 南方水产科学. 2015(06): 100-106 .  本站查看
本站查看
6. 肖雅元, 徐姗楠, 刘永, 李纯厚. 0~#柴油水溶液对翡翠贻贝CYP4基因表达的影响研究. 南方水产科学. 2014(02): 61-66 .  本站查看
本站查看
其他类型引用(1)




 下载:
下载:





 粤公网安备 44010502001741号
粤公网安备 44010502001741号
