Study on distribution characteristics and storage variation of semicarbazide in Macrobrachium rosenbergii
-
摘要: 氨基脲 (Semicarbazide, SEM) 为一种有毒物质,是判断呋喃西林是否违规使用的标记性残留物。为探讨甲壳类水产品中氨基脲的检出情况,采用高效液相色谱-串联质谱联用法 (High performance liquid chromatography-mass spectrometry, HPLC-MS/MS) 对罗氏沼虾 (Macrobrachium rosenbergii) 中的SEM进行了检测。结果显示,罗氏沼虾不同部位均检出SEM,其中头胸甲和虾壳等甲壳部位SEM检出值较高 [平均 (32.02±3.75) 和 (26.85±13.90) μg·kg−1],肌肉和肝脏的SEM检出值较低 [平均 (1.35±0.67) 和 (5.56±0.87) μg·kg−1],均超过我国现行规定的残留限量标准 (1 μg·kg−1);罗氏沼虾虾壳和虾肉中的SEM检出值随贮藏时间的增加而减小,甲壳组织中SEM检出值始终高于1.0 μg·kg−1,而不同贮藏温度对罗氏沼虾中SEM检出值影响较小。因此,以SEM为标志物对罗氏沼虾进行呋喃西林残留检测时,应考虑样品贮藏时间及本底含量因素,以避免误判;同时为确保检测结果的真实性和准确性,在制备样品时应避免将碎壳混入虾肉中。Abstract: Semicarbazide (SEM) is a toxic substance, which is a marker residue to determine whether Nitrofurazone is used illegally or not. To explore the detection of SEM in Crustacean aquatic products, we detected the SEM content of M. rosenbergii by High Performance Liquid Chromatography-Mass Spectrometry (HPLC-MS/MS). The results show that SEM was detected in different parts of M. rosenbergii, higher in the cephalothorax and shrimp shell [Average: (32.02±3.75) and (26.85±13.90) μg·kg−1], but lower in the muscle and liver [Average: (1.35±0.67) and (5.56±0.87) μg·kg−1], and all exceeded the residue limit standards in China (1 μg·kg−1). The SEM content in the shrimp shell and shrimp meat increased with the prolongation of storage time, but that in the shrimp shell was higher than 1.0 μg·kg−1. Different storage temperatures had a little effect on the SEM content of M. rosenbergii. Therefore, when taking SEM as a marker for Nitrofurazone residue detection of M. rosenbergii, the detection time and background content factors should be considered so as to avoid false judgment; and in order to ensure the authenticity and accuracy of the test results, the crushed shell should be avoided in preparing samples.
-
氨氮 (NH4 +-N) 和亚硝酸盐 (NO2 −-N) 等无机氮是水产养殖主要的氮素污染物,对养殖动物具有较强的毒性,研究显示氨氮能明显抑制养殖动物的生理和免疫系统,而亚硝酸根离子 (NO2 −) 能够抑制血液载氧能力,通常在较低的浓度下危害水生动物健康,甚至导致死亡[1-5]。随着养殖密度不断提高,水体氨氮和亚硝酸盐浓度的快速累积造成了潜在危险。传统方法依靠大量换水降低氨氮和亚硝酸盐的浓度,会给周边环境造成污染,引起水体富营养化。近年来,随着国家对环境保护要求日趋严格,直排直灌的养殖方式已经不可持续,如何环保、高效地去除水体有害氮素是促进水产养殖成功的关键。
微生物在生态链中扮演分解者角色,是物质和能量循环的重要组成,利用有益微生物调控养殖水质是近年的研究热点[6-8]。胡晓娟等[9]发现菌株NB5对水体氨氮具有显著的去除效果,信艳杰等[10]利用光合细菌吸收水体氮 (N)、磷 (P)。不同的细菌具有不同的生态功能,在循环养殖系统中多用硝化细菌来消除氨氮和亚硝酸盐,但自养硝化细菌生长缓慢,且容易受环境影响,目前还未在水产养殖中大范围推广应用[11-12]。红球菌作为一类重要的模式微生物,在自然环境中分布广泛且菌株种类多样。由于红球菌具有降解有机污染物、生物转化和降解毒素等作用,在环境治理、生物合成与转化以及医药领域具有潜在的应用价值,其中赤红球菌 (Rhodococcus ruber) 生长快且易于培养,具有消除环境中氨氮和亚硝酸盐的潜力[13-14]。本实验室前期筛选到一株赤红球菌HDRR2Y,初步研究发现其可去除水体氨氮和亚硝酸盐[15]。细菌的功能与环境因素往往密切相关,为了更好地应用于水产养殖生产中,本文研究了赤红球菌HDRR2Y发酵液去除氨氮和亚硝酸盐的效果,并探讨了细菌浓度、温度、底物浓度、转速和盐度等5种常见的环境因子对HDRR2Y发酵液去除氨氮和亚硝酸盐功能的影响,以期为菌株HDRR2Y在水产养殖中的应用提供理论依据。
1. 材料与方法
1.1 菌株来源
赤红球菌HDRR2Y由中国水产科学研究院南海水产研究所提供,该菌种保藏于中国典型培养物保藏中心 (CCTCC NO: M2019009),已申请发明专利 (申请号:202010159584.2)。
1.2 菌株发酵
采用德国贝朗生物系统公司Biostat B型体积为2 L的发酵罐进行发酵培养,培养基为(g·L−1):三水合醋酸钠 [C2H3NaO2·3(H2O)] 3.0,酵母膏1.8,硫酸镁 (MgSO4) 0.2,磷酸二氢钾 (KH2PO4) 0.5,氯化钙 (CaCl2) 0.5,氯化钠 (NaCl) 9.0,硫酸锰 (MnSO4) 0.025,硫酸铁 (FeSO4) 0.05,谷氨酸 (C5H9NO4) 0.002。发酵条件为:29 ℃,36 h,pH 7.0,装液量1.2 L (60%),初始接种菌量1%,通气量3 L·min−1,搅拌转速400 r·min−1。
1.3 发酵过程中菌株浓度测定与形态观察
在菌株发酵第0、第18、第24、第30、第36小时通过50 mL注射器针筒以抽气、排气的方式获取发酵液,取样口在取样前后需用酒精灯灼烧,非取样时间用无菌锡箔纸包裹取样口。通过梯度稀释法将发酵原液制成十倍系列稀释匀液,取3个最适稀释度,每个稀释浓度设置3个平行组,然后进行平板涂布,置于培养箱内,在30 ℃、湿度90%的条件下培养24 h,待菌落形成后进行菌落计数。同时通过显微镜将菌株细胞放大1 000倍进行观察,记录下不同时间点采集的发酵液中细菌的细胞形态。
1.4 菌株培养液去除氨氮和亚硝酸盐效果测定
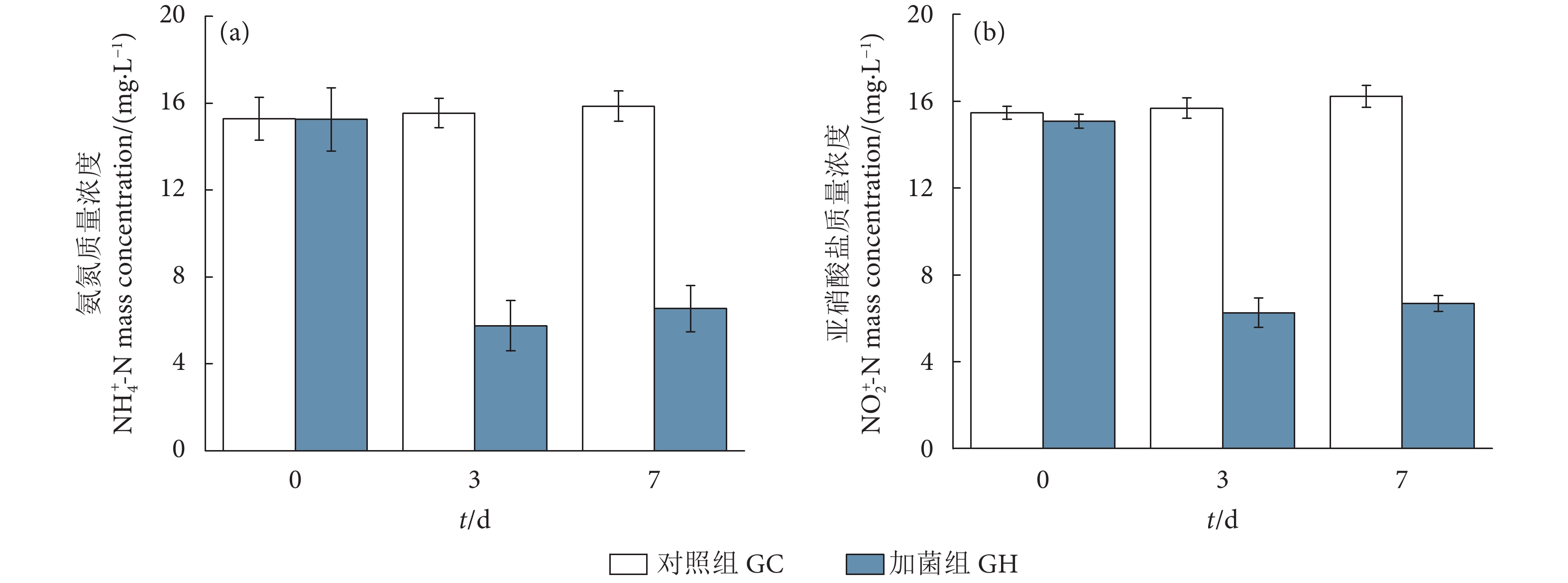
菌株发酵完成后,在无菌条件下取适量培养液加入对虾养殖池塘水 (来自陆丰某养殖场),至水体赤红球菌初始浓度为5×104 CFU·mL−1 (加菌组,GH),水体总氨氮和亚硝酸盐的初始质量浓度均为15 mg·L−1,实验条件为水温30 ℃、溶解氧质量浓度5 mg·L−1、pH 8.0,在实验第0、第3和第7天取适量水体,分别依照GB 17378.4—2007中靛酚蓝分光光度法和盐酸萘乙二胺分光光度法测定水体氨氮和亚硝酸盐浓度。对照组取相同体积的池塘水,不加入赤红球菌,其他操作与GH组一致 (对照组,GC)。
1.5 5种环境因子对赤红球菌去除底物效果的影响
取赤红球菌培养液加入对虾养殖水体中,然后按照温度、转速、盐度、接种菌量、底物(氨氮和亚硝酸盐) 浓度等5种因子进行Plackett-Burman实验设计。实验条件为溶解氧质量浓度5 mg·L−1、pH 8.0,其他条件依据表1和表2,实验周期为7 d,7 d后检测氨氮和亚硝酸盐浓度,并计算两者的去除率。
表 1 Plackett-Burman实验因素及与水平设计Table 1. Factors and levels design of Plackett-Burman因素 Factor 水平 Level −1 1 A:菌浓度Bacterial concentration/(CFU·mL−1) 104 107 B:底物 (氨氮/亚硝酸盐) 质量浓度Substrate concentration (Ammonia nitrogen/Nitrite)/(mg·L−1) 15 30 C:盐度 Salinity/‰ 15 30 D:转速 Rotating speed/(r·min−1) 150 225 E:温度 Temperature/℃ 20 30 表 2 Plackett-Burman设计Table 2. Plackett-Burman experimental design序号 No. A:菌浓度Bacterial concentration B:底物 (氨氮/亚硝酸盐) 浓度Substrateconcentration (Ammonia nitrogen/Nitrite) C:盐度Salinity D:转速Rotating speed E:温度Temperature 1 1 −1 −1 −1 1 2 1 −1 1 1 1 3 1 −1 1 1 −1 4 −1 1 −1 1 1 5 −1 1 1 −1 1 6 −1 −1 −1 1 −1 7 −1 −1 1 −1 1 8 1 1 −1 −1 −1 9 −1 −1 −1 −1 −1 10 −1 1 1 1 −1 11 1 1 −1 1 1 12 1 1 1 −1 −1 1.6 数据统计与分析
底物浓度去除率的计算公式为:R=(C0− Ct)/ C0×100%。式中:R为去除率;C0为初始浓度;Ct实验后的浓度。采用Design-Expert 11软件对实验进行设计与分析,以OriginPro 2016软件作图,通过SPSS 20.0软件进行单因素方差分析 (One-way ANOVA) ,比较各组数据的差异显著性,显著水平设定为P<0.05。
2. 结果
2.1 赤红球菌发酵过程中生长情况
如图1所示,在0~24 h菌株HDRR2Y数量快速增加,为生长对数期;在24~36 h菌株生长逐渐进入稳定期。发酵结束后,菌浓度达4.08×109 CFU·mL−1。
2.2 菌株形态变化情况
菌株HDRR2Y在发酵第0、第18、第24、第30、第36小时的细胞形态变化见图2。在第0小时,菌株细胞呈球状或短杆状,多由1或2个细胞构成;第18小时,菌株细胞变长呈弯曲杆状,处于分裂增殖期;第24小时,菌株细胞多为弯曲杆状,进一步增殖;第30小时,菌株长细胞分裂为短细胞,呈弯曲杆状;第36小时,菌株细胞进一步变短,开始出现球状 (图2)。
2.3 菌株HDRR2Y发酵液对氨氮和亚硝酸盐的去除效果
如图3所示,添加菌株HDRR2Y发酵液后第3天,养殖水体的氨氮和亚硝酸盐浓度明显降低,氨氮质量浓度从第0天的15 mg·L−1降至5.56 mg·L−1,去除率为62.96%;亚硝酸盐质量浓度从15 mg·L−1降至6.95 mg·L−1,去除率为59.37%。第7天,水体氨氮和亚硝酸盐浓度略有上升,但与第3天比较无显著性差异 (P>0.5)。实验过程中,对照组水体的氨氮和亚硝酸盐浓度基本保持不变,与添加菌组相比较差异极显著 (P<0.01) (表3)。
表 3 养殖水体中氨氮和亚硝酸盐去除率Table 3. Removal rate of ammonia nitrogen and nitrite in aquaculture water被测指标Measured index 时间Time 去除率 Removal rate/% 对照组 GC 加菌组 GH 氨氮 NH4 +-N 第3天 −5.16±6.87a 62.92±1.53b 第7天 −4.06±7.31a 57.50±2.16b 亚硝酸盐 NO2 −-N 第3天 −1.43±2.10a 59.37±2.49b 第7天 −4.92±1.41a 56.36±1.67b 注:同行数据的不同字母代表对照组和加菌组差异显著 (P<0.05)。 Note: Values with different letters within the same column indicate significant difference (P<0.05). 2.4 5种因素对赤红球菌去除氨氮和亚硝酸效果的影响
Plackett-Burman实验因素水平与回归方程的方差分析结果显示,5种因素的回归方程为,氨氮:Y1=45.74+1.11A+3.43B −0.075C+1.84D+ 5.74E。式中:Y1表示氨氮去除率;A表示菌浓度;B为氨氮质量浓度;C为盐度;D为转速;E为温度。该模型的显著性达到极显著水平 (P<0.001),且判定系数R2为0.893 7 (R2>0.8),说明该模型可信度高,拟合度可靠;亚硝酸盐:Y2=45.42+0.77A+0.82B−0.97C+3.57D+3.67E。式中:Y2表示亚硝酸盐去除率;A表示菌浓度;B为亚硝酸盐质量浓度;C为盐度;D为转速;E为温度。此模型的可信度同样较高 (P<0.01),拟合度可靠 (R2=0.805 3>0.8)。结果显示赤红球菌HDRR2Y能显著去除水体中的氨氮 (P<0.05),最高去除率为59.3%,氨氮质量浓度从30.00 mg·L−1降至12.21 mg·L−1 (表4)。5种因子中,温度、氨氮浓度可显著影响赤红球菌HDRR2Y去除氨氮效果 (P<0.05),转速、菌量和盐度对赤红球菌HDRR2Y去除氨氮效果的影响不显著 (P>0.05),对权重的影响程度依次为:温度>氨氮浓度>转速>菌量>盐度 (表5)。
表 4 Plackett-Burman实验底物去除率Table 4. Removal rate of substrate in Plackett-Burman experiment序号No. Y1:氨氮去除率Removal rate of ammonia nitrogen/% Y2:亚硝酸盐去除率 Removal rate of nitrite/% 1 48.4 42.5 2 51.3 36.6 3 36.2 40.2 4 52.4 47.1 5 53.6 36.8 6 42.5 42.9 7 43.9 39.9 8 40.7 32.5 9 31.6 43.7 10 43.8 38.7 11 59.3 53.4 12 45.2 30.7 表 5 Plackett-Burman实验因素水平与回归方程方差分析 (底物为氨氮)Table 5. Plackett-Burman's experimental factor level and ANOVA of regression equation (Substrate is ammonia nitrogen)因素Factor 平方和Sum of squares 自由度df 均方Mean square F P>F 显著性Significance 重要性排序Importance ranking 模型 Model 591.88 5 118.38 10.09 0.007 0 ** A:菌浓度Bacterial concentration/(CFU·mL−1) 14.74 1 14.74 1.26 0.305 2 4 B:氨氮质量浓度 Ammonia nitrogen mass concentration/ (mg·L−1) 140.77 1 140.77 12.00 0.013 4 * 2 C:盐度 Salinity/‰ 0.0675 1 0.067 5 0.005 8 0.942 0 5 D:转速 Rotating speed/(r·min−1) 40.70 1 40.70 3.47 0.111 9 3 E:温度 Temperature/℃ 395.60 1 395.60 33.71 0.001 1 * 1 残留误差 Residual error 70.41 6 11.74 总差 Total difference 662.29 11 注:判定系数R2=0.893 7;*. 差异显著 (P<0.05);**. 差异极显著( P<0.001)。 Note: Determination coefficient (R2)= 0.893 7; *. Significant difference (P<0.05); **. Very significant difference (P<0.001). 赤红球菌HDRR2Y同样能显著去除水体中的亚硝酸盐 (P<0.05),最高去除率为53.4%,亚硝酸盐质量浓度从30.00 mg·L−1降至13.98 mg·L−1 (表4)。在养殖水体中,5种因子影响赤红球菌HDRR2Y去除亚硝酸盐效果的权重程度依次为:温度>转速>盐度>亚硝酸盐浓度>菌量。其中,温度和转速显著影响赤红球菌HDRR2Y对亚硝酸盐的去除效果 (P<0.05),亚硝酸盐浓度、菌量和盐度对赤红球菌HDRR2Y去除亚硝酸盐效果的影响不显著 (P>0.05) (表6)。
表 6 Plackett-Burman实验因素水平与回归方程方差分析 (底物为亚硝酸盐)Table 6. Plackett-Burman's experimental factor level and ANOVA of regression equation (Substrate is nitrite)因素Factor 平方和Sum of squares 自由度df 均方Mean square F P>F 显著性Significance 重要性排序Importance ranking 模型 Model 340.26 5 68.05 4.96 0.038 2 * A:菌浓度 Bacterial concentration/(CFU·mL−1) 7.05 1 7.05 0.514 5 0.500 2 5 B:氨氮质量浓度Ammonia nitrogen mass concentration/(mg·L−1) 8.00 1 8.00 0.583 8 0.473 8 4 C:盐度 Salinity/‰ 11.21 1 11.21 0.817 9 0.400 6 3 D:转速 Rotating speed/(r·min−1) 152.65 1 152.65 11.13 0.015 7 * 2 E:温度 Temperature/℃ 161.33 1 161.33 11.77 0.014 0 * 1 残留误差 Residual error 82.26 6 13.71 总差 Total difference 422.52 11 注:判定系数R2=0.8053;*. 差异显著 (P<0.05)。 Note: Determination coefficient (R2)= 0.8053; *. Significant difference (P<0.05). 3. 讨论
赤红球菌属于化能异养细菌,需通过氧化有机物获得生长的能量和碳源,可利用无机氮或有机氮作为氮源。本研究发现,采用前期响应面优化的发酵培养参数,在以三水合醋酸钠为碳源、酵母膏为氮源的培养基中能快速生长,培养液细菌浓度在24 h内从104 CFU·mL−1增至109 CFU·mL−1,之后快速进入稳定期,发酵效果良好。与简单的摇瓶培养相比,发酵罐培养中的通气、控制pH能使微生物生长代谢更加旺盛[16-18]。发酵培养中持续的通气能使发酵液中的溶解氧一直处于较高水平,本研究中的赤红球菌HDRR2Y为好氧细菌,在氧气充足的前提下能快速分裂增殖,从而提高菌量。从细菌的形态同样可以观察到,第18和第24小时的细胞形态绝大多数呈长条形,是细胞分裂增殖期的特点,第30小时之后的细胞又逐渐回归至球形或短杆形,说明细菌生长已经处于稳定期。细菌的细胞形态是细菌种类鉴定及活力评判的重要指标之一,如葡萄球菌 (Staphyloccocus) 一般呈球形,乳酸菌 (Lactobacillus) 多呈短杆状。此外,细胞形态一定程度上反映了细菌的生长状态,毛青钟和胡金凤[19]发现细菌形态不正常的发酵醪其酸度升高较快,容易引起发酵醪的酸败,周丽英等[20]发现假单胞菌 (Pseudomonas) 在质量浓度为100 mg·L−1的镉 (Cd) 环境中,细胞表面出现丝状物及不同程度的凹陷,推测可能与重金属离子所起的胁迫密切相关。
赤红球菌喜欢生长在有机质丰富的环境中,目前多应用于生活污水或工业废水的生物处理[21-23]。陈静和龚艳华[14]应用赤红球菌处理污水、废水,可有效去除水体氨氮。罗固源等[13]发现一株赤红球菌在好氧的条件下可去除废水中的亚硝酸盐。本研究中,将赤红球菌HDRR2Y发酵液添加至富含氨氮和亚硝酸盐的养殖水体后,第3天氨氮和亚硝酸盐浓度去除率约达60%,去除效果显著 (P<0.05),但第7天的氨氮、亚硝酸盐浓度比第3天略有上升,推测可能是水体营养不足,限制了赤红球菌的生长。
温度能够显著影响赤红球菌HDRR2Y降解氨氮和亚硝酸盐效果,主要是因为温度影响微生物的生长代谢,从而影响微生物对外界物质的吸收效率。高温使细菌细胞内蛋白质变性、酶失活,使细菌灭亡,低温会抑制微生物生长,微生物体内酶的活性在最适温度下可提高1~2倍[24]。多数研究显示,硝化菌在约30 ℃时硝化功能得到最大发挥,而在20 ℃及以下时硝化作用受到极大抑制[25-26]。本研究显示在30 ℃时,菌株HDRR2Y对氨氮和亚硝酸盐降解效果最好,与多数研究结果相符。因此菌株HDRR2Y适合在高温养殖季使用。
底物浓度是影响微生物代谢活性的重要因子,底物浓度越高,微生物代谢活性越高。本研究发现,底物亚硝酸盐的浓度不是影响菌株降解亚硝酸盐效果的显著因素,而底物氨氮的浓度则显著影响菌株降解氨氮的效果,说明菌株HDRR2Y更易利用氨氮。王晓明和王杰[27]发现随着进水氨氮浓度的不断升高,硝化系统对氨氮的去除率随之升高,但过高的氨氮浓度会抑制硝化反应效率[28]。本研究结果表明,菌株HDRR2Y更适合用于高浓度氨氮的去除。
转速是另一个影响赤红球菌去除氨氮和亚硝酸盐效果的重要因子。本研究发现,较高的转速有助于赤红球菌HDRR2Y去除氨氮和亚硝酸盐,且转速对于赤红球菌代谢亚硝酸盐的影响大于氨氮代谢。已有研究发现水体流速可显著影响硝化及反硝化的效率[29-30],搅动的主要作用是让微生物与水体中的氨氮和亚硝酸盐更充分的接触,同时还能增加水体的溶解氧,通常在一定范围内,转速与溶解氧浓度成正比[31-32]。赤红球菌是好氧细菌,氧气不足时代谢会受到抑制,氧气充足时,新陈代谢速度达到最快,底物利用率达到最高。刘玉沛等[33]研究赤红球菌对苯酚的降解效果时,氧气充足条件下降解率为61.87%,而氧气不足条件下降解率显著降低 (50.44%)。因此,在养殖过程中使用赤红球菌,要充分利用水车等增氧设备,提高水体流速和溶解氧浓度,发挥菌株最大的功效。
微生物细胞浓度与其生态功能密切相关,利用自养硝化细菌去除环境中的氨氮、亚硝酸盐往往起效时间较长,因为硝化细菌生长缓慢,一般需要富集5~8周才能发挥明显的硝化效应[34-35]。本研究结果显示,赤红球菌的浓度对氨氮和亚硝酸盐的去除无显著影响,可能是由于低浓度组的赤红球菌浓度已经达到发挥效应的水平。此外,赤红球菌属于异养菌,在适宜的环境中能迅速生长,这也是异养硝化细菌的优势。水体盐度也会影响硝化反应,目前多数研究认为,盐分对硝化反应存在抑制作用,且对亚硝酸盐氧化反应的抑制要大于对好氧氨氧化反应的抑制作用[36-37]。但经过盐分驯化培养后,在较高的盐分浓度下仍然维持较好的硝化效果[38]。本研究发现在盐度为15‰和30‰时,赤红球菌去除氨氮和亚硝酸盐的效率并未受到太大的影响,这可能与该株菌自身广盐性有关[15]。因此,该株菌在高盐度或低盐度的水域中均具有推广使用的潜力,拥有广泛的应用前景。
4. 结论
赤红球菌HDRR2Y在装液量60% (V/V)、29 ℃、pH 7.0、机械搅拌转速400 r·min−1、接种量1%、通气量3 L·min−1的条件下培养36 h,发酵完成后的其质量浓度达4.08×109 CFU·mL−1。发酵后的菌株可在72 h内显著降低养殖水体中的氨氮和亚硝酸盐,说明该菌株具有作为优良渔业微生物菌剂的应用前景。此外,温度、底物浓度及水体流速是对菌株代谢氨氮和亚硝酸盐效率影响最显著的3个环境因子,因此在实际应用当中需要注意水体的温度和流速,以确保菌株使用效果的最大化。
-
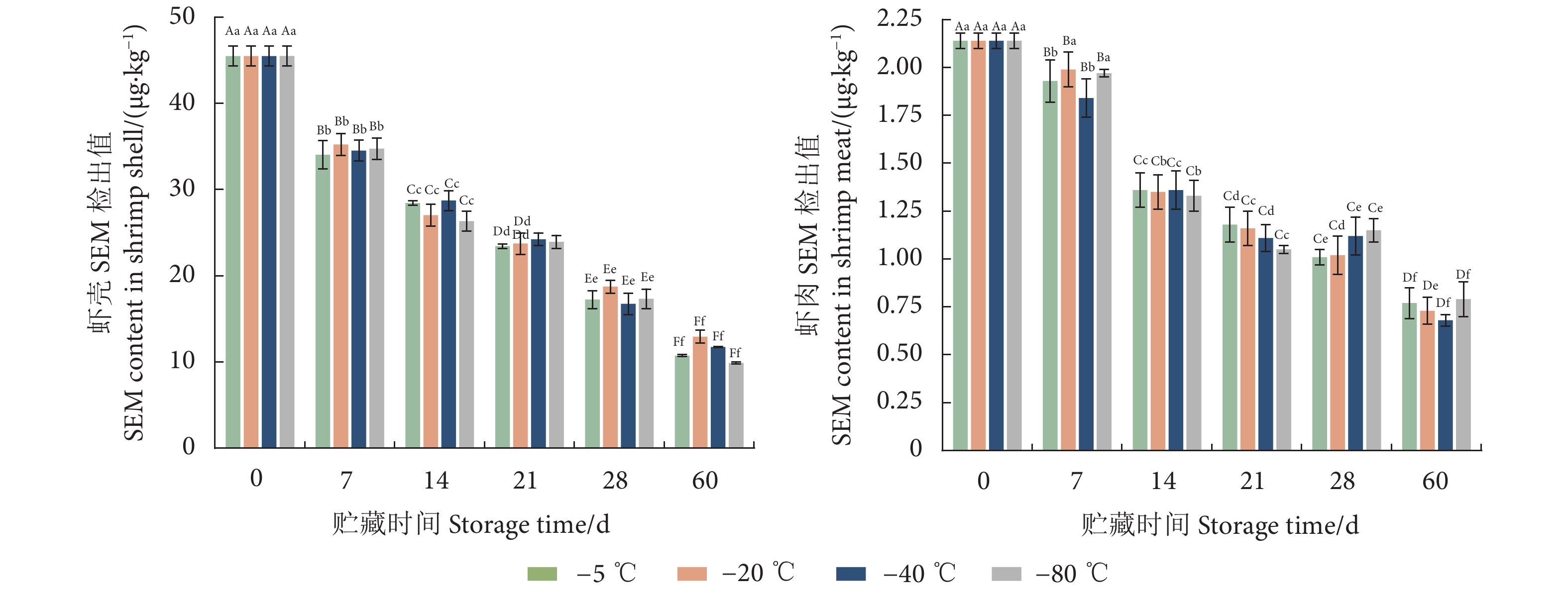
图 4 罗氏沼虾贮藏期间SEM检出值变化
注:不同大写字母表示不同贮藏时间下罗氏沼虾SEM检出值差异显著 (P<0.05);不同小写字母表示不同贮藏温度下罗氏沼虾SEM检出值差异显著 (P<0.05)。
Figure 4. Changes of SEM contents during storage of M. rosenbergii
Note: Different uppercase letters indicate significant difference in the SEM content of M. rosenbergii at different storage times (P<0.05); different lowercase letters indicate significant difference in the SEM content of M. rosenbergii at different storage temperatures (P<0.05).
表 1 液相色谱梯度洗脱条件
Table 1 Program of gradient elution
时间 t/min 流速 Flow rate/(mL·min−1 ) 流动相 AMobile phase A/% 流动相 B Mobile phase B/% 0 0.35 75 25 3.0 0.35 70 30 4.0 0.35 30 70 4.5 0.35 75 25 6.0 0.35 75 25 表 2 呋喃西林代谢物及其内标的质谱条件
Table 2 Nitrofurazone metabolites and their internal target mass spectrometry conditions
被测物Analyte 母离子Precursor ion/(m/z) 子离子Product ion/(m/z) 锥孔电压DP/V 碰撞能量CE/V 氨基脲 SEM 209.1 166.1* 24 9 192.1 24 10 氨基脲内标SEM-15N2-13C 212.1 168.1 24 9 注:*. 定量离子。 Note: *. Quantitative ion. 表 3 样品中SEM的加标回收率和精密度
Table 3 Standard recovery and precision of SEM in samples
加标量Added amount/(μg·kg−1) 回收率Recovery rate/% 相对标准偏差RSD/% 1 96.00 8.84 5 92.20 6.11 10 97.30 2.02 表 4 罗氏沼虾不同部位SEM检出值
Table 4 SEM content in different parts of M. rosenbergii
样品Sample 样品数Number of samples SEM检出值 SEM content/(μg·kg−1) 均值±标准差$ \overline { X}\pm { \rm {SD}} $/(μg·kg−1) 检出率Detection rate/% 头胸甲 Cephalothorax 8 26.31~37.54 32.02±3.75 100 虾壳 Shrimp shell 8 10.80~50.17 26.85±13.90 100 尾扇 Shrimp tail 8 16.45~30.11 23.97±4.11 100 肢足 Shrimp foot 6 17.45~24.15 21.03±2.51 100 肝 Shrimp liver 6 4.59~7.31 5.56±0.87 100 虾肉 Shrimp meat 8 ND~2.72 1.35±0.67 87.5 注:ND. 检测结果小于0.50 μg·kg−1。 Note: ND. The result is less than 0.50 μg·kg−1. 表 5 罗氏沼虾虾壳和虾肉中SEM的检出值
Table 5 Detection of SEM in shrimp shell and meat of M. rosenbergii
样品Sample SEM检出值 SEM content/(μg·kg−1) 平行样1Replicate 1 平行样2Replicate 2 平行样3Replicate 3 平行样4Replicate 4 平均值Mean 虾壳 Shrimp shell 31.80±1.11 27.63±1.67 29.18±2.03 32.23±1.76 30.21±1.64 虾肉 Shrimp meat 1.93±0.17 1.63±0.09 1.38±0.13 1.73±0.29 1.66±0.17 比值 Ratio 16.47 16.95 21.14 18.63 18.19 -
[1] 薛瑾, 林慧, 潘玉宁, 等. 动物源性食品中呋喃西林及其代谢物检测方法研究[J]. 江苏预防医学, 2022, 33(1): 47-50. doi: 10.13668/j.issn.1006-9070.2022.01.013 [2] 魏涯, 岑剑伟, 郝淑贤, 等. 高效液相色谱法测定池塘底泥中呋喃西林的研究[J]. 南方水产科学, 2014, 10(1): 71-77. doi: 10.3969/j.issn.2095-0780.2014.01.011 [3] WANG Q, WANG X F, JIANG Y Y, et al. Determination of 5-nitro-2-furaldehyde as arker residue for nitrofurazone treatment in farmed shrimps and with addressing the use of a novel internal standard[J]. Sci Rep, 2019, 9(1): 19243-19251. doi: 10.1038/s41598-019-55809-0
[4] POINTS J, BURNS D T, WALKER M J. Forensic issues in the analysis of trace nitrofuran veterinary residues in food of animal origin[J]. Food Control, 2015, 50(11): 92-103.
[5] TIAN W R, SHANG Y X, WANG X H. Semicarbazide from state of the art analytical methods and exposure to toxicity: a review[J]. Food Addit Contam Part A, 2014, 31(11): 1850-1860. doi: 10.1080/19440049.2014.953012
[6] 杨曦, 李红光. 水产品在消毒水作用下产生呋喃西林代谢物的研究[J]. 食品工业科技, 2011, 32(4): 158-159. doi: 10.13386/j.issn1002-0306.2011.04.112 [7] 赵飞越, 赵芳, 王桥, 等. 长江中下游地区克氏原鳌虾氨基脲污染现状及组织分布特征[J]. 食品安全质量检测学报, 2022, 13(5): 1648-1653. doi: 10.19812/j.cnki.jfsq11-5956/ts.2022.05.049 [8] 曹爱玲, 陈怡琳, 蔡路昀, 等. 不同烘干温度对甲壳类水产品中氨基脲检出量的影响[J]. 中国动物检疫, 2020, 37(1): 94-99. doi: 10.3969/j.issn.1005-944X.2020.01.020 [9] STADLER RH, VERZEGNASSI L, SEEFELDER W, et al. Why semicarbazide (SEM) is not an appropriate marker for the usage of nitrofurazone on agricultural animals[J]. Food Addit Contam, 2015, 32(11): 1842-1850. doi: 10.1080/19440049.2015.1086028
[10] 辛少平, 邓建朝, 杨贤庆, 等. 高效液相色谱法测定硝基呋喃类药物代谢物及其在对虾体内的代谢[J]. 食品科学, 2014, 35(24): 151-157. doi: 10.7506/spkx1002-6630-201424029 [11] 朱盼盼, 邢丽红, 李兆新, 等. 甲壳类水产品中氨基脲研究进展[J]. 青岛大学学报 (工程技术版), 2021, 36(3): 55-64. [12] 杨国梁, 陈雪峰, 王军毅, 等. 罗氏沼虾产业在中国持续增长的经济与社会原因分析[J]. 浙江海洋学院学报 (自然科学版), 2011, 30(5): 450-457. [13] 罗茵. 《2020中国渔业统计年鉴》出版广东水产品总产量首次全国第一[J]. 海洋与渔业, 2020(6): 12-13. doi: 10.3969/j.issn.1672-4046(s).2020.06.002 [14] 范清涛. 养殖虾类中SEM的检测方法与来源研究[D]. 舟山: 浙江海洋大学, 2021: 29-36. [15] 范清涛, 陈胜军, 邓建朝, 等. 甲壳类水产品中氨基脲产生及控制方法研究进展[J]. 食品安全质量检测学报, 2020, 11(5): 1439-1445. doi: 10.19812/j.cnki.jfsq11-5956/ts.2020.05.015 [16] 莫梦松, 蔡楠, 李来好, 等. 罗氏沼虾成虾中氨基脲的分布特征[J]. 渔业科学进展, 2022, 43(3): 103-109. doi: 10.19663/j.issn2095-9869.20210322001 [17] MCCRACKEN R, HANNA B, ENNIS D, et al. The occurrence of semicarbazide in the meat and shell of Bangladeshi fresh-water shrimp[J]. Food Chem, 2013, 136(34): 825-832.
[18] 王鼎南, 周凡, 李诗言, 等. 甲壳类水产品中呋喃西林代谢物SEM的本底调查及来源分析[J]. 中国渔业质量与标准, 2016, 6(6): 6-11. [19] 倪永付, 朱莉萍, 王勇, 等. 微山湖小青虾各部分呋喃西林代谢物含量测定[J]. 食品与发酵科技, 2012, 48(1): 86-88. doi: 10.3969/j.issn.1674-506X.2012.01.022 [20] van POUCKE C, DETAVERNIER C, WILLE M, et al. Investigation into the possible natural occurence of semicarbazide in Macrobrachium rosenbergii prawns[J]. J Agr Food Chem, 2011, 59(5): 2107-2112. doi: 10.1021/jf103282g
[21] 于慧娟, 李冰, 蔡友琼, 等. 液相色谱-串联质谱法测定甲壳类水产品中氨基脲的含量[J]. 分析化学, 2012, 40(10): 1530-1535. [22] 舒秀君. 日本沼虾中氨基脲的存在特征研究[D]. 上海: 上海海洋大学, 2020: 36-47. [23] 张平安, 张建威, 乔明武, 等. 高效液相色谱-串联质谱法测定蜂蜜 中硝基呋喃代谢物的研究[J]. 浙江农业科学 , 2010(3): 611-614. doi: 10.3969/j.issn.0528-9017.2010.03.065 [24] 高洋洋, 刘鑫, 陈广全. 蜂蜜中硝基呋喃代谢物的超高效液相色谱-串联质谱测定法[J]. 职业与健康, 2018, 34(13): 1764-1768. [25] 赵天祎, 马占峰, 张莹. 蜂蜜中氨基脲本底来源研究[J]. 食品安全质量检测学报, 2019, 10(11): 3401-3404. doi: 10.3969/j.issn.2095-0381.2019.11.028 [26] SAARI L, PELTONEN K. Novel source of semicarbazide: levels of semicarbazide in cooked crayfish samples determined by LC/MS/MS[J]. Food Addit Contam, 2004, 21(9): 825-832. doi: 10.1080/02652030400002329
[27] 彭婕, 吕磊, 喻亚丽, 等. 中华绒螯蟹中内源性SEM的产生途径研究[J]. 淡水渔业, 2019, 49(3): 108-112. doi: 10.3969/j.issn.1000-6907.2019.03.018 [28] 周萍, 胡福良, 章征天, 等. 雄蜂蛹中硝基呋喃类代谢物含量的测定及超标原因分析[J]. 中国蜂业, 2008(7): 5-9. doi: 10.3969/j.issn.0412-4367.2008.07.001 [29] 彭婕, 甘金华, 陈建武, 等. 中华绒螯蟹中SEM的分布及产生机理分析[J]. 淡水渔业, 2015, 45(4): 108-112. doi: 10.3969/j.issn.1000-6907.2015.04.020 [30] YU W L, LIU W H, TIAN W R. Semicarbazide universality study and its speculated formation pathway[J]. J Food Saf, 2019, 39(1): 1-8.
[31] CAO A L, CAI L Y, CHEN Y L, et al. Production mechanism of semicarbazide from protein in chinese softshell turtles at different trying temperatures based on TMT-tagged quantitative proteomics[J]. J Food Compost Anal, 2021, 99(1): 103872.
[32] 王建. 甲壳类水产中呋喃西林及SEM的研究[D]. 杭州: 浙江工商大学, 2015: 47-59. [33] 高素, 汝少国. SEM的毒性效应研究进展[J]. 环境科学研究, 2013, 26(6): 637-644. [34] 李培源, 周泉, 贾智若. 氨基硫脲型钌配合物的合成和结构研究[J]. 广州化工, 2019, 47(14): 42-44. doi: 10.3969/j.issn.1001-9677.2019.14.016 -
期刊类型引用(11)
1. 张婷娟,吴风超,周纷. 市售生姜油对白鲢鱼糜凝胶品质特性的影响. 食品科技. 2025(01): 146-153 .  百度学术
百度学术
2. 金铮,于婉莹,赵文宇,刘宇轩,祁立波,白帆,董秀萍. 鲟鱼重组鱼排3D打印特性的研究. 食品与发酵工业. 2024(03): 241-249 .  百度学术
百度学术
3. 步营,程亚佳,厉寒,朱文慧,励建荣,李学鹏,季广仁. 发芽糙米匀浆对带鱼鱼糜凝胶特性的影响. 农业工程学报. 2024(18): 292-301 .  百度学术
百度学术
4. 林雅文,刘佳晨,李艾靑,高月,励建荣,李学鹏. 不同干燥方法对南美白对虾理化特性和微观结构的影响. 食品科学. 2023(19): 74-81 .  百度学术
百度学术
5. 邹怡茜,陈海强,潘卓官,肖苏尧,周爱梅. 超高压耦合热处理对鳙鱼鱼糜凝胶特性和水分迁移的影响. 现代食品科技. 2022(12): 272-280 .  百度学术
百度学术
6. 宋春勇,洪鹏志,周春霞,陈艾霖,冯瑞. 大豆油和预乳化大豆油对金线鱼鱼糜凝胶品质的影响. 食品科学. 2021(08): 90-97 .  百度学术
百度学术
7. 梁雯雯,杨天,郑志红,郭建,陈胜军,汪秋宽,丛海花. 升温方式对二段加热鲢鱼糜水分分布和品质的影响. 大连海洋大学学报. 2021(04): 646-652 .  百度学术
百度学术
8. 刘芳芳,林婉玲,李来好,吴燕燕,杨少玲,黄卉,杨贤庆,林织. 海鲈鱼糜加工及凝胶形成过程中蛋白质的变化机理. 食品科学. 2020(14): 15-22 .  百度学术
百度学术
9. 郑静静,林琳,张艳凌,陆剑锋,姜绍通. 不同解冻方式对熟制小龙虾理化特性的比较分析. 现代食品科技. 2020(09): 188-194+108 .  百度学术
百度学术
10. 李钊,李宁宁,刘玉,赵圣明,康壮丽,朱明明,计红芳,何鸿举,马汉军. 超高压对肌原纤维蛋白结构及其凝胶特性影响的研究进展. 食品与发酵工业. 2020(21): 304-309 .  百度学术
百度学术
11. 王菲,隋好林. 不同水产养殖区福寿鱼的鱼糜凝胶品质研究. 江西水产科技. 2019(06): 10-14 .  百度学术
百度学术
其他类型引用(14)



 下载:
下载:




 粤公网安备 44010502001741号
粤公网安备 44010502001741号
