Effects of water temperature in transportation on mortality and physiological indicators of Sepiella japonica
-
摘要:
增殖放流是曼氏无针乌贼 (Sepiella japonica) 渔业资源修复的重要手段,而水温可能会影响增殖放流运输过程中乌贼的生存状态。为优化曼氏无针乌贼成体增殖放流运输技术,通过实验室内模拟不同水温 (14、17、20、23、26、29 ℃)下的运输过程,分析了不同运输温度下乌贼死亡率和肝脏生理指标的变化。结果显示,运输水温显著影响乌贼成体死亡率 (p<0.05),14和29 ℃处理组的死亡率较高,分别为30.0%和63.3%。相较于20 ℃处理组,肝糖原含量在14和17 ℃下显著下降,在29 ℃下显著上升 (p<0.05);乳酸含量在23和29 ℃下显著上升(p<0.05);超氧化物歧化酶 (SOD) 活性在17 ℃下显著下降,在26 ℃下显著上升 (p<0.05);碱性磷酸酶 (AKP) 活性在各水温下显著下降(p<0.05);随水温变化,谷草转氨酶 (AST) 活性先下降后上升,而谷丙转氨酶 (ALT) 活性则先上升后下降。乌贼死亡率与肝脏糖原、乳酸含量和AST活性显著正相关 (p<0.05)。研究表明,在5 只·L−1密度下水温过低或过高均不适宜乌贼运输,建议水温控制在17~26 ℃。
Abstract:Restocking and releasing is an important means to restore the resources of Sepiella japonica, and the water temperature during the transportation process of restocking and releasing may affect its survival status. In order to optimize the transportation techniques for the adult enrichment and release of S. japonica, we conducted an experiment to simulate the transportation environment in laboratory and performed transportation experiments of adult S. japonica with different water temperatures (14, 17, 20, 23, 26, 29 ℃), and explored its mortality rate and liver physiological indicators. The results show that the water temperature in transportation affected the mortality rate significantly (p<0.05), and the mortality rates in 14 and 29 ℃ groups were higher, reaching 30.0% and 63.3%, respectively. Compared with 20 ℃ group, the glycogen content decreased significantly in 14 and 17 ℃ groups, but increased significantly in 29 ℃ group (p<0.05). The lactic acid content increased significantly in 23 and 29 ℃ groups (p<0.05). SOD decreased significantly in 17 ℃ group but increased significantly in 26 ℃ group (p<0.05). AKP decreased significantly at all water temperatures (p<0.05). With the change of water temperature, AST decreased initially and then increased, while ALT increased initially and then decreased. The mortality rate of squids was significantly positively correlated with glycogen, lactic acid content and AST activity in liver (p<0.05). In conclusion, too low or too high water temperature is not suitable for squid transportation at a density of 5 ind·L−1, and it is recommended to control the water temperature between 17 ℃ and 26 ℃.
-
曼氏无针乌贼 (Sepiella japonica) 俗称墨鱼,属软体动物门、头足纲、十腕总目、乌贼目、乌贼科,曾是我国“四大海产”之一,广泛分布于印度东海岸至西太平洋,在我国黄海、渤海、东海、南海均有分布,其中以东海群体最为庞大[1],具有很高的经济价值。作为浙江省重要的经济物种,曼氏无针乌贼历史上最高年产量曾达6万多吨,占海洋捕捞产量的9.3%。但20世纪80年代后,曼氏无针乌贼捕捞产量占比持续降至3.0%以下[2],80年代中后期起无法形成渔汛[3]。国内主要开展曼氏无针乌贼受精卵增殖放流并取得了一定成效,但受精卵易被海水冲散或因环境因素而不能完全孵化[4]。曼氏无针乌贼成体有护卵行为且受精卵对雌性成体有吸引作用,成体主动选择适宜的产卵基,可在一定程度上提高受精卵孵化率,提升放流效果[5-6]。
水温是影响鱼类运输的重要因素,在适宜的温度范围内,适当降低温度可以提高运输成活率和鱼肉品质[7]。乌贼是变温动物而无法自行调节体温,更易受环境温度变化的影响[8]。对虎斑乌贼 (S. pharaonis) 和金乌贼 (S. esculenta) 幼体的研究发现,温度会影响排氨率和卵黄吸收速率,即在一定范围内温度上升会提高机体代谢速率[9-10]。对六斑刺鲀 (Diodon holocanthus) 幼鱼、哲罗鲑 (Hucho taimen)、黑鲷 (Acanthopagrus schlegeli) 幼鱼的研究表明,温度是影响运输成活率的重要因素,水温改变会导致鱼体产生应激反应,导致糖原、乳酸含量发生变化,而糖原、乳酸含量是反映机体能量代谢和应激胁迫状态的重要指标[11-13]。此外,谷丙转氨酶 (ALT) 和谷草转氨酶 (AST) 活性主要与机体肝脏损伤密切相关,超氧化物歧化酶 (SOD)、碱性磷酸酶 (AKP) 是反映机体抗氧化酶活性和免疫功能的重要指标[14-16]。目前,国内外学者针对曼氏无针乌贼的研究主要聚焦于生态学[17-18]、人工繁育[19]、生长发育[20-22]、资源分布[23-24]等方面,迫切需要开展增殖放流运输过程中水温对曼氏无针乌贼成体死亡及生理状态影响的研究。因此,本研究通过实验室内模拟不同水温下曼氏无针乌贼成体的运输过程,分析其死亡率、生理相关指标变化,探索乌贼成体运输过程适宜的运输水温,优化乌贼成体的增殖放流运输技术。
1. 材料与方法
1.1 实验材料
实验所用乌贼为曼氏无针乌贼成体 (以下简称乌贼),由浙江省海洋水产研究所试验场培育。每天定时6:00、17:00投喂冰鲜饵料虾,饲喂后换水,用氧气泵不断向水中充氧,保持水中溶解氧 (DO) 质量浓度 >5.5 mg·L−1、盐度27‰~28‰、pH 7.8~7.9、水温 (20±1) ℃,光暗周期为12 h∶12 h。乌贼平均胴背长介于 (5.9±0.1) cm,体质量介于 (24.4±4.6) g,各组间胴背长和体质量无显著性差异 (p>0.05)。
1.2 不同运输温度模拟实验
曼氏无针乌贼的密度胁迫研究表明,高密度运输会导致其大量死亡,运输密度不宜超过1.8 只·L−1[25]。本研究中乌贼规格较小,根据体质量选择5 只·L−1的密度开展实验。根据放流经验,一般选择在夏季 (5—8月) 开展曼氏无针乌贼的增殖放流活动,而乌贼从养殖场装运到放流地 (中街山列岛) 约3~4 h。王平等[26]研究显示东海夏季海表温为23~28 ℃。大量研究表明适当低温运输可以降低代谢,有利于鱼类的保活运输[11-13]。因此,结合养殖水温和海表温,本研究将水温梯度设置为14、17、20、23、26、29 ℃,每个温度组设置4个重复,为探究不同运输温度下时间的影响,将运输时间设置为8 h。实验以养殖水温 (20 ℃) 为对照组,每个圆桶放15只乌贼,实验水体3 L。实验前停食1 d,实验开始时先将乌贼从暂养池中轻柔放入容积为9 L的亚克力圆桶中,亚克力桶置于水箱中并固定在振荡器上,使用冰袋和加热棒隔水降温和加热,待水温达到要求后打开振荡器 (上海力辰仪器科技有限公司HY-4A调速多用振荡器,振荡幅度20 mm,频率0~300 r·min−1) 开始实验,振荡器的振荡频率设置为100 r·min−1。每个圆桶中均放有温度计,若观察到水温发生变化则调整冰袋数量和加热棒功率,以保证水温稳定在 ±1 ℃。实验期间使用气泵持续充气,海水盐度、pH同暂养池,实验过程中不投饵。
1.3 死亡率统计与样本采集
实验过程中观察到乌贼浮于表面、鳍摆动停止、触碰无反时,应判定为死亡,记录对应时间并捞出。实验结束后,每个重复随机取1只乌贼,测量胴背长和体质量 (精确至0.1 g),随后置于冰上取肝脏组织后用液氮速冻并保存于−80 ℃冰箱,实验共采集24个肝脏样品。
1.4 生化指标测定
糖原、乳酸:取0.1 g肝脏组织,加1 mL的提取液研磨,粗提液全部转移到1.5 mL离心管中,于TGL16M台式高速冷冻离心机 (上海卢湘仪离心机仪器有限公司) 12 000 r·min−1离心10 min,取上清液待测。
酶活性:取1.0 g肝脏组织于15 mL离心管中,加9 mL的0.9% (w) 生理盐水冰水浴制备匀浆(2 500~3 000 r·min−1,离心10 min),取匀浆上清液待测。
参照酶联生物提供的试剂盒说明书测量肝脏中糖原、乳酸含量,糖原含量测量期间吸光度设置为510 nm,乳酸含量测量期间吸光度设置为530 nm。肝脏中ALT、AST、AKP、SOD活性均采用南京建成生物工程研究所试剂盒进行检测,酶活测量期间吸光度均设置为450 nm。
实验过程中操作人员严格遵守实验动物福利和动物实验伦理规范,并按照浙江海洋水产研究所实验动物管理及动物福利伦理委员会制定的规章制度执行。
1.5 数据分析
数据采用SPSS 17.0软件进行统计分析,并以“平均数±标准误 ($\overline { x}\pm s_{\overline { x}}$)”表示。采用单因素方差分析 (One-way ANOVA)和Duncan's法多重比较,对乌贼胴背长、死亡率、糖原、乳酸、酶活性等数据进行差异分析,显著性差异设为0.05。采用皮尔逊相关系数 (Pearson correlation coefficient) 和斯皮尔曼相关系数 (Spearman correlation coefficient) 对乌贼死亡率和生理指标进行相关性分析,显著性水平为0.05,极显著性水平为0.01。
2. 结果
2.1 运输温度对乌贼行为和死亡率的影响
模拟运输过程中不同水温导致乌贼的行为发生了改变 (图1)。水温较低时乌贼活动减缓,在14 ℃时几乎停止运动;运输水温介于20~26 ℃时,乌贼大部分时间匍匐在水底,偶尔缓慢游动,生存状态较为舒适;水温为29 ℃时,乌贼游动速度加快且体色变深,部分乌贼的触腕伸出。同时观察到23 ℃时乌贼出现少量喷墨,29 ℃时大量喷墨。
![]() 图 1 运输温度对乌贼行为的影响注:a. 模拟运输前乌贼在静息在水中;b. 模拟运输开始后乌贼在水中缓慢游动;c. 模拟低温运输乌贼运动减慢;d. 模拟高温运输下乌贼体色加深,触腕伸出。Figure 1. Effect of transportation temperature on squid behaviorsNote: a. Squid rested in water before transportation; b. Squid swam slowly in water after the transportation began; c. Squid movement slowed down in low-temperature transportation; d. During high-temperature transportation, the squid's body color deepened and the tentacles stretched out.
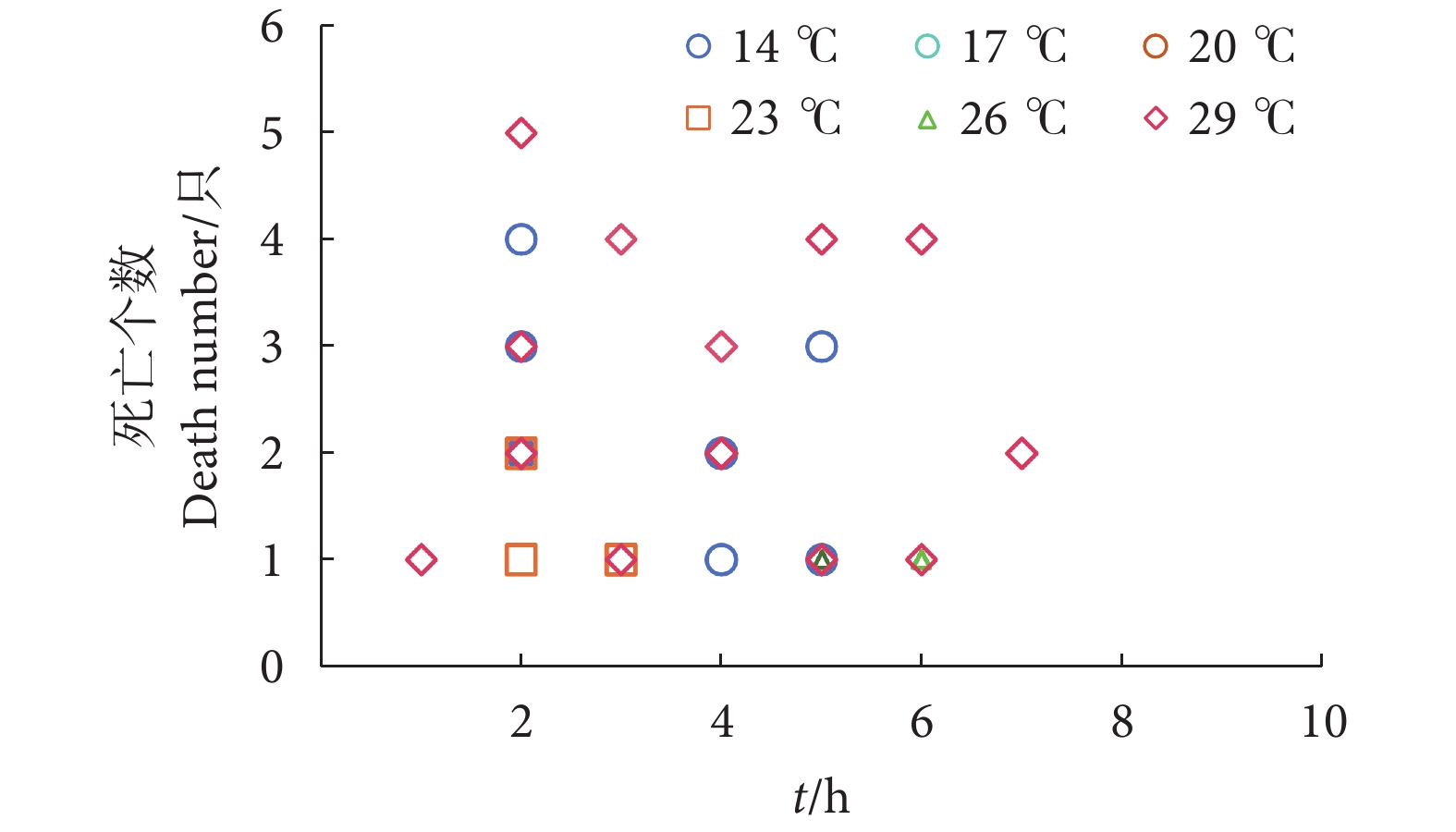
图 1 运输温度对乌贼行为的影响注:a. 模拟运输前乌贼在静息在水中;b. 模拟运输开始后乌贼在水中缓慢游动;c. 模拟低温运输乌贼运动减慢;d. 模拟高温运输下乌贼体色加深,触腕伸出。Figure 1. Effect of transportation temperature on squid behaviorsNote: a. Squid rested in water before transportation; b. Squid swam slowly in water after the transportation began; c. Squid movement slowed down in low-temperature transportation; d. During high-temperature transportation, the squid's body color deepened and the tentacles stretched out.乌贼的死亡时间主要出现在模拟运输后1~6 h,各水温下乌贼的主要死亡时间不同 (图2)。14 ℃组模拟运输1~2 h共死亡11只,3~5 h又死亡7只;17和20 ℃组未出现死亡;23 ℃组在模拟运输1~2 h死亡3只,2~3 h又死亡2只;26 ℃组在4~6 h共死亡3只;29 ℃组在模拟运输1 h内死亡1只,1~6 h共死亡35只,6~7 h共死亡2只。
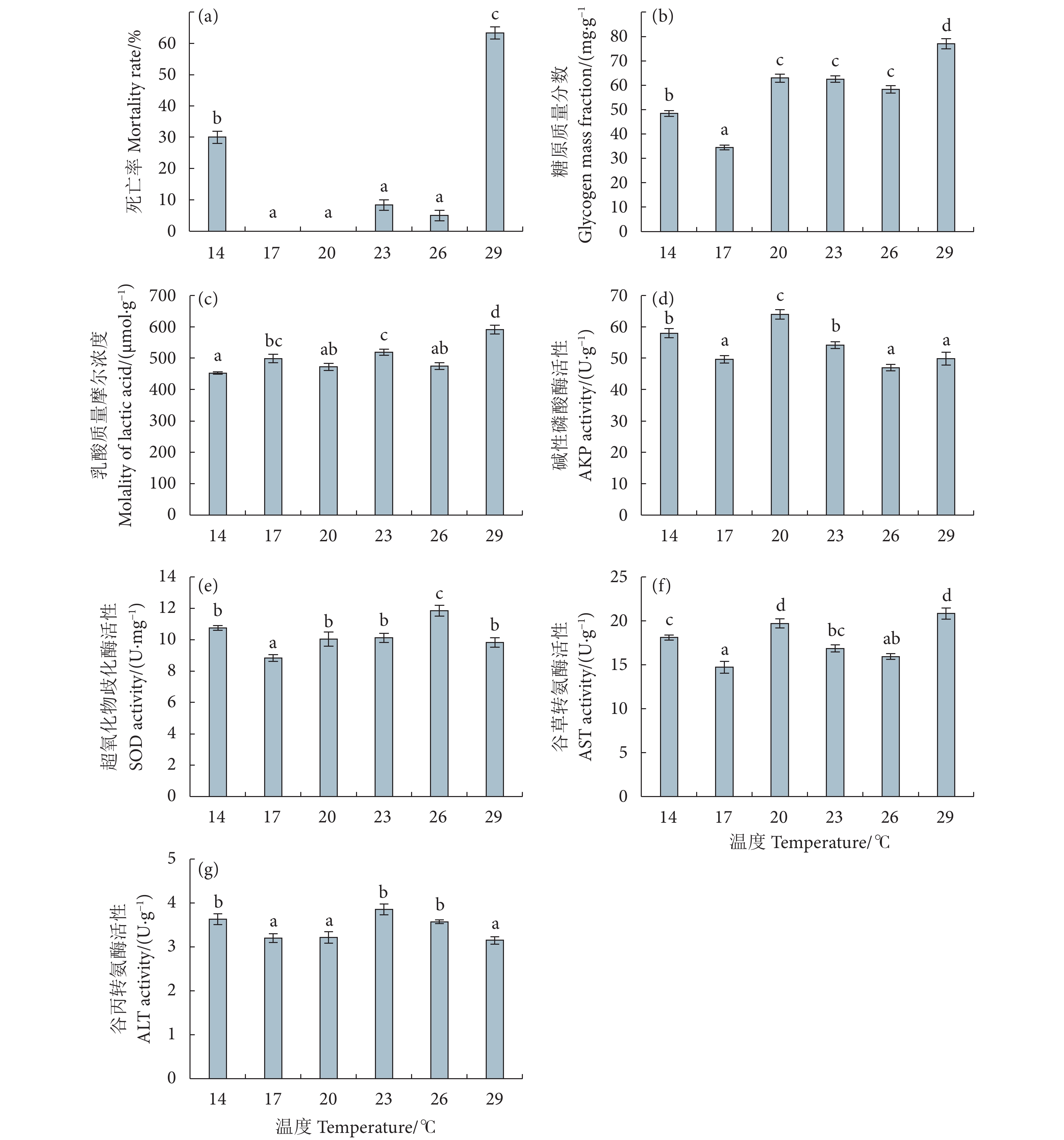
在模拟运输8 h后,29 ℃ 组死亡率最高 (63.3%),显著高于其他处理组 (p<0.05);14 ℃组死亡率达30.0%,显著高于17、20、23、26 ℃组 (p<0.05);23和26 ℃组死亡率分别为8.3%和5.0%,17和20 ℃组无死亡个体,17、20、23、26 ℃组间无显著性差异 (图3)。
2.2 运输温度对乌贼肝脏糖原含量的影响
糖原含量随运输温度的上升呈先降后升的趋势 (图3-b)。29 ℃组最高 (77.00 mg·g−1),显著高于其他处理组 (p<0.05);其次为20、23、26 ℃组,显著高于14和17 ℃组;17 ℃组最低 (34.46 mg·g−1),显著低于其他处理组 (p<0.05)。
2.3 运输温度对乌贼肝脏乳酸含量的影响
乳酸含量随温度的上升呈先升后降再升的趋势 (图3-c)。其中,29 ℃组最高 (591.51 μmol·g−1),显著高于其他处理组 (p<0.05);其次是23 ℃组 (518.92 μmol·g−1),显著高于14、20、26 ℃组 (p<0.05);14 ℃组最低 (452.86 μmol·g−1),显著低于17、23、29 ℃组 (p<0.05)。
2.4 运输温度对乌贼AKP和SOD活性的影响
AKP活性随温度的上升呈先降后升再降的趋势 (图3-d)。20 ℃组最高 (64.02 U·g−1),显著高于其他组 (p<0.05);其次是14 (57.96 U·g −1) 和23 ℃组 (54.17 U·g−1),显著高于17、26、29 ℃组 (p<0.05);17、26、29 ℃组的AKP活性较低,且组间无显著性差异。
SOD活性随温度的上升呈先降后升再降的趋势 (图3-e)。26 ℃组最高 (11.85 U·mg−1),显著高于其他处理组 (p<0.05);其次是14 ℃组 (10.75 U·mg−1),与20、23、29 ℃组无显著性差异;17 ℃组最低 (8.83 U·mg−1),显著低于其他处理组 (p<0.05)。
2.5 温度对乌贼肝脏AST和ALT活性的影响
AST活性随温度上升呈“W”型波动 (图3-f)。其中,20和29 ℃组较高,分别为19.72和20.85 U·g−1,显著高于14、17、23、26 ℃组 (p<0.05);其次为14 ℃组 (18.12 U·g−1),显著高于17和26 ℃组 (p<0.05);17 ℃组最低 (14.74 U·g−1),显著低于14、20、23、29 ℃组 (p<0.05)。
ALT活性呈先下降后上升再下降的趋势 (图3-g)。其中,23 ℃组最高 (3.86 U·g−1),显著高于17、20、29 ℃组 (p<0.05);29 ℃组最低 (3.15 U·g−1),显著低于14、23、26 ℃组 (p<0.05)。
2.6 死亡率与生理指标相关性分析
Pearson分析结果显示,不同温度下乌贼死亡率与肝脏糖原、乳酸含量及AST活性呈显著正相关(p<0.05);Spearman分析结果显示,不同温度下乌贼死亡率与肝脏糖原含量和AST活性呈显著正相关(p<0.05),其中死亡率与AST活性的相关性最高 (表1)。
表 1 死亡率与生理指标相关性分析Table 1. Correlation analysis of mortality and physiological indicators生理指标
Physiological indicatorPearson相关系数
Pearson correlation
coefficientSpearman相关系数
Spearman correlation
coefficient肝脏糖原含量
Lactate content in liver0.561** 0.412* 肝脏乳酸含量
Lactate content in liver0.630** 0.298 碱性磷酸酶活性
AKP activity−0.181 −0.112 超氧化物歧化酶活性
SOD activity−0.024 0.205 谷草转氨酶活性
AST activity0.632** 0.472* 谷丙转氨酶活性
ALT activity−0.183 0.093 注:*. 显著相关 (p<0.05);**. 极显著相关(p<0.01)。 Note: *. Significant correlation (p<0.05); **. Extremely significant correlation (p<0.01). 3. 讨论
3.1 运输水温对乌贼行为和死亡率的影响
水生生物通常有最适生存水温,曼氏无针乌贼在养成阶段的养殖水温宜为20~30 ℃,而产卵亲体的饲养水温一般不宜超过25 ℃[27]。对曼氏无针乌贼的生境适宜性研究也发现温度是影响其分布的重要生态因子之一,野外环境下乌贼偏好海域的表层水温通常在25.5~28.5 ℃[28]。本研究发现,水温改变会导致乌贼体色发生变化并对其行为产生影响,相较于20 ℃,各处理组水温降低乌贼活动减少,水温上升则游动速度加快。文菁等[29]对不同水温下虎斑乌贼幼体研究的结果与本研究相似,其在20 ℃时成活率最高,乌贼活动随水温降低减少,而水温升高乌贼则会较为活跃,水温过高或过低均会导致虎斑乌贼幼体死亡。本研究中,14和29 ℃水温下乌贼成体出现了较高的死亡率,水温过高和过低均不适宜乌贼成体的运输。对曼氏无针乌贼幼体的生态因子耐受性研究同样发现水温变化对幼体存活有较大影响,乌贼幼体在14和30 ℃水温下死亡率大幅上升[30]。尽管17、20、23、26 ℃组间死亡率差异不显著,但17和20 ℃组显示出较低的死亡率,可能是因为在较低运输水温条件下乌贼活动减少,基础代谢降低,从而减少了乌贼的死亡。
3.2 运输水温对乌贼肝脏糖原和乳酸含量的影响
糖原主要储存于动物的肝脏和肌肉中,肝糖原作为机体主要的储能物质,会在酶促作用下水解生成葡萄糖后进入血液成为血糖,并随血液循环为机体提供能量;肌糖原则会在为机体运动提供能量的同时产生乳酸,当代谢活动加快和剧烈运动时可能造成乳酸堆积[31]。对栉孔扇贝 (Chlamys farreri) 的研究发现,温度下降时机体内的糖原会停止积累并开始分解为机体提供能量,使肝脏组织中糖原含量不断下降,同时糖原分解生成的葡萄糖等小分子糖也会参与对低温的耐受过程,在机体抗寒系统中发挥作用[32]。本研究中,14和17 ℃组的乌贼肝脏糖原含量均显著低于20 ℃组,乌贼大量分解肝糖原以抵抗低温胁迫。水温会对水生动物的代谢产生影响,在适温范围内其代谢水平一般会随温度的上升而增加[33]。乐可鑫等[34]研究发现,温度会影响虎斑乌贼的新陈代谢,水温降低乌贼活动迟缓、代谢降低,水温升高乌贼活动频繁、代谢加快。本研究中,水温从17 ℃降至14 ℃时乌贼能量代谢水平进一步降低,肝糖原分解速度减慢,表现为14 ℃水温下乌贼肝脏糖原含量高于17 ℃组;在20~26 ℃水温下乌贼处于较为合适的温度区间,代谢水平随水温上升缓慢增加,此时23和26 ℃组乌贼肝脏糖原含量相较于20 ℃时略有下降但不显著。Tejpal等[35]指出鱼类在受到胁迫应激后肝脏中AST和ALT活性会显著增加并加强糖异生途径合成糖原。本研究中,29 ℃组乌贼大量喷墨,AST活性处于较高水平,乌贼肝脏糖原含量较高可能是因为乌贼启动了糖异生以抵抗高温胁迫。
乳酸主要由糖酵解作用产生,当受到胁迫或剧烈运动时机体会在短时间内大量分解肌糖原并生成乳酸[36-38]。本研究中,水温从17 ℃降至14 ℃时乌贼活动减缓,乳酸生成减少,肝脏组织的乳酸含量显著下降。赵晨曦等[39]研究发现,虎斑乌贼在环境不适宜时会出现喷墨行为,这会造成其体质虚弱进而易出现死亡,并大量产生乳酸。本研究中,23 ℃时乌贼出现少量喷墨,而29 ℃时出现大量喷墨,可能是喷墨行为导致乌贼肝脏乳酸含量上升。此外,29 ℃下水温的上升也提高了乌贼的代谢水平,乳酸含量进一步升高。
3.3 运输水温对乌贼肝脏SOD和AKP活性的影响
抗氧化和免疫防御在机体应对环境因子改变时发挥着重要作用。SOD是生物体内重要的抗氧化酶之一,具有清除代谢产生的活性氧和自由基的功能[40]。当机体受到轻度胁迫时,为保护机体免受氧化损伤,SOD上升以清除产生的活性氧和自由基;当胁迫增强时,活性氧和自由基过量产生,造成的氧化损伤超出机体的调节能力,抗氧化能力被抑制,导致SOD活性降低[41]。李豫等[42]对军曹鱼 (Rachycentron canadum) 幼鱼抗氧化能力的研究表明,低温会降低幼鱼的新陈代谢速度和活动水平,并对肝脏造成损伤,导致其抗氧化能力减弱。对大黄鱼 (Larimichthys crocea) 的研究表明低温胁迫会引起脂质过氧化和体内线粒体结构与功能破坏,导致活性氧大量产生[43]。本研究中,水温从20 ℃降至17 ℃时乌贼肝脏中SOD活性显著下降,可能是因为乌贼活动减弱、代谢降低,产生的活性氧减少;水温从17 ℃降至14 ℃时SOD活性显著上升,表明乌贼受到了低温胁迫,活性氧大量产生,抗氧化系统被激活。对虹鳟 (Oncorhynchus mykiss) 的研究表明在一定范围内水温升高会提高生物体内代谢水平并导致活性氧产物增加,SOD活性上升以清除产生的活性氧,当超出机体的调节能力时,抗氧化酶活性对高温胁迫的响应不敏感[44]。李亮[45]在温度骤变对黑盘鲍 [H. discus hannai (♀)×H. iris (♂)] 的SOD活性影响的研究中发现,以19 ℃为基点温度,随温度上升,SOD活性升高,但29 ℃时SOD活性又有所降低。本研究在水温20~29 ℃时乌贼肝脏SOD活性先上升后下降,与虹鳟和黑盘鲍的研究结果一致。当水温从23 ℃升至26 ℃时,乌贼受到轻度胁迫,机体产生的活性氧增加,抗氧化系统被激活,SOD活性显著增加,当水温继续升至29 ℃时,高温胁迫进一步增加,乌贼的抗氧化能力不足以清除产生的活性氧和自由基,机体抗氧化系统破坏并出现氧化损伤,肝脏中SOD活性显著下降。
软体动物不具备特异性免疫功能,其免疫系统主要由凝集素、溶血素、溶酶体酶等非特异性酶构成。AKP作为动物溶酶体酶系的重要组成部分,在软体动物免疫上具有重要作用[46-47]。研究表明,水温骤变会减弱大鳞副泥鳅 (Paramisgurnus dabryanus) 机体非特异性免疫功能,造成肝脏组织中AKP活性下降[48]。低温胁迫 (10 ℃) 会提高大黄鱼的炎症反应,激活机体的非特异性免疫,表现为肝脏中AKP活性升高[49]。本研究中,相较于20 ℃组,各处理组AKP活性均显著下降,表明水温升高或降低均会对乌贼的免疫能力产生影响,导致乌贼非特异性免疫能力下降。相较于17 ℃组,水温降至14 ℃时AKP活性显著上升,表明乌贼为抵抗低温胁迫提高了免疫反应。
3.4 运输水温对乌贼肝脏AST和ALT活性的影响
AST主要分布在肝细胞的线粒体中,ALT主要分布在肝细胞浆中,AST和ALT活性的变化反映了肝脏组织的生理状态[50]。当肝细胞受到环境胁迫产生损伤时,肝脏中贮存的AST和ALT会释放到血液中,导致其在肝脏中的活性下降,且下降程度与肝脏损伤程度正相关[51]。而在环境胁迫继续增强时可能会引起肝细胞大量坏死,导致肝脏中的AST和ALT停止释放到血液中[52]。本研究发现,不同水温下乌贼肝细胞AST和ALT活性的变化不同,这可能是与AST和ALT在肝细胞中的分布不同有关,不同水温下乌贼肝脏细胞受到的损伤程度不同。高权新等[53]研究发现,在胁迫12 h后低温组 (22 ℃) 和高温组 (32 ℃) 肝脏AST活性均显著下降,高温胁迫使银鲳 (Pampus argenteus)幼鱼产生应激反应,使其细胞膜通透性增加,肝脏受损导致ALT活性显著下降。袁新程等[54]认为美洲鲥 (Alosa sapidissima) 受到长时间的高温胁迫后可能对肝脏造成一定的损伤,导致肝脏AST活性显著升高,在6~24 h内水温从24 ℃升至28 ℃时ALT活性显著上升,水温从28 ℃升至30 ℃时ALT活性显著下降。本研究中,相较于20 ℃,17、23、26 ℃水温下乌贼肝脏AST活性下降,可能是温度胁迫导致肝细胞线粒体出现损伤,肝细胞中的AST释放到血液中,随着胁迫程度增加乌贼肝细胞线粒体损伤程度加重,AST减少释放,表现为14和29 ℃水温下肝细胞AST活性上升。以20 ℃组为基准点,ALT活性在14、23、26 ℃水温下上升,表明乌贼肝细胞出现了轻度损伤。对普通乌贼 (S. officinalis) 的研究发现,乌贼墨中含有酪氨酸酶,导致乌贼墨具有一定的细胞毒性,在喷墨后对乌贼造成损伤[55]。本研究中29 ℃水温下乌贼出现大量喷墨,此时乌贼受高温胁迫和喷墨的共同影响,可能造成肝脏损伤,导致ALT活性下降。
3.5 死亡率与生理指标间的相关性
Pearson相关系数和Spearman相关系数是统计学中均用来衡量两个变量之间关系强度和方向的统计量,广泛应用于生理指标的研究[56-57]。本研究中,不同运输温度下乌贼死亡率与肝脏糖原含量、乳酸含量、AST活性呈正相关,温度下降则乌贼代谢水平下降,乳酸含量下降,同时肝糖原分解以抵抗低温胁迫,温度上升则乌贼代谢水平增加,乳酸生成增加,这与杜可等[32]、吴加莹等[33]、乐可鑫等[34]的研究结果相似。周珊珊等[14]对曼氏无针乌贼的振荡胁迫研究发现,乌贼死亡率与SOD活性、肌肉乳酸含量、ALP活性之间呈极显著正相关,与肌肉和消化腺糖原含量、AST活性、ALT活性之间呈极显著负相关,与本研究结果不同,这可能是因为胁迫因子不同导致乌贼死亡率与生理指标的相关性出现差异。
4. 总结
综上所述,运输温度会影响曼氏无针乌贼成体的生存状态和生理指标,温度过高或过低均不适宜乌贼成体的生存且会对肝脏生理造成影响。低温运输下乌贼代谢下降,及高温运输下氧化损伤和喷墨可能是导致乌贼死亡的主要原因。为降低曼氏无针乌贼的运输死亡率,在运输密度为5 只·L−1时,建议运输水温控制在17~26 ℃较为合适。
-
图 1 运输温度对乌贼行为的影响
注:a. 模拟运输前乌贼在静息在水中;b. 模拟运输开始后乌贼在水中缓慢游动;c. 模拟低温运输乌贼运动减慢;d. 模拟高温运输下乌贼体色加深,触腕伸出。
Figure 1. Effect of transportation temperature on squid behaviors
Note: a. Squid rested in water before transportation; b. Squid swam slowly in water after the transportation began; c. Squid movement slowed down in low-temperature transportation; d. During high-temperature transportation, the squid's body color deepened and the tentacles stretched out.
表 1 死亡率与生理指标相关性分析
Table 1 Correlation analysis of mortality and physiological indicators
生理指标
Physiological indicatorPearson相关系数
Pearson correlation
coefficientSpearman相关系数
Spearman correlation
coefficient肝脏糖原含量
Lactate content in liver0.561** 0.412* 肝脏乳酸含量
Lactate content in liver0.630** 0.298 碱性磷酸酶活性
AKP activity−0.181 −0.112 超氧化物歧化酶活性
SOD activity−0.024 0.205 谷草转氨酶活性
AST activity0.632** 0.472* 谷丙转氨酶活性
ALT activity−0.183 0.093 注:*. 显著相关 (p<0.05);**. 极显著相关(p<0.01)。 Note: *. Significant correlation (p<0.05); **. Extremely significant correlation (p<0.01). -
[1] 李继姬, 郭宝英, 吴常文. 浙江海域曼氏无针乌贼资源演变及修复路径探讨[J]. 浙江海洋学院学报 (自然科学版), 2011, 30(5): 381-385. [2] 乌贼资源增殖研究课题组. 浙江近海曼氏无针乌贼资源增殖及繁殖保护的研究[J]. 浙江水产学院学报, 1986(2): 99-104. [3] 吴常文, 董智勇, 迟长凤, 等. 曼氏无针乌贼(Sepiella maindro ni)繁殖习性及其产卵场修复的研究[J]. 海洋与湖沼, 2010, 41(1): 39-46. doi: 10.11693/hyhz201001005005 [4] 徐开达, 周永东, 王洋, 等. 浙北近海曼氏无针乌贼增殖放流效果评估[J]. 中国水产科学, 2018, 25(3): 654-662. [5] 陈佳怡, 龙进霞, 徐汉祥, 等. 曼氏无针乌贼(Sepiella japoni ca)繁殖期行为谱特征的研究[J]. 海洋与湖沼, 2021, 52(6): 1549-1556. doi: 10.11693/hyhz20210500119 [6] BOAL J G, PROSSER K N, HOLM J B, et al. Sexually mature cuttlefish are attracted to the eggs of conspecifics[J]. J Chem Ecol, 2010, 36(8): 834-836. doi: 10.1007/s10886-010-9816-0
[7] 王琪, 梅俊, 谢晶. 低温保活运输对海鲈鱼应激及品质的影响[J]. 中国食品学报, 2022, 22(7): 203-213. [8] 龙华. 温度对鱼类生存的影响[J]. 中山大学学报 (自然科学版), 2005, 44(B06): 254-257. [9] 王林龙, 王展, 张雪梅, 等. 不同底质和温度对金乌贼仔乌饥饿耐受能力的影响[J]. 中国水产科学, 2018, 25(5): 1071-1081. [10] 王鹏帅, 蒋霞敏, 韩庆喜, 等. 盐度和温度对不同规格虎斑乌贼幼体的耗氧率、排氨率和窒息点的影响[J]. 水生生物学报, 2017, 41(5): 1027-1035. doi: 10.7541/2017.128 [11] 岳彦峰, 彭士明, 苏志星, 等. 六斑刺鲀幼鱼运输方法探讨[J]. 水产养殖, 2021, 42(8): 44-45. doi: 10.3969/j.issn.1004-2091.2021.08.011 [12] 包玉龙, 张涛, 刘圣聪. 大规格哲罗鲑活鱼运输的研究[J]. 安徽农学通报, 2017, 23(18): 87-89. doi: 10.3969/j.issn.1007-7731.2017.18.038 [13] 朱越, 王凯, 吴松, 等. 水温和摇晃对黑鲷幼鱼运输生存状态的影响[J]. 上海海洋大学学报, 2020, 29(4): 533-541. doi: 10.12024/jsou.20190402605 [14] 周珊珊, 周永东, 李哲, 等. 振荡频率对曼氏无针乌贼成体死亡率及生存状态的影响[J]. 水产学报, 2024, 48(2): 189-1981. [15] 樊甄姣, 夏灵敏, 吴常文, 等. 亚硝酸氮对曼氏无针乌贼幼体的急性毒性及免疫系统的影响[J]. 河北渔业, 2009(7): 8-11. doi: 10.3969/j.issn.1004-6755.2009.07.004 [16] 尹飞, 彭士明, 范帆, 等. 硫化物急性毒性对曼氏无针乌贼幼体血液生理生化指标的影响[J]. 安全与环境学报, 2011, 11(4): 9-13. doi: 10.3969/j.issn.1009-6094.2011.04.003 [17] 隋宥珍, 刘连为, 徐开达, 等. 春季洞头洋曼氏无针乌贼生物学特性研究[J]. 浙江海洋大学学报 (自然科学版), 2021, 40(6): 486-490. [18] 徐晓萱, 隋宥珍, 刘姝含, 等. 基于角质颚外部形态特征的曼氏无针乌贼2个地理群体判别[J]. 广东海洋大学学报, 2023, 43(1): 127-133. doi: 10.3969/j.issn.1673-9159.2023.01.016 [19] 蒋霞敏, 陆珠润, 何海军, 等. 几种生态因子对曼氏无针乌贼野生和养殖卵孵化的影响[J]. 应用生态学报, 2010, 21(5): 1321-1326. [20] 谢慕原, 徐汉祥, 张涛, 等. 养殖环境下曼氏无针乌贼生长的初步研究[J]. 浙江海洋大学学报 (自然科学版), 2021, 40(5): 400-406. [21] 黄伟卿, 陈宇光, 张艺, 等. 盐度胁迫对曼氏无针乌贼胚胎发育和生长性能的影响[J]. 渔业现代化, 2022, 49(6): 100-107. doi: 10.3969/j.issn.1007-9580.2022.06.013 [22] 张建设, 迟长凤, 吴常文. 曼氏无针乌贼胚胎发育生物学零度和有效积温的研究[J]. 南方水产科学, 2011, 7(3): 45-49. doi: 10.3969/j.issn.2095-0780.2011.03.008 [23] 徐晓萱, 谢玉, 刘姝含, 等. 基于GAM模型的浙江近海曼氏无针乌贼时空分布研究[J]. 浙江海洋大学学报 (自然科学版), 2022, 41(5): 400-407. [24] 刘姝含, 刘连为, 徐开达, 等. 浙江中北部近海曼氏无针乌贼资源现状[J]. 浙江海洋大学学报 (自然科学版), 2022, 41(4): 286-293. [25] 周珊珊, 蒋永生, 镇小蔓, 等. 运输密度对曼氏无针乌贼亲体死亡率及生理指标的影响[J]. 浙江海洋大学学报 (自然科学版), 2022, 41(5): 436-441. [26] 王平, 毛克彪, 孟飞, 等. 中国东海海表温度时空演化分析[J]. 国土资源遥感, 2020, 32(4): 227-235. [27] 史会来, 张涛, 平洪领, 等. 曼氏无针乌贼规模化人工繁育及增殖放流技术探讨[J]. 科学养鱼, 2015(12): 44-46. [28] 张漫瑶, 石雯静, 桂峰, 等. 利用MaxEnt模型的舟山海域曼氏无针乌贼生境适宜性研究[J]. 南方水产科学, 2023, 19(5): 22-31. doi: 10.12131/20230080 [29] 文菁, 曹观蓉, 李施颖, 等. 环境因子对虎斑乌贼幼体存活率及行为的影响[J]. 水产科学, 2011, 30(6): 321-324. doi: 10.3969/j.issn.1003-1111.2011.06.003 [30] 尹飞, 王春琳, 宋微微. 曼氏无针乌贼幼体生态因子耐受性的研究[J]. 湛江海洋大学学报, 2005, 25(4): 39-43. [31] 陈燕园, 林志华, 刘圣, 等. 缢蛏糖原磷酸化酶基因多态性与糖原含量的关联分析[J]. 海洋学报, 2022, 44(2): 77-83. [32] 杜可, 林岗, 李惠莲, 等. 低温胁迫对三沙湾华贵栉孔扇贝生理指标的影响[J]. 福建师范大学学报 (自然科学版), 2021, 37(6): 62-69. [33] 吴加莹, 戴明姝, 刘志刚, 等. 温度对织锦巴非蛤稚贝生存和生长的影响[J]. 南方水产科学, 2023, 19(2): 62-69. doi: 10.12131/20220155 [34] 乐可鑫, 蒋霞敏, 彭瑞冰, 等. 4种生态因子对虎斑乌贼幼体生长与存活的影响[J]. 生物学杂志, 2014, 31(4): 33-37. doi: 10.3969/j.issn.2095-1736.2014.04.033 [35] TEJPAL C S, PAL A K, SAHU N P, et al. Dietary supplementation of l-tryptophan mitigates crowding stress and augments the growth in Cirrhinus mrigala fingerlings[J]. Aquaculture, 2009, 293(3): 272-277.
[36] 苗增良, 李鹏, 周秀锦, 等. 急性力竭性运动后日本黄姑鱼乳酸、糖原和葡萄糖水平变化[J]. 江苏农业科学, 2012, 40(9): 212-214. doi: 10.3969/j.issn.1002-1302.2012.09.086 [37] HYNDMAN C A, KIEFFER J D, BENFEY T J. The physiological response of diploid and triploid brook trout to exhaustive exercise[J]. Comp Biochem Physiol A, 2003, 134(1): 167-179. doi: 10.1016/S1095-6433(02)00245-3
[38] WANG Y, HEIGENHSUSER G J, WOOD C M. Integrated responses to exhaustive exercise and recovery in rainbow trout white muscle: acid-base, phosphogen, carbohydrate, lipid, ammonia, fluid volume and electrolyte metabolism[J]. J Exp Biol, 1994, 195(1): 227-258. doi: 10.1242/jeb.195.1.227
[39] 赵晨曦, 韩庆喜, 韩子儒, 等. 虎斑乌贼喷墨对其生长及存活的影响[J]. 宁波大学学报(理工版), 2020, 33(4): 6-11. [40] 李智巧, 刘旭佳, 姜发军, 等. 水温对糙海参幼参生长、抗氧化酶及免疫酶活力的影响[J]. 中国水产科学 2023, 30(12): 1429-1444. [41] CHAI Y H, PENG R B, JIANG M W, et al. Effects of ammonia nitrogen stress on the blood cell immunity and liver antioxidant function of Sepia pharaonic[J]. Aquaculture, 2022, 546: 737417. doi: 10.1016/j.aquaculture.2021.737417
[42] 李豫, 黄建盛, 陈有铭, 等. 低温胁迫对军曹鱼幼鱼鳃组织抗氧化能力、细胞凋亡和组织结构的影响[J]. 南方水产科学, 2023, 19(3): 68-77. doi: 10.12131/20220227 [43] 曾霖, 王永红, 宋炜, 等. 基于转录组解析铜驯化对低温胁迫下大黄鱼氧化损伤的影响[J]. 中国水产科学, 2022, 29(10): 1425-1436. doi: 10.12264/JFSC2022-0184 [44] 董福霖, 黄天晴, 刘恩慧, 等. 高温胁迫对虹鳟 (Oncorhynchus mykiss) 肝脏中抗氧化酶活性和免疫相关基因表达的影响[J]. 海洋与湖沼, 2023, 54(1): 225-232. doi: 10.11693/hyhz20220300064 [45] 李亮. 杂交鲍 (Haliotis discus hannai♀×Haliotis iris♂) 温度耐受性研究[D]. 济南: 山东大学, 2017: 20-24. [46] 孙虎山 李光友. 栉孔扇贝血淋巴中ACP和AKP活性及其电镜细胞化学研究[J]. 中国水产科学, 1999, 6(4): 6-9. doi: 10.3321/j.issn:1005-8737.1999.04.002 [47] 宁军号, 常亚青, 刘伟, 等. 温度骤降对光滑河兰蛤的胁迫效应[J]. 水产科学, 2016, 35(2): 117-122. [48] 范耘硕, 邵蓬, 贾旭颖, 等. 温度胁迫对大鳞副泥鳅抗氧化与非特异性免疫指标的影响[J]. 渔业科学进展, 2019, 40(2): 58-64. [49] 曾霖, 李文成, 宋炜, 等. 铜驯化改善大黄鱼低温耐受性的作用机制[J]. 中国水产科学, 2023, 30(5): 595-603. doi: 10.12264/JFSC2023-0009 [50] 李赟, 汝少国. 久效磷对金鱼肝脏和血浆谷丙、谷草转氨酶活性的影响[J]. 安全与环境学报, 2008, 8(5): 9-12. doi: 10.3969/j.issn.1009-6094.2008.05.003 [51] 袁仲瑾, 岑剑伟, 李来好, 等. 低温暂养对珍珠龙胆石斑鱼存活、非特异性免疫及抗氧化指标的影响[J]. 南方水产科学, 2022, 18(6): 118-126. doi: 10.12131/20220042 [52] KIEMER M C B, BLACK K D, LUSSOT D, et al. The effects of chronic and acute exposure to hydrogen sulphide on Atlantic salmon (Salmo salar L.)[J]. Aquaculture, 1995, 135(4): 311-327.
[53] 高权新, 谢明媚, 彭士明, 等. 急性温度胁迫对银鲳幼鱼代谢酶、离子酶活性及血清离子浓度的影响[J]. 南方水产科学, 2016, 12(2): 59-66. doi: 10.3969/j.issn.2095-0780.2016.02.009 [54] 袁新程, 蒋飞, 施永海, 等. 高温胁迫对美洲鲥1+ 龄鱼种抗氧化与非特异性免疫相关指标的影响[J]. 浙江大学学报 (农业与生命科学版), 2021, 47(1): 107-117. [55] ELLOUZ S C, BENMABROUK H, BAROUDI O, et al. Mediterranien cuttlefish Sepia officinalis squid ink is cytotoxic but does not inhibit Glioblastoma U87 tumor cells proliferation, with high nutritional values of edible viscera[J]. Int J Mol Sci, 2014, 3(2): 146-154.
[56] 王馨云, 谢晶. 不同冷藏条件下金枪鱼的水分迁移与脂肪酸变化的相关性[J]. 食品科学, 2020, 41(5): 200-206. doi: 10.7506/spkx1002-6630-20190303-017 [57] 吴艺文, 赵曼曼, 尤孝鹏, 等. 鲜活虹鳟鱼的呼吸频率与肌肉品质的相关性[J]. 食品工业科技, 2023, 44(12): 29-36. -
期刊类型引用(1)
1. 庄平,赵峰,罗刚,张涛,石小涛,冯广朋,王思凯. 水生生物资源增殖放流的发展历程与问题思考. 水生生物学报. 2025(01): 43-54 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
