Genetic variation of mtDNA COI sequence of Scomberomorus commerson populations in the South China Sea
-
摘要:
在测定的采自广东饶平、阳江和广西东兴海域的62尾康氏马鲛(Scomberomorus commerson)线粒体COI基因711 bp序列中,共检测到26个变异位点,18个单倍型,总体呈现出高单倍型多样性(Hd=0.808±0.040)和低核苷酸多样性(π=0.004 0±0.000 6)的特点。邻接树上出现了3个分支,分支间Fst为0.811~0.833且P<0.001,Nm为0.1~0.117;AMOVA分析显示分支间遗传变异占82.61%。表明3个分支间分化程度高,推测分歧时间为(89~22.67)万年前中更新世时期,可能原因是受到更新世冰期和间冰期交替的影响。但分支内与分支间都有不同地理来源的个体,没有出现明显的地理聚群;不同地理群体间Fst为-0.027~0.066,Nm均大于4或小于0;群体内个体间变异为96.34%。均表明群体间基因交流频繁,遗传分化程度并不高。3个分支中Clade A分支经历过种群快速扩张事件,可能是末次冰期期间康氏马鲛进入外海并受洋流及生存空间改变的影响。
Abstract:We analyzed 711 bp segment of the mtDNA cytochrome oxidase subunit Ⅰ of 62 individuals of Scomberomorus commerson collected from Raoping, Yangjiang in Guangdong Province and Dongxing in Guangxi Province, among which 26 mutations and 18 haplotypes were detected. Generally, the haplotype diversity (Hd=0.808±0.040) level was relatively high, while the nucleotide diversity was much poorer (π=0.004 0±0.000 6). Three shallow clades appeared in the Kimura 2-parameter based on neighbor-joining tree and parsimony network; pairwise fixation index Fst value ranged from 0.811 to 0.833 (P<0.001); gene flow ranged from 0.1 to 0.117. Analysis of molecular variance shows that the genetic variation among three clades was 82.61%, suggesting significantly high genetic differentiation. The deduced divergence time was about 890~226.7 ka BP (i.e., during the middle Pleistocene period), and the Glacial interglacial cycles in Pleistocene might be the reason of genetic differentiation. However, individuals from various locations were intertwined together in all clades; pairwise Fst (-0.027~0.066) and gene flow among sampling sites revealed no significant differentiation. AMOVA analysis shows that the percentage of population variation was 96.34%, suggesting a relatively high level of gene flow among sampling sites in the South China Sea. In Clade A, the significant negative values of neutral test and the unimodal mismatch distribution suggest a recent population expansion occurred in this clade about 890 000~226 700 years ago, due to the effects of changed living space and marine currents during Pleistocene glaciations.
-
康氏马鲛(Scomberomorus commerson)俗称鱼、康氏鲅,隶属鲈形目鲭科马鲛属,暖水性中上层肉食性鱼类,广泛分布于印度-西太平洋海域,国外自非洲东岸、红海,东至澳洲,北至韩国、日本均有分布[1],中国主要产于南海,东海和黄海北部可见少数洄游鱼群[2]。康氏马鲛游泳能力强,栖息深度为15~200 m,当南海北部近海水温下降时迁移至外海;水温上升时,从外海向近海作产卵和索饵洄游,表现出集群习性[2]。其肉质细腻、味道鲜美、营养丰富,兼具补气、平咳和提神等功效。康氏马鲛是各沿岸国重要的海产优质鱼类,全世界年产量(7~22)×104 t[3],是底拖网、流刺网及海钓的重要捕捞对象。鲭科鲔属、鲭属等鱼类都是常被人类食用的深海鱼,但近年来黄鳍金枪鱼(Thunnus albacores)产量严重下降[4]、黑鲔(Euthynnus lineatus)更被视为已濒临绝种[5],以往渔获尚称充足的马鲛也面临过度捕捞的压力。
遗传多样性体现了物种对不同环境的适应能力和开发利用的潜力,开展鱼类遗传多样性研究对渔业资源的保护和持续利用至关重要[6]。目前国外关于康氏马鲛遗传多样性和种群结构的研究已有一些报道,包括HOOLIHAN等[7]、SULAIMAN等[8]通过线粒体控制区分别研究ROPME海域、东南亚和澳大利亚北部康氏马鲛种群结构;HERWERDEN等[9]基于微卫星标记研究阿拉伯半岛康氏马鲛群体的遗传变异;FAUVELOT和BORSA[3]通过控制区、细胞色素b以及微卫星3种分子标记探究其种群结构等。但中国关于康氏马鲛的研究很少,仅有杨炳忠等[10]关于马鲛体型特征与网目尺寸关系的初步探讨等少量渔业资源方面的调查研究,尚未见到遗传多样性及种质资源方面的报道。线粒体DNA(mtDNA)是群体遗传学研究的理想分子标记,具有分子结构简单、无重组、进化速度快及遵循母系遗传等优点[11]。其中线粒体控制区序列进化速率较快,但存在模糊种群遗传结构及片段缺失的情况[12],而进化速率中等的COI基因,不仅是物种DNA条形码鉴定的首选分子标记,如HEBERT等[13]提出了DNA条形码的概念及应用,WARD等[14]对澳大利亚207种鱼类进行了分子鉴定;同时也被广泛应用于群体遗传结构和遗传分化分析[12],如WANG等[15]、BENTLEY等[16]和SUN等[17]运用COI序列分别对大黄鱼(Larimichthys crocea)、裸狐鲣(Gymnosarda unicolor)和银鲳(Pampus argenteus)进行遗传变异分析。南海是中国康氏马鲛的主要产区,文章通过对南海康氏马鲛COI基因序列变异的研究,旨在了解其遗传背景,为种质资源保护利用提供参考资料。
1. 材料与方法
1.1 实验材料、DNA提取和测序
野生康氏马鲛样品为2005年~2014年间由近海作业的渔船上直接采购而得,采自广东省潮州市饶平(编号RP,20尾)、阳江市(编号YJ,20尾)以及广西防城港市东兴(编号DX,22尾),共计62尾。样品经形态学鉴定后用95%乙醇固定保存。取康氏马鲛背部肌肉组织约100 mg,采用酚-氯仿方法提取基因组DNA并用乙醇沉淀,于40 μL TE溶液溶解后保存。基因组DNA的提取和PCR扩增条件均参照乐小亮等[18]方法,PCR扩增引物为笔者实验室自行设计Cox1Rm:5′-GDGAAATYATWCCRAATCCGGGA-3′和Cox1F:5′-TCYTACCTGTGG-CMATCACACG-3′,PCR产物送至华大基因有限公司切胶纯化并测序。
1.2 数据处理
使用BioEdit 7.0.9.0软件人工校对序列,在MEGA 6.0软件中统计碱基组成,计算转换与颠换比、群体内及群体间遗传距离,构建基于Kimura-2 Parameter(K2P)模型的邻接树,并以1 000次bootstrap计算分支支持率[19]。基于Network软件构建网络图,并结合邻接树以分析单倍型分布情况及种群结构[20]。根据DnaSP 5.10软件统计各地理群体及总体单倍型数、核苷酸多样性(π)、单倍型多样性(Hd)等遗传多样性指数;获得净遗传距离(Da)以计算不同分支间分化时间[21];进行Ramos-Onsins & Rozas′s R2检验[22]。使用Arlequin 3.5软件计算遗传分化系数(Fst),并通过1 000次重复抽样检验其显著性以评价群体间遗传差异,根据公式Nm=(1-Fst)/(2Fst)计算群体间基因流(Nm); 获得τ、SSD和Raggedness值,通过分子方差(AMOVA)分析检验群体遗传变异[23]。根据Tajima′s D和Fu′s Fs中性检验结果以及基于DnaSP 5.10软件获得的核苷酸不配对分析图来检测种群的历史动态。种群扩张时间(T)利用公式τ=2ut进行估算,其中t表示种群扩张至今所经历的代数,T=t×代时,代时为研究对象的生殖周期;τ为扩张时间参数,u=μk,μ为线粒体COI基因变异速率,k表示序列长度。
2. 结果
2.1 线粒体COI基因片段序列特征
在62尾康氏马鲛线粒体COI 5′端711 bp序列中,共检测到26个变异位点,其中11个简约信息位点,15个单一变异位点;转换与颠换比例为4.81,表明此片段没有饱和,适合遗传分析。序列中T、C、A和G含量分别为29.9%、28.7%、23.5%和17.9%,A+T的含量(53.4%)略高于C+G的含量(46.6%),与大多数硬骨鱼类COI基因片段特性一致[24]。共发现18个单倍型,其中13个为各群体所特有,5个为共享单倍型;H1、H2、H6为所有群体所共享,H4为饶平和东兴群体共享,H9为阳江和东兴群体共享。康氏马鲛总体62条序列(Hd=0.808±0.040,π=0.004 0±0.000 6)以及不同地理群体(Hd 0.758~0.840,π 0.003 2~0.004 8)均呈现高单倍型多样性、低核苷酸多样性的特点,其中单倍型多样性东兴群体最高(Hd=0.840±0.057),饶平群体最低(Hd=0.758±0.081);核苷酸多样性饶平群体最高(π=0.004 8±0.000 7),阳江群体最低(π=0.003 2±0.001 0)。具体遗传多样性参数见表 1。
表 1 中国南海康氏马鲛的遗传多样性指数Table 1. Genetic diversity parameters of S. commerson populations in the South China Sea群体
population经纬度
longitude and latitude数量
n单倍型数
N变异位点数
variable site单倍型多样性
Hd核苷酸多样性
π饶平(RP) 117.01°E,23.67°N 20 8 15 0.758±0.081 0.004 8±0.000 7 阳江(YJ) 111.99°E,21.82°N 20 8 14 0.805±0.070 0.003 2±0.001 0 东兴(DX) 108.10°E,21.55°N 22 10 15 0.840±0.057 0.003 6±0.001 0 Clade A 50 13 15 0.722±0.055 0.001 5±0.000 2 Clade B 2 1 0 - - Clade C 10 4 7 0.533±0.180 0.001 9±0.000 8 总体total 62 18 26 0.808±0.040 0.004 0±0.000 6 注:n. 数量;N. 单倍型数;Hd. 单倍型多样性;π. 核苷酸多样性;Clade A~C表示邻接树上3个分支
Note:n. number of samples;N. number of haplotypes;Hd. haplotype diversity;π. nucleotide diversity;Clade A,Clade B and Clade C represent three branches of neighbor-joining tree.2.2 康氏马鲛的遗传分化
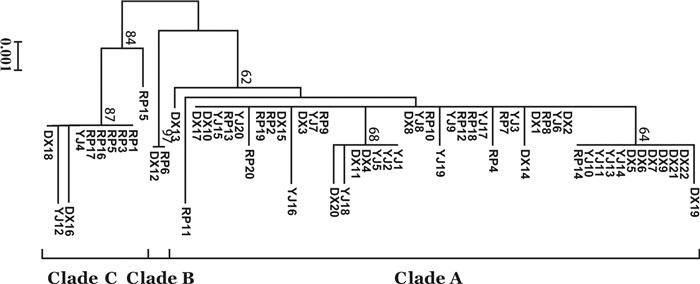
在邻接树上(图 1),所有个体聚为3个分支:1)Clade A有50个体,其中饶平、阳江和东兴分别为13、18、19个体;2)Clade B仅2个体,饶平和东兴各1个体;3)Clade C含10个体,饶平、阳江和东兴分别有6、2、2个体。Clade A单倍型多样性(Hd=0.722±0.055)高于Clade C(Hd=0.533±0.180),但两者核苷酸多样性相近(分别为0.001 5±0.000 2、0.001 9±0.000 8),且明显比康氏马鲛总体(π=0.004 0±0.000 6)低。3个分支中均有来自不同地理群体的个体,不呈现明显的地理聚群。康氏马鲛群体单倍型网络图(图 2)也显示不同地理来源的单倍型混杂分布在一起,没有形成各自的分支,而是呈现出以单倍型H2(为所有群体所共享)为中心单倍型的非典型星状的发散图。网络图中存在3个单倍型组:右边矩形框内由13个单倍型聚集成最大一组,中间单倍型H4形成单独一组,左边矩形框内4个单倍型为第3个组。单倍型网络关系图(图 2)与邻接树(图 1)的拓扑结构相一致。因Clade B和Clade C包含个体数量较少(19.4%),下文不作深入分析。
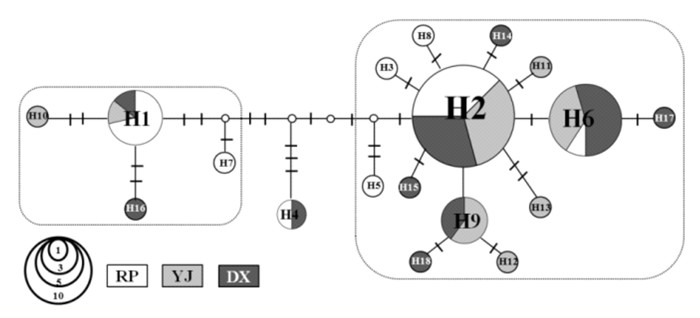
![]() 图 2 南海康氏马鲛COI基因单倍型网络每个饼图代表一个特有单倍型及其共享该单倍型的个体数;饼图同背景色及其面积表示地理来源及其相对丰度及其枝上短线为突变步数,RP,YJ和DX分别代表饶平、阳江和东兴;矩形框表示不同的单倍型组。Figure 2. Parsimony network of COI haplotypes of S. commerson in the South China SeaEach pie represents a unique haplotype and the number of included individuals. Small open circles represent haplotypes that were not sampled in the study. A dash on line indicates a mutation step. Sampling sites are color-coded and abbreviated as RP for Raoping, YJ for Yangjiang and DX for Dongxin, and the size of colored area indicates its relative abundance. Rectangle blocks represent haplotype groups.
图 2 南海康氏马鲛COI基因单倍型网络每个饼图代表一个特有单倍型及其共享该单倍型的个体数;饼图同背景色及其面积表示地理来源及其相对丰度及其枝上短线为突变步数,RP,YJ和DX分别代表饶平、阳江和东兴;矩形框表示不同的单倍型组。Figure 2. Parsimony network of COI haplotypes of S. commerson in the South China SeaEach pie represents a unique haplotype and the number of included individuals. Small open circles represent haplotypes that were not sampled in the study. A dash on line indicates a mutation step. Sampling sites are color-coded and abbreviated as RP for Raoping, YJ for Yangjiang and DX for Dongxin, and the size of colored area indicates its relative abundance. Rectangle blocks represent haplotype groups.南海康氏马鲛群体内与群体间平均遗传距离均为0.003~0.005;群体间Fst为-0.027~0.066,仅饶平与阳江之间P<0.05;基因流Nm均大于4或小于0,群体间遗传分化程度并不高(表 2)。进行AMOVA分子方差分析:1)将3个群体作为一组,群体内个体间变异为96.34%,群体间仅占3.66%;2)以琼州海峡为界,一组为东侧饶平和阳江群体,另一组为西侧东兴群体,群体内个体间变异为97.95%,两组间变异为-5.34%。分支间Fst为0.811~0.833且P<0.001,Nm为0.1~0.117;AMOVA分析显示82.61%的变异来自3个分支间,仅17.39%变异来自分支内个体间。参照线粒体COI序列变异速率为每百万年1%~3%[15],根据Clade A、Clade B间净遗传距离Da为0.006 8,Clade A、Clade C间Da为0.007 6以及Clade B、Clade C间Da为0.008 9,推算出分歧时间分别为(68~22.67)万年前、(76~25.33)万年前和(89~29.67)万年前,均处于中更新世时期。Clade A分支所含个体占总体的80.6%,进一步遗传分析发现这一分支内3个地理群体间Fst为-0.014~0.069,仅饶平与东兴之间P<0.05,Nm为-36.214~11.695;AMOVA分析表明Clade A分支内变异主要集中在群体内个体间(97.31%),显示Clade A分支内3个地理群体间遗传分化程度也不高。
表 2 康氏马鲛地理群体间及分支间遗传分化系数(Fst)和基因流(Nm)Table 2. Pairwise differentiation (Fst) and gene flow (Nm) among sampling sites and clades of S. commersonNm
Fst饶平
RP阳江
YJ东兴
DXClade A Clade B Clade C Clade A
RPClade A
YJClade A
DX饶平RP 7.076 8.121 阳江YJ 0.066* -19.018 东兴DX 0.058 -0.027 Clade A 0.117 0.105 Clade B 0.811*** 0.100 Clade C 0.827*** 0.833** Clade A(RP) 11.695 6.746 Clade A(YJ) 0.041 -36.214 Clade A(DX) 0.069* -0.014 注:*. 0.01<P<0.05;**. 0.001<P<0.01;***. P<0.001 表 3 中国南海康氏马鲛的分子方差分析Table 3. Analysis of molecular variance (AMOVA) of S. commerson in the South China Sea序号
ordinal分组
group项目
item组群间
among groups组群内群体间
among populations within groups群体内
within populations总计
totalI group (RP,YJ,DX) 平方和 5.16 85.23 90.39 变异组成 0.05 1.45 1.50 变异比例 3.66 96.34 Ⅱ group1(琼州海峡东侧RP,YJ) group2(琼州海峡西侧DX) 平方和 1.53 3.63 85.23 90.39 变异组成 0.08 0.11 1.45 1.48 变异比例 -5.34 7.39 97.95 Ⅲ group (Clade A,Clade B,Clade C) 平方和 56.21 34.18 90.39 变异组成 2.75 0.58 3.33 变异比例 82.61 17.39 Ⅳ group (Clade A RP,Clade A YJ、Clade A DX) 平方和 1.57 25.33 26.90 变异组成 0.02 0.53 0.55 变异比例 2.69 97.31 注:Ⅰ. 将康氏马鲛3个地理群体作为1组;Ⅱ. 按琼州海峡两侧分组;Ⅲ. 将3个分支作为1组;Ⅳ. 将Clade A分支中3个地理群体作为1组
Note:Ⅰ. three populations as a whole;Ⅱ. two groups on either sides of Qiongzhou Strait;Ⅲ. cladewise;Ⅳ. three populations of Clade A as a whole2.3 康氏马鲛的种群历史动态
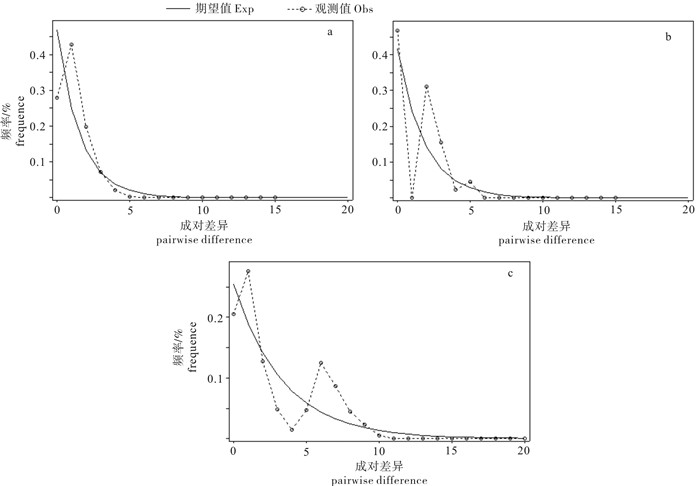
康氏马鲛的中性检验及不配对分布见表 4和图 3。Clade A核苷酸不配对分析(图 3-a)为明显单峰分布,中性检验为极显著负值(P<0.01),Ramos-Onsins & Rozas′s R2检验为0.10(P=0.04);Clade C核苷酸不配对分析(图 3-b)未呈单峰分布,虽Fu′s Fs为非显著负值(P=0.38),但Tajima′D为极显著负值(P=0.008),R2检验值为0.12。整体及3个群体中性检验都为非显著负值(P>0.05);R2检验结果为0.13~0.24(P>0.05),SSD和Raggedness值较大且不存在显著差异(P>0.05);核苷酸错配分析(图 3-c)为多峰分布。根据Clade A扩张参数τ为1.18,参考线粒体COI基因进化速率为每百万年1%~3%[15],以生殖周期为2年计[25],估算出Clade A扩张发生在末次冰期期间(8.30~2.77)万年前,扩张后的有效群体大小θ1(999 99)约是扩张前θ0(0.003 5)的2.8×107倍。
表 4 康氏马鲛的中性检验、不配对分布Table 4. Neutrality tests and mismatches distribution of S. commerson群体
populationTajima′s D Fu′s Fs R2 P SSD P Rg P D P Fs P 饶平RP -0.553 0.31 -0.286 0.50 0.13 0.08 0.06 0.08 0.11 0.22 阳江YJ -1.425 0.06 -1.558 0.20 0.19 0.22 0.02 0.17 0.07 0.47 东兴DX -1.254 0.11 -2.856 0.05 0.24 0.06 0.03 0.10 0.08 0.44 Clade A -2.025 0.003 -8.935 0 0.10 0.04 0.01 0.29 0.09 0.14 Clade B - - - - - - - - - - Clade C -1.839 0.008 -0.175 0.38 0.12 0.23 0.41 0 0.36 0.97 总体total -1.077 0.16 -1.567 0.25 0.16 0.14 0.04 0.12 0.09 0.38 3. 讨论
3.1 康氏马鲛的种群动态和遗传多样性
康氏马鲛总体中性检验为非显著负值;R2检验及SSD、Raggedness值较大且不存在显著差异;核苷酸错配分析(图 3-c)为多峰分布均表明总体从数据上分析未呈现出扩张现象,可能是3个分支叠加所致,但Clade A核苷酸不配对分析(图 3-a)、中性检验及R2检验均表明Clade A在(8.30~2.77)万年前末次冰期期间发生过扩张现象。种群经历了快速扩张与气候变化及其生活习性有关,末次冰期期间气温水温下降,康氏马鲛经历了海平面的大幅度下降,近海栖息范围不断缩小[26],但因康氏马鲛广泛分布于印度-西太平洋海域[1],相比只栖息于近海沿海的鱼类种群,康氏马鲛因能由近海沿海向外海迁移[2],在洋流的影响下基因交流更为频繁,种群因而发生了扩张。Clade C分支Tajima′D检验为极显著负值(P=0.008),表明这一分支也发生过种群扩张,但其核苷酸不配对分析及Fu′s Fs检验均未从数据上呈现出扩张现象,可能与取样点及取样量过少有关。
中国南海康氏马鲛线粒体COI序列总体及各地理群体均呈现出高单倍型多样性(Hd=0.808±0.040)、低核苷酸多样性特征(π=0.004 0±0.000 6),这与HOOLIHAN等[7](Hd=0.986,π=0.038)、FAUVELOT和BORSA[3](Hd=0.959,π=0.088)基于控制区序列分析康氏马鲛遗传多样性有相同的特点,符合GRANT和BOWEN[27]提出的4种海水鱼类遗传多样性模式中高Hd低π的分布模式。Clade A近期历史上发生过种群快速扩张,说明其在短时间内经历过由一个较小群体快速成长为一个大群体的过程[28],单倍型多样性随着群体数量的快速增加而变大,但核苷酸产生的变异没有足够的时间来积累,因此呈现高Hd低π特征。康氏马鲛与同分布于印度-西太平洋海域的裸狐鲣(Gymnosarda unicolor)(Hd=0.86±0.04,π=0.004±0.002)[16]相近,而明显高于银鲳(Pampus argenteus)(Hd=0.580±0.111,π=0.001 5±0.116)[17]、四指马鲅(Eleutheronema rhadinum)(Hd=0.530±0.089,π=0.001 6± 0.001 2)[29]等,说明其遗传多样性相对丰富,这可能是不同的地理分布和生活习性所致。
3.2 康氏马鲛的种群结构
基因流的阻隔及环境因子的影响会导致不同地理群体间遗传结构上的显著差异,大部分海水鱼常因其活动范围广、地理屏障少而被认为遗传分化较低,种群结构不明显[28]。文章中邻接树(图 1)和单倍型网络图(图 2)均聚集形成3个分支,分支间Fst、Nm及AMOVA分析均表明NJ树上3个分支间存在高度显著分化,分歧时间约为(89~22.67)万年前间,可能是更新世冰期的影响[30],更新世存在冰期和间冰期的交替,冰期海平面的下降、沿海大陆架大面积露出使群体被迫分隔在不同海域形成了遗传结构上的差异,从而分化出了不同的分支[31]。但分支中不同地理来源的个体杂乱分布在一起,不呈现明显的地理聚群,是由于冰期过后气候回升,随着海平面的上升被隔离的分支进行了再次接触[30]。
群体间Fst(表 2)为-0.027~0.066,基因流Nm均大于4或小于0,AMOVA分子方差分析(表 3)显示群体内的变异为96.34%,表明群体间遗传分化程度并不高;不同分支与群体地理分布无关,表明群体间无明显地理结构,可能的原因包括:卵子具漂浮性和较强的潜在扩散能力,且成鱼存在产卵和索饵洄游这一集群习性行为[1-2],因此具有使种群资源恢复和促进群体间基因交流的能力;以琼州海峡为界的AMOVA分析也显示变异主要集中在群体内个体间(97.95%),说明琼州海峡未对康氏马鲛起到屏障隔离的作用,南海内不存在明显阻碍康氏马鲛扩散的地理障碍[32];受到向北的南海暖流和向南的黑潮以及中国沿岸流的影响,成鱼和幼鱼可随海流进行扩散[33];更新世后的海平面上升事件对海洋鱼类的mtDNA遗传结构具有重要影响[30],Clade A发生扩张的时间较晚,缺乏足够的时间达到迁移和漂变的平衡[33];还有一个可能原因是由于其他马鲛属鱼类分布均在80°的经度和80°的纬度甚至更小的范围内,但康氏马鲛在印度-西太平洋海域内的分布跨越了160°的经度和80°的纬度范围(自非洲东岸、红海,东至澳洲,北至中国、韩国、日本)[3],其在广阔的世界栖息范围内存在地理结构的分化[3, 8],但中国南海海域未达到这一分化程度。
4. 小结与展望
物种遗传多样性的高低,与其生存进化潜力密切相关[34]。目前康氏马鲛遗传多样性总体较丰富,说明其资源虽有所下降但未影响到遗传多样性,具有潜在的资源恢复能力,这为种内杂交和选育提供了种质保障。南海康氏马鲛虽然出现了3个分支,但分支间遗传差异不大,分支内与分支间都有不同地理来源的个体,各地理群体个体均分散存在于不同分支中,均表明没有出现明显的地理聚群,因而可作为一个管理保护单位。3个地理群体中,饶平与阳江间存在具统计学意义的显著分化(Fst=0.066,P=0.036);Clade A分支内饶平与东兴群体间也出现了显著分化(Fst=0.069,P=0.027),说明南海康氏马鲛可能并不是一个随机交配群体。因文中仅采用线粒体COI分子标记对南海3个地理群体进行康氏马鲛遗传多样性进行分析,可考虑结合其他更灵敏分子标记包括核基因标记(如AFLP、微卫星等)和线粒体基因标记(如控制区、细胞色素b等)并增加采样点和样品数量,以更深入地了解中国沿海康氏马鲛群体结构和遗传多样性状况。
-
图 2 南海康氏马鲛COI基因单倍型网络
每个饼图代表一个特有单倍型及其共享该单倍型的个体数;饼图同背景色及其面积表示地理来源及其相对丰度及其枝上短线为突变步数,RP,YJ和DX分别代表饶平、阳江和东兴;矩形框表示不同的单倍型组。
Figure 2. Parsimony network of COI haplotypes of S. commerson in the South China Sea
Each pie represents a unique haplotype and the number of included individuals. Small open circles represent haplotypes that were not sampled in the study. A dash on line indicates a mutation step. Sampling sites are color-coded and abbreviated as RP for Raoping, YJ for Yangjiang and DX for Dongxin, and the size of colored area indicates its relative abundance. Rectangle blocks represent haplotype groups.
表 1 中国南海康氏马鲛的遗传多样性指数
Table 1 Genetic diversity parameters of S. commerson populations in the South China Sea
群体
population经纬度
longitude and latitude数量
n单倍型数
N变异位点数
variable site单倍型多样性
Hd核苷酸多样性
π饶平(RP) 117.01°E,23.67°N 20 8 15 0.758±0.081 0.004 8±0.000 7 阳江(YJ) 111.99°E,21.82°N 20 8 14 0.805±0.070 0.003 2±0.001 0 东兴(DX) 108.10°E,21.55°N 22 10 15 0.840±0.057 0.003 6±0.001 0 Clade A 50 13 15 0.722±0.055 0.001 5±0.000 2 Clade B 2 1 0 - - Clade C 10 4 7 0.533±0.180 0.001 9±0.000 8 总体total 62 18 26 0.808±0.040 0.004 0±0.000 6 注:n. 数量;N. 单倍型数;Hd. 单倍型多样性;π. 核苷酸多样性;Clade A~C表示邻接树上3个分支
Note:n. number of samples;N. number of haplotypes;Hd. haplotype diversity;π. nucleotide diversity;Clade A,Clade B and Clade C represent three branches of neighbor-joining tree.表 2 康氏马鲛地理群体间及分支间遗传分化系数(Fst)和基因流(Nm)
Table 2 Pairwise differentiation (Fst) and gene flow (Nm) among sampling sites and clades of S. commerson
Nm
Fst饶平
RP阳江
YJ东兴
DXClade A Clade B Clade C Clade A
RPClade A
YJClade A
DX饶平RP 7.076 8.121 阳江YJ 0.066* -19.018 东兴DX 0.058 -0.027 Clade A 0.117 0.105 Clade B 0.811*** 0.100 Clade C 0.827*** 0.833** Clade A(RP) 11.695 6.746 Clade A(YJ) 0.041 -36.214 Clade A(DX) 0.069* -0.014 注:*. 0.01<P<0.05;**. 0.001<P<0.01;***. P<0.001 表 3 中国南海康氏马鲛的分子方差分析
Table 3 Analysis of molecular variance (AMOVA) of S. commerson in the South China Sea
序号
ordinal分组
group项目
item组群间
among groups组群内群体间
among populations within groups群体内
within populations总计
totalI group (RP,YJ,DX) 平方和 5.16 85.23 90.39 变异组成 0.05 1.45 1.50 变异比例 3.66 96.34 Ⅱ group1(琼州海峡东侧RP,YJ) group2(琼州海峡西侧DX) 平方和 1.53 3.63 85.23 90.39 变异组成 0.08 0.11 1.45 1.48 变异比例 -5.34 7.39 97.95 Ⅲ group (Clade A,Clade B,Clade C) 平方和 56.21 34.18 90.39 变异组成 2.75 0.58 3.33 变异比例 82.61 17.39 Ⅳ group (Clade A RP,Clade A YJ、Clade A DX) 平方和 1.57 25.33 26.90 变异组成 0.02 0.53 0.55 变异比例 2.69 97.31 注:Ⅰ. 将康氏马鲛3个地理群体作为1组;Ⅱ. 按琼州海峡两侧分组;Ⅲ. 将3个分支作为1组;Ⅳ. 将Clade A分支中3个地理群体作为1组
Note:Ⅰ. three populations as a whole;Ⅱ. two groups on either sides of Qiongzhou Strait;Ⅲ. cladewise;Ⅳ. three populations of Clade A as a whole表 4 康氏马鲛的中性检验、不配对分布
Table 4 Neutrality tests and mismatches distribution of S. commerson
群体
populationTajima′s D Fu′s Fs R2 P SSD P Rg P D P Fs P 饶平RP -0.553 0.31 -0.286 0.50 0.13 0.08 0.06 0.08 0.11 0.22 阳江YJ -1.425 0.06 -1.558 0.20 0.19 0.22 0.02 0.17 0.07 0.47 东兴DX -1.254 0.11 -2.856 0.05 0.24 0.06 0.03 0.10 0.08 0.44 Clade A -2.025 0.003 -8.935 0 0.10 0.04 0.01 0.29 0.09 0.14 Clade B - - - - - - - - - - Clade C -1.839 0.008 -0.175 0.38 0.12 0.23 0.41 0 0.36 0.97 总体total -1.077 0.16 -1.567 0.25 0.16 0.14 0.04 0.12 0.09 0.38 -
[1] COLLETTE B B, RUSSO J L. Morphology, systematics and biology of the Spanish mackerel (Scomberomorus, Scombridae)[J]. Fish Bull, 1984, 82(4): 545-692.
[2] 陈再超, 刘继兴. 南海经济鱼类[M]. 广州: 广东科技出版社, 1982: 216-221. [3] FAUVELOT C, BORSA P. Patterns of genetic isolation in a widely distributed pelagic fish, the narrow-barred Spanish mackerel (Scomberomorus commerson)[J]. Biol J Linnean Soc, 2011, 104(4): 886-902. doi: 10.1111/j.1095-8312.2011.01754.x
[4] LI W, CHEN X, XU Q, et al. Genetic population structure of Thunnus albacares in the Central Pacific Ocean based on mtDNA COI gene sequences[J]. Biochem Genet, 2015, 53(1/2/3): 8-22. doi: 10.1007/s10528-015-9666-0
[5] KUMAR G, KUNAL S P. Historic demography and phylogenetic relationship of Euthynnus species based on COI sequence analyses[J]. Int J Bioinform Res Appl, 2013, 9(5): 547-555. doi: 10.1504/IJBRA.2013.056088
[6] 薛丹, 章群, 郜星晨, 等. 基于线粒体控制区的粤闽三线矶鲈地理群体的遗传变异分析[J]. 海洋渔业, 2014, 36(6): 496-502. doi: 10.3969/j.issn.1004-2490.2014.06.003 [7] HOOLIHAN J P, ANANDH P, van HERWERDEN L. Mitochond-rial DNA analyses of narrow-barred Spanish mackerel (Scomberomorus commerson) suggest a single genetic stock in the ROPME sea area (Arabian Gulf, Gulf of Oman, and Arabian Sea)[J]. ICES J Mar Sci, 2006, 63(6): 1066-1074. doi: 10.1016/j.icesjms.2006.03.012
[8] SULAIMAN Z H, OVENDEN J R. Population genetic evidence for the East-West division of the narrow-barred Spanish mackerel (Scomberomorus commerson, Perciformes: Teleostei) along Wallace's Line[J]. Biodivers Conserv, 2010, 19(2): 563-574. doi: 10.1007/s10531-009-9699-y
[9] van HERWERDEN L, MCILWAIN J, AL-OUFI H, et al. Development and application of microsatellite markers for Scomberomorus commerson (Perciformes; Teleostei) to a population genetic study of Arabian Peninsula stocks[J]. Fish Res, 2006, 79(3): 258-266. doi: 10.1016/j.fishres.2006.04.004
[10] 杨炳忠, 杨吝, 谭永光, 等. 马鲛体型特征与网目尺寸关系的初步探讨[J]. 南方水产科学, 2013, 9(5): 120-125. doi: 10.3969/j.issn.2095-0780.2013.05.018 [11] MULVEY M, LIU H P, KANDL K. Application of molecular genetic markers to conservation of freshwater bivalves[J]. J Shellfish Res, 1998, 17(5): 1395-1405.
[12] TAKESHIMA H, IGUCHI K, NISHIDA M. Unexpected ceiling of genetic differentiation in the control region of the mitochondrial DNA between different subspecies of the Ayu Plecoglossus altivelis[J]. Zool Sci, 2005, 22(4): 401-410. doi: 10.2108/zsj.22.401
[13] HEBERT P N, CYWINSKA A, BALL S L, et al. Biological identifications through DNA barcodes[J]. Proc Royal Soc London Biol Sci, 2003, 270(1512): 313-321. doi: 10.1098/rspb.2002.2218
[14] WARD R D, ZEMLAK T S, INNES B H, et al. DNA barcoding Australia's fish species[J]. Philos Trans R Soc Lond B Biol Sci, 2005, 360(1462): 1847-1857. doi: 10.1098/rstb.2005.1716
[15] WANG L, SHI X F, SU Y Q, et al. Genetic divergence and historical demography in the endangered large yellow croaker revealed by mtDNA[J]. Biochem Syst Ecol, 2013, 46: 137-144. doi: 10.1016/j.bse.2012.09.021
[16] BENTLEY B P, HARVEY E S, NEWMAN S J, et al. Local genetic patchiness but no regional differences between Indo-West Pacific populations of the dogtooth tuna Gymnosarda unicolor[J]. Mar Ecol Prog Ser, 2014, 506: 267-277. doi: 10.3354/meps10819
[17] SUN P, YIN F, SHI Z, et al. Genetic structure of Silver pomfret (Pampus argenteus (Euphrasen, 1788)) in the Arabian Sea, Bay of Bengal, and South China Sea as indicated by mitochondrial COI gene sequences[J]. J Appl Ichthyol, 2013, 29(4): 733-737. doi: 10.1111/jai.12130
[18] 乐小亮, 章群, 赵爽, 等. 一种高效快速的鱼类标本基因组DNA提取方法[J]. 生物技术通报, 2010(2): 202-204. https://biotech.aiijournal.com/CN/abstract/abstract5369.shtml [19] TAMURA K, STECHER G, PETERSON D, et al. MEGA6: molecular evolutionary genetics analysis version 6.0[J]. Mol Biol Evol, 2013, 30(12): 2725-2729. doi: 10.1093/molbev/mst197
[20] BANDELT H J, FORSTER P, RÖHL A. Median-joining networks for inferring intraspecific phylogenies[J]. Mol Biol Evol, 1999, 16(1): 37-48. doi: 10.1093/oxfordjournals.molbev.a026036
[21] LIBRADO P, ROZAS J. DnaSP v5: a software for comprehensive analysis of DNA polymorphism data[J]. Bioinformatics, 2009, 25(11): 1451-1452. doi: 10.1093/bioinformatics/btp187
[22] RAMOS-ONSINS S E, ROZAS J. Statistical properties of new neutrality tests against population growth[J]. Mol Biol Evol, 2002, 19(12): 2092-2100. doi: 10.1093/oxfordjournals.molbev.a004034
[23] EXCOFFIER L, LAVAL G, SCHNEIDER S. Arlequin (version 3.0): an integrated software package for population genetics data analysis[J]. Evol Bioinform Online, 2005, 1: 47-50. https://pubmed.ncbi.nlm.nih.gov/19325852/
[24] KARTAVTSEV Y P, SHARINA S N, GOTO T A, et al. Sequence diversity at Cytochrome Oxidase 1 (Co-1) gene among sculpins (Scorpaeniformes, Cottidae) and some other scorpionfish of Russia Far East with phylogenetic and taxonomic insights[J]. Genes Genom, 2009, 31(2): 183-197. doi: 10.1007/BF03191151
[25] GRANDCOURT E M, ABDESSALAAM T, FRANCIS F, et al. Preliminary assessment of the biology and fishery for the narrow-barred Spanish mackerel, Scomberomorus commerson (Lacépède, 1800), in the southern Arabian Gulf[J]. Fish Res, 2005, 76(2): 277-290. doi: 10.1016/j.fishres.2005.07.001
[26] 茅晟懿, 朱小畏, 吴能友, 等. 南海北部末次冰盛期晚期以来冰融水与气候事件记录: 长链脂肪醇陆源输入指示[J]. 热带海洋学报, 2015, 34(2): 52-65. doi: 10.11978/j.issn.1009-5470.2015.02.007 [27] GRANT W S, BOWEN B W. Shallow population histories in deep evolutionary linages of marine fishes: insights from sardines and anchovies and lessons for conservation[J]. J Heredity, 1998, 89(5): 415-426.
[28] 高天翔, 毕潇潇, 赵林林, 等. 基于线粒体Cytb基因全序列的松江鲈群体遗传结构分析[J]. 水生生物学报, 2013, 37(2): 199-207. doi: 10.7541/2013.5 [29] 邓春兴. 基于COI基因序列的中国东南沿海四指马鲅属鱼类的遗传多样性分析[D]. 广州: 暨南大学, 2014: 27-28.https://www.zhangqiaokeyan.com/academic-degree-domestic_mphd_thesis/020311700237.html [30] NI G, LI Q, KONG L, et al. Comparative phylogeography in marginal seas of the northwestern Pacific[J]. Mol Ecol, 2014, 23(3): 534-548. doi: 10.1111/mec.12620
[31] HEWITT G. The genetic legacy of the Quaternary ice ages[J]. Nature, 2000, 405(6789): 907-913. https://www.nature.com/articles/35016000
[32] 薛丹, 章群, 郜星晨, 等. 基于线粒体控制区序列的南海北部近岸的遗传多样性[J]. 中国水产科学, 2015, 22(4): 749-756. [33] 毕潇潇. 松江鲈(Trachidermus fasciatus)种群的形态学与遗传学研究[D]. 青岛: 中国海洋大学, 2013: 98.https://www.xueweilunwen.com/doc/560659 [34] AVISE J C. Phylogeography: the history and formation of species[M]. London: London Harvard University Press, 2000: 9-32.
-
期刊类型引用(2)
1. 钱静, 沈和定, 管菊. 平疣桑椹石磺生殖系统结构及精子储存场所. 动物学杂志. 2015(04): 600-606 .  百度学术
百度学术
2. 钱静, 沈和定, 管菊, 王成暖. 两种石磺胚胎发育比较. 上海海洋大学学报. 2014(04): 498-504 .  百度学术
百度学术
其他类型引用(1)



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
