The effect of recombinant growth hormone (GH)on insulin-like growth factor-Ⅰ (IGF-Ⅰ) expression in mud carp, Cirrhinus molitorella
-
摘要:
使用半定量RT-PCR方法,研究了鲮(Cirrhinus molitorella)各组织中IGF-ⅠmRNA组织表达,并分析重组鲮GH处理后鲮IGF-Ⅰ表达变化情况。结果表明,鲮IGF-ⅠmRNA在肝组织中表达最高,其次是肾和脑,另外在肠、鳃、脾、性腺和心脏组织中也有表达,而在肌肉、皮肤中没有检测到鲮IGF-ⅠmRNA的表达;按120 μg·g-1鱼体重的剂量经腹腔注射重组鲮GH,观察12 h后鲮IGF-Ⅰ表达变化情况,发现经重组鲮GH处理后,鲮肝组织IGF-ⅠmRNA表达水平显著升高,脑组织IGF-ⅠmRNA表达水平也稍有升高,而在肌肉中仍未检测到IGF-ⅠmRNA的表达;重组鲮GH处理前后,对照组中鲮血清中IGF-Ⅰ的含量为145.59±21.84 ng·mL-1,试验组中鲮血清中IGF-Ⅰ的含量为247.71±2.83 ng·mL-1,经t检验,P=0.043 < 0.05,表明重组鲮GH处理前后鲮血清中IGF-Ⅰ的含量存在显著性差异。
-
关键词:
- 鲮 /
- 胰岛素样生长因子-Ⅰ /
- 生长激素
Abstract:Expression patterns of IGF-ⅠmRNA in different tissues of mud carp (Cirrhinus molitorella)were studied using semi-quantitative RT-PCR method and the effects of recombinant mud carp growth hormone(rmcGH)on expression of IGF-Ⅰin mud carp were investigated. The IGF-ⅠmRNA was detected successfully in liver, kidney, brain, intestine, gill, spleen, gonad, and heart, and no IGF-ⅠmRNA was detected in skin and muscle. The IGF-Ⅰ mRNA detected was higher in liver than in other tissues. Mud carp were received either intra-peritoneal injections of rmcGH (120 μg·g-1 body weight) or vehicle, tissue samples and blood were collected 12 hour later. Total RNA was isolated and assayed for IGF-ⅠmRNA using semi-quantitative RT-PCR. Blood was extracted to determine the levels of IGF-Ⅰ in serum. IGF-Ⅰlevels increased from 145.59±21.84 to 247.71±2.83 ng·mL-1 (P=0.043) in the serum after rmcGH injection.
-
Keywords:
- mud carp /
- Cirrhinus molitorella /
- insulin-like growth factor-Ⅰ /
- growth hormone
-
鸢乌贼(Sthenoteuthis oualaniensis)隶属于柔鱼科鸢乌贼属,广泛分布在印度洋、太平洋的赤道和亚热带等海域,以印度洋西北部海域的资源量为最大[1]。前苏联和日本学者[2-3]曾多次对印度洋鸢乌贼资源进行调查,同时根据种类的发光器、形态特征、肥满度等初步分为大型、中型和小型3个群体,主要是侧重于对其资源量的研究;SNYDER[4]曾对阿拉伯海鸢乌贼大型群体进行了生物学的初步研究;杨德康[5]根据中国拖网渔船在亚丁湾海域兼捕的鸢乌贼,从捕捞时间和渔获物的性腺成熟度来分析,认为鸢乌贼由春生群、夏生群和秋生群3个群体组成;我国于2003~2005年对印度洋西北部海域鸢乌贼资源进行调查研究,对其资源密度及其分布、钓捕技术、渔场形成机制与海洋环境因子之间的关系等作了较全面的分析,对其生物学特性也作了初步分析[6-9],但是对该海域鸢乌贼的种群及其遗传结构没有作出进一步研究。文章是根据2004~2005年2次对印度洋西北部公海海域(13°N~20°N、59°E~64°E)鸢乌贼资源调查中所采集的鸢乌贼肌肉样本,利用随机扩增多态性DNA(random amplified polymorphic DNA,RAPD)检测方法,对该海域鸢乌贼种群及其遗传结构进行研究,为其资源评估、群体数量变动分析提供最基础的资料。
1. 材料和方法
1.1 材料来源
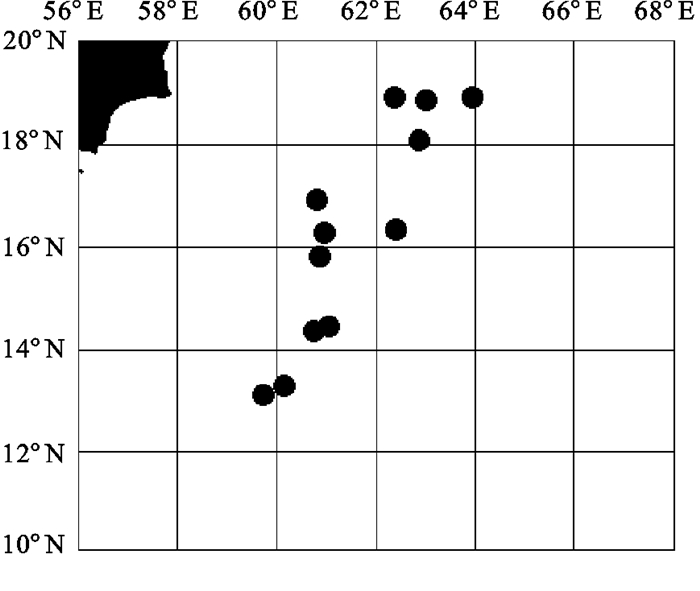
根据2004年9~12月和2005年3~5月2次印度洋西北部公海海域鸢乌贼资源调查结果,在27个站点中共采集鸢乌贼肌肉样本200尾(表 1),其胴长范围为20.3~53.0 cm,平均胴长为36.7 cm。肌肉样本用75%的酒精固定并保存于4℃的冰箱中备用。根据形态学特征及其空间分布,选取了12个站点48尾鸢乌贼的肌肉样本进行RAPD分析(图 1)。
表 1 印度洋西北部海域鸢乌贼肌肉样品取样时间、地点、样本尾数以及分析的样本尾数Table 1. Sampling localities, sampling dates, total numbers and the numbers used for RAPD analysis ofS.oualaniensis in the northwestern Indian Ocean取样时间
sampling date经度/°N
longitude纬度/°E
latitude尾数/ind
numberRAPD分析尾数/ind
numbers used for RAPD analysis2004-10-11 65.25 12.78 5 0 2004-10-12 63.37 13.45 5 0 2004-10-14 62.55 14.55 5 0 2004-10-15 62.35 16.38 5 4 2004-10-16 62.33 18.93 5 4 2004-10-18 63.00 18.88 5 4 2004-10-21 63.93 18.95 5 4 2004-10-22 63.48 18.47 5 0 2004-10-24 62.83 18.12 5 4 2004-10-25 61.45 17.17 5 0 2004-10-26 61.45 17.72 5 0 2004-10-27 61.50 17.78 10 0 2004-10-31 60.93 16.32 10 4 2004-11-01 60.92 15.57 10 0 2004-11-02 59.42 15.08 10 0 2004-11-06 59.67 13.17 10 4 2004-11-07 60.10 13.33 10 4 2004-11-09 60.92 14.13 10 0 2004-11-10 61.02 14.50 10 4 2004-11-12 60.72 14.42 10 4 2004-11-14 60.78 16.97 10 4 2004-11-15 60.53 16.87 10 0 2004-11-17 60.82 15.87 10 4 2004-11-20 60.45 15.40 10 0 2005-03-27 60.43 13.00 4 0 2005-03-31 60.00 15.00 5 0 2005-04-03 61.05 16.95 6 0 合计 total 200 48 1.2 试验方法和数据处理
1.2.1 基因组DNA的提取和检测
取肌肉样本25~30 mg加液氮后碾碎,-70℃保存备用。采用基因组DNA纯化试剂盒(SK1252,Sangon公司生产)提取基因组DNA。用Beckman DU-650紫外分光光度计检测DNA的含量,并用1%的琼脂糖凝胶电泳检测基因组DNA的质量。检测后的基因组DNA放置于-20℃冰箱中备用。
1.2.2 PCR-RAPD扩增反应及电泳
PCR-RAPD所采用的随机引物由上海Sangon公司合成。扩增反应中体积为25 μL,其中包括10×Taq buffer 2.5 μL,dNTPs(Fermentas公司生产,25 mol·L-1)0.5 μL,MgCl2(Fermentas公司生产,25 mmol·L-1)2.5 μL,Taq DNA Polymerase(Fermentas公司生产,5 μ·μL-1)0.2 μL,随机引物(Sangon公司生产,50 μmol·μL-1)0.5 μL,基因组DNA 1μL(50~100 ng·μL-1),ddH2O 17.8 μL。
PCR扩增在GeneAmp PCR System 9700 PCR仪上进行,所有样本对每一个引物都进行1~2次扩增反应。反应条件为经94℃预变性2 min后,接着40个循环,每个循环包括94℃变性15 s,35℃复性60 s,72℃延伸90 s,最后是72℃终延伸10 min,4℃保温。扩增产物用1.5%琼脂糖凝胶电泳分离,EB染色,凝胶成像系统(genius bio imaging system,GENE公司生产)观察、拍照并记录。
1.2.3 数据处理
根据电泳后记录下清晰的扩增条带进行数据统计,在RAPD图谱中相对位置无条带的用“0”表示,在相对位置有条带的用“1”表示,将RAPD图谱转化成0、1矩阵,利用Popgene 1.31软件计算不同站点鸢乌贼样本的遗传相似度(S)和遗传距离(D)。计算公式为:
$$ S=\frac{2 N_\mathtt{x y}}{N_\mathtt{x}+N_\mathtt{y}} ; D=1-S $$ 式中Nxy为X、Y 2个样本共有的扩增条带,Nx、Ny分别为X、Y样本各自拥有的扩增带。
采用PHYLIP(phylogeny inference package,Ver.3.5)软件包中的NEIGHBOR程进行UPGMA(unweighted pair-group method with arithmetic average)聚类分析。参照恽锐等[10]的方法,用Shannon多样性指数计算种群的遗传多样性,其平均值即为种群的遗传多样性。计算公式为:
$$ h=-\sum p_i \log _2 p_i $$ 式中pi为某位点的表型频率,包括有带样本的频率和无带样本的频率,h为该位点的表型多样性,即样本在该位点出现“有带”或“无带”的不确定性。
利用Arlequin 2.0软件进行分子方差分析(analysis of molecular variance,AMOVA),计算其遗传分化指数(GST),GST即为种群间的遗传多样性占种群多样性的比例,以检测鸢乌贼种群内和种群间的遗传变异情况的显著性。计算公式为:
$$ G_{\mathrm{ST}}=\frac{H_{\mathrm{T}}-H_{\mathrm{S}}}{H_{\mathrm{T}}} $$ 式中HT为种群的总遗传多样性,HS为种群内平均遗传多样性。
2. 结果
2.1 RAPD扩增结果
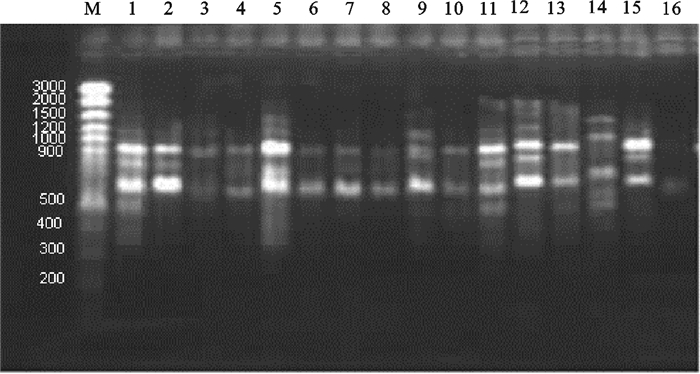
PCR-RAPD试验所使用的16个随机引物中,经过筛选,选取扩增条带丰富且稳定性好的8个引物进行分析,引物序列见表 2。每个引物均可得到条带清晰且重复性好的扩增图谱,扩增条带为3~8,其分子量大小为200~1 500 bp。图 2为引物R8的扩增图谱。
表 2 所用的随机引物及其序列Table 2. Primers and their sequence used for RAPD analysis引物
primers序列
sequence引物
primers序列
sequenceR1 5′-ccatcctacc R5 5′-ccatggtgtc R2 5′-acagtaccgcc R6 5′-aaccgcgtcc R3 5′-gatggctgtg R7 5′-ctcaccgtcc R4 5′-ctccccaact R8 5′-acggcgtatg 2.2 UPGMA分析
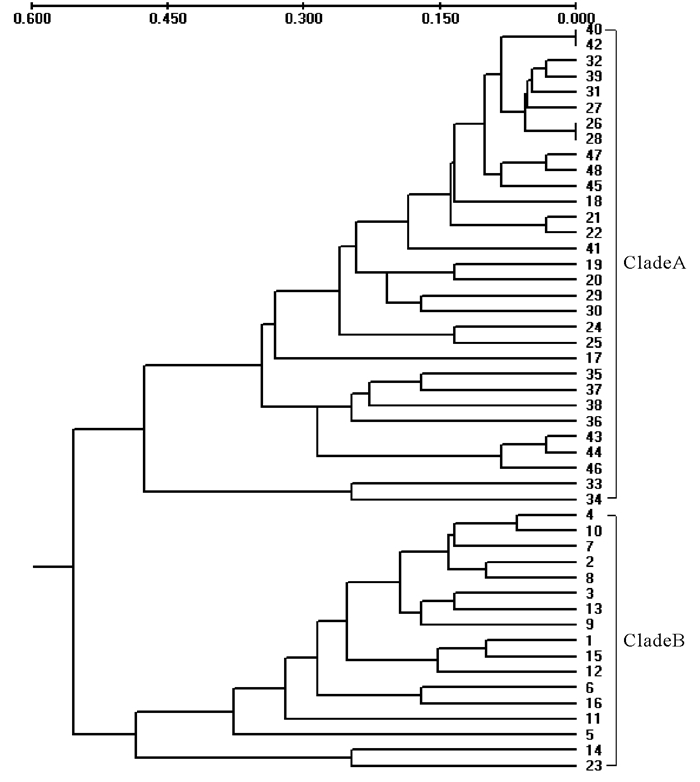
将RAPD图谱转化成0、1矩阵,经过POPGENE 1.31处理,根据NEI[11]的方法可得出各个样本间的遗传相似性指数(S)和遗传距离(D)。根据遗传距离,利用PHYLIP软件包中的NEIGHBOR程序进行UPGMA聚类分析,得出48尾鸢乌贼样本的聚类图(图 3)。
由图 3可知,18°N~20°N海域4个站点的16尾样本聚集在一起,且样本间的最大遗传距离为0.4858,可以推测认为,该海域的鸢乌贼形成一个种群。而在13°N~18°N海域的8个站点的32尾样本中,除第23号样本外,其余样本都聚集在一起,且样本间的最大遗传距离为0.4767,该海域的鸢乌贼也同样形成一个种群。因此,根据UPGMA聚类分析,可以得出在13°N以北的印度洋西北部海域鸢乌贼存在2个不同种群,且2个种群之间的遗传距离为0.1338,遗传相似性指数为0.8748。
2.3 遗传多样性
利用Shannon多样性指数计算印度洋西北部海域鸢乌贼种群的遗传多样性,其平均值即为种群的遗传多样性。计算结果表明,印度洋西北部海域鸢乌贼种群平均每个位点的多样性指数为0.3676±0.1801,由此可以看出其种群的遗传多样性较高,种群分化较大。
2.4 DNA多态性与遗传分化
根据获得的RAPD扩增带,计算种群间的多态位点比例(表 3),2个种群多态位点比例分别为68.75%和93.75%,这说明印度洋西北部海域鸢乌贼2个种群均保持较高的遗传多样性。以种群内不同扩增图谱类型之间的遗传差异值为基础,计算种群的遗传多样性,18°N~20°N海域鸢乌贼种群的遗传多样性为0.2072,13°N~18°N海域鸢乌贼种群为0.1656,其平均值为0.1864。
表 3 印度洋西北部海域鸢乌贼种群多态位点比例与遗传多态性Table 3. Proportion of polymorphic loci and genetic diversity of S.oualaniensis populations in the northwest Indian Ocean内容
content18°N~20°N种群
population located in 18°N~20°N13°N~18°N种群
population located in 13°N~18°N多态位点比例/%
proportion of polymorphic loci68.75 93.75 遗传多态性(平均值±标准差)
genetic diversity (Mean±SE)0.2072±0.1928 0.1656±0.1441 GST是用来判断种群间的遗传分化情况,当GST < 0.05时,种群间没有遗传分化;当0.05 < GST < 0.15时,种群间的遗传分化程度为中等;当0.15 < GST < 0.25时,种群间有高度的分化;当GST>0.25时,种群间的分化程度非常高。印度洋西北部12°N以北海域鸢乌贼种群总遗传多样性为0.2375,种群内平均遗传多样性为0.1864,可以得出其种群间遗传分化指数为0.2150,即21.5%的遗传变异来自于种群间,而78.5%来自于种群内。该结果表明,不同种群间在遗传背景上存在较大的差异,且种群内的遗传变异水平较高。
3. 讨论
3.1 关于印度洋西北部海域鸢乌贼种群结构的探讨
通过对印度洋西北部海域鸢乌贼样本的RAPD分析,并根据遗传距离对其进行UPGMA聚类,发现18°N~20°N海域4个站点的16尾鸢乌贼样本聚集在一起,形成了一个种群,而13°N~18°N海域8个站点的32尾鸢乌贼样本聚集在一起,形成了另一个种群。对这2个不同种群的形态学参数进行统计,18°N~20°N海域鸢乌贼胴长为45.4~53.0 cm,平均胴长为48.9±2.81 cm,而13°N~18°N海域胴长为20.3~51.2 cm,平均胴长为36.3±8.03 cm,优势胴长为32.0~42.0 cm。经单因素方差(ANOVA)分析2个种群间的胴长的P=0.00002 < 0.05,差异性显著。陈新军等[12]认为印度洋西北部海域鸢乌贼分为形态特征存在一定差异性的3个种群:大型种群、中型种群和小型种群,其中大型种群主要分布在18°N以北海域,中型种群主要分布在12°N~18°N海域,小型种群主要分布在12°N以南及赤道附近海域,且这3个种群重叠分布;谷津明彦[3]也认为该海域的鸢乌贼存在3个不同体型的种群,此文所得出的种群结构与陈新军、谷津明彦等研究的结果基本一致。因此,印度洋西北部13°以北海域鸢乌贼种群在形态学与遗传上都可以被区分为18°N~20°N、13°N~18°N 2个不同的种群。
3.2 印度洋西北部海域鸢乌贼的遗传多样性
Shannon多样性指数表示种群间的多样性占总多样性的比例,可以用来估测遗传多样性在种群内和种群间的分布,即估测种群的遗传分化程度。利用Shannon多样性指数计算出的印度洋西北部海域鸢乌贼的遗传多样性指数为0.3676±0.1801,为较高的水平。由于其遗传多样性水平较高,种群分化较大,从侧面可以说明印度洋西北部海域鸢乌贼2个种群在形态上差别很大的原因。
另外,此研究结果还揭示,与18°N~20°N海域鸢乌贼种群相比,13°N~18°N海域鸢乌贼种群拥有较高的多态性位点比例,而遗传多态性却相对较低(表 3),这一结果可能与所选用8条RAPD引物有关;笔者因此推测出13°N~18°N海域鸢乌贼可能所受的捕捞压力相对较大,生长速度较快。基于此研究的分析结果,该海域鸢乌贼2个种群间在遗传背景上存在较大的差异,且种群内的遗传变异水平较高,笔者认为,对该海域鸢乌贼资源的规模性开发还处于较合理水平。
3.3 RAPD结果的分析方法
种以下类群包括亚种、品种及地理种群等,遗传分析的目的在于了解遗传多样性、鉴别种群、分析种群间的差异大小和微进化等,多数学者采用2种方法对RAPD结果进行处理并对上述问题进行探讨[13-15]:(1)寻找种群的特有遗传标记,据此可以鉴别不同的种群;(2)基于遗传相似率的分析,包括相似率比较、遗传距离分析、聚类分析等。此研究在进行RAPD实验过程中未能寻找到用于区分印度洋西北部海域鸢乌贼2个种群的RAPD分子标记,这可能是由于在此次实验中使用引物较少的原因所造成的。因而,此研究选用了第2种分析方法。
RAPD技术能够快速、简便地检测大量基因组DNA的遗传变异,只要采用适当的分析方法,不仅可以用于鉴定头足类资源的品系、种群结构并探讨其进化关系,还可以在探讨头足类种群分化等方面发挥重要作用。
-
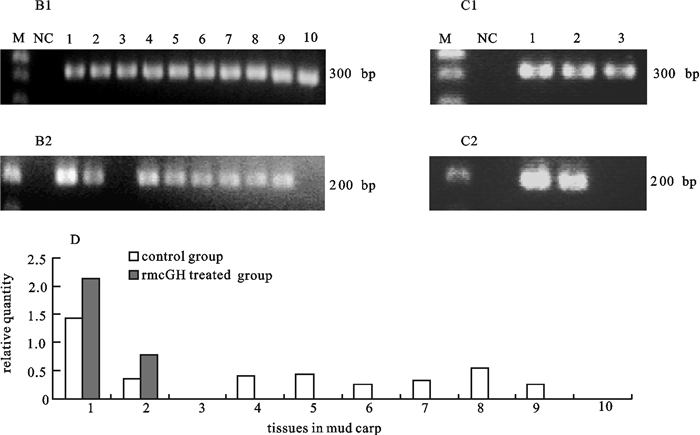
图 3 半定量RT-PCR检测重组鲮GH处理前后鲮actin和IGF-ⅠmRNA的组织表达
B1. 半定量RT-PCR检测对照组中鲮各组织中actin mRNA的表达;B2. 半定量RT-PCR检测对照组中鲮各组织中IGF-ⅠmRNA的表达;C1. 半定量RT-PCR检测处理组中鲮各组织中actin mRNA的表达;C2. 半定量RT-PCR检测处理组中鲮各组织中IGF-ⅠmRNA的表达;D. 处理前后鲮组织IGF-ⅠmRNA的相对表达;M. 100 bp DNA分子量标准;NC. 负对照;1~10. 肝、脑、肌肉、肾、肠、鳃、脾、性腺、心脏、皮肤
Figure 3. Semi-quantitative RT-PCR analysis of expression of Actin and IGF-Ⅰ mRNA in various tissues in mud carp
B1. Actin mRNA was detected in various tissues by semi-quantitative RT-PCR in control group; B2. IGF-ⅠmRNA was detected in various tissues by semi-quantitative RT-PCR in control group; C1. Actin mRNA was detected in various tissues by semi-quantitative RT-PCR in rmcGH in treated group; C2. IGF-Ⅰ mRNA was detected in various tissues by semi-quantitative RT-PCR in rmcGH in treated group; D. relative quantity of IGF-ⅠmRNA in various tissues in mud carp; M.100 bp DNA molecular weight marker; NC. a negative control (no template); 1~10. brain, liver, muscle, kidney, intestine, gill, spleen, gonad, heart, skin
表 1 扩增IGF-Ⅰ、Actin的引物序列
Table 1 Oligonucleotide primers used to amplify cDNA for mud carp IGF-Ⅰand Actin
引物 primer 序列 sequence Actin-F 5′-GTGTTGGCG/ATACAGGTCCTTACG-3′ Actin-R 5′-CAGACTACCTC/GATGAAGATCCTGAC-3′ IGF-Ⅰ-F 5′-ATGGAAAACCAGCGCCTCTTC-3′ IGF-Ⅰ-R 5′-TGCATGTCCTTCTTGAAGCAAG-3′ 表 2 对照组和重组鲮IGF-Ⅰ处理组鲮血清中GH和IGF-Ⅰ浓度
Table 2 The GH and IGF-Ⅰconcentration in sera in control and rmc IGF-Ⅰtreated fish
浓度±S.E.(n=3)/ng·mL-1 concentration±S.E. 对照组
control重组鲮IGF-Ⅰ处理组
rmcIGF-Ⅰtreated groupP值 胰岛素样生长因子-Ⅰ浓度
IGF-Ⅰconcentration145.59±21.84 247.71±2.83 P=0.043<0.05 生长激素浓度
GH concentration0.037±0.0067 0.053±0.0067 P=0.508>0.05 -
[1] LI Wensheng, LIN Haoran, WONG A O L. Effects of gonadotropin-releasing hormone on growth hormone secretion and gene expression in common carp pituitary[J]. Comp Biochem Physiol: Part B, 2002, 132(2): 335-341. doi: 10.1016/S1096-4959(02)00039-8
[2] LI Yinghua, BAI Junjie, JIAN Qing, et al. Expression of common carp growth hormone in the yeast Pichia pastoris and growth stimulation of juvenile tilapia (Oreochromis niloticus)[J]. Aquac, 2003, 216(13): 329-341. doi: 10.1016/S0044-8486(02)00406-4
[3] 江世贵, 张殿昌, 苏天凤, 等. 鲮生长激素cDNA的分子克隆和序列分析[J]. 中国水产科学, 2003, 10(2): 97-101. doi: 10.3321/j.issn:1005-8737.2003.02.003 [4] KOJI Inoue, HOZI Iwatani, YOSHIO Takei. Growth hormone and insulin-like growth factorⅠof a Euryhaline fish Cottus kazika: cDNA cloning and expression after seawater acclimation[J]. Gen Comp Endocrinol, 2003, 131(1): 77-84. doi: 10.1016/S0016-6480(02)00650-0
[5] BIGA P R, PETERSon B C, SCHELLING G T, et al. Bovine growth hormone treatment increased IGF-Ⅰin circulation and induced the production of a specific immune response in rainbow trout (Oncorhynchus mykiss)[J]. Aquac, 2005, 246(1/4): 437-445. doi: 10.1016/j.aquaculture.2005.01.019
[6] 张殿昌, 江世贵, 苏天凤, 等. 鲮胰岛素生长因子Ⅰ(IGF-Ⅰ)cDNA的分子克隆和序列分析[J]. 上海水产大学学报, 2002, 11(2): 97-101. doi: 10.3969/j.issn.1004-7271.2002.02.001 [7] 黄燕琴, 张殿昌, 苏天凤, 等. 重组鲮IGF-Ⅰ对鲮GH表达的影响[J]. 南方水产, 2006, 2(5): 19-24. doi: 10.3969/j.issn.2095-0780.2006.05.004 [8] ZHANG Dianchang, HUANG Yanqin, SHAO Yanqing, et al. Molecular cloning, recombinant expression and growth-promoting effect of mud carp (Cirrhinus molitorella) insulin-like growth factor-Ⅰ[J]. Gen Comp Endocrinol, 2006, 148(2): 203-212. doi: 10.1016/j.ygcen.2006.03.014
[9] SHINGO Kajimura, KATSUHISA Uchida, TAKASHI Yada, et al. Effects of insulin-like growth factors (IGF-Ⅰand-Ⅱ)on growth hormone and prolactin release and gene expression in euryhaline tilapia, Oreochromis mossambicus[J]. Gen Comp Endocrinol, 2002, 127(3): 223-231. doi: 10.1016/s0016-6480(02)00055-2
[10] BIGA P R, GERALD T, SCHELLINGA R, et al. The effects of recombinant bovine somatotropin (rbST)on tissue IGF-Ⅰ, IGF-Ⅰreceptor, and GH mRNA levels in rainbow trout, Oncorhynchus mykiss[J]. Gen Comp Endocrinol, 2004, 135(3): 324-333. doi: 10.1016/j.ygcen.2003.10.014
[11] VONG Q P, CHAN K M, CHENG C H K. Quantification of recombinant of mud carp IGF-Ⅰand IGF-ⅡmRNA by realtime PCR: differential regulation of expression by GH[J]. J Endocrinol, 2003, 17(8): 513-521. doi: 10.1677/joe.0.1780513
[12] KELLEY K M, DESAI P, ROTH J T, et al. Evolution of endocrine growth regulation: the insulin like growth factors (IGFs), their regulatory binding proteins (IGFBPs), and IGF receptors in fishes and other ectothermic vertebrates[M]//FINGERMAN M, THOMPSON M F, NAGABHUSHANAM R. Recent advances in marine biotechnology. New Delhi: Oxford and IBH Publishing, 2000: 189-228. https://www.semanticscholar.org/paper/Evolution-of-endocrine-growth-regulation%3A-the-like-Kelley-Desai/66de760e9df4bc320b7df3b39e8bc4c24dc1dfed
[13] MORIYAMA S, AYSon F G, KAWAUCHI H. Growth regulation by insulin-like growth factor-Ⅰin fish[J]. Biosci Biotechnol Biochem Rev, 2000, 64(11): 1 553-1 562. doi: 10.1271/bbb.64.1553
[14] PEREZ-SANCHEZ J. The involvement of growth hormone in growth regulation, energy homeostasis and immune function in the gilthead sea bream (Sparus aurata): a short review[J] Fish Physiol Biochem, 2000, 22(10): 135-144. doi: 10.1023/A:1007816015345
[15] THISSEN J P, UNDERWOOD L E, KETELSLEGERS J M. Regulation of insulin-like growth factor-Ⅰin starvation and injury[J]. Nutr Rev, 1999, 57(6): 167-176. doi: 10.1111/j.1753-4887.1999.tb06939.x
[16] HASHIMOTO H, MIKAWA S, TAKAYAMA E, et al. Molecular cloning and growth hormone-regulated gene expression of carp insulin-like growth factor-Ⅰ[J]. Biochem Mol Biol Int, 1997, 41(5): 877-886. doi: 10.1080/15216549700201921
[17] FUNKENSTEIN B, SILBERGELD A, CAVARI B, et al. Growth hormone increases plasma levels of insulin-like growth factor-Ⅰ(IGF-Ⅰ) in a teleost, the gilthead seabream (Sparus aurata)[J]. J Endocrinol, 1989, 120(7): 19-21. doi: 10.1677/joe.0.120r019
[18] MORIYAMA S. Increased plasma insulin-like growth hormone factor-Ⅰ (IGF-Ⅰ) following oral and intraperitoneal administration of growth hormone to raimbow trout, Oncorhynchus mykiss[J]. Growth Regul, 1995, 53(3): 164-167. https://pubmed.ncbi.nlm.nih.gov/7580868/
[19] CAO Q P. Nucleotide sequence and growth hormone regulated expression of salmon insulin-like growth factor Ⅰ mRNA[J]. Mol Endocrinol, 1989, 3(3): 2 006-2 010. doi: 10.1210/mend-3-12-2005
[20] SCHMID A C, REINECKE M, KLOAS W. Primary cultured hepatocytes of the bony fish, Oreochromis mossambicus, the tilapia: a valid tool for physiological studieson IGF-Ⅰexpression in liver[J]. J Endocrinol, 2000, 166(2): 265-273. doi: 10.1677/joe.0.1660265
[21] DUAN C, DUGUAY S J, PLISETSKAYA E M. Hormonal regulation of insulin-like growth factorⅠ(IGF-Ⅰ) mRNA expression in coho salmon[J]. Am Zool, 1992, 32: 13-20.
[22] TSE M C L, VONG Q P, CHENG C H K, et al. PCR cloning and gene expression studies in common carp (Cyprinus carpio) insulin-like growthfactor-Ⅱ[J]. Biochimica Biophysical Acta, 2002, 1 575(1/3): 63-74. doi: 10.1016/s0167-4781(02)00244-0
[23] PETEZ-SANCHEZ J, WEIL C, LE-BAI P Y. Effects of human insulin-like growth hormone factor-Ⅰon release of growth hormone by rainbow trout (Oncorhynchus mykiss) pituitary cells[J]. J Exp Zool, 1992, 262(3): 287-290. doi: 10.1002/jez.1402620308
[24] LEEDOM T A, UCHIDA K, YADA T, et al. Recombinant bovine growth hormone treatment of tilapia: growth response, metabolic clearance, receptor binding and immunoglobulin production[J]. Aquac, 2002, 207(3/4): 359-380. doi: 10.1016/S0044-8486(01)00767-0
[25] KAJIMURA S, UCHIDA K, YADA T, et al. Stimulation of insulin-like growth factor-Ⅰproduction by recombinant bovine growth hormone in Mozambique tilapia, Oreochromis mossambicus[J]. Fish Physiol Biochem, 2001, 25(3): 221-230. doi: 10.1023/A:1022268811599
[26] SILVERSTEIN J T, WOLTERS W R, SHIMIZU M, et al. Bovine growth hormone treatment of channel catfish: strain and temperature effectson growth, plasma IGF-Ⅰlevels, feed intake and efficiency, and body composition[J]. Aquac, 2000, 190(1): 77-88. doi: 10.1016/S0044-8486(00)00387-2



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
