Comparative study of intestinal microbial community structure in different species of carp in aquaponics system
-
摘要:
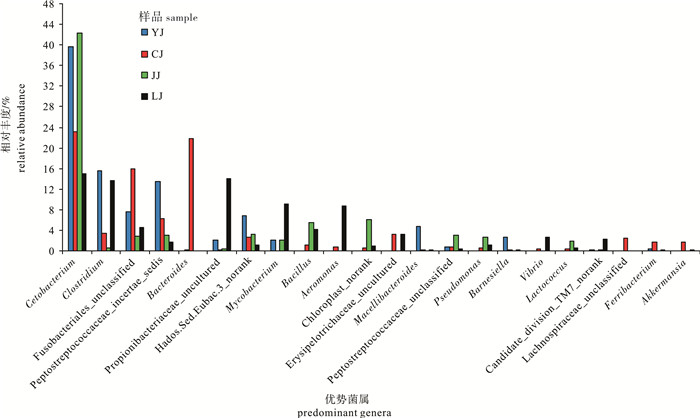
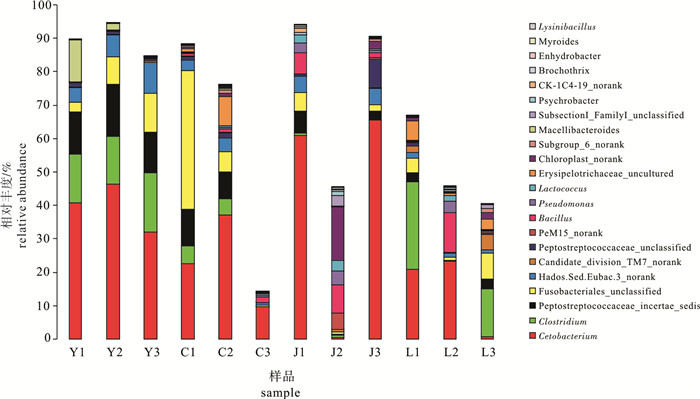
为研究鱼菜共生模式下不同鱼类肠道微生物的菌落结构,采用宏基因组学测序技术和生物信息学分析手段,构建了草鱼(Ctenopharyngodon idellus)、鲫(Carassius auratus)、鲢(Hypophthalmichthys molitrix)和鳙(Aristichthys nobilis)4种鲤科鱼类的肠道内含物等12个样品的16S rDNA测序克隆文库,分析了这4种鲤科鱼类肠道微生物的菌落组成和多样性。结果表明, 鱼菜共生模式下不同鲤科鱼类肠道内含物微生物优势菌落的组成十分相似(P>0.05,Kruskal-Wallis),优势微生物菌群均是鲸杆菌属(Cetobacterium)和梭状芽孢杆菌属(Clostridium)、拟杆菌属(Bacteroides)和芽孢杆菌属(Bacillus)等,其中鲸杆菌属和梭状芽孢杆菌属含量最丰富,且主要在非优势菌属之间具有显著差异(P<0.05,Kruskal-Wallis),研究结果还表明食性不是造成不同食性鲤科鱼类肠道微生物菌落差异的唯一决定性因素。
Abstract:To investigate the intestinal microbial community structure in different species of carp in the aquaponics system, we collected 12 intestine samples of four different species of carp(Ctenopharyngodon idellus, Carassius auratus, Hypophthalmichthys molitrix and Aristichthys nobilis)from the same pond, and investigated their composition and diversity of microbial communities based on high throughput sequencing of 16S rDNA. The dominant microbial genuses were Cetobacterium, Clostridium, Bacteroides and Bacillus; and Cetobacterium and Clostridium were the most abundant core intestinal microbiotas in the four species of carp with different feeding habits in the aquaponics system. The composition, diversity and their relative proportions of these dominant microbial genuses in different species of fish intestinal contents are very similar (P>0.05, Kruskal-Wallis), and the microbiota diversity difference exists between non-dominant microbial genuses in the different species of carp (P < 0.05, Kruskal-Wallis). Moreover, it is showed that feeding habit is not the only key factor that affects the intestinal microbiota of carp with different feeding habits.
-
Keywords:
- aquaponics system /
- carp /
- intestinal microbial community structure /
- feeding habits /
- 16S rDNA
-
任何形式的捕捞均有选择性, 其选择性主要取决于渔具选择性,它强烈影响着捕捞群体结构。为了实现渔业资源的可持续利用,开展生态渔业、负责任渔业的研究有重要的意义,渔具选择性和选择性渔具是生态渔业的核心内容之一。而在我国开展的渔具选择性研究尤其是定置渔具选择性能的研究并不多见。
日本沿海主要以小型底拖网、笼、筒捕捞星康吉鳗Conger myriaster(以下简称星鳗)。在我国星鳗也是重要的群众渔业捕捞对象,青岛近海渔民用筒、山东日照渔民利用延绳钓捕捞这种鱼。山东沿海渔民在利用地笼诱捕许氏平鲉、欧氏六线鱼时, 往往同时捕获大量星鳗。本文以东京湾星鳗笼为例,利用套网法研究了其网目选择性,以期为定置渔业的科学管理提供科学依据。
1. 材料和方法
1.1 海上实验
1995~2000年,每年的10~11月在东京湾进行实验。实验笼和生产的相同,不锈钢骨架,展开为640 mm×470 mm×150 mm。每个笼有2个椭圆形开口200 mm×90 mm, 和东京湾渔获对象星鳗(全长190~600 mm, 最大体周长28~104 mm)相比, 开口非常大。因此在研究笼的选择性时, 可以仅考虑网目的选择性。
笼的底部网目尺寸(内径)为10.8 mm,远小于其他部位的网目尺寸(表 1), 星鳗从笼中逃逸的部位是底部以外的其他部分。实验时,笼的底部以外结覆网目内径为10.8 mm的套网, 套网和笼之间有足够大的空间, 且所有套网的规格相同。套网、笼均为锦纶制造,有结节菱形网片。实验时的作业方法和生产相同, 采用延绳钓作业方式。
表 1 实验笼的数量以及网目尺寸(MC)Table 1. The number and mesh size of test net pot(MC)网目尺寸/mm mesh size 1995年 1996年 1997年 1998年 1999年 2000年 21.0±0.68 4 4 4 4 4 4 18.1±0.82 3 3 4 4 4 4 15.5±0.63 3 3 4 4 4 4 13.6±0.44 3 3 4 4 4 4 11.6±0.38 3 3 4 4 4 4 将笼网、套网捕获的星鳗分别装入化纤袋,回实验室测量全长、最大体周长,体重。最大体周长是胸鳍稍后鱼体最粗部位的周长。
1.2 解析方法
如果1尾鱼被捕获的概率是p, 那么Ni尾行为独立有相同特征的鱼遭遇笼,ni尾鱼被捕获的概率$p=C_{N_i}^{n_i} p^{n_i}(1-\$p)^{N_i-n_i}$。
假设1群鱼遭遇渔具, 该鱼群依据全长可以划分为k组,组中值为li,每组鱼Ni,每组被捕的数量mi,那么$\sum_\limits{i=1}^k$尾鱼被捕获的概率$F=\prod_\limits{i=i}^k C_{N_i}^{n_i} p^{n_i}(1-p)^{N_i-n_i}$。
如果套网和笼捕获的鱼的数量为nli, mli(i=1,2,3,…,k), 那么笼捕获的全长li鱼的占该类鱼总渔获量的比例为
$$ \phi_{l_i}=\frac{n_{l_i}}{n_{l_i}+m_{l_i}} $$ (1) 依据概率的统计学定义, F可用$\phi_{l_i}$估计, 而p是渔具的选择率SL[1], 可用Logistic方程表示[2],
$$ S_L=\frac{\exp (s+b L)}{1+\exp (s+b L)} $$ (2) a,b为待估参数,L为鱼类的特征变量(全长l,相对体周长$\frac{G}{M_e}$等)。由F和$\phi_{l_i}$, p和SL的关系, 利用极大似然估计法可以得到待估参数a,b的值。
由不同网目尺寸得到的不同的网目选择性曲线, 利用不同的处理方式可以得到不同的主选择性曲线。为比较这些曲线, 引入AIC(akayike information criterion),AIC=-2 max {ln F}+2K作为判断标准,为待估参数的数目,AIC较小的模型更合适[3]。
2. 结果与讨论
2.1 星鳗的体重、全长,最大体周长间的关系
捕获的星鳗的全长l(cm)与体重w(g)、体周长G(cm)的关系分别为,
w=0.1998l2-7.9106l+93.5290(R2=0.9610, n=2 102),
G=0.1906l-0.6786(R2=0.8488, n=2 102)。
2.2 全长选择性曲线
笼的选择性由2部分组成,网目选择性、出入口的选择性。在东京湾可仅考虑网目的选择性[4]。以全长为方程2的变量,由算式1, 2得到的网目选择性曲线的各个参数(表 2)。
表 2 全长选择性曲线的各参数Table 2. Parameters of whole body length selectivity curve网目尺寸/mm mesh size a b MLL AIC l0.5 S.R. 21.0 -17.26 0.58 -22.01 48.02 29.80 3.80 18.1 -13.83 0.52 -37.65 79.30 26.80 4.30 15.5 -14.44 0.63 -56.77 117.54 23.00 3.50 13.6 -16.11 0.73 -53.71 111.42 22.00 3.00 11.6 -14.65 0.73 -173.71 351.41 20.00 3.00 注: l0.5, 50%选择全长; S.R., 选择域; MLL=Max{lnF}
Notes:l0.5, 50% selective whole body length; S.R., selective range; MLL=Max{lnF}由上述的各参数可知,网目尺寸21.0、18.1、15.5、13.6、11.6 mm笼的全长选择性能,全长0 < l < 25.50 cm、0 < l < 22.50 cm、0 < l < 18.50 cm、0 < l < 18.50 cm、0 < l < 16.50 cm时,全长选择率几乎为0;全长25.50 < l < 35.50 cm、22.50 < l < 32.50 cm、18.50 < l < 27.50 cm、18.50 < l < 26.50 cm、16.50 < l < 24.00 cm时,全长选择率随全长不断增长而逐渐增大;全长在l>35.50 cm、l>32.50 cm、l>27.50 cm、l>26.50 cm、l>24.00 cm时,全长选择率几乎接近于1.00,50%选择全长l0.5分别为29.8、26.8、23.0、22.0、20.0 cm;全长选择域为3.80、4.30、3.50、3.00、3.00 cm。因此,全长选择性曲线沿全长增加方向,随网目增大而向右移,并且网目越小,选择越尖锐。
笼的网目尺寸分别为21.0、18.1、15.5、13.6、11.6 mm,和套网的网目尺寸的比值依次为1.07、1.26、1.44、1.68、1.94。所对应的AIC逐渐减少(表 2)。由于实验中,除笼的网目尺寸有差别外,其他条件尽可能相同,因此造成这种趋势的原因很可能来自套网对实验笼的影响(例如局部流场的改变程度),即可能是在一定范围内,实验网和套网的网目尺寸差别越大,套网对实验网的影响越小;而当两者相当时,套网的影响相当显著。是否是这种原因,有待于更多关于鱼类行为以及渔具和捕捞对象相互作用的实验检验。
2.3 主选择性曲线
鱼能否穿过网目,主要取决于鱼沿体高方向的截面形状以及相对于网目内径的大小[4]。由或为方程1的变量,所得到的方程为主选择性方程,它描绘的曲线为主选择性曲线(master selectivity curve)。有2种方法,each curve model和single curve model可得到主选择性曲线。前者是求得每一网目尺寸所对的主选择性曲线。后者将所有的网目尺寸所对应的相对体周长$\frac{G}{M_c}$或相对全长$\frac{l}{M_c}$值合并,看作一组数值,求得一条反映渔具选择性的曲线。
以$\frac{G}{M_c}$为方程2的变量,由single curve model和each curve model,利用极大似然估计法,得到待估参数(表 3)。因∑ (AICeach curve model)=250.18,而AICsingle curve model=244.32,其差值│244.32-250.18│>1,所以可以认为single curve model与each curve model之间的差异并非偶然,single curve model得到的主选择性曲线可更好地反映网目选择性。
表 3 主选择性曲线的各参数Table 3. Parameters of master selectivity curve模式models a b $\frac{G}{M_{e0.5}}$ S.R. MLL AIC single curve model -4.71 4.25 1.11 0.52 -120.16 244.32 each curve model- 115.09 250.18 21.0 mm -10.47 8.68 1.21 0.25 -16.96 37.92 18.1 mm -8.92 7.70 1.16 2.87 -24.45 52.90 15.5 mm -1.58 2.87 0.55 0.77 -24.54 53.07 13.6 mm -4.87 4.62 1.06 0.48 -16.95 37.91 11.6 mm -0.01×10-2 1.08 9.20×10-5 2.03 -32.19 68.38 50%选择相对体周长1.11,相对体周长的选择域为0.52。$0<\frac{G}{M_c}<0.55$,相对体周长选择率几乎为0;$0.55< \frac{G}{M_c}<1.60$,选择率随相对体周长增加而增加;$\frac{G}{M_c}>1.60$,选择率趋向于1.00。一般认为当$\frac{G}{M_c}=1$时,选择率就应当趋向于1.0,而本实验当$\frac{G}{M_c}>1.60$,选择率才趋向1.00。这种结果和星鳗底拖网的网目选择性中的类似[5]。其最可能的原因是星鳗体表鳞片退化,凸起减少,且分泌大量粘液,使之容易穿过网目。另外,网线对星鳗的刺激,也有促进星鳗积极逃逸的可能。
3. 小结
比较显示,套网和实验网的网目尺寸差别较大时,套网的影响较小。而在两者接近时,套网的影响极为显著。
此外,本文中给出了利用套网法得到的星鳗笼的网目选择性能, 但套网对入笼的星鳗行为存在影响, 这种影响到底有多大, 以及入网的星鳗如何从笼中逃逸, 逃逸后的残存率有多大, 都是将来要研究的重点所在。
-
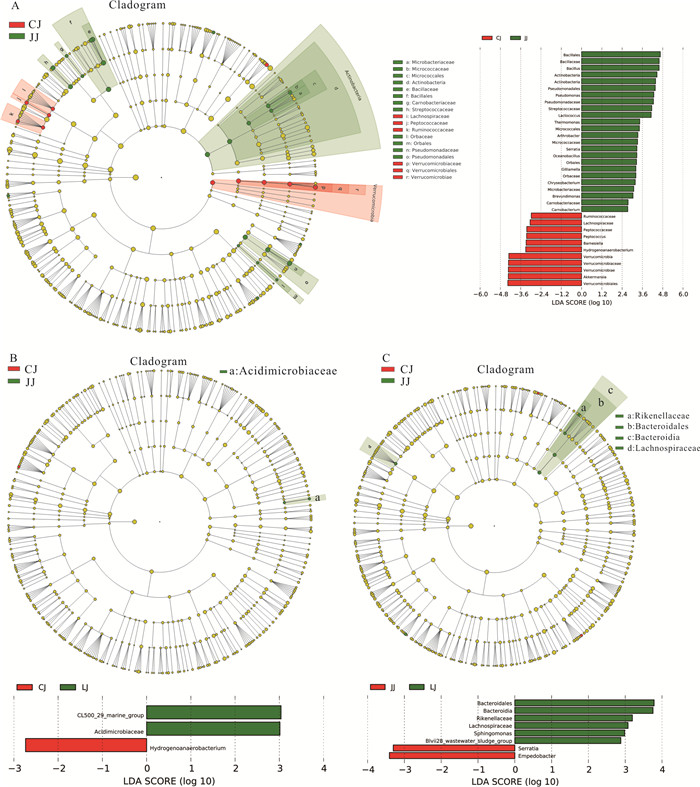
图 4 不同鱼类肠道内含物菌落的LEfSE分析图
分支图中的红色和绿色节点分别表示在红色组别和绿色组别中起到重要作用的微生物类群。节点亮度和大小成比例。只显示LDA值大于2.5的微生物类群。
Figure 4. LEfSE identifing the most differentially abundant taxons between fish
Red and green in the taxonomic cladogram taxa are enriched in the two group, respectively. The brightness of each dot is proportional to its effect size. Only taxa meeting an LDA significant threshold >2.5 are shown.
表 1 样品的多样性指数
Table 1 Alpha-diversity of samples
样品编号
sample可操作分类单元
out香浓指数
Shannon辛普森指数
Simpson覆盖率
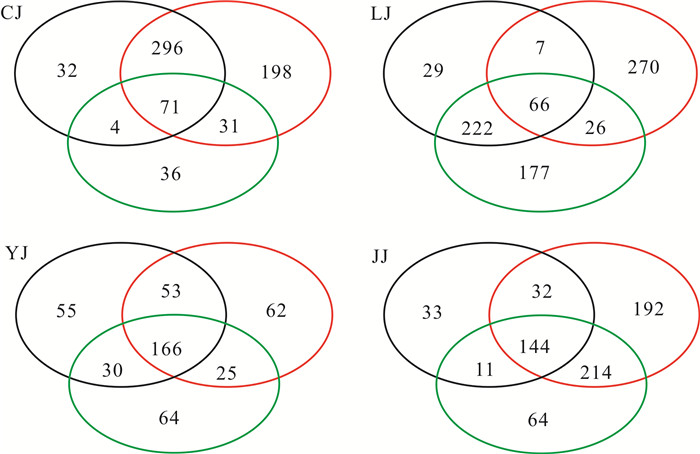
coverageYJ 298 2.21 0.207 0.998 5 CJ 380 2.39 0.275 0.998 7 JJ 412 2.74 0.283 0.998 3 LJ 395 3.09 0.114 0.998 9 注:YJ、CJ、JJ和LJ分别代表Y1~Y3、C1~C3、J1~J3和L1~L3;后表、后图同此。
Note:YJ.Y1~Y3;CJ.C1~C3;JJ.J1~J3;LJ.L1~L3;the same case in the following tables and figures.表 2 各样品优势细菌门类及相对丰度
Table 2 Advantage bacterial phyla and relative abundance of each sample
% YJ CJ JJ LJ 梭杆菌门Fusobacteria 54.15 41.95 48.56 20.79 厚壁菌门Firmicutes 30.91 20.70 17.06 25.51 变形菌门Proteobacteria 1.77 5.90 13.58 17.20 放线菌门Actinobacteria 4.48 0.69 6.00 25.03 拟杆菌门Bacteroidetes 7.64 24.27 0.44 1.59 合计total 98.94 93.52 85.64 90.12 -
[1] 李志斐, 王广军, 陈鹏飞, 等. 生物浮床技术在水产养殖中的应用概况[J]. 广东农业科学, 2013, 40(3): 106-108, 114. https://cstj.cqvip.com/Qikan/Article/Detail?id=45244691&from=Qikan_Article_Detail [2] 吴伟, 胡庚东, 金兰仙, 等. 浮床植物系统对池塘水体微生物的动态影响[J]. 中国环境科学, 2008, 28(9): 791-795. doi: 10.3321/j.issn:1000-6923.2008.09.005 [3] 唐莹莹, 李秀珍, 周元清, 等. 浮床空心菜对氮循环细菌数量与分布和氮素净化效果的影响[J]. 生态学报, 2012, 32(9): 2837-2846. https://www.ecologica.cn/stxb/article/abstract/stxb201103240370 [4] 沈南南, 李纯厚, 贾晓平, 等. 小球藻与芽孢杆菌对对虾养殖水质调控作用的研究[J]. 海洋水产研究, 2008, 29(2): 48-52. https://wenku.baidu.com/view/5c8ba9065f0e7cd1842536a9?fr=xueshu_top [5] 付保荣, 曹向宇, 冷阳, 等. 光合细菌对水产养殖水质和水生生物的影响[J]. 生态科学, 2008, 27(2): 102-106. https://qikan.cqvip.com/Qikan/Article/Detail?id=1000003885566 [6] KIM D H, BRUNT J, AUSTIN B. Microbial diversity of intestinal contents and mucus in rainbow trout (Oncorhynchus mykiss)[J]. J Appl Microbiol, 2007, 102(6): 1654-1664. doi: 10.1111/j.1365-2672.2006.03185.x
[7] 陈孝煊, 吴志新, 周文豪. 鱼类消化道菌群的作用与影响因素研究进展[J]. 养殖与饲料, 2006, 24(3): 37-40. http://hnxbl.cnjournals.net/hznydxzr/article/abstract/200505127 [8] 胡雄. 鱼-菜混养模式的构建与初步应用研究[D]. 武汉: 华中农业大学, 2011: 1-66.https://d.wanfangdata.com.cn/thesis/Y2004182 [9] 黄海平. 水蕹菜浮床在精养鱼池中的应用效果研究[D]. 武汉: 华中农业大学, 2012: 1-88.https://d.wanfangdata.com.cn/thesis/ChJUaGVzaXNOZXdTMjAyNDAxMDkSCFkyMTYyMTIzGgh6bW12djlwOQ%253D%253D [10] RINGØ E, OLSEN R E, MAYHEW T M, et al. Electron microscopy of the intestinal microflora of fish[J]. Aquaculture, 2003, 227(1/2/3/4): 395-415. https://www.sciencedirect.com/science/article/abs/pii/S0044848603005179
[11] GANGULY S, PRASAD A. Microflora in fish digestive tract plays significant role in digestion and metabolism[J]. Rev Fish Biol Fish, 2012, 22(1): 11-16. doi: 10.1007/s11160-011-9214-x
[12] WU S, WANG G, ANGERT E R, et al. Composition, diversity, and origin of the bacterial community in grass carp intestine[J]. PLoS ONE, 2012, 7(2): e30440. https://pubmed.ncbi.nlm.nih.gov/22363439/
[13] MORAN D, TURNER S J, CLEMENTS K D. Ontogenetic development of the gastrointestinal microbiota in the marine herbivorous fish Kyphosus sydneyanus[J]. Microb Ecol, 2005, 49(4): 590-597. https://pubmed.ncbi.nlm.nih.gov/16041474/
[14] MOORE A M, MUNCK C, SOMMER M O, et al. Functional metagenomic investigations of the human intestinal microbiota[J]. Front Microbiol, 2011, 2(1): 188. https://pubmed.ncbi.nlm.nih.gov/22022321/
[15] FLINT H J, BAYER E A, RINCON M T, et al. Polysaccharide utilization by gut bacteria: potential for new insights from genomic analysis[J]. Nat Rev Microbiol, 2008, 6(2): 121-131. doi: 10.1038/nrmicro1817
[16] DIMITROGLOU A, MERRIFIELD D L, CARNEVALI O, et al. Microbial manipulations to improve fish health and production: a Mediterranean perspective[J]. Fish Shellfish Immunol, 2011, 30(1): 1-16. doi: 10.1016/j.fsi.2010.08.009
[17] KASIWADA K, TEJIMA S, KANAZAWA A. Studies on the production of B vitamins by intestinal bacteria of fish. V. Evidence of the production of B12 by microorganisms in the intestinal canal of carp, Cyprinus carpio[J]. Bull Jap Soc Fish, 1970, 36(4): 421-424. doi: 10.2331/suisan.36.421
[18] SMITH T B, WAHL D H, MACKIE R I. Volatile fatty acids and anaerobic fermentation in temperate piscivorous and omnivorous freshwater fish[J]. J Fish Biol, 2005, 48(5): 829-841. doi: 10.1111/j.1095-8649.1996.tb01479.x
[19] RAWLS J F, MAHOWALD M A, GOODMAN A L, et al. In vivo imaging and genetic analysis link bacterial motility and symbiosis in the zebrafish gut[J]. Proc Natl Acad Sci USA, 2007, 104(18): 7622-7627. doi: 10.1073/pnas.0702386104
[20] FISH G R. Digestion in Tilapia esculenta[J]. Nature, 1951, 167(4257): 900-901. doi: 10.1038/167900a0
[21] YOKOE Y, YASUMASU I. The distribution of cellulase in invertebrates[J]. Comp Biochem Physiol, 1964, 13(4): 323-338. https://www.sciencedirect.com/science/article/abs/pii/0010406X64900271
[22] 冯雪, 吴志新, 祝东梅, 等. 草鱼和银鲫肠道产消化酶细菌的研究[J]. 淡水渔业, 2008, 38(3): 51-57. https://wenku.baidu.com/view/35cb5c1ff12d2af90242e642?fr=xueshu_top [23] TSUCHIYA C, SAKATA T, SUGITA H. Novel ecological niche of Cetobacterium somerae, an anaerobic bacterium in the intestinal tracts of freshwater fish[J]. Lett Appl Microbiol, 2008, 46(1): 43-48. doi: 10.1111/j.1472-765X.2007.02258.x
[24] PANIGRAHI A, KIRON V, KOBAYASHI T, et al. Immune responses in rainbow trout Oncorhynchus mykiss induced by a potential probiotic bacteria Lactobacillus rhamnosus JCM 1136[J]. Vet Immunol Immunopathol, 2004, 102(4): 379-388. doi: 10.1016/j.vetimm.2004.08.006
[25] PANIGRAHI A, KIRON V, PUANGKAEW J, et al. The viability of probiotic bacteria as a factor influencing the immune response in rainbow trout Oncorhynchus mykiss[J]. Aquaculture, 2005, 243(1/2/3/4): 241-254. https://www.sciencedirect.com/science/article/abs/pii/S0044848604005630
[26] HUGO C J, BRUUN B, JOOSTE P J. The genera Empedobacter and Myroides[M]//DWORKIN M, FALKOW S, ROSENBERG E, et al. The prokaryotes. 3rd ed. New York: Springer, 2005: 630-637.ttps://link.springer.com/referenceworkentry/10.1007/0-387-30747-8_24
[27] MOTWANI B, KREZOLEK D, SYMEONIDES S, et al. Myroides odoratum cellulitis and bacteremia: a case report[J]. Infect Dis Clin Prac, 2004, 12(6): 343-344. doi: 10.1097/01.idc.0000144904.51074.79
[28] LI T, LONG M, GATESOUPE F J, et al. Comparative analysis of the intestinal bacterial communities in different species of carp by pyrosequencing[J]. Microb Ecol, 2015, 69(1): 25-36. doi: 10.1007/s00248-014-0480-8
[29] LI J, NI J, LI J, et al. Comparative study on gastrointestinal microbiota of eight fish species with different feeding habits[J]. J Appl Microbiol, 2014, 117(6): 1750-1760. https://pubmed.ncbi.nlm.nih.gov/25294734/
[30] NAYAK S K. Role of gastrointestinal microbiota in fish[J]. Aquac Res, 2010, 41(11): 1553-1573. doi: 10.1111/j.1365-2109.2010.02546.x
[31] SULLAM K E, ESSINGER S D, LOZUPONE C A, et al. Environmental and ecological factors that shape the gut bacterial communities of fish: a meta-analysis[J]. Mol Ecol, 2012, 21(13): 3363-3378. doi: 10.1111/j.1365-294X.2012.05552.x
[32] WARD N L, STEVEN B, PENN K, et al. Characterization of the intestinal microbiota of two Antarctic notothenioid fish species[J]. Extremophiles, 2009, 13(4): 679-685. doi: 10.1007/s00792-009-0252-4
[33] INGERSLEV H C, von GERSDORFF JØRGENSEN L, LENZ STRUBE M, et al. The development of the gut microbiota in rainbow trout (Oncorhynchus mykiss) is affected by first feeding and diet type[J]. Aquaculture, 2014, 424/425 (2): 24-34.
[34] NI J, YAN Q, YU Y, et al. Factors influencing the grass carp gut microbiome and its effect on metabolism[J]. FEMS Microbiol Ecol, 2014, 87(3): 704-714. doi: 10.1111/1574-6941.12256
[35] VERNER-JEFFREYS D W, SHIELDS R J, BRICKNELL I R, et al. Changes in the gut-associated microflora during the development of Atlantic halibut (Hippoglossus hippoglossus L.) larvae in three British hatcheries[J]. Aquaculture, 2003, 219(1/2/3/4): 21-42. doi: 10.1016/S0044-8486(02)00348-4
-
期刊类型引用(1)
1. 张静,胡长圣,刘前,戴佳玥,王学锋,汤保贵. 流速对卵形鲳鲹游泳行为及运动生理的影响. 中国水产科学. 2024(04): 381-390 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
