Specificity of algicidal activity against four species of microalgae by algicidal bacterium A2
-
摘要:
将溶藻菌菌株A2以初始浓度107 CFU · mL-1接入到锥状斯氏藻(Scrippsiella trochoidea)、条纹小环藻(Cyclotella striata)、蛋白核小球藻(Chlorella pyrenoidosa)和四尾栅藻(Scenedesmus quadricauda)的纯培养与混合培养藻液中,研究A2对不同微藻的溶藻专一性,并通过16S rDNA序列分析对A2菌株进行菌株鉴定。结果表明,经16S rDNA鉴定,菌株A2属于海杆菌属(Marinobacter sp.);在微藻纯培养与混合培养环境下,A2皆可有效溶解甲藻类的锥状斯氏藻,对硅藻类的条纹小环藻具有一定的溶解效果,对绿藻类的四尾栅藻生长无影响,可以促进绿藻类蛋白核小球藻的生长。在多种微藻共存环境下,A2菌组锥状斯氏藻死亡率可高达98.29%和95.37%,蛋白核小球藻的浓度较对照组提高237.6%。结果表明,菌株A2具有良好的溶藻专一性,可作为研发养殖池塘甲藻调控剂的备选菌株。
Abstract:To investigate the specificity of algicidal activity against Scrippsiella trochoidea, Cyclotella striata, Chlorella pyrenoidosa and Scenedesmus quadricauda by bacterial Strain A2, we added Strain A2 to monoculture and mix-culture systems of these four microalage at concentration of 107CFU · mL-1, and analyzed the algicidal effects. The results show that the Strain A2 was identified as Marinobacter sp. by homology comparisons based on 16S rDNA sequences. Strain A2 produced high lytic effect to S. trochoidea under monoculture and mix-culture systems, and had some algicidal effect to C. striata. The growth of S. quadricauda was not affected by Strain A2. However, Strain A2 could promote the growth of C. pyrenoidosa. Besides, 98.29% and 95.37% of S. trochoidea were killed under the mix-culture systems of four microalage. The cell density of C. pyrenoidosa increased by 237.6%, compared with the control under the mix-culture of S. trochoidea, C. striata and C. pyrenoidosa. It is indicated that Strain A2 has good specificity of algicidal activity to S. trochoidea, and can be potentially used to develop probiotics against dinoflagellate blooms in aquaculture ponds.
-
Keywords:
- Scrippsiella trochoidea /
- algicidal bacteria /
- specificity
-
池塘水体中微藻的种类、数量与养殖生物的生长状况密切相关,一般以绿藻、硅藻为优势种的水体,养殖病害少有发生[1-2]。池塘水体中锥状斯氏藻(Scrippsiella trochoidea)等有害甲藻,不仅抑制绿藻和硅藻的生长,而且对养殖生物产生直接危害[3-4]。因此,在养殖生产中有效控制有害甲藻,避免其成为优势种,是水质调控的主要内容之一。关于养殖池塘中甲藻的调控,以往多采用物理、化学、生物化感作用以及生物竞争等方法,然而利用改性粘土等物理方法可能对底栖生物造成负面影响,采用硫酸铜等化学药剂易对环境产生二次污染,生物化感作用以及生物竞争等方法控藻成效较为缓慢[5-9]。溶藻菌控藻作为一种控制有害藻类的新型生物方法,具有高效快速、无次生污染、成本低等优点,日益受到广泛关注[10-11]。
目前国内外利用溶藻菌调控甲藻的报道较多,但较多针对单一种类甲藻,缺乏针对多种微藻的溶藻专一性的报道 [11-15]。WANG等[11]从蛋白水平分析了弧菌DHQ25和假交替单胞菌DHY3对塔玛亚历山大藻(Alexandrium tamarense)的溶藻效应;李东等[13]从用菌浓度、溶藻方式等方面分析了微泡菌BS03对塔玛亚历山大藻的溶藻效果;史荣君等[14]和张俊[16]则从赤潮藻环境中分离了溶藻菌株,于微藻纯培养条件下逐一分析菌株对原甲藻(Prorocentrum sp.)、锥状斯氏藻等微藻的溶解效应。然而自然水体中的微藻以群落形式存在[17],将溶藻菌应用于养殖水体中,溶藻菌在有效调控有害甲藻的同时是否对其中的有益绿藻、硅藻产生溶藻效果,这需要引起关注。因此,有必要研发以微生物干预为核心的微藻群落定向优化技术,使用对特定微藻有选择性抑制效应的菌株,在去除目标微藻的同时不影响水体中其他有益微藻的生长,促使水环境中的微藻群落维持其原有的生态功能。
文章通过将A2分别置于锥状斯氏藻、条纹小环藻(Cyclotella striata)、蛋白核小球藻(Chlorella pyrenoidosa)、四尾栅藻(Scenedesmus quadricauda)的纯培养与混合培养体系中,分析A2对不同微藻的影响,以期获得既可专一性溶解锥状斯氏藻等有害甲藻又不危害绿藻、硅藻等有益微藻的菌株,为今后研发养殖池塘甲藻控制菌剂提供备选菌种资源,也为养殖水体微藻藻相调控提供理论依据。
1. 材料与方法
1.1 实验材料
菌株A2从中肋骨条藻(Skeletonema costatum)的藻际环境中筛选获得[16]。实验藻种锥状斯氏藻、蛋白核小球藻、条纹小环藻、四尾栅藻由中国水产科学研究院南海水产研究所提供。取处于对数生长期的4种藻的藻液,按500 U · mL-1的浓度加入青霉素、庆大霉素、链霉素、卡那霉素混合抗生素,处理4~8 h制备无菌藻液[16]。藻液经1 800 g ·min-1离心5 min,弃上清,沉淀以无菌f/2培养液反复洗涤3次,再以培养液重悬,最后进行无菌培养。
1.2 实验方法
1.2.1 A2菌株鉴定
以细菌基因组提取试剂盒(TIANamp Bacteria DNA Kit)提取菌株A2的DNA,选取8F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1492R(5′-GGTTACCTTGTTACGACTT-3′) [16]引物对16S rDNA片段进行PCR扩增。产物送上海英潍捷基有限公司测序,测序结果提交GenBank数据库,利用BLAST程序将A2序列在GenBank数据库中进行同源性检索。选取与A2的16S rDNA序列相似性较接近的菌株,用MEGA 5.1软件以Neighbor Joining法构建系统发育树[14]。
1.2.2 A2生长曲线及溶藻专一性实验
以活菌计数方法测定生长曲线[18]。将A2以约105 CFU ·mL-1的浓度接种至2216E液体培养基,于28 ℃、250 r · min-1振荡培养。每6 h取样涂布测定细菌浓度,持续5 d。以菌浓度的对数为纵坐标,时间为横坐标,绘制生长曲线。
依照表 1设置4种微藻纯培养、两两混合培养及3种藻混合培养的实验系统。将A2菌液以初始浓度107 CFU · mL-1分别加入各组藻液中,对照组以等体积的f/2培养基代替A2菌液,各组均设3个平行。将各实验组置于23 ℃、光照强度2 000 lx、光暗周期12 h:12 h下培养。每48 h取样一次,藻样用5%甲醛固定[19],显微镜下观察藻细胞形态并检测细胞数量[14],实验周期10 d。
表 1 菌株溶藻专一性的实验设计Table 1 Experimental design for effects of algicidal bacteria on microalgae实验分组
group微藻接种量/个·mL-1 inoculum amount of mircoalgae 锥状斯氏藻
S. trochoidea条纹小环藻
C. striata蛋白核小球藻
C. pyrenoidosa四尾栅藻
S. quadricauda锥状斯氏藻S. trochoidea 1.44×104 条纹小环藻C. striata 4.68×105 蛋白核小球藻C. pyrenoidosa 3.28×106 四尾栅藻S. quadricauda 1.60×105 锥状斯氏藻-条纹小环藻S. trochoidea-C.striata 2.43×104 5.47×104 锥状斯氏藻-蛋白核小球藻S. trochoidea-C.pyrenoidosa 2.06×104 1.20×104 锥状斯氏藻-条纹小环藻-蛋白核小球藻S. trochoidea-C.striata-C.pyrenoidosa 4.82×104 6.87×104 1.20×104 锥状斯氏藻-条纹小环藻-四尾栅藻S. trochoidea-C.striata-S.quadricauda 3.18×104 4.33×104 1.40×104 1.2.3 数据处理
藻细胞死亡率(%) =(1-Nt/N0)×100(Nt为培养时间为t时的藻细胞密度,N0为初始藻细胞密度)。用SPSS 19.0进行数据分析,以单因子方差分析法(P<0.05)分析实验组间及其与对照组的差异性。
2. 结果与分析
2.1 菌株鉴定
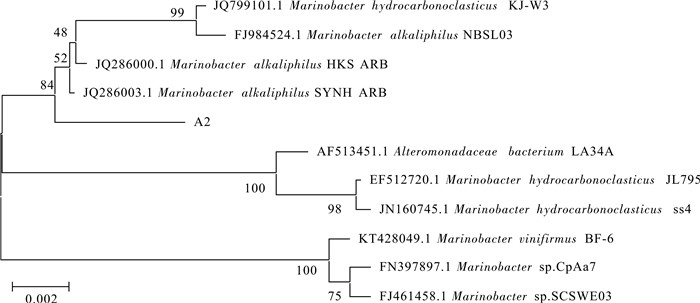
扩增菌株A2的16S rDNA序列,获得1 377 bp的DNA序列片段。于GenBank数据库进行同源性检索,以A2的16S rDNA序列及GenBank同源性搜索出的16S rDNA序列构建系统进化树(图 1)。结果显示A2菌株与海杆菌属(Marinobacter sp.)各菌株聚为一支,亲缘关系最近,序列相似度达到99%,推测该溶藻细菌A2属于海杆菌属。
2.2 A2生长曲线及对单一藻种的影响
2.2.1 A2生长曲线及对单一藻种生长的影响
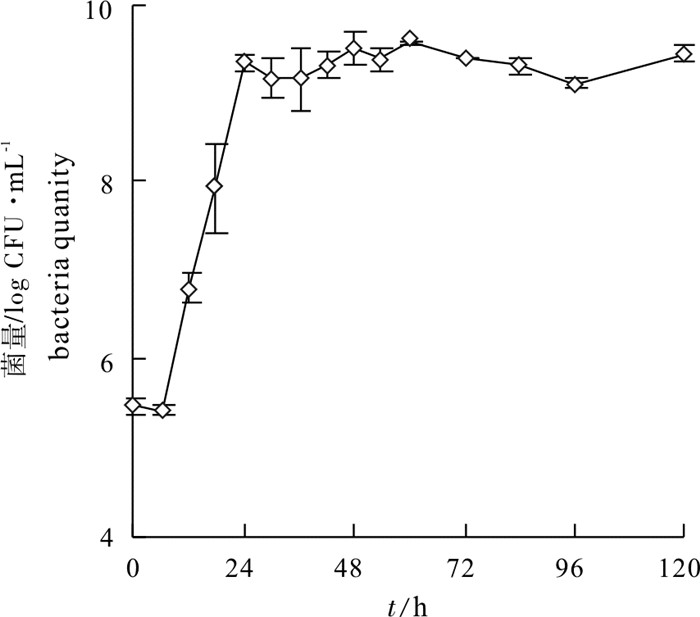
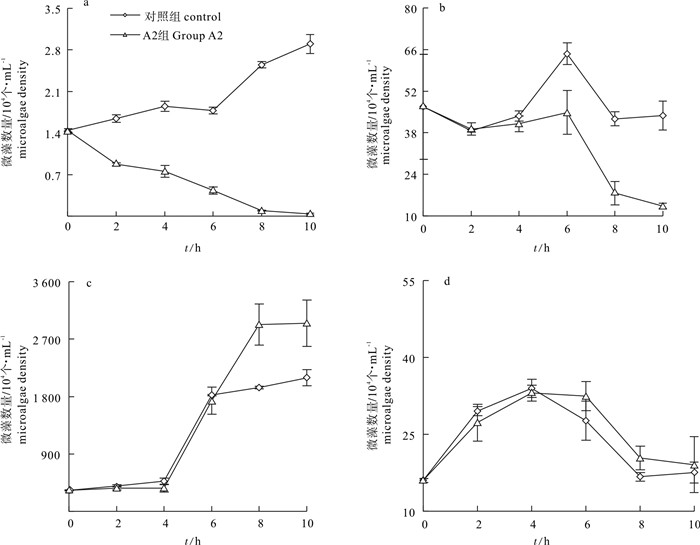
A2菌株生长延滞期为0~6 h,6 h后进入指数生长期,24 h后进入稳定期(图 2)。在微藻纯培养条件下,实验组锥状斯氏藻细胞数量持续下降,对照组则持续升高。培养第10天实验组锥状斯氏藻细胞死亡率为97.51%(图 3-a)。对照组条纹小环藻数量呈现先上升后下降的趋势,其在第10天的死亡率为6.34%;而实验组条纹小环藻数量在实验前6 d较为平稳,6 d后呈明显的下降趋势,第10天实验组条纹小环藻死亡率升为71.49%。第6天开始对照组条纹小环藻数量显著高于实验组(P<0.05) (图 3-b)。从第8天开始实验组蛋白核小球藻数量显著高于对照组(P<0.05)(图 3-c),而实验组四尾栅藻数量与对照组无显著差异(P>0.05)(图 3-d)。结果表明,在微藻纯培养条件下,菌株A2能够显著溶解锥状斯氏藻,对条纹小环藻具有一定的溶藻效果,可以促进蛋白核小球藻的生长,而对四尾栅藻生长无影响。
2.2.2 菌株A2对微藻细胞形态的影响
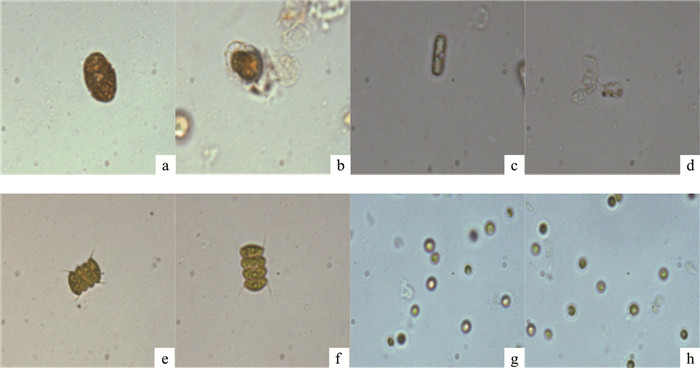
实验组锥状斯氏藻细胞于第1天失去运动活性,细胞变形,细胞壁破裂溶解(图 4-b);实验组条纹小环藻在第8天细胞溶解(图 4-d),四尾栅藻和蛋白核小球藻在第10天细胞形态仍保持完整,菌株A2对其无溶藻效果(图 4-e、f、g、h)。
![]() 图 4 菌株A2作用下不同微藻的细胞形态变化a. 实验起始时锥状斯氏藻细胞(×200);b. 第1天时实验组锥状斯氏藻藻细胞(×200);c. 实验起始时条纹小环藻细胞(×400);d. 第8天时实验组条纹小环藻细胞(×400);e. 实验起始时四尾栅藻细胞(×200);f. 第10天时实验组四尾栅藻细胞(×200);g. 实验起始时蛋白核小球藻细胞(×400);h. 第10天时实验组蛋白核小球藻细胞(×400)Fig. 4 Morphology variation of microalgal cell under effects of A2a. S. trochoidea at initial phase(×200); b. S. trochoidea of Group A2 on the first day(×200); c. C. striata of Group A2 at initial phase(×400); d. C. striata of Group A2 on 8th day(×400); e. S. quadricauda of Group A2 at initial phase(×200); f. S. quadricauda of Group A2 on 10th day(×200); g. C. pyrenoidosa of Group A2 at initial phase(×400); h. C. pyrenoidosa of Group A2 on 10th day(×400)
图 4 菌株A2作用下不同微藻的细胞形态变化a. 实验起始时锥状斯氏藻细胞(×200);b. 第1天时实验组锥状斯氏藻藻细胞(×200);c. 实验起始时条纹小环藻细胞(×400);d. 第8天时实验组条纹小环藻细胞(×400);e. 实验起始时四尾栅藻细胞(×200);f. 第10天时实验组四尾栅藻细胞(×200);g. 实验起始时蛋白核小球藻细胞(×400);h. 第10天时实验组蛋白核小球藻细胞(×400)Fig. 4 Morphology variation of microalgal cell under effects of A2a. S. trochoidea at initial phase(×200); b. S. trochoidea of Group A2 on the first day(×200); c. C. striata of Group A2 at initial phase(×400); d. C. striata of Group A2 on 8th day(×400); e. S. quadricauda of Group A2 at initial phase(×200); f. S. quadricauda of Group A2 on 10th day(×200); g. C. pyrenoidosa of Group A2 at initial phase(×400); h. C. pyrenoidosa of Group A2 on 10th day(×400)2.3 菌株A2对混合培养微藻的影响
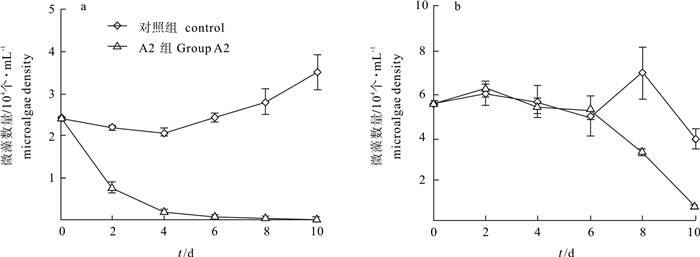
将菌株A2分别添加到锥状斯氏藻-条纹小环藻、锥状斯氏藻-蛋白核小球藻的混合培养体系中。结果显示,在2组实验中菌株A2对锥状斯氏藻均具有显著溶藻效果,第10天其死亡率分别达到98.06%(图 5-a)和93.68%(图 6-a),均显著高于对照组(P<0.05);菌株A2对条纹小环藻也具有一定的溶藻效果(图 5-b);菌株A2对蛋白核小球藻无溶藻效果,实验组和对照组的蛋白核小球藻细胞数量持续升高,并且第10天时实验组藻细胞数量显著高于对照组(P<0.05)(图 6-b)。结果表明,锥状斯氏藻与条纹小环藻混合培养时,菌株A2对2种微藻均具有溶藻效果,但对前者的溶解效果显著强于后者;锥状斯氏藻与蛋白核小球藻混合培养时,菌株A2仅对锥状斯氏藻有溶藻效果,可以促进蛋白核小球藻生长。
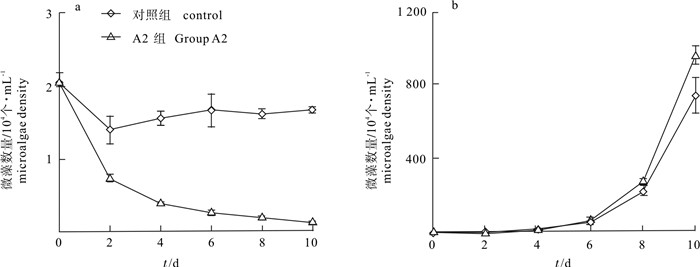
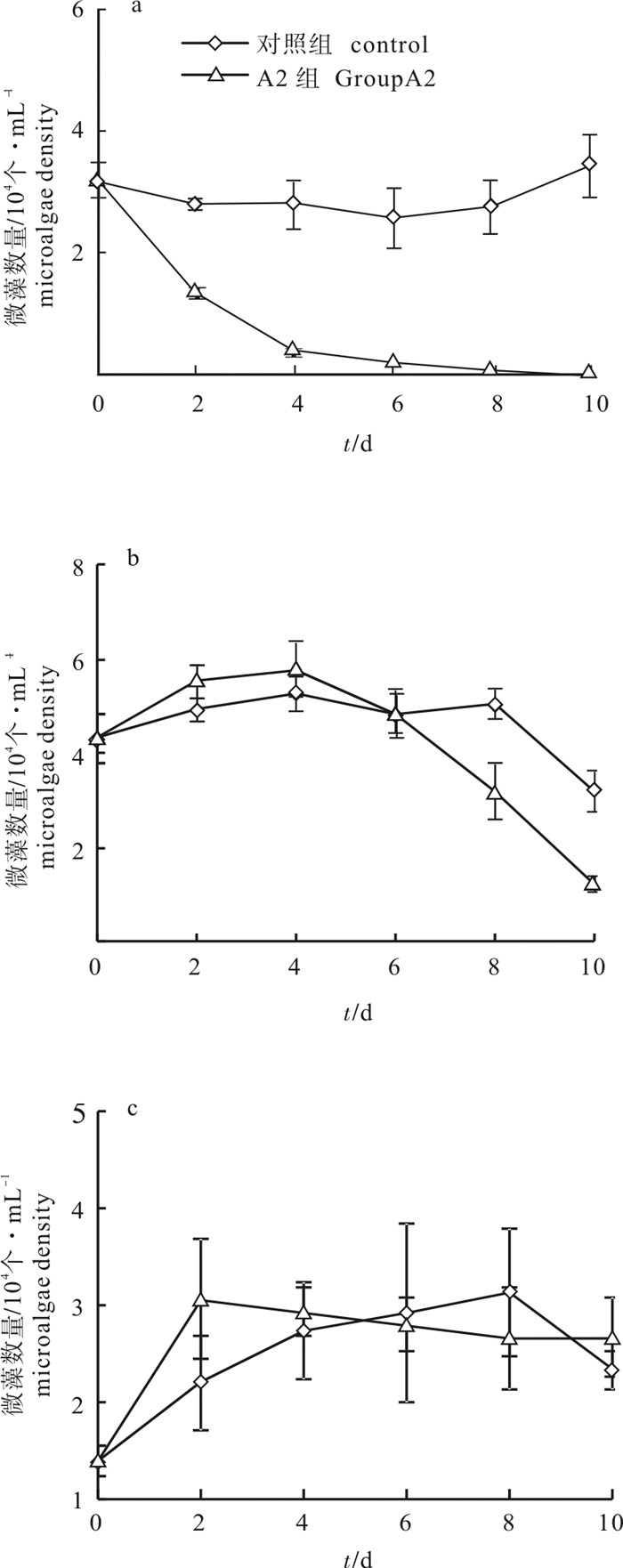
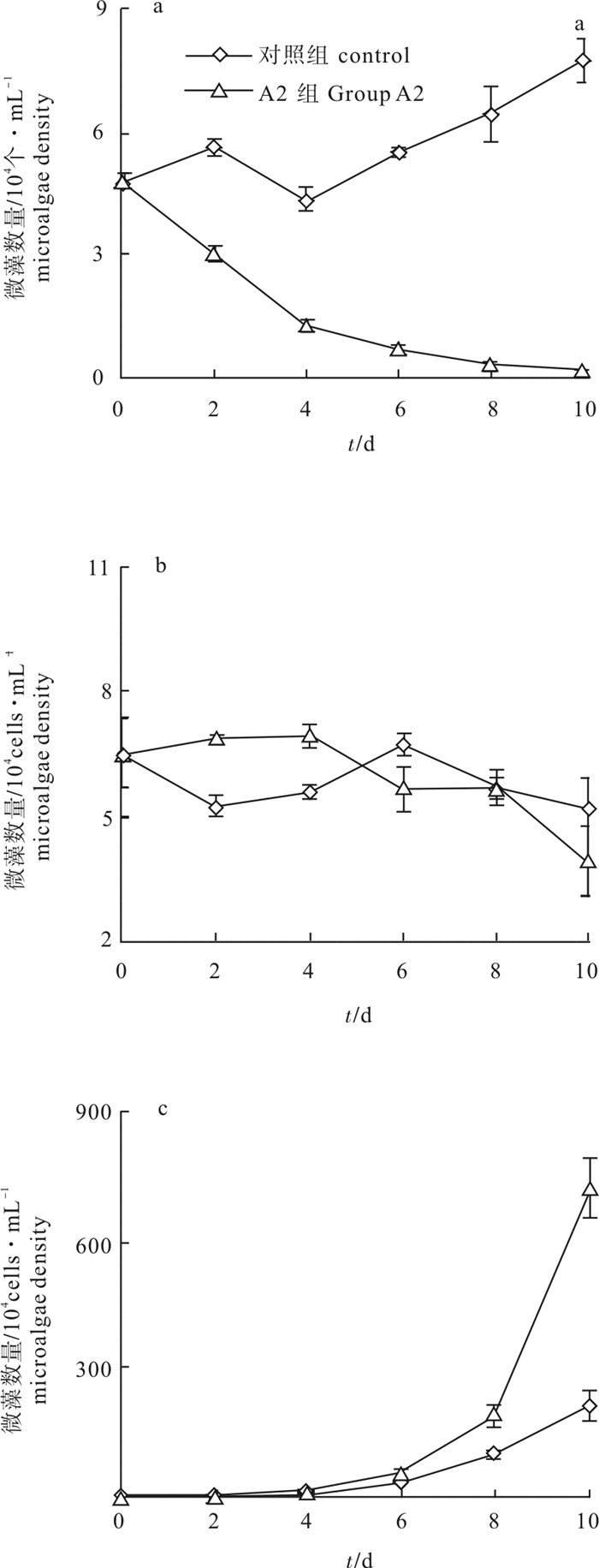
将菌株A2分别加入到锥状斯氏藻-条纹小环藻-四尾栅藻、锥状斯氏藻-条纹小环藻-蛋白核小球藻的混合培养体系中。结果显示,在两组实验中实验组的锥状斯氏藻细胞数量均显著低于对照组(P<0.05),其死亡率分别高达98.29%和95.37%(图 7-a、图 8-a);条纹小环藻也受到一定程度的溶解作用,实验组的藻细胞数量较对照组分别降低了62.50%和24.37%(图 7-b、图 8-b);而实验组四尾栅藻藻细胞数量与对照组无显著差异(P>0.05)(图 7-c),实验组蛋白核小球藻未受到溶解作用,并且第10天实验组的蛋白核小球藻数量较对照组升高了237.6%,实验组蛋白核小球藻细胞数量显著高于对照组(P<0.05)(图 8-c)。结果表明,在两组藻的混合培养体系中,菌株A2都可以将锥状斯氏藻有效溶解,对条纹小环藻具有一定的溶解效果,可以促进蛋白核小球藻生长,对四尾栅藻的生长无影响。
3. 讨论
3.1 菌株鉴定
已报道的具有溶藻活性的细菌种类包括弧菌属(Vibrio)[11]、交替单胞菌属(Alteromonas)[20]、短波单胞菌属(Brevundimonas)[21]、微小杆菌属(Exiguobacterium)[22]、不动杆菌属(Acinetobacter)[23]、红细菌属(Rhodobacteraceae)[24]、芽孢杆菌属(Bacillus)[25]等。该研究表明溶藻细菌A2属于海杆菌属(Marinobacter)。目前,有关海杆菌的研究主要集中于海杆菌对海水中烷烃等有害污染物的降解 [26-28],缺乏海杆菌溶藻方面的研究报道。该研究证明海杆菌属菌株A2具有溶藻特性,能够将锥状斯氏藻有效溶解,可为海杆菌属溶藻功能特性的研究提供重要的理论基础。
3.2 菌株A2对单一藻种的溶藻专一性
研究认为溶藻细菌具有溶藻特异性,一种溶藻细菌只能溶解一种或一类微藻 [29-30]。如TIAN等 [22]研究发现溶藻菌A27对铜绿微囊藻(Microcystis aeruginosa)、颤藻(Oscillatoria sp.)、念珠藻(Nostoc sp.)、水华束丝藻(Aphanizomenon flosaquae)、聚球藻(Synechococcus sp.)等多种蓝藻具有溶藻效果,溶藻效率高达82.9%,而对实验中的2种绿藻Chlorophyta sp. M7与Chlamydomonas sp. BS3的溶藻效率分别为0.7%与27.2%,可见菌株A27能够选择性的溶解蓝藻种类。HARE等[31]研究发现细菌Shewanella IRI-160对费氏藻(Pfiesteria piscicida)、微小原甲藻(Prorocentrum minimum)、环沟藻(Gyrodinium uncatenum)3种甲藻具有明显的抑制调控作用,而对硅藻类的威氏海链藻(Thalassiosira weissflogii)、绿藻类的四爿藻(Tetraselmis sp.)具有促进生长的作用。综合以上研究表明,一种溶藻菌只能溶解一类藻类。该研究将菌株A2以浓度为107 CFU · mL-1分别加入到锥状斯氏藻、条纹小环藻、蛋白核小球藻、四尾栅藻纯培养藻液中,结果显示菌株A2可以将锥状斯氏藻有效溶解,对条纹小环藻具有一定的溶藻效果,可以促进蛋白核小球藻生长,对四尾栅藻生长无影响。表明菌株A2具有溶藻专一性,可选择性溶解锥状斯氏藻。由于一种溶藻菌只能溶解一类藻类,推测菌株A2可以用于养殖池塘中选择性的调控有害甲藻而对绿藻、硅藻没有危害或危害很小。
3.3 菌株A2对混合培养藻类的影响
微藻在水体环境中并不是以单一种类存在,而是与其他藻类共同存在于水体环境中 [17, 19]。微藻中的绿藻与硅藻种类具有稳定水体藻相结构,提升养殖综合效益的功能[32-34]。目前,利用溶藻菌调控甲藻的研究主要集中于单一种类甲藻的作用效果与机制方面,缺乏关于菌株溶藻专一性的研究[35-37]。利用溶藻菌A2调控养殖水体中有害微藻的同时是否会对其中的优良绿藻、硅藻产生不良影响,这需要引起广泛的关注。该研究将溶藻菌A2以浓度107 CFU · mL-1分别加入到锥状斯氏藻、条纹小环藻、蛋白核小球藻、四尾栅藻的2种藻与3种藻混合培养藻液中。结果显示,在所有的混合实验中,A2菌都能够有效溶解甲藻类的锥状斯氏藻,对硅藻类的条纹小环藻有一定的溶解效果,可以促进绿藻类蛋白核小球藻生长,对绿藻类的四尾栅藻生长无影响。由于一种溶藻菌只能溶解一类藻类[22, 31],推测菌株A2能够调控水体有害甲藻,对水体中的绿藻和硅藻无危害或者危害很小。也有学者报道将溶藻菌放入自然水体中,可使原有微藻群落中的有害微藻优势种演替为绿藻和硅藻 [38]。综上,A2菌株具有良好的甲藻溶藻专一性,可作为研发池塘甲藻调控剂的备选菌株。
研究溶藻菌的溶藻专一性可以为养殖水体中有害微藻调控,营造适宜对虾生长的良好的藻相环境提供一定的理论支持。然而该研究只进行了溶藻专一性的探究,溶藻菌对养殖生物的影响、生态适应性等研究仍有待于进一步开展。
-
图 4 菌株A2作用下不同微藻的细胞形态变化
a. 实验起始时锥状斯氏藻细胞(×200);b. 第1天时实验组锥状斯氏藻藻细胞(×200);c. 实验起始时条纹小环藻细胞(×400);d. 第8天时实验组条纹小环藻细胞(×400);e. 实验起始时四尾栅藻细胞(×200);f. 第10天时实验组四尾栅藻细胞(×200);g. 实验起始时蛋白核小球藻细胞(×400);h. 第10天时实验组蛋白核小球藻细胞(×400)
Figure 4. Morphology variation of microalgal cell under effects of A2
a. S. trochoidea at initial phase(×200); b. S. trochoidea of Group A2 on the first day(×200); c. C. striata of Group A2 at initial phase(×400); d. C. striata of Group A2 on 8th day(×400); e. S. quadricauda of Group A2 at initial phase(×200); f. S. quadricauda of Group A2 on 10th day(×200); g. C. pyrenoidosa of Group A2 at initial phase(×400); h. C. pyrenoidosa of Group A2 on 10th day(×400)
表 1 菌株溶藻专一性的实验设计
Table 1 Experimental design for effects of algicidal bacteria on microalgae
实验分组
group微藻接种量/个·mL-1 inoculum amount of mircoalgae 锥状斯氏藻
S. trochoidea条纹小环藻
C. striata蛋白核小球藻
C. pyrenoidosa四尾栅藻
S. quadricauda锥状斯氏藻S. trochoidea 1.44×104 条纹小环藻C. striata 4.68×105 蛋白核小球藻C. pyrenoidosa 3.28×106 四尾栅藻S. quadricauda 1.60×105 锥状斯氏藻-条纹小环藻S. trochoidea-C.striata 2.43×104 5.47×104 锥状斯氏藻-蛋白核小球藻S. trochoidea-C.pyrenoidosa 2.06×104 1.20×104 锥状斯氏藻-条纹小环藻-蛋白核小球藻S. trochoidea-C.striata-C.pyrenoidosa 4.82×104 6.87×104 1.20×104 锥状斯氏藻-条纹小环藻-四尾栅藻S. trochoidea-C.striata-S.quadricauda 3.18×104 4.33×104 1.40×104 -
[1] 米振琴, 谢骏, 潘德博, 等. 精养虾池浮游植物、理化因子与虾病的关系[J]. 上海水产大学学报, 1999, 8(4): 304-308. http://shhydxxb.ijournals.cn/shhy/article/pdf/19990468 [2] CAO Y C, WEN G L, LI Z J, et al. Effects of dominant microalgae species and bacterial quantity on shrimp production in the final culture season[J]. J Appl Phycol, 2014, 26(4): 1749-1757. doi: 10.1007/s10811-013-0195-0
[3] 梁忠秀, 李健, 谭志军, 等. 塔玛亚历山大藻对中国明对虾肝胰腺及鳃SOD、GST和MDA的影响[J]. 水产学报, 2013, 37(8): 1192-1197. doi: 10.3724/SP.J.1231.2013.38501 [4] ALONSO-RODRIÍGUEZ R, PÁEZ-OSUNA F. Nutrients, phytoplankton and harmful algal blooms in shrimp ponds: a review with special reference to the situation in the Gulf of California[J]. Aquaculture, 2003, 219(1/2/3/4): 317-336.
[5] JUNG S W, YUN S M, YOO J W, et al. Can the algicidal material Ca-aminoclay be harmful when applied to a natural ecosystem? An assessment using microcosms[J]. J Hazard Mater, 2015, 298: 178-187. doi: 10.1016/j.jhazmat.2015.05.012
[6] 王志富. 改性粘土治理藻华对典型底栖生物的影响研究[D]. 北京: 中国科学院大学, 2014: 27-38.http://www.shidacloud.com/?p=13407 [7] NAGAYAMA K, SHIBATA T, FUJIMOTO K, et al. Algicidal effect of phlorotannins from the brown alga Ecklonia kurome on red tide microalgae[J]. Aquaculture, 2003, 218(1/2/3/4): 601-611. doi: 10.1016/S0044-8486(02)00255-7
[8] WANG Y, TANG X E. Interactions between Prorocentrum donghaiense Lu and Scrippsiella trochoidea (Stein) Loeblich Ⅲ under laboratory culture[J]. Harmful Algae, 2008, 7(1): 65-75. doi: 10.1016/j.hal.2007.05.005
[9] 葛蔚, 汪芳, 柴超. 氮和磷浓度对中肋骨条藻和锥状斯氏藻种间竞争的影响[J]. 植物生态学报, 2012, 36(7): 697-704. doi: 10.3724/SP.J.1258.2012.00697 [10] 谢静, 潘伟斌, 曾嘉韫. 溶藻细菌L7代谢物对水华鱼腥藻的溶藻效应[J]. 环境保护科学, 2014, 40(1): 36-40. doi: 10.3969/j.issn.1004-6216.2014.01.009 [11] WANG B X, YANG X R, LU J L, et al. A marine bacterium producing protein with algicidal activity against Alexandrium tamarense[J]. Harmful Algae, 2012, 13: 83-88. doi: 10.1016/j.hal.2011.10.006
[12] JAUZEIN C, EVANS A N, ERDNER D L. The impact of associated bacteria on morphology and physiology of the dinoflagellate Alexandrium tamarense[J]. Harmful Algae, 2015, 50: 65-75. doi: 10.1016/j.hal.2015.10.006
[13] 李东, 安新丽, 傅丽君, 等. 溶藻细菌BS03分离、鉴定及其对塔玛亚历山大藻生长的影响[J]. 环境科学学报, 2013, 33(1): 44-52. https://tsg.actasc.cn/hjkxxb/ch/reader/view_abstract.aspx?flag=1&file_no=20120227001&journal_id=hjkxxb [14] 史荣君, 黄洪辉, 齐占会, 等. 海洋细菌N3对几种赤潮藻的溶藻效应[J]. 环境科学, 2013, 34(5): 1922-1929. https://www.doc88.com/p-0127155226374.html [15] LI Y, ZHU H, LEI X, et al. The first evidence of deinoxanthin from Deinococcus sp. Y35 with strong algicidal effect on the toxic dinoflagellate Alexandrium tamarense[J]. J Hazard Mater, 2015, 290: 87-95. doi: 10.1016/j.jhazmat.2015.02.070
[16] 张俊. 赤潮藻藻际细菌溶藻效应研究[D]. 广州: 暨南大学, 2010: 21-54.https://cdmd.cnki.com.cn/Article/CDMD-10559-2010124227.htm [17] 吴蕾, 徐亮亮, 胡春香. 新疆的微藻及其群落结构[J]. 水生生物学报, 2015, 39(6): 1207-1216. doi: 10.7541/2015.157 [18] 陶令霞, 夏铁骑, 常慧萍. 两种测定固氮菌NT06菌株生长曲线方法的比较[J]. 生物学杂志, 2007, 24(5): 57-58. https://wenku.baidu.com/view/b248a97327d3240c8447ef51?fr=xueshu_top [19] 刘孝竹, 曹煜成, 李卓佳, 等. 高位虾池养殖后期浮游微藻群落结构特征[J]. 渔业科学进展, 2011, 32(3): 84-91. [20] WANG H, BUTT L, ROOKS P, et al. Characterisation of algicidal bacterial exometabolites against the lipid-accumulating diatom Skeletonema sp. [J]. Algal Res, 2016, 13: 1-6. doi: 10.1016/j.algal.2015.11.012
[21] LIN S Q, PAN J L, LI Z H, et al. Characterization of an algicidal bacterium Brevundimonas J4 and chemical defense of Synechococcus sp. BN60 against bacterium J4[J]. Harmful Algae, 2014, 37: 1-7. doi: 10.1016/j.hal.2014.05.002
[22] TIAN C, LIU X, TAN J, et al. Isolation, identification and characterization of an algicidal bacterium from Lake Taihu and preliminary studies on its algicidal compounds[J]. J Environ Sci (China), 2012, 24(10): 1823-1831. doi: 10.1016/s1001-0742(11)60983-2
[23] YI Y L, YU X B, ZHANG C, et al. Growth inhibition and microcystin degradation effects of Acinetobacter guillouiae A2 on Microcystis aeruginosa[J]. Res Microbiol, 2015, 166(2): 93-101. https://www.sciencedirect.com/science/article/pii/S0923250815000133
[24] CHEN Z, ZHANG J, LEI X, et al. Influence of plaque-forming bacterium, Rhodobacteraceae sp. on the growth of Chlorella vulgaris[J]. Bioresour Technol, 2014, 169: 784-788. doi: 10.1016/j.biortech.2014.07.021
[25] SHAO J H, HE Y X, CHEN A W, et al. Interactive effects of algicidal efficiency of Bacillus sp. B50 and bacterial community on susceptibility of Microcystis aeruginosa with different growth rates[J]. Int Biodeterior Biodegradation, 2015, 97: 1-6. doi: 10.1016/j.ibiod.2014.10.013
[26] CUI Z S, XU G S, GAO W, et al. Isolation and characterization of Cycloclasticus strains from Yellow Sea sediments and biodegradation of pyrene and fluoranthene by their syntrophic association with Marinobacter strains[J]. Int Biodeterior Biodegradation, 2014, 91: 45-51. doi: 10.1016/j.ibiod.2014.03.005
[27] ARUN PRASAD A S, SATYANARAYANA V S, BHASKARA RAO K V. Biotransformation of Direct Blue 1 by a moderately halophilic bacterium Marinobacter sp. strain HBRA and toxicity assessment of degraded metabolites[J]. J Hazard Mater, 2013, 262: 674-684. doi: 10.1016/j.jhazmat.2013.09.011
[28] KLEIN B, GROSSI V, BOURIAT P, et al. Cytoplasmic wax ester accumulation during biofilm-driven substrate assimilation at the alkane-water interface by Marinobacter hydrocarbonoclasticus SP17[J]. Res Microbiol, 2008, 159(2): 137-144. doi: 10.1016/j.jhazmat.2013.09.011
[29] 黄姿, 李春强, 于晓玲, 等. 一株溶藻细菌(Pseudoalteromonas sp.)的分离鉴定及溶藻活性初探[J]. 海洋技术, 2008, 27(3): 56-60. [30] 王赟, 张业猛, 李佩佩. 醋酸钙不动杆菌的分离鉴定及溶藻特性[J]. 生物技术通报, 2015, 31(3): 140-145. https://biotech.aiijournal.com/CN/Y2015/V31/I3/140 [31] HARE C E, DEMIR E, COYNE K J, et al. A bacterium that inhibits the growth of Pfiesteria piscicida and other dinoflagellates[J]. Harmful Algae, 2005, 4(2): 221-234. doi: 10.1016/j.hal.2004.03.001
[32] 彭聪聪, 李卓佳, 曹煜成, 等. 虾池浮游微藻与养殖水环境调控的研究概况[J]. 南方水产, 2010, 6(5): 74-80. doi: 10.3969/j.issn.1673-2227.2010.05.012.pdf [33] 曹煜成, 李卓佳, 杨莺莺, 等. 浮游微藻生态调控技术在对虾养殖应用中的研究进展[J]. 南方水产, 2007, 3(4): 70-73. https://qikan.cqvip.com/Qikan/Article/Detail?id=27484750 [34] 陆家昌. 菌、藻改善水体环境提高凡纳滨对虾幼虾免疫指标和抗逆性的研究[D]. 湛江: 广东海洋大学, 2010: 32-42.https://www.doc88.com/p-1965954366560.html [35] ROTH P B, TWINER M J, MIKULSKI C M, et al. Comparative analysis of two algicidal bacteria active against the red tide dinoflagellate Karenia brevis[J]. Harmful Algae, 2008, 7(5): 682-691. doi: 10.1016/j.hal.2008.02.002
[36] SOMDEE T, SUMALAI N, SOMDEE A. A novel actinomycete Streptomyces aurantiogriseus with algicidal activity against the toxic cyanobacterium Microcystis aeruginosa[J]. J Appl Phycol, 2013, 25(5): 1587-1594. doi: 10.1007/s10811-013-9999-1
[37] 黄思明, 尹平河, 赵玲. 一株芽孢杆菌对球形棕囊藻的溶藻效果[J]. 暨南大学学报(自然科学与医学版), 2013, 34(3): 337-342. https://www.doc88.com/p-6901971731337.html [38] 何鉴尧, 潘伟斌, 林敏. 溶藻细菌对富营养化水体藻类群落结构的影响[J]. 环境污染与防治, 2008, 30(11): 70-74. https://www.doc88.com/p-5095474798648.html -
期刊类型引用(7)
1. 赵张琪,蒋之琛,堵飞超,詹皓禹,王婷婷,李宇航,颜天,孔凡洲,张德超. 海州湾赤潮高发区可培养细菌的多样性及其溶藻特性研究. 生态与农村环境学报. 2025(02): 242-251 .  百度学术
百度学术
2. 丁宁,郑宁宁,王仁君,孙丽,李晨,高配科. 赤潮藻米氏凯伦藻(Karenia mikimotoi)藻际细菌群落及其原位抑藻效应. 生态学杂志. 2020(07): 2356-2363 .  百度学术
百度学术
3. 郑宁宁,孙丽,丁宁,李晨,傅宝燕,王超,高配科,王仁君. 有害微藻抑藻细菌多样性及抑藻机制研究进展. 微生物学通报. 2019(05): 1204-1219 .  百度学术
百度学术
4. 田雅洁,曹煜成,胡晓娟,黄小帅,徐煜,许云娜,李卓佳,文国樑. 4种因子对玫瑰红红球菌XH2氨氮去除效果的影响. 渔业科学进展. 2018(06): 164-172 .  百度学术
百度学术
5. 胡晓娟,徐创文,李卓佳,文国樑,杨铿,许云娜,李莎莎,曹煜成. 响应面法优化蓝藻溶藻菌CZBC1发酵培养工艺. 南方农业学报. 2017(11): 2092-2099 .  百度学术
百度学术
6. 李莎莎,曹煜成,李卓佳,胡晓娟,徐煜,徐武杰,杨铿,苏浩昌,文国樑. 碳氮营养和培养条件对芽孢杆菌(Bacillus sp.)A4生长的影响. 渔业科学进展. 2017(06): 119-126 .  百度学术
百度学术
7. 李莎莎,曹煜成,胡晓娟,李卓佳,徐煜,杨铿,徐创文,文国樑. 响应面法优化芽孢杆菌(Bacillus sp.)A4的培养参数. 南方水产科学. 2017(05): 85-93 .  本站查看
本站查看
其他类型引用(5)



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
