Analysis of population genetic structure of bullet tuna(Auxis rochei) in the South China Sea based on mitochondrial control region sequences
-
摘要:
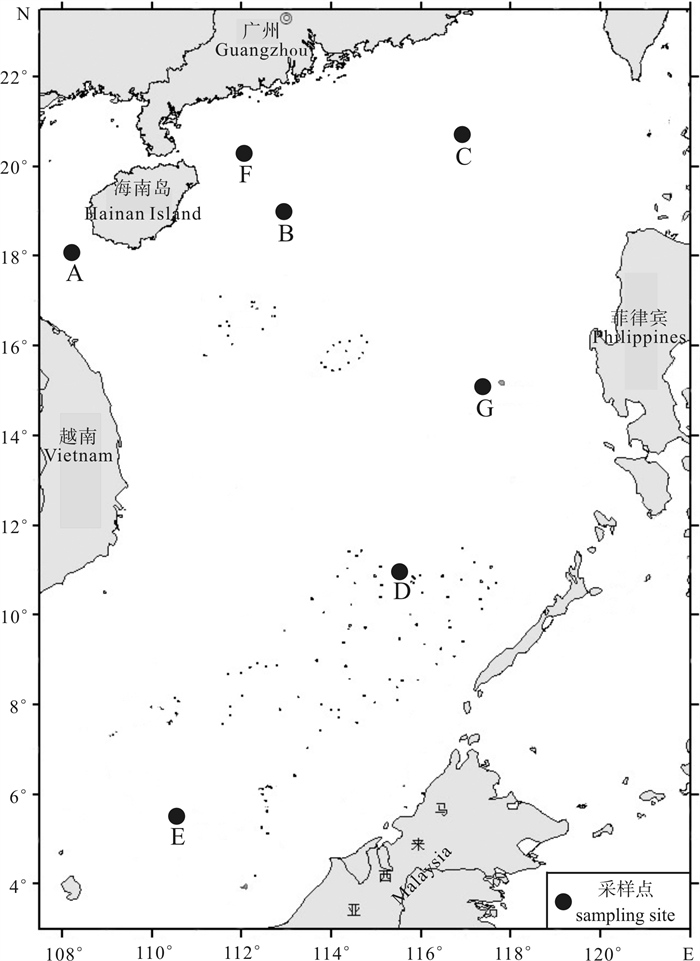
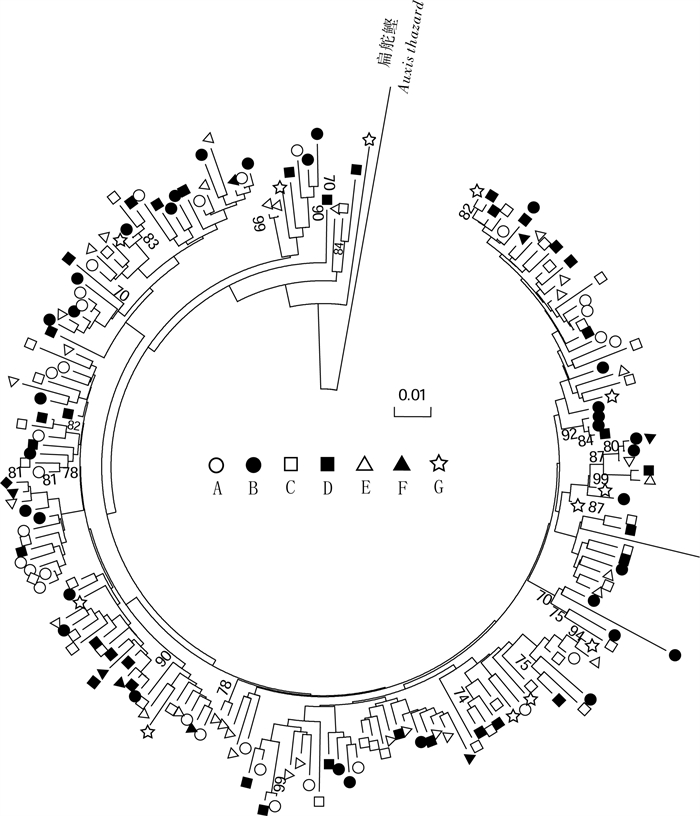
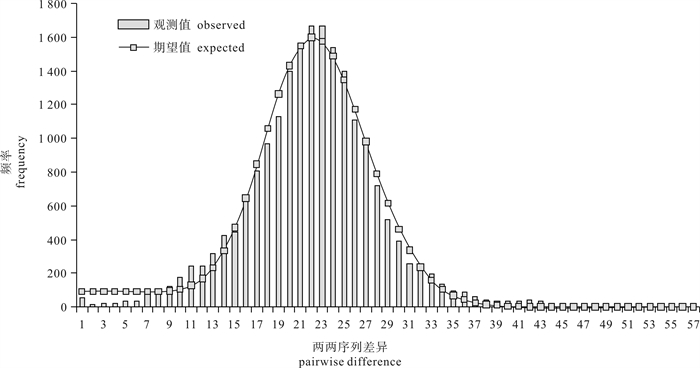
利用线粒体控制区(D-loop)高变区序列作为遗传标记,分析了中国南海5°N~21°N之间7个圆舵鲣(Auxis rochei)地理群体的遗传结构特征。201尾样本的D-loop区序列共检测到185种单倍型。各个采样点均呈现出很高的单倍型多样性(0.958 2~1.000 0)和较高的核苷酸多样性(0.034 327~0.041 235)的特征。单倍型邻接关系树未呈现与地理群体对应的谱系结构。分子方差分析和成对遗传分化系数(FST)显示南海海域圆舵鲣的遗传变异主要来自群体内(98.33%),群体间基因交流频繁,是一个随机交配群。核苷酸不配对分布和中性检验表明南海圆舵鲣在更新世晚期曾经历过种群的快速扩张。结果表明,南海圆舵鲣具有丰富的遗传多样性水平,遗传分化不显著,在渔业上可以作为一个单元来管理。
Abstract:Based on hypervariable region of mitochondrial control region (D-loop) sequences, we examined the population genetic structure of the bullet tuna (Auxis rochei) collected from seven locations between 5°N to 21°N in the South China Sea. A total of 185 haplotypes were defined from 201 individuals of fishes. The genetic diversity analysis shows that the samples of A.rochei from the seven locations in the South China Sea possessed quite high haplotype diversity (0.958 2~1.000 0) and high nucleotide diversity (0.034 327~0.041 235). The neighbor-joining tree for D-loop haplotypes reveals no significant genealogical clades of the fish samples corresponding to the sampling locations. Analyses of molecular variance and pairwise FST suggest most of the genetic variation (98.33%) was attributed to variability within populations. A high rate of gene flow between different populations implies a panmixia for A.rochei in the South China Sea. Both mismatch distribution analysis and neutrality tests indicate a late Pleistocene expansion in A.rochei. The results demonstrate that A.rochei in the South China Sea belong to the same population with high genetic diversity. Thus, a single-stock management regime can be supported in fishery management.
-
大伙房水库地处辽河支流浑河中上游,辽宁省抚顺市境内,位于41°47′N~41°57′N,124°05′E~124°22′E,为带状河谷型水库。东西长约35 km,最大水深37 m,最大蓄水面积114 km2,总库容21.87×109 m3。水库渔获鱼类11种,主要经济鱼类5种,为鲢(Hypophthalmichthys molitrix)、鳙(Aristichthys nobilis)、鲤(Cyprinus carpio)、鲫(Carassius auratus)、草鱼(Ctenopharyngodon idellus)。鲢、鳙为该水库主要增殖品种,约占总量的85%。每年10月投放鱼苗40 t左右,其中鳙58%、鲢27%,规格为35~100 g·尾-1。作为中国9大重点饮用水源保护地,合理的鱼类放养捕捞既可以优化水质、维持水库生态稳定,又能创造较高的经济价值。对库区鱼类资源不同季节现存量以及分布状况的把握,可为制定增殖放养和捕捞计划提供科学依据。
由于淡水水域多采用人工增殖放养和定置网箔大规格体长鱼类选择性捕捞,传统的渔业资源调查评估方法较难实施。近年来随着渔业声学测量技术在中国推广,渔业资源声学评估方法在淡水的应用逐渐增多且收到较好效果。包括武汉东湖、长江葛洲坝、新疆塞里木湖、青海湖、辽宁清河水库、三峡水库和楠溪江等不同种类鱼类的声学资源调查和空间分布[1-7]。中国虽然在2007年编制了针对海洋调查的《渔业声学资源调查与评估》规范[8],但是由于湖泊江河相对海洋水域范围狭窄且鱼类组成各异,目前已成熟的海洋声学评估技术尚不能简单复制于淡水调查,需要针对调查水域实际情况开展研究,获得最佳的调查方法。国外淡水渔业声学研究较少,鱼种与中国差异较大,可参考的结果也较少[9-13]。
因此该研究选择春、夏、秋(冬季冰层较厚不能进行声学调查)季节,在2012年7月19~21日、9月14~16日和2013年5月12~14日分别对水库进行鱼类资源声学调查,对鱼类的回波特征、单体目标大小和分布、资源现存量和分布及主要水文参数进行分析,考察鱼类资源分布随季节和水文参数变化的规律,为确定北方水库合理的声学调查方法提供科学依据。
1. 材料与方法
1.1 调查航线和站位的设定
大伙房水库为T型交叉带状河谷型水库,综合考虑水库形状、水深分布、采样点及网箱位置等因素,声学调查采用“之”字形航线对库区(上游有网箱的区域除外)进行断面声学回波采样。水文参数采样按上、中、下游设置共计8个采样站位,分别为位于上游支流交汇处的A1、A2,位于中游断面点B1、B2、B3,以及位于两主流交汇处C1、南侧C2及北侧大坝附近的C3,图 1为7月的调查航迹线和站位分布图,其余2次调查航线与7月航线基本相同。
1.2 调查方法和数据后处理
使用多参数水质分析仪(美国YSI,6100型)在设置站位对水温、pH、溶解氧(DO)等参量进行垂直剖面测量,叶绿素a使用荧光法测量。声学调查使用小艇(长6 m,宽2.5 m)走航测量,平均航速6 kn。分裂波束科学鱼探仪(挪威Simrad,EY60型,70 kHz)的波束半功率指向全角为7°、脉冲宽度0.256 ms、发射功率300 W、脉冲收发间隔0.1 s。换能器放置于导流罩内,使用钢管悬挂固定于船弦右侧,吃水1 m。调查前用水质分析仪测量水温、盐度,计算声速和吸收系数,使用直径38.1 mm钨钢合金标准球对科学鱼探仪进行校正。使用GPS导航仪(美国Garmin,60CS型)测量位置信息,数据通过RS232接口与科学鱼探仪数据进行同步显示和保存。使用专用声学数据后处理软件Echoview 4.0(澳大利亚,Myriax)进行单体目标统计和资源评估。
1.3 鱼类资源声学评估方法
库区鱼类资源声学评估主要参考《渔业资源声学调查与评估》规范[8]中回波积分法进行。由于大伙房历年捕捞渔获物中鲢、鳙种类的比例占绝对优势(2011年鳙为52%,鲢为22%),且库区在6月~11月期间主要以定置网箔方式进行活鱼捕捞,无法提供对应声学回波的网具采样,因此现阶段暂按鳙的声学参数对整体资源量进行评估。
鳙的姿态平均目标强度(target strength,TS)与体长的关系式,使用基尔霍夫近似射线(KRM)模型计算的姿态平均TS结果[14-15]:
$$ T S_{\mathrm{a}}=21.1 \log L_{\mathrm{cm}}-67.1 $$ (1) 其中Lcm为鱼标准体长(cm)。分裂波束科学渔探仪调查时,TSa可以直接对单体回波进行检测后现场测量。
资源质量可以利用体长与体质量的拟合关系式进行换算,该研究使用鲢鳙的关系式为[14]:
$$ W=0.0167 L^{2.9806} $$ (2) 其中W表示质量(g);L为标准体长(cm)。最终在面积As(m2)内鱼类资源总质量为:
$$ W_T=A_S \sum\limits_{i=1}^k<n_i>W_i $$ (3) 其中下标i表示不同体长鱼类, < n>为单位水面的鱼类平均密度。在回波积分处理单元内,不同体长鱼类的密度为下式[15-17]:
$$ n_i=\frac{S_a}{<\mathsf{σ}_{b s}>} \frac{p_i<\mathsf{σ}_{b s}>_i}{^i\sum\limits_{i=1}^k p_i<\mathsf{σ}_{b s}>_i} $$ (4) 其中sa为回波积分值(单位水面的散射强度),p为通过单体检测并进行目标跟踪后,不同TS鱼类数量的频度值, < σbs>为姿态平均后向散射截面(与TS的线性值相等)。
在数据后处理过程中,根据库区鱼类回波分散分布以及库区狭长的地理特征,选择积分处理单元水平距离为100 m。使用Echoview软件数据处理按以下步骤进行:1)进行气泡和干涉信号等剔除;2)进行单体目标检测、跟踪和频度计算,获得不同TSa(< σbs>)频度p值;3)在积分处理单元内进行回波积分,获得积分值sa;4)利用公式(4)计算不同TS鱼类的密度(尾·m-2);5)根据公式(2)和(3)计算上、中、下游的鱼类资源体质量;6)统计库区内不同体长鱼类水平和垂直空间密度分布。
2. 结果
2.1 主要水文参数
不同季节各站位水温剖面见图 2。2013年5月和2012年7月有较明显的温跃层,5月上游6~8 m,中下游8~10 m,7月15~20 m,温跃层下的等温层水温为4~6 ℃。2012年9月15 m以深水温逐渐降低,无明显温跃层变化。表层水温5月、7月和9月别分为10~15 ℃,18~27 ℃和20~22 ℃,7月水温的下降梯度最大。
不同季节ρ(DO)剖面见图 3。ρ(DO)随深度增加而逐渐减小。7月表层ρ(DO)明显高于5月和9月。7月5 m以浅水层ρ(DO)为10~14 mg·L-1,5 m以深水层ρ(DO)随深度下降逐渐降低。5月ρ(DO)随深度变化不大,从表层至底层均维持在3~5 mg·L-1。9月15 m以浅水层ρ(DO)维持在7~10 mg·L-1,15 m之后ρ(DO)随深度下降逐渐减少。5月和9月下游ρ(DO)要低于中上游,7月上游ρ(DO)最低。其他水文参数均值:5月pH为7.71、叶绿素a质量浓度为12.09 μg·L-1、透明度为1.96 m。7月pH为8.27、叶绿素a质量浓度为27.7 μg·L-1、透明度为1.50 m。9月pH为7.62、叶绿素a质量浓度为12.06 μg·L-1,透明度为2.25 m。
大伙房水库水质呈弱碱性,pH夏季高于春秋季。受春季融冰等因素影响,5月ρ(DO)较低,7月夏季受高温、降水和径流影响,表层较高,9月蓄水后表层ρ(DO)减少。浮游植物夏季受降水径流和高日照影响呈峰值状态。7月受降水和径流影响透明度较低。
2.2 声学调查结果
2.2.1 鱼类声学回波及单体目标强度特征
不同季节鱼类回波特征见图 4~图 6。2012年7月鱼类回波密度较大,回波信号分层分布,主要集中于在0~5 m及5~15 m水层,15 m以下有分散的单体回波信号(图 4),偶尔有鱼群回波(图 4中c回波)。9月回波较7月分散,10 m以下水层有带状回波,中游区域偶尔出现鱼群,底层也有鱼类回波(图 5)。2013年5月整个水库单体回波信号较少,鱼群回波较多,主要分布在5~10 m水层,集中在中游(图 6)。
目标识别主要通过单体目标检测、不同鱼类的捕捞方式和渔获物水层分布的经验来判断。0~5 m层的TS较小(-70~-58 dB)、结合


不同季节单体目标检测结果见图 7。检测的数量,7月数量最多、9月次之、5月受鱼类集群的影响检测数量最小。7月调查TS峰值主要集中在-66~ -62 dB区域;9月调查TS主要集中分布在-64 dB附近;5月TS存在-54 dB、-48 dB和-42 dB 3个峰值。库区投放鲢、鳙鱼苗规格大于10 cm,根据公式(1)小于-46 dB的单体目标为非鲢、鳙的其他小型鱼类等。因此,在资源评估中该部分不计入资源量内。根据不同季节目标强度的频度能够反映出浮游动物数量夏季最多、秋季数量略为降低但规格增大、春季大幅度减少的特征。7月表层1~4 m为浮游动物的散射层。5~15 m水层浮游动物和鱼类混在一起。
2.2.2 鱼类资源密度和资源量
不同季节不同体长规格鱼类所对应的平均密度见图 8。2012年7月上游鱼类密度较高,9月体长大于20 cm规格鱼类下游密度高。2013年5月上、中、下游鱼类密度差异不大。因此,5月鱼类在库区分布比较均匀;7月主要集中在较浅的上、中游,下游分布较少;9月主要在较深的下游分布,上、中游较少。资源量调查结果见图 9。7月、9月和5月分别在4 634 t,1 522 t和1 012 t左右。7月由于上游调查时间进入夜间、船上灯光的诱集效果以及浮游动物和小气泡等影响,造成评估结果过大。5月由于鱼类以小型集群形式存在,单体检测较少且航线短,资源量评估偏小。9月水文环境垂直变动小,鱼类呈单体分散状态,较为适合单体目标检测和声学评估。调查结果与利用历年各龄鱼渔获尾数和最大年龄和最后一年的资源尾数的POPO(1972)方法推算的资源量结果1 513 t基本一致[16]。
2.2.3 渔业资源的垂直分布
通过对不同水层的单体目标回波检测,分析获得不同体长鱼类在不同季节的垂直分布特征,分布频度特征见图 10。5月鱼类主要集中在0~10 m水层;7月鱼类集中在5~15 m水层。体长小于50 cm的鱼类主要分布在0~15 m水层,大于50 cm的鱼类主要分布在5~15 m水层;9月鱼类主要分布于10~20 m水层,其中5~15 m水层较为集中,0~5 m水层鱼类分布密度较5月和7月少,而15 m以深水层鱼类密度较5月和7月大。
2.3 水文参数对鱼类垂直分布的影响
5月库区鱼类主要分布在0~10 m水层,即温跃层以浅水层,水温在6~12 ℃(图 2-a);7月主要集中在5~15 m的温跃层以浅水层,相比于表层较高的水温,鲢、鳙更适宜中层的水温16~21 ℃;9月主要分布在10~20 m附近水层,表层的分布少,9月水温垂直梯度变化不大(18~21 ℃)。与7月相比鱼类分布的水层范围进一步扩大(图 2-c)。不同季节的DO、pH及叶绿素a质量浓度等对鲢、鳙的分布影响不明显,受温度影响较大。
3. 讨论
该研究选取夏季、初秋和春末季节进行调查,对应库区融冰对流结束(5月)、放水(7月)和储水(9月)的水体变化过程。结合各季节主要水文参数剖面和声学调查的水平及垂直鱼类目标空间分布结果,可以获得鱼类在不同季节的行为变动规律[17-19]。该方法对研究北方冬季结冰型水库湖泊鱼类资源季节变动有较好的效果。
3.1 鱼类的垂直分布特征
对于鲢、鳙的垂直分布规律,传统的捕捞经验一般认为鲢、鳙鱼类主要分布于10 m附近的水层且较大个体分布在相对较深的水层。该研究结果显示鲢、鳙主要集中在10~15 m之间的水层,这与传统经验相吻合。而

3.2 声学调查季节的选择
秋季库区蓄水,上游径流水的影响相对夏季少,库区整体水文环境较稳定,水温随深度增加变化不是明显,声学调查结果显示,整个库区鱼类回波呈均匀分散分布,无集群现象。通过对比各季节库区水文和声学调查所得数据,再结合放苗量、渔获物抽样对2012年2~5龄资源量推算所得的结果(1 513 t,未公开),秋季进行声学调查结果1 522 t与渔获物抽样推算的资源量结果基本一致,因此大伙房水库进行声学调查的最适季节为秋季。
3.3 库区声学调查与资源量评估
根据库区狭长的地形特点,该研究声学调查采用“之”字型走航方法,其优点是可以简单避开库区内设置的定置网箔。由于调查范围相对海洋调查较小,航线的断面间隔也远小于一般海洋调查[8]。从调查结果看,夏秋季节库区内的鲢、鳙基本分布较为密集和连续,调查航线基本满足随机性和相邻航线的非相关性的声学采样要求,能够较好地反映鱼类在库区内的水平和垂直分布。由于使用较小的快艇调查,航行稳定性较差,航迹线与设计航线相比存在偏差。但是考虑到夏秋季节鱼类较均匀分布的现状,对资源量评估影响不大。
《渔业资源声学调查与评估》规范[8]要求配合网具的生物采样,用于识别鱼种和确定体长分布。由于该研究中无法进行拖网采样,参考定置网箔渔获数据进行鱼种分配。但网具的大规格鱼类选择性导致评估产生误差,今后可以使用无选择性的三重刺网进行采样,配合声学调查。大伙房鱼类种类较多,约11种,根据历年的生产,鳙占52%以上,因此资源评估模型按鳙的声学参数进行,虽有一定的偏差,但考虑到其他鱼类的体长范围较大规格鲢、鳙要小很多,对较大个体鱼类资源量评估影响较小。
淡水鱼类的TS测量相对较少[10-11],现在一般参考相近鱼类或者使用理论模型进行TS计算,影响了声学资源评估的精度[4-7],该文使用公式(1)进行其他鱼种和鲢、鳙幼鱼等的体长推算也尚不够严密,还需要在今后的工作中对不同鱼种和体长的TS进行精密测量。另外,一般水库会有植物淹没而产生的小气泡,对声学调查会有一定的影响,该研究通过连续垂直分布回波(图 4的a、b型回波)的观测进行消除[20-21]。对于气泡的自动识别还需要在将来研究。图 4和图 6中的斜线规律回波为干涉噪声,来自于小型船艇的部分材料共振,在数据后处理中消除。
声学测量技术的应用提高了淡水鱼类资源分布和资源量调查的效率,且鱼类回波数据可以长期保存,通过数据的累计和对比分析可以为揭示淡水鱼类的生态行为规律提供科学依据。
-
表 1 南海圆舵鲣样本信息及D-loop区遗传多样性参数
Table 1 Specimen information of A.rochei and genetic diversity parameters based on D-loop sequences
采样点
sampling site采样时间
sampling date经度/纬度
longitude/latitude样本量(N)
number of samples单倍型数量(H)
number of haplotypes多态性位点数(S)
number of polymorphic sites单倍型多样性
(h±SD) haplotype diversity核苷酸多样性
(π±SD) nucleotide diversityA 2014-11-22 108°03′E /18°12′N 30 30 103 1.000 0±0.008 6 0.034 966±0.017 627 B 2015-03-17 112°58′E /18°29′N 42 34 130 0.958 2±0.025 3 0.037 692±0.018 765 C 2015-04-22 116°53′E /20°28′N 36 36 125 1.000 0±0.006 5 0.035 815±0.017 933 D 2013-03-27 115°32′E /11°01′N 38 35 116 0.994 3±0.008 2 0.037 030±0.018 494 E 2013-03-20 110°31′E / 5°34′N 32 32 103 1.000 0±0.007 8 0.034 327±0.017 276 F 2014-11-28 112°03′E /20°14′N 10 9 31 0.977 8±0.054 0 0.034 347±0.018 732 G 2013-04-05 117°28′E /15°04′N 13 13 83 1.000 0±0.030 2 0.041 235±0.021 749 总计 total - - 201 185 202 0.997 2±0.001 5 0.036 807±0.017 981 表 2 圆舵鲣5个地理群体D-loop区遗传变异的分子方差分析
Table 2 Analysis of molecular variance for five populations of A.rochei based on D-loop sequences
变异来源
source of variation自由度
degree of freedom变异百分比
percentage of variation分化系数
F statisticsP值
P value群体间 among populations 4 1.67 FST = 0.016 74 0.000 50 群体内 within populations 173 98.33 所有样本 total 177 表 3 圆舵鲣两两地理群体间D-loop区的遗传分化系数(对角线下方)及显著性水平(对角线上方)
Table 3 Pairwise FST (below diagonal) and P values (above diagonal) among geographic populations of A.rochei based on D-loop sequences
A B C D E A 0.004 36 0.056 23 0.327 59 0.429 86 B 0.036 45 0.001 09 0.002 48 0.005 35 C 0.015 65 0.033 77 0.847 24 0.336 11 D 0.002 12 0.034 59 -0.007 26 0.645 38 E -0.000 13 0.033 57 0.001 82 -0.003 69 表 4 圆舵鲣两两地理群体间随机交配假设检验的显著性水平
Table 4 P values of exact test of sample differentiation of A.rochei based on D-loop haplotype frequencies
A B C D B 0.000 01 C 1.000 00 0.000 01 D 0.128 85 0.000 01 0.128 70 E 1.000 00 0.001 60 1.000 00 0.112 95 表 5 圆舵鲣D-loop区序列核苷酸不配对分布分析的参数估计值
Table 5 Mismatch distribution parameter estimates for A.rochei based on D-loop sequence
核苷酸不配对分布 mismatch distribution 吻合度检验 goodness-of-fit test 扩张时间
τ初始值
θ0最终值
θ1平方和
SSD显著性
P粗糙指数
HRI显著性
PA 21.7 0.003 52 248.325 00 0.001 82 0.817 20 0.003 80 0.926 20 B 19.8 3.636 91 152.992 97 0.004 68 0.202 30 0.011 64 0.016 80 C 21.3 0.047 46 387.304 30 0.001 53 0.713 70 0.004 09 0.710 80 D 22.7 0.007 03 189.716 41 0.001 71 0.740 30 0.004 31 0.653 60 E 19.9 0.451 76 703.750 00 0.001 40 0.818 30 0.004 54 0.735 10 总计 total 21.8 0.029 88 219.521 48 0.000 37 0.680 50 0.001 35 0.831 20 表 6 圆舵鲣D-loop区序列的Tajima′s D和Fu′s FS统计值及显著性水平
Table 6 Tajima′s D, Fu′s FS statistics, corresponding P values for A.rochei based on D-loop sequences
Tajima′s D Fu′s FS D P FS P A -0.858 93 0.208 60 -15.264 13 0.000 40 B -1.044 75 0.145 60 -7.948 97 0.022 00 C -1.170 23 0.113 00 -20.597 32 0.000 01 D -0.851 71 0.203 60 -13.510 01 0.000 80 E -0.840 11 0.209 60 -17.268 99 0.000 01 总计 total -1.215 72 0.089 00 -23.701 30 0.003 60 -
[1] LAIKRE L, PALM S, RYMAN N. Genetic population structure of fishes: implications for coastal zone management[J]. Ambio, 2005, 34(2): 111-119. doi: 10.1579/0044-7447-34.2.111
[2] MCHICH R, CHAROUKI N, AUGER P, et al. Optimal spatial distribution of the fishing effort in a multi fishing zone model[J]. Ecol Model, 2006, 197(3/4): 274-280.
[3] LOESCHCKE V, TOMIUK J, JIAN S K, et al. Conservation genetics[M]. Basel: Birkhauser Veriag, 1994: 37-53.
[4] COLLETTE B B, NAUEN C E. FAO species catalogue, vol. 2. Scombrids of the world. An annotated and illustrated catalogue of tunas, mackerels, bonitos, and related species known to date[M]. FAO Fisheries Synopsis, 1983, 125: 1-137.
[5] FROESE R, PAULY D. FishBase[DB/OL]. [2016-01-25]. http://www.fishbase.se/summary/Auxis-rochei.html.
[6] FAO. Global production statistics 1950-2014, frigate and bullet tunas[R]. Rome: FAO, 2015.
[7] 晏磊, 张鹏, 杨吝, 等. 2011年春季南海中南部海域灯光罩网渔业渔获组成的初步分析[J]. 南方水产科学, 2014, 10(3): 97-103. doi: 10.3969/j.issn.2095-0780.2014.03.015 [8] 张鹏, 曾晓光, 杨吝, 等. 南海区大型灯光罩网渔场渔期和渔获组成分析[J]. 南方水产科学, 2013, 9(3): 74-79. doi: 10.3969/j.issn.2095-0780.2013.03.012 [9] 张鹏, 张俊, 李渊, 等. 秋季南海中南部海域的一次灯光罩网探捕调查[J]. 南方水产科学, 2016, 12(2): 67-74. doi: 10.3969/j.issn.2095-0780.2016.02.010 [10] 张仁斋. 圆舵鲣仔、稚鱼的形态特征和产卵期[J]. 海洋水产研究, 1984, 7 (6): 79-84. [11] 张玉玲. 圆舵鲣的生物学和渔业[J]. 动物学杂志, 1999, 34(3): 44-47. [12] 江素菲, 王德明. 闽南-台湾浅滩渔场金枪鱼类仔鱼的分布和产卵期[J]. 厦门大学学报(自然科学版), 1986, 25(4): 476-483. [13] 童铃, 金毅, 徐坤华, 等. 3种鲣鱼背部肌肉的营养成分分析及评价[J]. 南方水产科学, 2014, 10(5): 51-59. doi: 10.3969/j.issn.2095-0780.2014.05.008 [14] 李敏, 张鹏, 李玉芳, 等. 南海扁舵鲣种群遗传结构和遗传多样性评价[J]. 南方水产科学, 2015, 11(5): 82-89. doi: 10.3969/j.issn.2095-0780.2015.05.010 [15] HALL T A. BioEdit: a user-friendly biological sequence alignment editor and analysis program for Windows 95/98/NT [J]. Nucl Acids Symp, 1999, 41: 95-98.
[16] TAMURA K, STECHER G, PETERSON D, et al. MEGA6: molecular evolutionary genetics analysis Version 6.0[J]. Mol Biol Evol, 2013, 30(12): 2725-2729.
[17] POSADA D, CRANDALL K A. MODELTEST: testing the model of DNA substitution[J]. Bioinformatics (Oxford, England), 1998, 14(9): 817-818.
[18] LIBRADO P, ROZAS J. DnaSP v5: a software for comprehensive analysis of DNA polymorphism data[J]. Bioinformatics (Oxford, England), 2009, 25(11): 1451-1452.
[19] EXCOFFIER L, LISCHER H E. Arlequin suite ver 3.5: a new series of programs to perform population genetics analyses under Linux and Windows[J]. Mol Ecol Resour, 2010, 10(3): 564-567.
[20] EXCOFFIER L, SMOUSE P E, QUATTRO J M. Analysis of molecular variance inferred from metric distances among DNA haplotypes: application to human mitochondrial DNA restriction data[J]. Genetics, 1992, 131(2): 479-491.
[21] TAMURA K, NEI M. Estimation of the number of nucleotide substitutions in the control region of mitochondrial DNA in humans and chimpanzees[J]. Mol Biol Evol, 1993, 10(3): 512-526.
[22] EXCOFFIER L. Patterns of DNA sequence diversity and genetic structure after a range expansion: lessons from the infinite-island model[J]. Mol Ecol, 2004, 13(4): 853-864.
[23] RAY N, CURRAT M, EXCOFFIER L. Intra-deme molecular diversity in spatially expanding populations[J]. Mol Biol Evol, 2003, 20(1): 76-86.
[24] HARPENDING H C. Signature of ancient population growth in a low-resolution mitochondrial DNA mismatch distribution[J]. Hum Biol, 1994, 66(4): 591-600.
[25] RAMOS-ONSINS S E, ROZAS J. Statistical properties of new neutrality tests against population growth[J]. Mol Biol Evol, 2002, 19(12): 2092-2100.
[26] TAJIMA F. Statistical method for testing the neutral mutation hypothesis by DNA polymorphism[J]. Genetics, 1989, 123(3): 585-595.
[27] FU Y X. Statistical tests of neutrality of mutations against population growth, hitchhiking and background selection[J]. Genetics, 1997, 147(2): 915-925.
[28] ROGERS A R, HARPENDING H. Population growth makes waves in the distribution of pairwise genetic differences[J]. Mol Biol Evol, 1992, 9(3): 552-569.
[29] LEE W J, CONROY J, HOWELL W H, et al. Structure and evolution of teleost mitochondrial control regions[J]. J Mol Evol, 1995, 41(1): 54-66.
[30] 熊丹, 李敏, 陈作志, 等. 南海短尾大眼鲷的种群遗传结构分析[J]. 南方水产科学, 2015, 11(2): 27-34. doi: 10.3969/j.issn.2095.0780.2015.02.004 [31] ZHANG J B, CAI Z P, HUANG L G. Population genetic structure of crimson snapper Lutjanus erythropterus in East Asia, revealed by analysis of the mitochondrial control region[J]. ICES J Mar Sci, 2006, 63(4): 693-704.
[32] HAN Z Q, LI Y Z, CHEN G B, et al. Population genetic structure of coral reef species Plectorhinchus flavomaculatus in South China Sea[J]. Afr J Biotechnol, 2008, 7(11): 1774-1781.
[33] FRANKHAM R, BALLOU J D, BRISCOE D A. Introduction to conservation genetics[M]. Cambridge: Cambridge University Press, 2002: 78-104.
[34] WANG P. Response of western Pacific marginal seas to glacial cycles: paleoceanographic and sedimentological features[J]. Mar Geol, 1999, 156(1): 5-39.
[35] IMBRIE J, BOYLE E A, CLEMENS S C, et al. On the structure and origin of major glaciation cycles, 1. Linear responses to Milankovitch forcing[J]. Paleoceanography, 1992, 7(6): 701-738.
[36] WANG P. Response of western Pacific marginal seas to glacial cycles: paleoceanographic and sedimentological features[J]. Mar Geol, 1999, 156(1): 5-39.
[37] FREELAND J R. Molecular ecology[M]. Chichester: John Wiley & Sons Ltd., 2005: 112-116.
[38] WRIGHT S. The genetical structure of populations[J]. Annals of Eugenics, 1951, 15(4): 323-354.
[39] WRIGHT S. Evolution and the genetics of population: variability within and among Natural Population [M]. Chicago: University of Chicago Press, 1978: 79-103
[40] GRANT W S, BOWEN B W. Shallow population histories in deep evolutionary lineages of marine fishes: insights from sardines and anchovies and lessons for conservation[J]. J Hered, 1998, 89(5): 415-426.
[41] HEWITT G. The genetic legacy of the Quaternary ice ages[J]. Nature, 2000, 405(6789): 907-913.
[42] PALUMBI S R. Genetic divergence, reproductive isolation, and marine speciation[J]. Annu Rev Ecol Syst, 1994, 25: 547-572.
[43] 陈真然, 魏淑珍. 南海东北部海域夏季浮性鱼卵和仔稚鱼的种类组成及其分布特征[C]//南海海洋生物研究论文集(一). 北京: 海洋出版社, 1983: 192-198. [44] 张仁斋. 西沙群岛附近海区金枪鱼类仔稚鱼的调查研究报告[J]. 水产学报, 1981, 5(4): 301-315. [45] 陈真然, 魏淑珍. 南海中部海域金枪鱼类仔稚鱼的分布[J]. 水产学报, 1981, 4(1): 41-47. [46] 苏纪兰. 南海环流动力机制研究综述[J]. 海洋学报(中文版), 2005, 27(6): 1-8. [47] 苏纪兰. 中国近海水文[M]. 北京: 海洋出版社, 2005: 1-367. -
期刊类型引用(5)
1. 柯宏基,陈傅晓,李向民,樊佳伟,王永波,符书源,谭围. 基于线粒体控制区的海南岛3种弹涂鱼的遗传多样性. 热带生物学报. 2023(02): 203-213 .  百度学术
百度学术
2. 张帅,李敏,闫帅,孔啸兰,朱江峰,徐姗楠,陈作志. 基于线粒体Cyt b基因序列的棘头梅童鱼种群遗传结构. 中国水产科学. 2021(01): 90-99 .  百度学术
百度学术
3. 范江涛,张鹏,冯雪,陈作志. 南海圆舵鲣栖息地影响因素分析. 中国水产科学. 2021(02): 215-221 .  百度学术
百度学术
4. 李敏,黄梓荣,许友伟,陈作志. 基于线粒体cytb序列的花斑蛇鲻种群遗传结构研究. 南方水产科学. 2019(06): 41-48 .  本站查看
本站查看
5. 王桢璐,姚东林,谢少林,范兰芬,邹记兴,周爱国. 基于线粒体Cyt b和COⅠ基因序列的华南鲤群体遗传结构分析. 江苏农业科学. 2018(18): 179-183 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载:









 粤公网安备 44010502001741号
粤公网安备 44010502001741号
