Regulation of Bacillus cereus to microalgae community in shrimp aquaculture water
-
摘要:
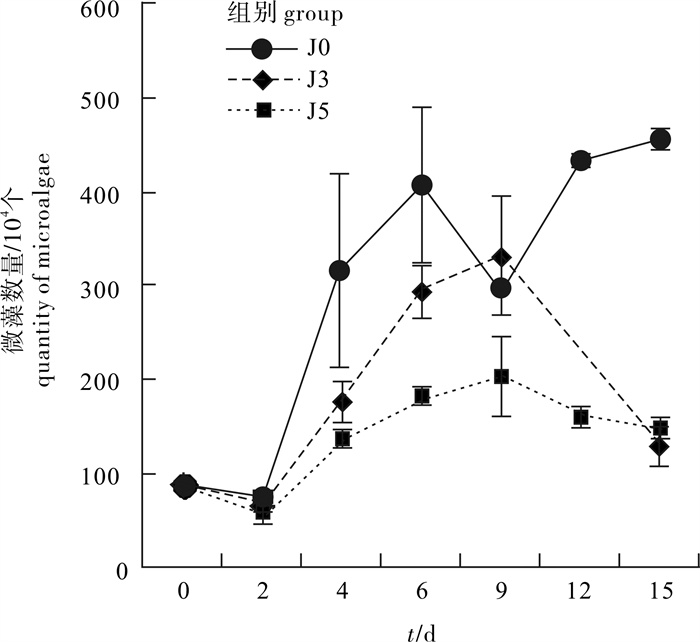
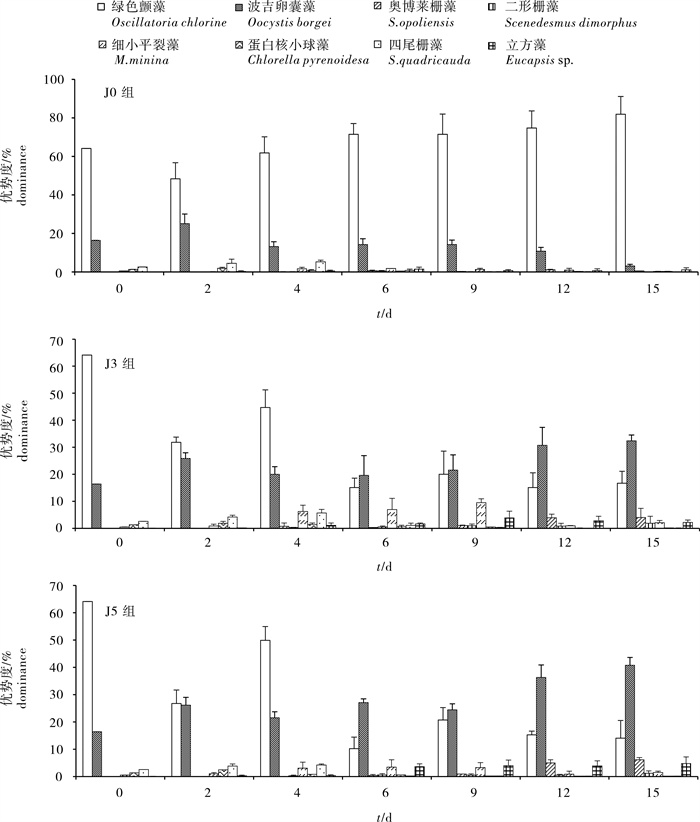
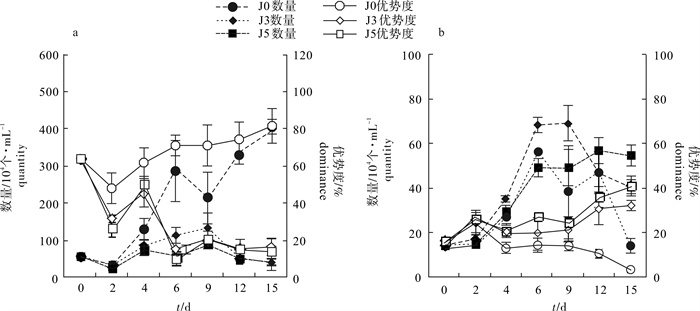
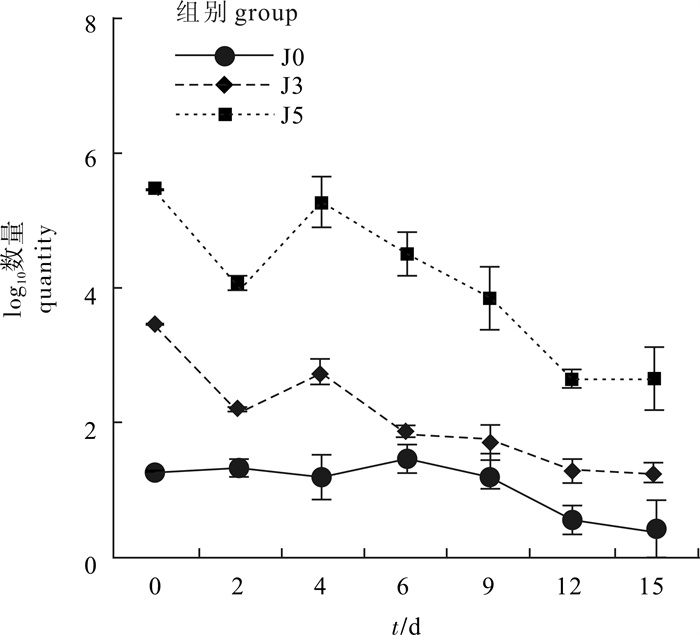
运用实验生态学方法分析了溶藻细菌——蜡样芽孢杆菌(Bacillus cereus)CZBC1对对虾养殖水体微藻群落的影响。根据用菌量,实验分为J0组(不施菌)、J3组(用菌量3.00×103 CFU · mL-1)和J5组(用菌量3.00×105 CFU · mL-1),每组3个平行,各实验水体优势种绿色颤藻(Oscillatoria chlorine)和波吉卵囊藻(Oocystis borgei)的初始优势度为64.14%和16.42%,实验周期15 d。结果显示,经过15 d的实验,J0组绿色颤藻优势度显著高于J3组和J5组(P<0.01),波吉卵囊藻优势度显著低于J3组和J5组(P<0.01)。其中,J0组绿色颤藻优势度升高至81.86%,J3组和J5组则分别降低至16.7%和14.6%;J0组波吉卵囊藻优势度降低至3.13%,J3组和J5组则分别升高至32.42%和47.14%。J0组、J3组和J5组对虾死亡率在第6天时分别为82.2%、46.7%和31.1%,J0组显著高于J3组和J5组(P<0.01),第15天时J0组仍然高于J3组和J5组。可见,CZBC1可有效抑制绿色颤藻(蓝藻)的生长,从而为波吉卵囊藻(绿藻)占据生态优势提供有利空间,为养殖对虾提供良好的水生态环境。
Abstract:We analyzed the effect of Bacillus cereus (algicidal bacteria CZBC1) on microalgae community in shrimp aquaculture water by method of experimental ecology. According to the algicidal bacteria amount,we set Group J0 (0 CFU · mL-1),Group J3 (3.0×103 CFU · mL-1) and Group J5 (3.0×105 CFU · mL-1) with three parallels. The initial dominances of Oscillatoria chlorine and Oocystis borgei,the dominant species in water,were 64.14% and 16.42%,respectively. The results show that the dominance of O.chlorine in Group J0 was significantly higher than those in Group J3 and Group J5 after 15-day culture (P<0.01),and their dominances were 81.86%,16.7% and 14.6%,respectively. While the dominance of O.borgei in Group J0 was significantly lower than those in Group J3 and Group J5 (P<0.01),and their dominances were 3.13%,32.42% and 47.14%,respectively. The mortality of shrimp in Group J0 was significantly higher than those in Group J3 and Group J5 on the 6th day (P<0.01),which were 82.2%,46.7% and 31.1%,respectively. Furthermore,the mortality in Group J0 was also higher than those in Group J3 and Group J5 on the 15th day. The results indicate that algicidal bacteria CZBC1 can inhibit the growth of O.chlorine (Cyanophyta) effectively,which helps occupy the ecological advantage for O.borgei (Chlorophyta),providing better water environment for the growth of shrimp.
-
Keywords:
- algicidal bacteria /
- Oscillatoria /
- microalgae /
- community
-
广东鲂 (Megalobrama terminalis) 是一种江河洄游鱼类,在我国南方水系中占有重要的渔业生产地位[1-2]。我国南方水系复杂多样,并经历了多次河流袭夺,而气候变化导致的海平面波动是形成其特有河网系统的重要因素之一[3]。由于广东鲂对淡水环境依赖性较强,因此,海平面波动产生的地理隔离,对广东鲂种群的遗传结构产生了一定影响。Chen等[3]指出3个广东鲂地理遗传种群分别为珠江、漠阳江和海南岛万泉河种群,并发现广东鲂种群在不同的淡水栖息地中表现出明显的适应性分化。刘凯等[4]研究表明,受地理分布、食物来源、遗传特征和栖息环境等因素的叠加影响,鱼类的不同地理种群在肌肉营养成分上能够产生相对稳定的变异。然而,不同广东鲂地理种群肌肉营养成分是否存在显著差异尚不清楚。目前,对广东鲂研究多在于早期资源、资源捕捞量、性腺发育、繁殖策略、消化生理等方面[1-3,5-8],针对不同广东鲂种群肌肉营养成分和能量密度的研究尚未见报道。由于人类活动的不断加强 (如水利水电工程、航道治理、水污染、过度捕捞等),珠江野生广东鲂种群数量持续下降[2,7-8],漠阳江和万泉河广东鲂种群则呈现规模小、片段化分布特征,在其他陆河河流如榕江、鉴江、韩江中已难以监测到野生样本。因此,本研究测定了万泉河、漠阳江、西江广东鲂种群肌肉营养成分和能量密度,探究不同地理广东鲂种群肌肉营养成分差异,以期充实鱼类营养学和能量生态学研究材料,也为不同广东鲂的野生地理种群的分类保护和合理利用提供科学依据。
1. 材料与方法
1.1 样本采集
2020年6—7月分别于海南省琼海市万泉河琼海段 (QH, 110°27"36'E, 19°12"36'N)、广东省阳江市漠阳江段 (YJ, 111°42"2'E, 22°48"7'N) 以及广东省肇庆市珠江干流 (西江) 肇庆江段 (ZQ, 112°24"35'E, 23°5"24'N) 采集到150尾广东鲂,各采样点50尾 (雌、雄各25尾) 。采用哈希水质分析仪测量取样点的水温、盐度、溶解氧 (Dissolved oxygen, DO) 和pH,并测量样品的体长和体质量。采样站位的环境信息和样本生物学信息见表1。采用液氮快速冷冻样本,于–20 ℃冷冻保存,随后带回实验室−80 ℃保存。采集背部中后段肌肉 (每尾在相同位置采集20 g肌肉) 用于检测肌肉成分。各项指标由广东省质量监督食品检验站进行检测,各实验组均设置3个重复,每个重复含10尾样本 (背部肌肉捣碎)。
表 1 3个广东鲂地理种群环境信息和样本生物学信息Table 1. Basic environmental information, biological information of three M. terminalis populations指标
Index采样点 Sampling site 琼海 QH 阳江 YJ 肇庆 ZQ 环境指标 Environmental index 水温 Water temperature/℃ 30.0±0.2 29.2±0.4 28.6±0.3 盐度 Salinity 0.03±0.01 0.01±0.02 0.01±0.01 酸碱度 pH 7.7±0.3 7.9±0.3 7.8±0.3 溶解氧质量浓度 DO/(mg∙L−1) 6.8±0.2 6.7±0.2 7.0±0.2 生物学指标 Biological index 体长 Body length ($\overline { X}\pm { \rm {SD}} $)/mm 233±17.6 253±20.7 271±27.3 体质量 Body mass ($\overline { X}\pm { \rm {SD}} $)/g 354±19.4 424±33.1 521±30.1 1.2 肌肉营养成分和能量密度测定方法
样本水分测定采用GB 5009.3—2016;粗蛋白测定采用GB 5009.5—2016;脂肪测定采用GB 5009.4—2016;灰分测定采用GB 5009.4—2016;氨基酸测定采用GB T5009.124—2016;脂肪酸测定采用GB 5009.168—2016。采用电感耦合等离子体质谱仪 (7700 Series) 依据GB 5009—2016测定样本中钾 (K)、钙 (Ca)、钠 (Na)、磷 (P)、镁 (Mg)、锌 (Zn)、铁 (Fe)、铜 (Cu)、锰 (Mn) 等矿质元素含量。根据联合国粮农组织/世界卫生组织 (FAO/WHO) 提出和1991年中国预防医学科学院营养与食品卫生研究所提出的氨基酸评分模式,计算氨基酸评分 (Amino acid score, AAS)、化学评分 (Chemical score, CS) 和必需氨基酸指数 (Essential amino acid index, EAAI) [9-10]。Phillipson微量能量仪 (Gentry Instruments Inc., Aiken, South Carolina, USA) 测定能量密度。
1.3 数据分析
采用单因素方差分析 (One-way ANOVA) 检验不同广东鲂地理种群肌肉营养成分差异显著性。如差异显著,则采用多重比较方法比较平均数之间的差异,显著性水平为0.05。数据分析采用SPSS 19.0统计软件进行。实验数据均用“平均值±标准差 (
$\overline X \pm {\rm{SD}} $ )”表示。采用R (3.1.14) 对3个广东鲂种群肌肉生化分析结果进行主成分分析 (Principal component analysis, PCA)。2. 结果
2.1 一般营养成分和能量密度分析
万泉河广东鲂肌肉水分质量分数显著高于西江种群,而粗蛋白质质量分数则显著低于西江种群 (P<0.05,表2)。粗脂肪和灰分质量分数在3个地理种群中均无显著性差异。西江种群肌肉能量密度显著高于万泉河和漠阳江种群 (P<0.05)。
表 2 3个广东鲂地理种群肌肉中的一般营养成分和能量密度Table 2. Nutritional composition of muscle of three M. terminalis populations项目
Item广东鲂种群 M. terminalis population 琼海 QH 阳江 YJ 肇庆 ZQ 水分质量分数 Moisture mass fraction/% 79.0±0.5a 78.2±0.9ab 77.0±0.6b 粗蛋白质质量分数 Crude protein mass fraction/% 18.3±0.5b 19.1±0.7ab 20.2±0.5a 粗脂肪质量分数 Crude lipid mass fraction/% 1.2±0.1 1.1±0.1 1.3±0.1 粗灰分质量分数 Ash mass fraction/% 1.1±0.1 1.2±0.1 1.2±0.1 能量密度 Energy density/(kJ·g−1) 3.1±0.1b 3.2±0.2b 3.6±0.2a 注:同行不同上标字母表示差异显著 (P<0.05),下表同此。 Note: Different superscript letters within the same row indicate significant difference (P<0.05). The same case in the following tables. 2.2 氨基酸组成分析与评价
3个广东鲂地理种群共检测出18种常见氨基酸 (表3)。西江种群肌肉中的总氨基酸含量 (Total amino acids, TAA) 最高,漠阳江种群次之,万泉河种群最低。在必需氨基酸 (Essential aamino acid, EAA) 中,西江种群的赖氨酸和亮氨酸含量显著高于万泉河种群 (P<0.05),漠阳江种群介于两者之间。呈味氨基酸中,西江种群肌肉中的天冬氨酸、谷氨酸、甘氨酸和丙氨酸含量均显著高于万泉河种群 (P<0.05)。漠阳江种群肌肉中必需氨基酸/总氨基酸 (EAA/TAA) 最高,而西江种群最低。呈味氨基酸/总氨基酸 (DAA/TAA) 在3个广东鲂地理种群肌肉中无明显差异。芳香氨基酸/支链氨基酸 (BCAA/AAA) 在万泉河种群肌肉中最高,漠阳江种群次之,西江种群最低。将3个广东鲂地理种群肌肉的EAAI进行标准模式 (FAO/WHO) 及全鸡蛋蛋白质模式2种评价 (表3),分别计算出各EAA的AAS、CS和EAAI (表4)。万泉河、漠阳江和西江种群肌肉中的第一限制性氨基酸为蛋氨酸+半胱氨酸,第二限制性氨基酸为缬氨酸,其余各EAA的AAS均高于1;各EAA的CS与AAS结果保持一致。3个广东鲂地理种群肌肉中的EAAI达80以上,说明其氨基酸组成十分均衡。其中西江种群肌肉EAAI最高 (85.05)。
表 3 3个广东鲂地理种群肌肉氨基酸组成Table 3. Comparison of amino acid composition of muscles of three M. terminalis populations项目
Item广东鲂种群 M. terminalis population 琼海 QH 阳江 YJ 肇庆 ZQ 天冬氨酸* Asp 1.80±0.04b 1.82±0.07b 1.99±0.05a 苏氨酸# Thr 0.80±0.02 0.80±0.03 0.86±0.04 丝氨酸 Ser 0.72±0.02 0.73±0.03 0.80±0.04 谷氨酸* Glu 2.78±0.06b 2.68±0.10b 2.99±0.14a 脯氨酸 Pro 0.61±0.02 0.63±0.02 0.66±0.04 甘氨酸* Gly 0.83±0.04b 0.87±0.04ab 0.97±0.06a 丙氨酸* Ala 1.06±0.02b 1.09±0.03b 1.18±0.08a 缬氨酸#△ Val 0.85±0.02 0.87±0.03 0.92±0.04 蛋氨酸 Met 0.53±0.01 0.53±0.02 0.57±0.03 异亮氨酸#△ Ile 0.78±0.02 0.79±0.02 0.83±0.03 亮氨酸#△ Leu 1.41±0.03b 1.41±0.05ab 1.52±0.05a 半胱氨酸 Cys 0.11±0.07 0.19±0.03 0.43±0.15 酪氨酸◆ Tyr 0.62±0.02 0.61±0.02 0.66±0.02 苯丙氨酸# Phe 0.72±0.02 0.74±0.02 0.80±0.03 赖氨酸# Lys 1.73±0.05a 1.73±0.09ab 1.87±0.03b 组氨酸○ His 0.42±0.01 0.45±0.04 0.48±0.05 精氨酸○ Arg 1.07±0.04 1.07±0.04 1.17±0.07 色氨酸# Trp 0.27±0.04 0.35±0.03 0.37±0.05 氨基酸总量 TAA 17.11±0.58a 17.37±0.69a 19.07±0.57b 呈味氨基酸总量 DAA 6.47±0.06a 6.46±0.08a 7.13±0.07b 必需氨基酸/非必需氨基酸 EAA/NEAA/% 72.41 73.03 69.95 必需氨基酸/总氨基酸 EAA/TAA/% 38.34 38.51 37.60 半必需氨基酸/总氨基酸 SEAA/TAA/% 8.36 8.41 8.26 芳香氨基酸/支链氨基酸 BCAA/AAA/% 4.90 5.03 4.05 注:#. 必需氨基酸;○. 半必需氨基酸;*. 呈味氨基酸;△. 支链氨基酸;◆. 芳香氨基酸。 Note: #. Essential amino acid; ○. Semiessential amino acid; *. Delicious amino acid; △. Branched chain amino acid; ◆. Aromatic amino acid. 表 4 3个广东鲂地理种群肌肉氨基酸评价Table 4. Evaluation of essential amino acids composition of muscle of three M. terminalis populations评价模式
Evaluation method氨基酸
Amino acids广东鲂种群 M. terminalis population 琼海 QH 阳江 YJ 肇庆 ZQ 氨基酸评分 AAS 苏氨酸 Thr 1.09 1.05 1.07 缬氨酸 Val 0.94 0.92 0.92 色氨酸 Trp 1.53 1.91 1.91 异亮氨酸 Ile 1.06 1.03 1.03 亮氨酸 Leu 1.09 1.05 1.07 赖氨酸 Lys 1.73 1.66 1.70 苯丙氨酸 Phe+酪氨酸 Tyr 1.20 1.17 1.19 蛋氨酸 Met+半胱氨酸 Cys 0.82 0.78 0.80 化学评分 CS 苏氨酸 Thr 0.93 0.90 0.91 缬氨酸 Val 0.71 0.69 0.69 色氨酸 Trp 0.96 1.24 1.31 异亮氨酸 Ile 0.80 0.78 0.78 亮氨酸 Leu 0.90 0.86 0.88 赖氨酸 Lys 1.34 1.28 1.31 苯丙氨酸 Phe+酪氨酸 Tyr 0.81 0.78 0.80 蛋氨酸 Met+半胱氨酸 Cys 0.47 0.45 0.46 必需氨基酸指数 EAAI 83.31 83.37 85.05 2.3 脂肪酸组成分析
3个广东鲂地理种群肌肉中共检测出23种常见脂肪酸 (表5),其中包括7 种饱和脂肪酸 (Saturated fatty acid, SFA) 7种单不饱和脂肪酸 (Monounsaturated fatty acid, MUFA) 和9种多不饱和脂肪酸 (Polyunsaturated fatty acids, PUFA)。SFA中C14:0、C16:0和C22:0在万泉河种群肌肉中的含量显著高于漠阳江和西江种群 (P<0.05)。万泉河种群肌肉中MUFA总量显著低于西江和漠阳江种群 (P<0.05)。其中,C16:1、C18:1 n-9t、C18:1 n-9c漠阳江种群肌肉中含量最高,而在万泉河种群肌肉中含量最低。C22:1 n-9、C24:1在漠阳江种群肌肉中含量显著低于西江和万泉河种群。西江种群肌肉中二十二碳六希酸 (DHA) 含量最高,显著高于万泉河和漠阳江种群 (P<0.05)。PUFA在万泉河种群肌肉中含量最高,西江种群次之,漠阳江种群最低。
表 5 3个广东鲂地理种群肌肉脂肪酸组成Table 5. Comparison of fatty acids of muscles of three M. terminalis populations% 项目
Item广东鲂种群 M. terminalis population 琼海 QH 阳江 YJ 肇庆 ZQ 肉豆蔻酸 C14:0 5.36±0.85a 3.53±0.41b 3.40±0.32b 十五碳酸 C15:0 1.02±0.25 0.66±0.05 0.70±0.13 棕榈酸 C16:0 27.33±1.47 a 21.83±1.16 b 21.80±1.99 b 珠光脂酸 C17:0 2.03±0.35 0.99±0.18 1.13±0.33 硬脂酸 C18:0 11.34±1.79a 5.97±1.03b 8.14±1.65ab 花生酸 C20:0 0.29±0.05a 0.15±0.02b 0.21±0.07ab 花生酸 C22:0 0.30±0.08a 0.10±0.01c 0.17±0.01b ∑饱和脂肪酸 SFA 47.67±2.12a 33.23±2.85b 35.56±4.35b 肉豆蔻烯酸 C14:1 0.06±0.02 0.12±0.02 0.08±0.01 棕榈油酸 C16:1 6.21±1.22b 10.45±1.73a 8.10±0.52ab 顺-11-二十碳一烯酸 C20:1 2.32±0.36 1.85±0.08 2.06±0.15 顺-15-二十四碳一烯酸 C24:1 0.27±0.09a 0.06±0.01b 0.24±0.10a 反式油酸 C18:1 n-9t 0.21±0.05b 0.43±0.07a 0.35±0.07ab 油酸 C18:1 n-9c 16.73±3.87b 35.53±4.35a 31.80±3.65a 二十二碳一烯酸 C22:1 n-9 1.09±0.36a 0.11±0.03b 1.03±0.61a ∑单不饱和脂肪酸 MUFA 26.89±3.93a 48.54±5.20b 43.66±7.08b 亚油酸 C18:2 n-6c 4.30±0.64a 2.23±0.33b 1.59±0.64b α-亚麻酸 C18:3 n-3 5.54±0.86a 4.03±1.56ab 2.35±0.51b γ-亚麻酸 C18:3 n-6 0.14±0.02a 0.08±0.02ab 0.01±0.00b 顺,顺-11,14-二十碳二烯酸 C20:2 0.39±0.08 0.34±0.01 0.36±0.04 顺-11,14,17-二十碳三烯酸 C20:3 n-3 0.32±0.05 0.27±0.06 0.21±0.08 顺,顺,顺-8,11,14-二十碳三烯酸 C20:3 n-6 0.39±0.09a 0.22±0.03b 0.14±0.01c 花生四烯酸 C20:4 n-6 (ARA) 5.27±0.89a 2.94±0.42b 4.88±0.95a 二十碳五烯酸 C20:5 n-3 (EPA) 3.16±0.72 4.06±0.10 4.09±0.87 二十二碳六烯酸 C22:6 n-3 (DHA) 5.74±1.03b 3.95±0.13c 7.03±1.28a ∑多不饱和脂肪酸 PUFA 25.11±2.83a 18.04±2.47b 20.64±5.61ab 2.4 矿质元素组成分析
3个广东鲂地理种群肌肉中均含有丰富的矿质元素,其中K质量分数最高,Ca次之 (表6)。西江种群肌肉中K和Ca质量分数显著高于万泉河种群,而Na和Mg质量分数则显著低于万泉河种群 (P<0.05)。万泉河种群肌肉Zn质量分数显著高于漠阳江和西江种群,而Mn和Fe质量分数显著低于漠阳江和西江种群 (P<0.05)。
表 6 3个广东鲂地理种群肌肉矿质元素组成Table 6. Mineral element of muscle of three M. terminalis populationsmg∙kg−1 元素
Element广东鲂种群 M. terminalis population 琼海 QH 阳江 YJ 肇庆 ZQ 钾 K 3 340.05±105.36b 3 460.04±192.92ab 3 820.36±221.12a 钙 Ca 1 050.12±28.87 b 1 100.25±40.02 ab 1 200.11±34.64 a 钠 Na 487.34±58.96a 345.35±7.23b 385.57±30.66b 镁 Mg 298.65±3.79 303.05±2.65 332.31±5.51 磷 P 241.59±25.97 230.45±2.08 247.78±4.04 锌 Zn 6.47±0.15a 4.16±0.18b 3.82±0.17b 铁 Fe 3.06±0.13c 4.75±0.14b 6.43±0.18a 铜 Cu 0.12±0.00 0.12±0.01 0.13±0.01 锰 Mn 0.21±0.01c 0.38±0.02b 0.64±0.01a 2.5 3个广东鲂种群生化分析结果的主成分分析
综合3个广东鲂种群生化分析结果,并进行PCA。西江种群分布距均万泉河和漠阳江种群较远,万泉河种群和漠阳江种群相对较近。PCA共提取了2个主成分,对变异的累积贡献率为80.25%。其中主成分1的贡献率为50.75%,主成分2的为29.50% (图1)。
3. 讨论
鱼类肌肉中蛋白质和脂肪含量是评价其营养价值的重要指标[11]。3 个广东鲂地理种群肌肉的粗蛋白质量分数 (18.3%~20.2%) 高于团头鲂 (Megalobrama amblycephala)、鲤 (Cyprinus carpio)、鲢 (Hypophthalmichthys molitrix)、鳙 (H. nobilis) 和草鱼 (Ctenopharyngodon idella),与翘嘴鲌 (Culter alburnus) 接近[12-13]。3个广东鲂地理种群肌肉粗脂肪质量分数 (1.1%~1.3%) 较团头鲂、翘嘴鲌、鲢、鳙、斑鳜 (Siniperca scherzeri) 等低[12-14],与常见的海水鱼类如牙鲆 (Paralichthys olivaceus)[15]、黄斑篮子鱼 (Siganus oramin)[16]和日本鳗鲡 (Anguilla japonica)[17]类似,表现出典型的低脂肪、高蛋白的特点。本研究发现,3个广东鲂种群肌肉生化PCA结果显示西江种群分布距万泉河和漠阳江种群较远,可能是由于栖息地环境因子以及饵料生物种类存在明显差异。本研究还发现,西江种群能量密度显著高于漠阳江和万泉河种群。能量密度被认为是衡量鱼体能量储备水平的重要指标,能直接反映鱼类发育状况以及对外界环境因子的适应性[18]。鱼类生殖洄游是主动的、定期定向的高耗能运动,且鱼体自身能量储备有限,因此鱼类洄游须尽可能地调节自身身体结构、能量储备和代谢能力以适应生殖洄游的需要[19-20]。3个广东鲂种群生殖洄游距离存在明显差异,可能是导致种群间肌肉中能源物质的积累程度不同的主要原因之一。有研究发现鱼类肌肉能量累积和消耗与其洄游能力密切相关[21-22]。
鱼类肌肉中蛋白质的营养价值由各种EAA含量和组成比例决定[23-24]。本研究显示,在3个广东鲂种群肌肉中谷氨酸含量均最高,谷氨酸作为一种重要呈味氨基酸,具有促进脑发育、治疗神经系统疾病等作用[25]。3个广东鲂种群肌肉中谷氨酸含量均高于团头鲂与翘嘴鲌[12]。西江种群肌肉中谷氨酸含量显著高于漠阳江和万泉河种群,表明西江种群肌肉较万泉河和漠阳江种群风味更佳。3个广东鲂种群肌肉中赖氨酸含量均较高,其中,西江种群肌肉中赖氨酸含量最高。赖氨酸是人体EAA之一,不仅具有提高蛋白质利用率和促进人体生长发育的作用,还可以增强免疫力、改善神经系统、预防骨质疏松[24,26]。在FAO/WHO提出的人体均衡蛋白需求理想模式中,EAA/NEAA>60%的蛋白质质量较好[27],3个野生广东鲂种群肌肉均属于良好的蛋白源。西江种群肌肉中的EAAI最高 (85.05),说明其肌肉中EAA组成最为平衡,蛋白质营养价值最高。肌肉中的脂肪酸含量是影响肌肉风味的重要因素之一[28]。本研究发现,西江和漠阳江种群肌肉均表现出MUFA的高占比。有研究表明,MUFA在调节人体脂质代谢方面具有重要的生理作用[29]。PUFA中DHA与EPA含量是评价鱼类营养成分的关键指标[30]。西江种群肌肉中的DHA含量显著高于漠阳江和万泉河种群,表明西江种群肌肉的脂肪质量较高。
矿物质元素是构成人体组织的重要成分,参与人体内多种物质的代谢和生理活动[31]。3个广东鲂种群肌肉中Na、K、Ca等常规矿质元素以及Fe、Zn、Cu、Mn等微量元素均有检出。K、Fe、Zn等矿质元素含量低于异齿裂腹鱼 (Schizothoraxo connori)[32]。Ca含量显著高于褐点石斑鱼 (Epinephelus fuscoguttatus) 和青石斑鱼 (E. awoara) 等多种海鱼[31]。西江种群肌肉中Fe含量显著高于漠阳江和万泉河种群,而Zn含量则显著低于万泉河种群。Fe具有造血功能和促进人体生长的作用等,Zn可以促进儿童智力的正常发育[33]。3个广东鲂地理种群肌肉多种微量元素含量差异显著,这可能是由于栖息水环境的差异所致。万泉河种群相对西江种群,其主要栖息水域为河口,盐度相对较高,易受潮汐影响。有研究发现淡水环境中Fe含量均显著高于海水,Zn含量明显低于海水环境[34-35]。因此,栖息地环境差异导致了Zn在万泉河种群肌肉中富集度更高,Fe和Mn则在西江种群肌肉中富集度更高。
-
表 1 起始实验水体浮游微藻种类及丰富度
Table 1 Species and richness of microalgae in initial experimental water
种类
species丰富度
richness种类
species丰富度
richness蓝藻门(Cyanophyta) 狭形纤维藻(A.angustus) + 绿色颤藻(Oscillatoria chlorine) +++ 多芒藻(Golenkinia radiata) + 铜绿微囊藻(Microcystis aeruginosa) + 中华螺翼藻(Scotiella fristch) + 水华微囊藻(M.floslutea) + 微芒藻(Micractinium pusillum) + 点形平裂藻(Merismopedia punctata) + 斜生栅藻(Scenedesmus obliqnus) + 细小平裂藻(M.minina) + 棘球藻(Echinosphaerella limnetica) + 微小色球藻(Chroococcus minutus) + 针形纤维藻(A.acicularis) + 立方藻(Eucapsis sp.) + 湖生卵囊藻(O.lacustris) + 微小隐球藻(Aphanocapsa delicatissima) + 硅藻门(Bacillariophyta) 大螺旋藻(Spirulina major) + 线形菱形藻(Nitzschia linearis) + 绿藻门(Chlorophyta) 新月菱形藻(N.closterium) + 波吉卵囊藻(Oocystis borgei) +++ 奥尔韦舟形藻(Navicula bacillum) + 蛋白核小球藻(Chlorella pyrenoidesa) ++ 谷皮菱形藻(N.palea) + 二形栅藻(Scenedesmus dimorphus) + 牟氏角毛藻(Chaetoceros muelleri) + 四尾栅藻(S.quadricauda) ++ 条纹小环藻(Cyclotella striata) + 奥波莱栅藻(S.opoliensis) + 披针形桥弯藻( Cymbella lanceolata) + 卷曲纤维藻(Ankistrodesmus convolutus) + 甲藻门(Dinophyta) 三角四角藻(Tetra dron trigonum) + 二角多甲藻(Peridinium bipes) + 螺带鼓藻(Spirotaenia condensata) + 裸藻门(Euglenophyta) 双对栅藻交错变种(Scenedesmus bijuga) + 绿色裸藻(Euglena viridia) + 四角十字藻(Crucigenia quadrata) + 注:+代表稀有种;+ +代表常见种;+ + +代表优势种
Note:“+” indicates dominant species;“+ +” indicates common species;“+ + +” indicates rare species -
[1] 彭聪聪.南方半集约化养殖池塘微藻群落特征及其与水质因子关系研究[D]. 上海: 上海海洋大学, 2011: 1-56. https://xueshu.baidu.com/usercenter/paper/show?paperid=bd56ba2d8059495b7c3c14d143486086 [2] 刘孝竹, 李卓佳, 曹煜成, 等. 低盐度养殖池塘常见浮游微藻的种类组成、数量及优势种群变动[J]. 南方水产, 2009, 5(1): 9-16. doi: 10.3969/j.issn.1673-2227.2009.01.002 [3] 周亚, 李万文, 王敬, 等. 养殖水体蓝藻水华的防治[J]. 农业灾害研究, 2013, 3(4): 48-49. https://apps.wanfangdata.com.cn/perios/article:nyzhyj201304017 [4] 赵以军, 刘永定. 有害藻类及其微生物防治的基础──藻菌关系的研究动态[J]. 水生生物学报, 1996, 20(2): 173-181. http://qikan.cqvip.com/Qikan/Article/Detail?id=2145734 [5] 裴海燕, 胡文容, 曲音波, 等. 一株溶藻细菌的分离鉴定及其溶藻特性[J]. 环境科学学报, 2005, 25(6): 796-802. doi: 10.3321/j.issn:0253-2468.2005.06.015 [6] 王祥荣, 胡欢, 母锐敏, 等. 1株铜绿微囊藻降解菌的分离鉴定及其溶藻特征[J]. 复旦学报(自然科学版), 2010, 49(1): 94-98. https://xueshu.baidu.com/usercenter/paper/show?paperid=3341c522cee494839944d32267785d77&site=xueshu_se [7] YANG Y F, HU X J, ZHANG J, et al. Community level physiological study of algicidal bacteria in the phycosphere of Skeletonema costatum and Scrippsiella trochoidea[J]. Harmful Algae, 2013, 28: 88-96. doi: 10.1016/j.hal.2013.05.015
[8] SOMDEE T, SUMALAI N, SOMDEE A. A novel actinomycete Streptomyces aurantiogriseus with algicidal activity against the toxic cyanobacterium Microcystis aeruginosa[J]. J Appl Phycol, 2013, 25(5): 1587-1594. doi: 10.1007/s10811-013-9999-1
[9] KEAWTAWEE T, FUKAMI K, SONGSANGJINDA P. Use of a Noctiluca-killing bacterium Marinobacter salsuginis strain BS2 to reduce shrimp mortality caused by Noctiluca scintillans[J]. Fish Sci, 2012, 78(3): 641-646. doi: 10.1007/s12562-012-0497-1
[10] 贾雯, 黄翔鹄, 李长玲, 等. 侧孢短芽孢杆菌溶藻活性代谢产物对虾池颤藻的溶藻效果[J]. 水产学报, 2013, 37(3): 465-472. https://xueshu.baidu.com/usercenter/paper/show?paperid=53074ec9b68e5fc2760d4f0ce9bb6691&site=xueshu_se&hitarticle=1 [11] 曹煜成, 王丽花, 文国樑, 等. 一种溶解池塘颤藻的蜡样芽胞杆菌菌株CZBC1及其应用: ZL201310203745.3[P]. 2014-12-17. https://xueshu.baidu.com/usercenter/paper/show?paperid=6c172dc1aeae7b847f54e53b1201ae8e&site=xueshu_se [12] 李煜, 赵素娟, 张鹏, 等. 17株蜡样芽孢杆菌安全性评价[J]. 毒理学杂志, 2012, 26(3): 233-235. https://xueshu.baidu.com/usercenter/paper/show?paperid=3114f35fe34ec3aaaf2ea19bda934a36&site=xueshu_se&hitarticle=1 [13] 李侠, 徐华, 詹玲, 等. 蜡样芽孢杆菌活菌制剂与蒙脱石联合治疗小儿病毒性腹泻[J]. 中国新药与临床杂志, 2001, 20(5): 396-398. doi: 10.3969/j.issn.1007-7669.2001.05.030 [14] 蒋光吉, 徐云, 傅红春, 等. 蜡样芽孢杆菌治疗对肝硬化患者肠道菌群的影响及其意义研究[J]. 西南国防医药, 2008, 18(2): 180-181. doi: 10.3969/j.issn.1004-0188.2008.02.010 [15] 阳钢. 几种微生态制剂对刺参养殖水体及刺参肠道菌群结构的影响[D]. 青岛: 中国海洋大学, 2012: 18-37. https://xueshu.baidu.com/usercenter/paper/show?paperid=175f841e93e84ded09577f68badfc291&site=xueshu_se [16] 何鉴尧, 潘伟斌, 林敏. 溶藻细菌对富营养化水体藻类群落结构的影响[J]. 环境污染与防治, 2008, 30(11): 70-74. doi: 10.3969/j.issn.1001-3865.2008.11.017 [17] 王丽花. 虾池有害蓝藻藻际溶藻细菌的筛选及溶藻效应[D]. 大连: 大连海洋大学, 2012: 1-59. [18] 曹煜成. 虾池微藻优势种群调控机理[D]. 广州: 中山大学, 2014: 98-112. [19] 彭聪聪, 李卓佳, 曹煜成, 等. 斑节对虾滩涂养殖池塘浮游微藻群落演变特征[J]. 安全与环境学报, 2012, 12(5): 95-101. doi: 10.3969/j.issn.1009-6094.2012.05.021 [20] 中华人民共和国卫生部. GB/T4789.14-2003食品卫生微生物学检验-蜡样芽孢杆菌检验[S]北京: 中国标准出版社, 2006: 3-6. [21] 胡鸿钧, 魏印心. 中国淡水藻类[M]. 北京: 科学出版社, 2006: 1-1023. https://xueshu.baidu.com/usercenter/paper/show?paperid=0811d270a919bdc44fa61ce8e4ad990d [22] 郭玉洁, 钱树本. 中国海藻志: 第五卷第一册[M]. 北京: 科学出版社, 2003: 1-493. https://xueshu.baidu.com/usercenter/paper/show?paperid=7d4fd5803146c942ed239191f2fa7247&site=xueshu_se [23] 沈国英, 施并章. 海洋生态学[M]. 厦门: 厦门大学出版社, 1990: 158-159. https://xueshu.baidu.com/usercenter/paper/show?paperid=358c512581341647de3eb0cd4b368df1&site=xueshu_se [24] 麦雄伟. 南美白对虾温棚化养殖水体生态特征研究[D]. 广州: 中山大学, 2003: 10-11. https://xueshu.baidu.com/usercenter/paper/show?paperid=e83f29592884bb89304c9799ffb0142c&site=xueshu_se&hitarticle=1 [25] 李东, 李祎, 郑天凌. 海洋溶藻功能菌作用机理研究的若干进展[J]. 地球科学进展, 2013, 28(2): 243-252. https://xueshu.baidu.com/usercenter/paper/show?paperid=b5e2638edc409078088643be41bf45b5&site=xueshu_se [26] 伊扬磊. 杀灭铜绿微囊藻细菌A2的分离、鉴定及其溶藻特性研究[D]. 杨凌: 西北农林科技大学, 2013: 23-31. https://xueshu.baidu.com/usercenter/paper/show?paperid=00d55bf046e5ec0a0e67912e75fae327&site=xueshu_se&hitarticle=1 [27] 李卓佳, 郭志勋, 冯娟, 等. 应用芽孢杆菌调控虾池微生态的初步研究[J]. 海洋科学, 2006, 30(11): 28-31. doi: 10.3969/j.issn.1000-3096.2006.11.007 [28] 王小冬, 顾兆俊, 朱浩, 等. 春季不同营养类型池塘浮游植物群落结构特征的研究[J]. 水产学杂志, 2013, 26(6): 35-39. doi: 10.3969/j.issn.1005-3832.2013.06.008 [29] 陈纯, 李思嘉, 肖利娟, 等. 营养盐加富和鱼类添加对浮游植物群落演替和多样性的影响[J]. 生态学报, 2013, 33(18): 5777-5784. https://xueshu.baidu.com/usercenter/paper/show?paperid=05185369b65c9ff5ad1fef123f8ed841&site=xueshu_se&hitarticle=1 [30] 魏小岚, 李纯厚, 颉晓勇, 等. 对虾高位池循环水养殖水体浮游植物生态特征研究[J]. 农业环境科学学报, 2014, 33(2): 392-403. https://xueshu.baidu.com/usercenter/paper/show?paperid=1n580vp054100ms0dv2808e0cn696750&site=xueshu_se&hitarticle=1 [31] 曾建刚, 蒋霞敏. 对虾养殖塘浮游植物的动态变化[J]. 海洋湖沼通报, 2010(1): 71-81. doi: 10.3969/j.issn.1003-6482.2010.01.011 [32] 李凡. 两种蓝藻对WSSV潜伏感染对虾的影响[D]. 大连: 大连海洋大学, 2014: 1-6. https://xueshu.baidu.com/usercenter/paper/show?paperid=b68d490f0b88fa11fb7204cdac9dadb6&site=xueshu_se&hitarticle=1 [33] 彭聪聪, 李卓佳, 曹煜成, 等. 凡纳滨对虾半集约化养殖池塘浮游微藻优势种变动规律及其对养殖环境的影响[J]. 海洋环境科学, 2011, 30(2): 193-198. doi: 10.3969/j.issn.1007-6336.2011.02.010 [34] CAO Y C, WEN G L, LI Z J, et al. Effects of dominant microalgae species and bacterial quantity on shrimp production in the final culture season[J]. J Appl Phycol, 2014, 26(4): 1749-1757. doi: 10.1007/s10811-013-0195-0
[35] 王丽花, 曹煜成, 李卓佳. 溶藻细菌控藻作用及其在对虾养殖池塘中的应用前景[J]. 南方水产科学, 2012, 8(4): 76-82. doi: 10.3969/j.issn.2095-0780.2012.04.012 -
期刊类型引用(13)
1. 杨燕,孙锟焜,谢艳萍,马燕天,张赫. 溶藻菌治理藻华的研究进展. 渔业研究. 2024(04): 413-424 .  百度学术
百度学术
2. 胡晓娟,杨铿,文国樑,苏浩昌,许云娜,徐创文,徐煜,徐武杰,曹煜成. 溶藻菌CZBC1在氯化物型盐碱水中对铜绿微囊藻的溶藻效果研究. 南方水产科学. 2024(05): 169-175 .  本站查看
本站查看
3. 陈皓祥,邓益琴,程长洪,马红玲,郭志勋,冯娟. 养殖池塘14株芽孢杆菌的分离鉴定及抑菌效果. 热带生物学报. 2022(06): 605-613 .  百度学术
百度学术
4. 赵鄢鹏,蔡忠贞,王冰,耿金峰,白雪梅. 眼点拟微绿球藻养殖过程中致死细菌的分离鉴定与治理. 江西农业学报. 2019(03): 16-22 .  百度学术
百度学术
5. 孙卫芳,黄小帅,胡晓娟,文国樑,曹煜成,张建设. 广东沿海地区凡纳滨对虾EHP、VP_(AHPND)和SHIV感染情况调查与分析. 南方农业学报. 2019(10): 2343-2349 .  百度学术
百度学术
6. 罗智伟,罗剑飞,林炜铁. 南美白对虾养殖水体中抑藻细菌的分离及鉴定. 现代食品科技. 2019(11): 109-113+51 .  百度学术
百度学术
7. 王慧博,宋聃,黄晓丽,霍堂斌,王秋实,都雪. 生物絮团养殖池塘中浮游植物的群落结构特点. 水产学杂志. 2019(06): 29-35 .  百度学术
百度学术
8. 耿金峰,赵鄢鹏,冯倩,蔡忠贞,王慧岭,张晋阳,王冰,刘敏胜,白雪梅. 眼点拟微绿球藻养殖过程中细菌污染的治理方法. 安徽农业科学. 2018(26): 63-67+76 .  百度学术
百度学术
9. 张洪玉,王海波,杨移斌,赵明军,夏磊. 虾源蜡样芽孢杆菌D7的生态安全性评价. 浙江农业学报. 2018(09): 1585-1591 .  百度学术
百度学术
10. 田雅洁,曹煜成,胡晓娟,黄小帅,徐煜,许云娜,李卓佳,文国樑. 4种因子对玫瑰红红球菌XH2氨氮去除效果的影响. 渔业科学进展. 2018(06): 164-172 .  百度学术
百度学术
11. 胡晓娟,徐创文,李卓佳,文国樑,杨铿,许云娜,李莎莎,曹煜成. 响应面法优化蓝藻溶藻菌CZBC1发酵培养工艺. 南方农业学报. 2017(11): 2092-2099 .  百度学术
百度学术
12. 徐煜,徐武杰,文国樑,胡晓娟,苏浩昌,杨铿,李卓佳,曹煜成. 颤藻浓度和水温对凡纳滨对虾响应颤藻粗提液毒性的影响. 南方水产科学. 2017(01): 26-32 .  本站查看
本站查看
13. 孙志伟,邱丽华,曹煜成,李卓佳,胡晓娟,苏浩昌,蔡卓平,文国樑. 蓝藻水华对水产养殖业影响的研究进展. 生态科学. 2017(01): 231-235 .  百度学术
百度学术
其他类型引用(12)



 下载:
下载:


 粤公网安备 44010502001741号
粤公网安备 44010502001741号
