Population structure of purpleback flying squid (Sthenoteuthis oualaniensis) in Nansha area in spring
-
摘要:
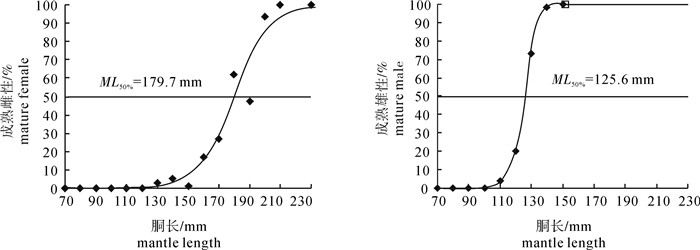
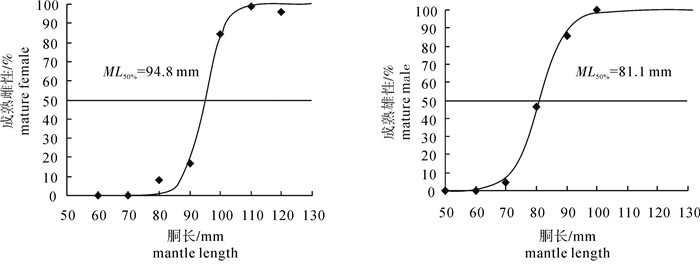
种群问题是渔业生物学研究的基础。根据2011年春季罩网渔船调查数据,研究了南沙海域鸢乌贼(Sthenoteuthis oualaniensis)的种群组成、胴长分布、雌雄比例、性腺发育等种群结构特征。结果显示:1)南沙海域存在中型和微型2个鸢乌贼种群,分别占渔获总尾数的88.92%和11.08%,微型种群渔获量少但也遍布整个调查海域;2)中型和微型种群渔获胴长范围分别为69~231 mm和51~125 mm,2个种群雌性的平均胴长均大于雄性;3)中型和微型种群中雌性个体分别占48.48%和61.88%,2个种群不同胴长组性比随着胴长的增加变化规律相似,即由开始阶段雌雄基本接近,到雄性个体占优,再到雌性个体占优,直至全部为雌性;4)微型种群性腺发育早于中型种群,雄性个体性腺发育早于雌性个体,雌、雄初次性成熟胴长(ML50%)中型种群分别为179.7 mm和125.6 mm,微型种群分别为94.8 mm和81.1 mm。鸢乌贼雌雄比例的变化与雄性个体的生长发育密切相关。
Abstract:Research on fish population is foundamental for studies on fishery biology. Based on the survey data of purpleback flying squid (Sthenoteuthis oualaniensis) collected by Chinese falling-net vessels in Nansha area of the South China Sea during April to May in 2011,we studied the population composition,mantle length distribution,sex ratio and maturity of S.oualaniensis in that area. The results show that two populations of S.oualaniensis existed in Nansha area. The medium-form and dwarf-form individuals accounted for 88.92% and 11.08% of the total catches,respectively. The dwarf-form population was less abundant but occurred throughout the survey area. Mantle length (ML) of S.oualaniensis ranged from 69 mm to 231 mm for medium-form population and from 51 mm to 125 mm for dwarf-form population,respectively. The average ML of females was higher than that of males for two populations. The females accounted for 48.48% and 61.88% in the medium-form and dwarf-form populations,respectively. The variation of sex ratio by different ML groups was similar for two populations. The sex ratio of females to males was approximately the same among young squids with increasing ML,i.e.,males were first dominant,then were females and finally there were all females. The maturity stage of dwarf-form population was higher than that of medium-form population. The maturity stage of males was higher than that of females for two populations. By fitting Logistic function,the MLs at first maturity for females and males of medium-form population were 179.7 mm and 125.6 mm,respectively;and those for females and males of dwarf-form population were 94.8 mm and 81.1 mm,respectively. It is suggested that the variation of sex ratio is closely related to the growth and maturity of males.
-
Keywords:
- Sthenoteuthis oualaniensis /
- population structure /
- Nansha area /
- spring
-
孔雀石绿(MG)和结晶紫(CV)是一类三苯甲烷类染料,最先应用在纺织工艺,因其具有消毒和杀菌作用而被广泛应用于水产品的养殖过程中。由于MG和CV具有高毒、高残留和致癌、致畸、致突变等特点,当其进入生物体内,会产生具有更强危害的隐色孔雀石绿(LMG)和隐色结晶紫(LCV),因此,包括中国在内的许多国家都将MG和CV列为水产养殖中的禁用药物[1-4]。然而,由于MG和CV具有价格低廉、效果显著等优点,其在水产养殖中的使用屡禁不止,这不但对人体健康造成威胁,而且严重影响了中国水产品的出口[5];因此,如何快速、准确地测定该类禁用药物、特别是其代谢物在水产品中的残留量,对于水产品出口企业非常重要。
目前国内外检测MG、CV、LMG和LCV的分析方法有气相色谱质谱法[6]、高效液相色谱法[7-11]和液相色谱-质谱法[12-16],同时国内检测此类药物的标准方法有GB/T 19857-2005[17]、GB/T 20361-2006[18]和SN/T 1768-2006[19]等。然而,上述方法不是检出限高达不到出口要求,就是检测方法繁琐,特别是存在前处理操作步骤多、耗时较长、费用高及检测过程使用大量有毒试剂等缺点,因此,笔者在应用SN/T 1768-2006检测方法的基础上,多次利用超高效液相色谱-串联质谱对水产品中MG、CV及其代谢物的残留量进行检测,总结了一些经验,并对方法中的一些环节进行了改进。改进后的方法在FAPAS国际能力验证中得以证实,该法快速、准确、灵敏度高,完全可以达到水产品出口检测的要求。
1. 材料与方法
1.1 仪器与试剂
超高效液相色谱-串联四极杆质谱仪(Waters公司出品);MASSLYNX 4.1质谱工作站软件;T10均质器(德国IKA公司出品);旋转蒸发仪(瑞士BUCHI公司出品);WH-3旋涡混合仪(上海沪西产);离心机(德国Beckman Coulter公司出品);CP224S电子分析天平(德国Sartorius公司出品);乙腈(Fisher色谱纯);试验用水为Milli-Q超纯水;乙酸铵(分析纯);标准品结晶紫盐酸盐购自Riedel-de公司(CV,纯度89.0%);孔雀石绿草酸盐(MG,纯度90.0%)、隐色孔雀石绿(LMG,纯度92.0%)、隐色结晶紫(LCV,纯度99.0%)及内标氘代隐色孔雀石绿(D6-LMG,纯度98.5%)均购自Dr. Ehrenstorfer公司;氘代孔雀石绿购自WITEGA公司(D5-MG,纯度99.0%);标准溶液:分别准确称取适量MG、CV、LMG、LCV、D5-MG和D6-LMG标准品,用乙腈分别配制成100 μg · mL-1的标准贮备液,-18 ℃避光保存。使用前,根据需要用初始流动相配制混合标准溶液,现配现用。试验样品为斑点叉尾

1.2 液相色谱条件
色谱柱为ACQUITY UPLCTM BEH C18柱(2.1 mm×100 mm,1.7 μm);流动相:溶剂A为乙腈,溶剂B为5 mmol乙酸铵溶液(pH=4.5),梯度洗脱条件见表 1;样品室温度10 ℃;进样体积10 μL;流速0.3 mL · min-1。
表 1 梯度洗脱条件Table 1. Gradient elution conditionst/min ϕ(乙腈)/% acetonitrile ϕ(乙酸铵缓冲液)/% ammonium acetate buffer 曲线curve 0 60 40 - 8 90 10 6 10 60 40 1 1.3 质谱条件
电喷雾离子源ESI+;毛细管电压0.7 kV;离子源温度120 ℃;锥孔反吹气50 L · h-1;脱溶剂气温度350 ℃;脱溶剂气流量650 L · h-1。第一重四极杆和第二重四极杆的低端分辨率及高端分辨率均为13;碰撞气流量0.2 mL · min-1;锥孔电压和碰撞能量见表 2,检测方式为多反应监测(MRM)扫描模式。
表 2 MRM扫描模式的参数Table 2. MRM parameters待测物analyte 母离子/m/z parent ion 子离子/m/z daughter ion 锥孔电压/V cone voltage 碰撞能量/eV collision energy 孔雀石绿MG 329.10 208.00, 313.10* 65 36, 36 隐色孔雀石绿LMG 331.10 239.10*, 315.90 50 34, 22 结晶紫CV 372.10 340.10, 356.10* 75 50, 38 隐色结晶紫LCV 374.16 238.30, 358.20* 55 32, 30 氘代孔雀石绿D5-MG 334.10 318.10* 65 40 氘代隐色孔雀石绿D6-LMG 337.16 322.10* 50 22 注:*.定量离子
Note: *. quantitative ion1.4 样品处理
准确称取已搅碎的样品5.00 g于50 mL离心管中,加入适量D5-MG和D6-LMG内标混合标准溶液,使2种内标最终测定质量浓度为2 ng · mL-1(标准曲线的制作与样品处理同步,分别在空白样品中加入最终测定质量浓度为0、0.2、0.5、1.0、5.0和10 ng · mL-1的MG、CV、LMG和LCV标准溶液),加入孔雀石绿和结晶紫快速检测前处理试剂盒中的提取剂1(液体20.0 mL),用均质器以8 000 r · min-1的速度均质30 s,再加入提取剂2(固体粉末),振荡1 min,4 000 r · min-1离心5 min,取上清液4.0 mL于鸡心瓶中,40 ℃水浴减压旋转蒸干,加入2 mL初始流动相涡旋混合1 min,充分溶解残留物,0.22 μm滤膜过滤后,供上机测试。
2. 结果
2.1 LC-MS/MS分析
采用电喷雾离子源,正离子扫描模式,分别对MG、CV、LMG、LCV和D5-MG、D6-LMG监测其母离子和2个信号较强的子离子,以母离子和子离子组成监测离子对,以多反应监测模式对待测物进行定性和定量分析。该法完全满足欧盟2002/675/EC指令规定对于禁用药物的质谱确证方法需要4个确证点(IP)的要求(其中1个母离子1 IP和2个子离子2×1.5 IP),其中样品定量离子与定性离子的离子强度比不超过其标准系列相应的离子强度比均值的±20%作为定性确证的质量控制依据[20]。
在上述测定条件下,选择空白鱼肉加混合标准样品(0.5 μg · kg-1)进行测定,谱图见图 1。试验结果表明,MG、CV、LMG、LCV、D5-MG和D6-LMG保留时间分别为1.43、1.99、5.74、5.88、1.41和5.64 min。
2.2 标准曲线线性和检出限
用空白鱼肉样品作基质,加入最终测定质量浓度为0、0.2、0.5、1.0、5.0和10 ng · mL-1的MG、CV、LMG和LCV混合标准溶液(相当于样品中添加0、0.4、1.0、10.0和20.0 μg · kg-1的待测物),加入2 ng · mL-1的D5-MG和D6-LMG内标混合标准溶液,用HPLC-MS/MS进行测定。试验结果以标样质量浓度(ng · mL-1)为横坐标,以MG和CV(LMG、LCV)的标准峰面积与内标D5-MG(D6-LMG)的峰面积之比值为纵坐标制作标准曲线,线性回归方程和相关系数见表 3。以10倍信噪比计算检出限,MG、CV、LMG和LCV检出限均为0.1 μg · kg-1,满足水产品出口检测要求。
表 3 标准曲线线性回归方程及相关系数Table 3. Linear equations and correlation coefficients of standard curves待测物analyte 线性回归方程linear equation 相关系数correlation coefficient 孔雀石绿MG Y=0.7903X+0.0209 0.999 6 结晶紫CV Y=1.9924X+0.1134 0.996 0 隐色孔雀石绿LMG Y=1.0259X+0.0939 0.998 7 隐色结晶紫LCV Y=0.5141X-0.0075 0.999 7 2.3 回收率与精密度
对空白鱼肉样品在0.5和1.0 μg · kg-1 2个水平上进行加标回收试验(表 4)。试验结果表明, MG、CV、LMG和LCV的回收率在92.1%~111.0%之间,测定结果的相对标准偏差为2.2%~9.5%。
表 4 样品加标回收率及精密度(n=4)Table 4. Recovery and RSD of fortified samples待测物analyte 加标量/μg·kg-1 fortification level 平均回收率/% average recovery 精密度/% RSD 孔雀石绿MG 0.5 96.5 6.2 1.0 101.0 6.1 结晶紫CV 0.5 111.0 4.0 1.0 109.1 2.6 隐色孔雀石绿LMG 0.5 96.6 2.2 1.0 97.9 9.5 隐色结晶紫LCV 0.5 92.1 4.4 1.0 98.4 2.2 3. 讨论
3.1 方法选择及改进
目前,国内同时检测MG、CV及其代谢物的标准方法有GB/T 19857-2005和GB/T 20361-2006和SN/T 1768-2006等,但GB/T 19857-2005和GB/T 20361-2006存在检测方法繁琐,特别是前处理操作步骤多、耗时较长、费用高及检测过程使用大量有毒试剂等缺点,因此,笔者采用SN/T 1768-2006快速检测方法进行水产品出口检测。然而,由于待测物的不稳定性,完全采用SN/T 1768-2006方法检测,其MG和CV回收率偏低,而LMG和LCV回收率偏高,不能满足检测要求。该法在应用SN/T 1768-2006检测方法的基础上,采用空白样品添加不同质量浓度标准溶液的方式绘制校准曲线,以最大限度排除基体干扰。同时定量方法采用D5-MG和D6-LMG为内标进行内标法检测,降低由于前处理过程中目标化合物的损失所带来的偏差,从而提高定量的准确性,加标回收率稳定、重现性好,整个检测过程仅需30 min左右。
3.2 色谱条件的选择
研究采用了超高效液相色谱仪和1.7 μm填料的超高效液相色谱柱对样品进行分离,与传统的高效液相色谱柱相比,该法能更好地使待测物与抑制电离的基质分离,降低基质对质谱检测的影响,同时提高分离效率。对于电喷雾离子源正离子扫描模式,流动相在弱酸性环境条件下加入适量乙酸铵可以提高待测物离子化效率,因此,试验中采用乙腈和5 mmol乙酸铵溶液(pH=4.5)作为流动相体系,并且对流动相比例进行优化。结果显示,当乙腈和乙酸铵溶液初始比例为60︰40梯度洗脱条件下(表 1),待测物在6 min左右全部出峰,并且灵敏度高、分离效果好,满足检测要求。
3.3 样品溶液放置时间对检测结果的影响
由于MG、CV及其代谢物的不稳定性,文章研究了样品溶液放置时间对检测结果的影响。研究比较了4种待测物平均添加水平为3.0 μg · kg-1的鱼肉样品处理完后在10 ℃下避光放置0、30、60 min及6、12 h检测对回收率的影响。结果显示,MG和CV在研究时间内对放置时间影响较小,而LMG和LCV回收率随着放置时间的延长而呈下降趋势。与样品处理好后及时上机相比,LMG在放置30、60 min及6、12 h后检测的回收率分别下降了13%、24%、30%和34%,而LCV分别下降了10%、19%、25%和30%;因此,为了保证检测数据准确可靠,样品前处理时间不宜太长,样品处理完后应及时上机检测,可考虑对标准工作溶液和样品溶液进行穿插进样检测,特别是检测隐色代谢物。同时为了保证检测数据准确可靠,检测过程也应注意以下事项:1)整个检测过程要尽量避光,防止待测物降解;2)标准贮备液应在-18 ℃以下避光保存,有效期3个月,混合标准工作溶液应现配现用;3)待测样品应在-18 ℃以下避光保存,尽量避免样品的反复解冻;4)检测过程避免交叉污染,包括样品之间、样品与标准溶液之间等。
3.4 方法的验证
运用该法,2009年6月笔者参加了英国FAPAS(食品分析领域全球第一的国际评价体系)组织的鳗鱼中MG、CV质量分数的能力验证测试,MG、LMG、MG总量、CV、LCV和CV总量6项结果全部满意。结果表明,该法能够满足美国FDA对水产品MG、CV及其代谢物残留量检测的准确性和检出限的要求,且更加简单快速。
-
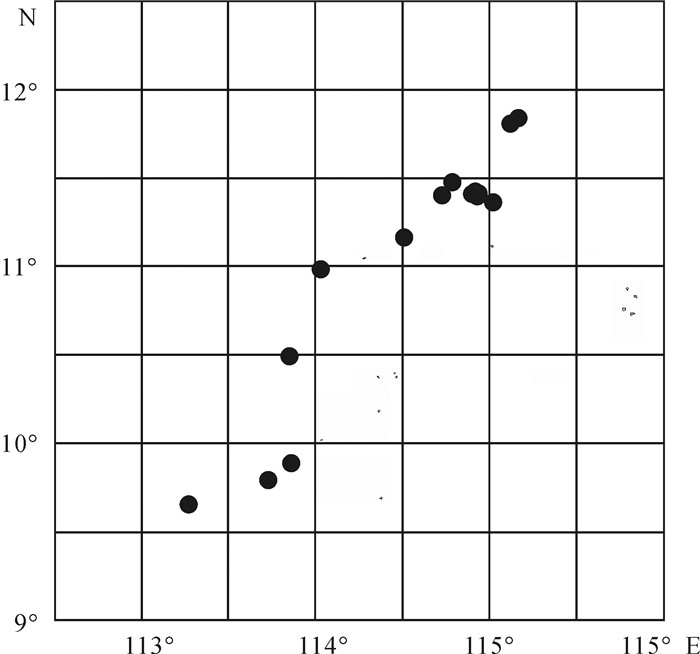
表 1 取样站位和鸢乌贼渔获概况
Table 1 Sampling stations and catches of S.oualaniensis
夜晚
No.日期
date作业地点 position 作业网次
fishing times产量/t
yield抽样网次
sampling times抽样尾数/尾
sampling number微型占比/%
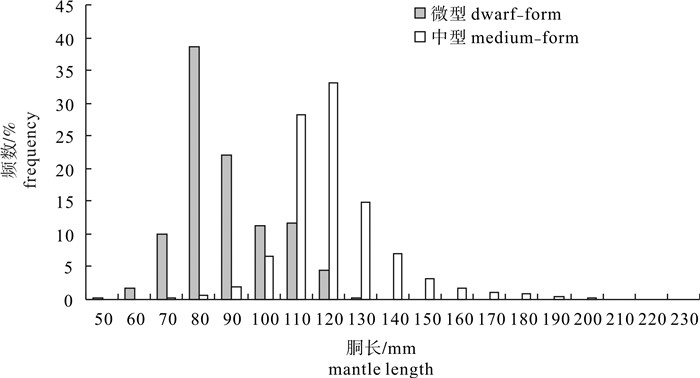
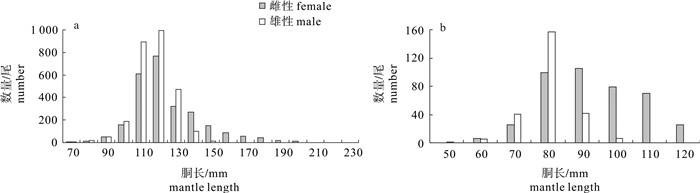
drawf-form/totalLat.(N) Long.(E) 1 04-20 114°44′ 11°24′ 10 1.65 4 200 4.00 2 04-21 114°02′ 10°59′ 13 3.33 13 651 4.30 3 04-22 114°31′ 11°10′ 10 1.54 10 501 12.57 4 04-23 113°52′ 09°53′ 12 3.90 10 501 3.59 5 04-24 113°44′ 09°48′ 12 2.91 9 453 5.30 6 04-25 113°16′ 09°39′ 15 3.59 10 505 15.84 7 04-26 113°51′ 10°29′ 12 2.68 6 302 16.56 8 04-27 115°01′ 11°22′ 16 5.10 8 401 19.95 9 04-28 115°07′ 11°51′ 14 10.94 7 349 10.32 10 04-29 115°10′ 11°50′ 13 4.62 7 351 16.52 11 04-30 115°07′ 11°49′ 11 3.08 7 350 30.29 12 05-01 114°56′ 11°25′ 13 6.90 7 350 3.14 13 05-02 114°54′ 11°25′ 16 5.87 7 350 18.29 14 05-03 114°56′ 11°24′ 16 9.15 8 400 2.75 15 05-04 114°55′ 11°25′ 11 2.79 6 300 8.00 表 2 鸢乌贼渔获胴长组成
Table 2 Composition of mantle length of S.oualaniensis
种群
population性别
sex尾数
number胴长范围/mm
mantle length range优势胴长 dominant mantle length 平均胴长/mm
average mantle length标准差/mm
SD范围/mm 比例/% 中型 medium-form 雌性 2 571 71~231 110~140 82.77 125.5 20.1 雄性 2 732 69~153 100~130 93.23 117.5 10.3 合计 5 303 69~231 100~140 90.01 121.4 16.4 微型 dwarf-form 雌性 409 56~125 80~110 86.31 93.5 14.1 雄性 252 51~104 70~90 95.24 80.8 6.9 合计 661 51~125 70~110 94.40 88.6 13.4 表 3 鸢乌贼性腺成熟度组成
Table 3 Composition of sex maturity of S.oualaniensis
种群
population性别
sex样本数/尾
number性腺成熟度/% sexual maturity 性未成熟
immature性成熟
mature产卵后
spawned中型 medium-form 雌性 1 407 94.88 5.12 0 雄性 1 519 75.71 24.29 0 合计 2 926 84.93 15.07 0 微型 dwarf-form 雌性 243 60.49 39.51 0 雄性 194 54.64 45.36 0 合计 437 57.89 42.11 0 -
[1] 王尧耕, 陈新军. 世界大洋性经济柔鱼类资源及其渔业[M].北京:海洋出版社, 2005:284-296. https://xueshu.baidu.com/usercenter/paper/show?paperid=57f1b5f4013df538c63ee7185e9bea0a [2] 刘必林, 陈新军, 钟俊生. 采用耳石研究印度洋西北海域鸢乌贼的年龄、生长和种群结构[J]. 大连水产学院学报, 2009, 24(3): 206-212. doi: 10.3969/j.issn.1000-9957.2009.03.004 [3] NESIS K N. Population structure of oceanic Ommastrephids, with particular reference to Sthenoteuthis oualaniensis: a review[C]//Recent advances in Cephalopod fisheries biology. Tokyo: Takai University Press, 1993: 375-383. https://www.semanticscholar.org/paper/Population-structure-of-oceanic-Ommastrephids%2C-with-Nesis/510610895740d037d8d13fbc2fe86ea5a60150f8
[4] 刘金立. 利用形态学和RAPD方法鉴定印度洋西北部海域莺乌贼的种群结构[D]. 上海: 上海水产大学, 2006. https://med.wanfangdata.com.cn/Paper/Detail?id=DegreePaper_Y918053 [5] 刘必林. 利用耳石微结构研究印度洋西北海域莺乌贼的年龄和生长[D]. 上海: 上海水产大学, 2006. https://www.doc88.com/p-3999078058671.html [6] 陈新军, 刘金立. 利用形态学方法分析印度洋西北部海域鸢乌贼种群结构[J]. 上海水产大学学报, 2007, 16(2): 174-179. https://www.doc88.com/p-7317011198694.html [7] CHEN Xinjun, LIU Bilin, TIAN Siquan, et al. Fishery biology of purpleback squid, Sthenoteuthis oualaniensis, in the northwest Indian Ocean[J]. Fish Res, 2007, 83(1): 98-104. doi: 10.1016/j.fishres.2006.09.005
[8] 张鹏, 曾晓光, 杨吝, 等. 南海区大型罩网渔场渔期和渔获组成分析[J]. 南方水产科学, 2013, 9(3): 74-79. doi: 10.3969/j.issn.2095-0780.2013.03.012 [9] SIRIRAKSOPHON S, NAKAMURA Y, NATINEE S. Exploration of purpleback flying squid, Sthenoteuthis oualaniensis resources in the South China Sea[R]. Samutprakan, Thailand: Southeast Asian Fisheries Development Center Training Department, 2001: 1-81. doi: 10.3390/w13010065
[10] SIRIRAKSOPHON S. Experimental fishing on offshore resources in the region: report of the first meeting of the Regional Advisory Committee on Fisheries Management in Southeast Asia, Bangkok, Thailand, 22-24 September, 2008[C]. Bangkok: SEAFDEC Secretariat, 2009: 45-47. https://www.nature.com/articles/s41597-023-02883-9
[11] 张引. 南海产南鱿资源之资源声学研究[D]. 台北: 台湾大学海洋研究所, 2005. [12] 张鹏, 杨吝, 张旭丰, 等. 南海金枪鱼和鸢乌贼资源开发现状及前景[J]. 南方水产, 2010, 6(1): 68-74. doi: 10.3969/j.issn.1673-2227.2010.01.012 [13] 颜云榕, 冯波, 卢伙胜, 等. 南沙群岛北部海域鸢乌贼夏季渔业生物学研究[J]. 海洋与湖沼, 2012, 43(6): 1177-1186. doi: 10.11693/hyhz201206021021 [14] 杨权, 李永振, 张鹏, 等. 基于灯光罩网法的南海鸢乌贼声学评估技术研究[J]. 水产学报, 2013, 37(7): 1032-1039. doi: 10.3724/SP.J.1231.2013.38513 [15] LABE L L. Catch rate of oceanic squid by Jigging method in the South China Sea, Area III: Western Philippines: proceedings of the third Technical Seminar on Marine Fishery Resources Survey in the South China Sea, Area III: Western Philippines, Manila, July 13-15, 1999[C]. Bangkok, Thailand: SEAFDEC, 2000: 19-31. http://repository.seafdec.org/handle/20.500.12066/4341
[16] BASIR S. Biological feature of an oceanic squid, Sthenoteuthis oualaniensis in the South China Sea, Area III: Western Philippines: proceedings of the Third Technical Seminar on Marine Fishery Resources Survey in the South China Sea, Area III: Western Philippines, Manila, July 13-15, 1999[C]. Bangkok, Thailand: SEAFDEC, 2000: 135-147. http://hdl.handle.net/20.500.12066/4349
[17] ZAKARIA M Z. Age and growth studies of oceanic squid, Sthenoteuthis oualaniensis using statoliths in the South China Sea, Area III: Western Philippines: proceedings of the Third Technical Seminar on Marine Fishery Resources Survey in the South China Sea, Area III: Western Philippines, Manila, July 13-15, 1999[C]. Bangkok, Thailand: SEAFDEC, 2000: 118-134. http://hdl.handle.net/20.500.12066/4348
[18] SIRIRAKSOPHON S, NAKAMURA Y, PRADIT S, et al. Ecological Aspects of Oceanic Squid, Sthenoteuthis oualaniensis (Lesson) in the South China Sea, Area III: Western Philippines: proceedings of the third Technical Seminar on Marine Fishery Resources Survey in the South China Sea, Area III: Western Philippines, Manila, July 13-15, 1999[C]. Bangkok, Thailand: SEAFDEC, 2000: 101-117. http://repository.seafdec.org/handle/20.500.12066/4347
[19] 刘必林, 陈新军, 田思泉, 等. 西南大西洋公海阿根廷滑柔鱼性成熟的初步研究[J]. 上海水产大学学报, 2008, 17(6): 721-725. doi: 10.3969/j.issn.1000-9957.2010.04.013 [20] WORMUTH J H. The biogeography and numerical taxonomy of the oegopsid squid family Ommastrephidae in the Pacific Ocean[C]//Bull Scripps Inst Oceanogr. California: University of California Press, 1976: 9-10. https://searchworks.stanford.edu/view/7634355
[21] STAAF D J, RUIZ-COOLEY R I, ELLIGER C, et al. Ommastrephid squids Sthenoteuthis oualaniensis and Dosidicus gigas in the eastern Pacific show convergent biogeographic breaks but contrasting population structures[J]. Mar Ecol Prog Ser, 2010, 418(11): 165-178. doi: 10.3354/meps08829
[22] 陈新军. 新西兰海域双柔鱼的生物学研究[J]. 中国水产科学, 1999, 6(1): 27-32. doi: 10.3321/j.issn:1005-8737.1999.01.007



 下载:
下载:

 粤公网安备 44010502001741号
粤公网安备 44010502001741号
