Limiting concentrations of nitrogen, phosphorus, iron on growth of Oscillatoria chlorine
-
摘要:
绿色颤藻(Oscillatoria chlorine)在虾池中大幅度增加时会释放微囊藻毒素, 给对虾的健康养殖带来危害。文章分析不同质量浓度的氮(N)、磷(P)、铁(Fe3+)对绿色颤藻叶绿素a和藻体质量浓度的影响, 探讨水中N、P、Fe3+的质量浓度对绿色颤藻生长的限制性条件。结果显示, 限制绿色颤藻叶绿素a质量浓度增加的条件是ρ(N)<0.06 mg·L-1, ρ(P)<9.93×10-2 mg·L-1和>1.99 mg·L-1, ρ(Fe3+)<2.58×10-2 mg·L-1和>51.67 mg·L-1; 限制藻体质量浓度增加的条件是ρ(N)<12.36 mg·L-1, ρ(P)<9.93×10-3 mg·L-1, ρ(Fe3+)<5.16×10-3 mg·L-1和>51.67 mg·L-1。绿色颤藻生长的阈值ρ(N)为0.06 mg·L-1、ρ(P)为9.93×10-3 mg·L-1、ρ(Fe3+)为5.16×10-3 mg·L-1。ρ(N)为7.42 mg·L-1、ρ(P)为4.96×10-2 mg·L-1和ρ(Fe3+) 为5.16×10-3 mg·L-1是限制绿色颤藻叶绿素和藻体质量浓度增加的最低条件组合; N是影响绿色颤藻叶绿素a和藻体质量浓度的主要因子, 其次是Fe3+和P。在对虾养殖过程中可以通过换水或循环水系统除去水体中的含N污染物, 降低养殖水体中溶解态N含量, 从而控制绿色颤藻的快速增长。
Abstract:The proliferation of Oscillatoria chlorine will release toxins which are harmful to prawn growth in the aquaculture ponds. We investigated the limiting concentrations of nitrogen (N), phosphorus (P) and iron (Fe3+) to the growth of O.chlorine as well as the effects of different N, P and Fe3+ concentrations on chlorophyll a content and dry weight of O.chlorine. The results show that N concentration < 0.06 mg·L-1, P concentration < 9.93×10-2 mg·L-1 and >1.99 mg·L-1, and Fe3+ concentration < 2.58×10-2 mg·L-1 and > 51.67 mg·L-1, limited the increase of chlorophyll a content; N concentration < 12.36 mg·L-1, P concentration < 9.93×10-3 mg·L-1 and the Fe3+ concentration < 5.16×10-3 mg·L-1 and > 51.67mg·L-1, limited the increase of dry weight. The threshold concentrations of N, P and Fe3+for the growth of O.chlorine were 0.06 mg·L-1, 9.93×10-3 mg·L-1 and 5.16×10-3 mg·L-1, respectively. The combined concentrations which limited the increase of chlorophyll a contents and dry weight of O.chlorine were 7.42 mg·L-1 of N, 4.96×10-2 mg·L-1 of P and 5.16×10-3 mg·L-1 of Fe3+, respectively. Nitrogen had the strongest effect on chlorophyll a content and dry weight, followed by Fe3+ and P. It is suggested that the rapid proliferation of the O.chlorine might be controlled through water exchange or circulation to reduce the dissolved nitrogen content in the aquaculture ponds.
-
Keywords:
- Oscillatoria chlorine /
- nitrogen /
- phosphorus /
- iron /
- chlorophyll a content /
- dry weight
-
近江牡蛎(Crassostrea rivulari)和波纹巴非蛤(Paphia undulate)是2种主要的养殖经济贝类,因其具有营养丰富、味道鲜美和食用方便等特点,深受消费者欢迎。它们能为人体提供丰富的蛋白质和氨基酸,尤其牡蛎还享有“海中牛奶”的美称[1],作为高灰分、低脂肪的食物[2],对不同年龄段的人、特别是老年人具有营养与保健功能[3]。同时近江牡蛎和波纹巴非蛤还富含人体必需的微量元素铁(Fe)、铜(Cu)等,常作为治疗缺乏微量元素(如Fe)辅助治疗的食疗材料[4]。
贝类作为食物进入人体消化道后,只有部分营养物质会被消化吸收,同时贝类不同的食用方式也会对其消化吸收[5]有影响,为更好地评估摄入量,体外仿生模型被引入到贝类中微量金属的分析研究中,通过模拟人体胃肠消化过程,考察贝类中微量金属在人体消化过程中的生物可接受性[6-9]。目前采用体外仿生模型研究食品、药品的生物可接受性已被广泛应用和认可[10-12]。近江牡蛎和波纹巴非蛤微量金属元素分析主要集中在总量[13-17],关于生物可接受性研究、特别是食用方式影响的研究甚少。该研究采用体外全仿生消化方法对近江牡蛎和波纹巴非蛤进行处理,模拟2种贝类在人体消化道环境中的消化过程,对胃、肠消化过程中转运至仿生消化液中的微量金属进行测定,考察生、熟2种状态下贝类微量金属在提取液中提取量、生物可接受性的变化规律及特征,并进行微量元素摄入评估,以期为近江牡蛎和波纹巴非蛤的食用药用价值提供基础数据。
1. 材料与方法
1.1 材料与试剂
1.1.1 样品制备
2013年在广东省石栏洲海域、博贺湾、独湾海域、桂山岛海域4个主要贝类养殖区采集近江牡蛎106个,在柘林湾青屿、浮屿海域采集波纹巴非蛤贝类样品40个,采集的样品在现场用海水将外壳洗净后,冰冻保存带回实验室。在实验室取出贝类样品的软组织和体液,冻干至恒质量,用玛瑙研钵研磨后装于食品塑料袋内待用。
1.1.2 试验试剂
牛血清白蛋白(分析纯,广州威佳科技有限公司出品),黏液素(分析纯,广州鼎国公司出品),氯化钾、硫氰化钾、磷酸二氢钠、磷酸钠、氯化钠、氢氧化钠、尿素、a-淀粉酶、尿酸、氯化钙、氯化铵、氯化镁、碳酸氢钠、磷酸二氢钾、葡萄糖、葡萄糖醛酸、氨基葡萄糖盐酸盐、胃蛋白酶、胰液素、脂肪酶、胆汁(分析纯,上海晶纯生化科技股份有限公司出品)。
1.2 仪器与设备
试验过程使用的仪器设备主要有Milestone微波消解萃取系统(Ethos1)、智诚气浴恒温振荡器(ZHWY-2000)、Crist真空冷冻干燥机(ALPHA 1-4/Ldplue)、HITCH原子吸收分光光度计Z-2000。
1.3 方法
1.3.1 全仿生消化液的制备方法
试验所用唾液、胃液、肠液、胆汁等消化液的组成见表 1。参照LAIRD和CHAN[18]的方法,分别加入相应的无机物、有机物、消化酶,调节pH与4 ℃下保存备用。
表 1 唾液、胃液、十二指肠液、胆汁组成成分Table 1. Main components of saliva, gastric juice, duodenal juice and bile无机物inorganic matter 有机物organic matter 消化酶digestive enzyme pH 唾液sailiva 10 mL 189.6 g·L-1 KCl
10 mL 20 g·L-1 KSCN 10 mL 88.80 g·L-1 NaH2PO4
10 mL 57 g·L-1 Na3PO4
1.7 mL 175.3 g·L-1 NaCl
1.8 mL 40 g·L-1 NaOH8 mL 25 g·L-1尿素 145 mg α-淀粉酶
15 mg尿酸
50 mg粘液素6.5±0.2 胃液gastric juice 15.7mL 175.3 g·L-1 NaCl
3.0 mL 88.8 g·L-1 NaH2PO4
9.2 mL 89.6 g·L-1 KCl
18 mL 22.2 g·L-1 CaCl2
8.3 mL 37% HCl10 mL 65 g·L-1葡萄糖
10 mL 2 g·L-1葡萄糖醛酸
3.4 mL 25 g·L-1尿素
10 mL 33 g·L-1 氨基葡萄糖盐酸盐1 g牛血清蛋白
1 g胃蛋白酶
3 g脂肪酶1.07±0.07 十二指肠液
duodenal juice40 mL 175.3 g·L-1 NaCl
40 mL 84.7 g·L-1 NaHCO3
10 mL 8 g·L-1 KH2PO4
6.3 mL 89.6 g·L-1 KCl
10 mL 5 g·L-1 MgCl2
9 mL 22.2 g·L-1 CaCl2
0.18 mL 37% HCl4 mL 25 g·L-1尿素 1 g牛血清蛋白
3 g胰液素
0.5 g脂肪酶7.8±0.2 胆汁bile 30 mL 175.3 g·L-1 NaCl
68.3 mL 4.7 g·L-1 NaHCO3
4.2 mL 89.6 g·L-1 KCl
0.2 mL 37% HCl
10 mL 2.2 g·L-1 CaCl21 g牛血清蛋白
6 g胆汁8.0±0.2 注:用盐酸或碳酸氢钠溶液调pH,用超纯水定容至500 mL,在4 ℃下保存
Note: The pH values of all solutions were adjusted using HCl or NaHCO3 and the total volume of each digestion solution was diluted to 500 mL with ultrapure water before storage at 4 ℃.1.3.2 贝类全仿生消化方法
样品仿生消化具体步骤[18]为:称取贝类样品(生食样品)1.00 g,加入10 mL仿生唾液,在37 ℃恒温振荡5 min后加入150 mL仿生胃液,再于37 ℃恒温振荡2 h后取100 mL胃仿生消化食糜离心,得胃提取液待测;余下部分加入200 mL仿生十二指肠和80 mL仿生胆汁,恒温振荡8 h后取100 mL肠道仿生食糜离心,得肠提取液待测。熟食样品为制备好的贝类样品(生食样品)加入15 mL高纯水加热,沸腾10 min所得,仿生消化步骤同上。
1.3.3 贝类样品和提取液中重金属测定方法
取0.5 g贝类样品或30 mL仿生提取液(1.3.1制得),加入8 mL浓硝酸、1 mL双氧水微波消解后转移至烧杯加热,最终定容到10 mL的容量瓶,用原子吸收分光光度计分别测定贝类样品和仿生提取液中的Fe、Cu。样品平行双份,测定结果以平均值表示。
1.3.4 数据处理
$$ \;\;\;\;\;\;生物可接受性 (\%)=\\\frac{\text { 贝类消化液中金属质量分数 }\left(\mathrm{mg} \cdot \mathrm{kg}^{-1}\right)}{\text { 贝类样品中金属质量分数 }\left(\mathrm{mg} \cdot \mathrm{kg}^{-1}\right)} \times 100 $$ 居民日微量元素摄入量(mg · d-1)=每日膳食贝类摄入量(g)×贝类金属元素质量分数(mg · g-1)×生物可接受性;式中每日膳食贝类摄入量:男为19.4 g、女为17.7 g[19]。
2. 结果
2.1 贝类样品Fe、Cu总量
分析结果表明近江牡蛎和波纹巴非蛤均富含Fe元素,贝类样品近江牡蛎w(Fe)变化范围为0.97~1.83 mg · g-1,波纹巴非蛤w(Fe)的变化范围为0.96~1.24 mg · g-1,近江牡蛎w(Fe)平均值略大于波纹巴非蛤;与w(Fe)相比w(Cu)较低,2种贝类w(Cu)相差较大,近江牡蛎w(Cu)平均值为0.31 mg · g-1,而波纹巴非蛤w(Cu)平均值不及近江牡蛎的十分之一。
2.2 消化阶段提取液中Fe、Cu的变化
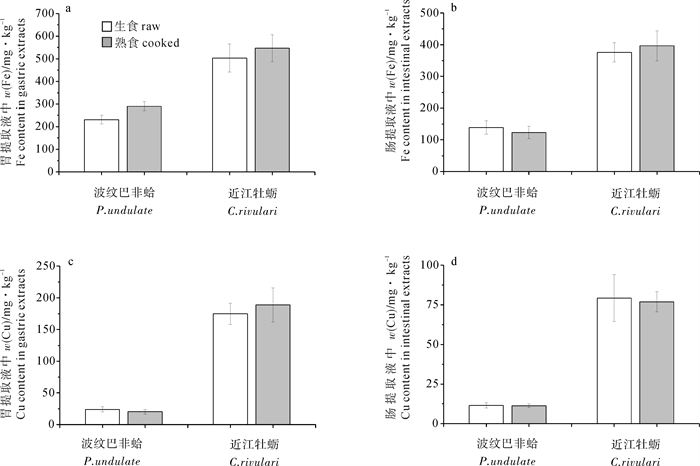
胃、肠仿生消化过程中(图 1-a,图 1-b),熟近江牡蛎仿生消化液中Fe的提取量比生的大。在胃仿生消化阶段,熟牡蛎提取液中Fe的提取量为547 mg · kg-1,而生牡蛎的只有503.5 mg ·kg-1。在肠仿生消化阶段,熟牡蛎提取液中Fe的提取量也比生牡蛎略高,是生牡蛎的1.05倍。熟牡蛎中Cu在胃肠消化阶段变化不一致,在胃消化阶段Cu的提取量比生牡蛎高,但是在肠消化阶段则比生牡蛎低,纵观整个仿生消化过程,熟牡蛎被仿生消化液提取出来的Cu比生牡蛎的高。
熟的波纹巴非蛤仿生消化过程中,Fe、Cu元素变化规律相同。胃仿生消化阶段(图 1-a,图 1-c),熟的波纹巴非蛤提取液中Fe、Cu提取量均比生波纹巴非蛤高;而在肠仿生消化阶段,熟波纹巴非蛤Fe、Cu提取量均比生波纹巴非蛤低,分别是生波纹巴非蛤提取量的88%和97%(图 1-b,图 1-d),Fe提取量降低幅度大于Cu。
胃是人类消化系统中主要消化场所,此试验也印证了这一点。不管是煮熟还是生食,近江牡蛎和波纹巴非蛤中的Fe、Cu在胃仿生消化中释放的量比肠消化阶段多,胃和肠提取液中Cu差别比较大。有研究表明生牡蛎中经胃消化阶段被提取的Cu可高达80%[20]。
2.3 生物可接受性
经过仿生消化后,熟近江牡蛎中的Fe、Cu生物可接受性比生近江牡蛎高,加热后近江牡蛎的Fe生物可接受性平均值增加7.3%,Cu生物可接受性平均值增加4.6%(表 2),消化液Fe、Cu提取量均比总量低,近江牡蛎组织中有超过13.8%~74.6%的Fe和3.3%~22.3%的Cu留在食物残渣中未进入人体消化循环。AMIARD等[21]研究发现生牡蛎经过胃肠仿生消化后,3%~39%的Cu留在食物残渣中。食用方式对波纹巴非蛤中2种元素的生物可接受性影响不一致,熟波纹巴非蛤中Fe的生物可接受性平均比生的高11.5%,Cu则低了11.5%,可见熟食方式提高了波纹巴非蛤Fe生物可接受性同时降低了Cu的生物可接受性。
表 2 近江牡蛎和波纹巴非蛤中铁、铜的生物可接受性Table 2. Bioaccessibility of Fe and Cu in C.rivulari and P.undulate% 元素
element近江牡蛎C.rivulari 波纹巴非蛤P.undulate 生牡蛎raw 熟牡蛎cooked 生蛤raw 熟蛤cooked 铁Fe 52.0±32.7 55.8±30.4 40.7±13.2 45.4±11.2 铜Cu 83.4±11.6 87.2±9.5 87.8±10.3 77.7±12.7 无论是那种食用方式,近江牡蛎和波纹巴非蛤Cu的生物可接受性都比Fe高,但是2种贝类的Fe总量均比Cu高,可见2种贝类中Fe、Cu生物可接受性与其总量高低并没有明显关系。JORGE等[22]对5种贝类的Fe、Cu生物可接受性进行测定,结果显示Cu生物可接受性均比Fe高。
2.4 评价
食用方式变化会改变人体消化系统对贝类Fe、Cu的利用率,文章采用近江牡蛎和波纹巴非蛤Fe、Cu仿生消化结果进行评价,考察2种贝类对人体Fe、Cu摄入量的贡献(表 3)。参照唐洪磊等[19]估算贝类摄入量,食用近江牡蛎和波纹巴非蛤所摄入的Fe和Cu均未超过中国居民DRIs委员会[23]推荐的每日适宜摄入量,食用近江牡蛎每日可为人体提供1.97~2.32 mg的Fe,占适宜摄入量的9.9%~15.5%,同时提供人体所需Cu的22.6%~25.9%,熟近江牡蛎提供Fe、Cu均比生牡蛎高。食用波纹巴非蛤摄入的Fe、Cu均比近江牡蛎少,每日可为人体提供1.27~1.56 mg的Fe和0.06~0.08 mg的Cu,最高可提供10.4% Fe(熟蛤)和3.9%(生蛤)摄入量。PAWELPOH等[24]研究多种蜂蜜对人体微量元素摄入贡献,发现日食用100 g蜂蜜最高可为人体提供11.1%~19.2%的Fe和6.0%~7.5%的Cu[适宜摄入量(AI,mg ·d-1)为Fe:11~14、Cu:2.0~2.5],近江牡蛎和波纹巴非蛤为人体提供Fe、Cu元素摄入量不同,食用方式不同也略有影响,但总体而言所提供的Fe、Cu相对比较高。
表 3 居民日微量元素摄入量Table 3. Daily consumption of Fe and Cu in shellfishmg · d-1 元素
element适宜摄入量
AI可耐受摄入量
UI近江牡蛎C.rivulari 波纹巴非蛤P.undulate 生牡蛎raw 熟牡蛎cooked 生蛤raw 熟蛤cooked 男 女 男 女 男 女 男 女 男 女 男 女 铁Fe 15 20 50 50 2.16 1.97 2.32 2.12 1.39 1.27 1.56 1.47 铜Cu 2.0 2.0 8.0 8.0 0.50 0.45 0.52 0.47 0.08 0.07 0.07 0.06 注:适宜摄入量和可耐受摄入量采用成年居民(≥18岁)推荐值
Note:Values of Al an Ul using adult (age≥18) recommended values of DRIs.3. 讨论
此试验模拟人体胃肠消化过程,加入全仿生消化液对样品进行处理,考察近江牡蛎和波纹巴非蛤中金属元素Fe、Cu转移进入消化液的情况。结果表明,近江牡蛎和波纹巴非蛤样品中Fe、Cu进入到消化液中的量均小于其总量,其中Fe仅约50%转运到消化液中。FANNY等[25]研究智利贻贝(Mytilus chilensis)表明,无论是生贝还是熟贝,仿生消化液中镉(Cd)的提取量都比样品本身Cd总量低,同为金属元素的Fe、Cu也有相同表现。食物在消化道中的消化方式影响其金属元素被人体吸收利用的程度,消化是金属元素伴随营养物质进入人体、被吸收利用的重要途径,选用适宜、科学的消化方法是合理评估的基础。
煮熟的近江牡蛎中Fe、Cu的生物可接受性均有提高,而煮熟的波纹巴非蛤中Fe的生物可接受性提高的同时,Cu的生物可接受性却降低。METIAN等[26]研究紫贻贝(M.galloprovincialis)仿生消化也发现,煮熟后紫贻贝锰(Mn)、镅(Am)的生物可接受性提高,但Cd、钴(Co)、锌(Zn)等的生物可接受性却降低。贝类的不同食用方式可能引起其食糜在人体消化环境中消化过程的改变,不同元素受到的影响不一致,Fe、Cu生物可利用性发生不同程度改变,这种改变可能影响到近江牡蛎和波纹巴非蛤中Fe、Cu在人体中的吸收和利用,改变可能进入人体循环系统Fe、Cu的量。总体看2种试验贝类熟食比生食能为人体提供更多的Fe摄入量。
贝类品种的差异影响金属配合物的配体组成,近江牡蛎和波纹巴非蛤经过仿生消化后,形成了不同的仿生食糜成分,且仿生食糜基体成分复杂,食糜提取液中金属元素结合态、形态、结构态等存在差异,相同金属元素的不同形态分布可能影响其生物可接受性,而不同金属元素也可能由配位能力的因素,导致生物可接受性的不同。
近江牡蛎和波纹巴非蛤中Fe、Cu生物可接受性大小与其总量高低并没有明显的关系,且消化液提取量均比总量低。以往评估贝类样品为人体提供的微量元素摄入时,多数采用总量进行评估,结果可能导致摄入量被高估或是低估,考虑到实际食物进入人体消化系统并不是完全被消化吸收,此试验选择更加符合人体消化方式的全仿生消化方法处理样品,在进行评估的时候加入生物可接受性参数,结果可能更为科学有效。
-
表 1 正交试验设计表
Table 1 Orthogonal design table
编号
No.ρ(氮)/mg·L-1
Nρ(磷)/10-2 mg·L-1
Pρ(铁)/10-2 mg·L-1
Fe3+1 2.47 (1) 0.99 (1) 0.52 (1) 2 2.47 (1) 4.96 (2) 1.68 (2) 3 2.47 (1) 9.93 (3) 2.58 (3) 4 4.94 (2) 0.99 (1) 1.68 (2) 5 4.94 (2) 4.96 (2) 2.58 (3) 6 4.94 (2) 9.93 (3) 0.52 (1) 7 7.42 (3) 0.99 (1) 2.58 (3) 8 7.42 (3) 4.96 (2) 0.52 (1) 9 7.42 (3) 9.93 (3) 1.68 (2) 表 2 不同氮质量浓度对绿色颤藻叶绿素a和藻体质量浓度的影响
Table 2 Effect of N concentrations on chlorophyll-a contents and dry weight of O.chlorine
编号
No.ρ(氮)/mg·L-1
Nρ(叶绿素a)/μg·L-1
Chl-a叶绿素a增加率/%
increase rate of Chl-aρ(藻体)/g·L-1
dry weight增重率/%
weight gain rate1 0 27.82±7.60a -0.48 0.16±0.01a 0.29 2 0.01 46.53±10.47ab -0.13 0.16±0.01a 0.29 3 0.06 65.75±11.24b 0.24 0.16±0.02a 0.24 4 0.25 71.23±8.89b 0.34 0.18±0.02a 0.41 5 1.24 69.33±9.06b 0.30 0.16±0.03a 0.29 6 2.47 69.16±11.16b 0.30 0.17±0.01a 0.35 7 6.18 99.69±14.21c 0.88 0.19±0.01a 0.47 8 12.36 227.75±15.87d 3.28 0.30±0.03b 1.35 9 24.72 294.44±22.82e 4.54 0.36±0.04c 1.83 10 61.80 297.73±19.98e 4.60 0.36±0.02c 1.83 11 247.21 292.18±25.38e 4.50 0.35±0.03c 1.76 12 494.42 288.73±7.14e 4.43 0.24±0.09c 0.91 表 3 不同磷质量浓度对绿色颤藻叶绿素a和藻体质量浓度的影响
Table 3 Effect of P concentrations on chlorophyll-a contents and dry weight of O.chlorine
编号
No.ρ(磷)/mg·L-1
Pρ(叶绿素a)/μg·L-1
Chl-a叶绿素a增加率/%
increase rate of Chl-aρ(藻体)/g·L-1
dry weight增重率/%
weight gain rate1 0 44.21±3.64a -0.17 0.24±0.02a 0.94 2 9.93×10-4 51.39±16.12ab -0.03 0.26±0.07ab 1.06 3 1.99×10-3 52.45±16.87ab -0.01 0.29±0.04abc 1.29 4 9.93×10-3 66.79±3.44ab 0.26 0.31±0.04bcd 1.47 5 1.99×10-2 74.95±15.58b 0.41 0.34±0.01cde 1.71 6 9.93×10-2 104.95±19.05c 0.97 0.34±0.01cde 1.71 7 0.20 115.77±2.05cd 1.18 0.36±0.04def 1.83 8 0.99 120.43±9.49cd 1.27 0.37±0.03defg 1.94 9 1.99 164.68±10.57e 2.10 0.38±0.02efg 2.00 10 4.96 139.39±14.96d 1.62 0.42±0.03fg 2.29 11 9.93 137.84±25.95d 1.59 0.42±0.02g 2.35 12 19.85 120.11±19.70cd 1.26 0.42±0.03fg 2.29 表 4 不同铁质量浓度对绿色颤藻叶绿素a和藻体质量浓度的影响
Table 4 Effect of Fe3+ concentrations on chlorophyll-a contents and dry weight of O.chlorine
编号
No.ρ(铁)/ mg·L-1
Fe3+ρ(叶绿素a)/μg·L-1
Chl-a叶绿素a增加率/%
increase rate of Chl-aρ(藻体)/g·L-1
dry weight增重率/%
weight gain rate1 0 72.50±3.25a 0.36 0.22±0.01a 0.71 2 5.16×10-5 74.25±1.24ab 0.40 0.22±0.02ab 0.76 3 2.58×10-4 78.93±1.95abc 0.48 0.24±0.03abc 0.88 4 5.16×10-3 82.56±8.36abc 0.55 0.27±0.01cde 1.18 5 2.58×10-2 90.43±1.17bcd 0.70 0.28±0.01de 1.23 6 5.16×10-2 103.57±4.37de 0.95 0.30±0.05def 1.35 7 0.26 117.57±7.54ef 1.21 0.33±0.02f 1.64 8 0.52 121.77±7.81f 1.29 0.34±0.01f 1.71 9 2.58 121.48±3.72f 1.29 0.33±0.03f 1.59 10 25.81 113.92±3.95ef 1.14 0.31±0.02ef 1.47 11 51.67 91.70±1.07cd 0.73 0.26±0.03bcd 1.06 表 5 绿色颤藻叶绿素a质量浓度的正交试验结果
Table 5 Chlorophyll-a contents result of orthogonal design test of O.chlorine
编号
No.ρ(氮)/mg·L-1
Nρ(磷)/10-2 mg·L-1
Pρ(铁)/10-2 mg·L-1
Fe3+ρ(叶绿素a)/μg·L-1
content of Chl-a1 2.47 (1) 0.99 (1) 0.52 (1) 25.81 2 2.47 (1) 4.96 (2) 1.68 (2) 18.87 3 2.47 (1) 9.93 (3) 2.58 (3) 22.33 4 4.94 (2) 0.99 (1) 1.68 (2) 50.54 5 4.94 (2) 4.96 (2) 2.58 (3) 48.77 6 4.94 (2) 9.93 (3) 0.52 (1) 47.15 7 7.42 (3) 0.99 (1) 2.58 (3) 45.21 8 7.42 (3) 4.96 (2) 0.52 (1) 51.04 9 7.42 (3) 9.93 (3) 1.68 (2) 60.50 表 6 绿色颤藻藻体质量浓度的正交试验结果
Table 6 Dry weight result of orthogonal design test of O.chlorine
编号
No.ρ(氮)/mg·L-1
Nρ(磷)/10-2 mg·L-1
Pρ(铁)/10-2 mg·L-1
Fe3+ρ(藻体)/ g·L-1
dry weight1 2.47 (1) 0.99 (1) 0.52 (1) 0.11 2 2.47 (1) 4.96 (2) 1.68 (2) 0.11 3 2.47 (1) 9.93 (3) 2.58 (3) 0.09 4 4.94 (2) 0.99 (1) 1.68 (2) 0.11 5 4.94 (2) 4.96 (2) 2.58 (3) 0.10 6 4.94 (2) 9.93 (3) 0.52 (1) 0.12 7 7.42 (3) 0.99 (1) 2.58 (3) 0.11 8 7.42 (3) 4.96 (2) 0.52 (1) 0.13 9 7.42 (3) 9.93 (3) 1.68 (2) 0.13 -
[1] 马祖友. 蓝藻的生长生理特征及其竞争优势研究[D]. 杨凌: 西北农林科技大学, 2005. [2] 戴瑾瑾, 陈德辉, 高云芳, 等. 蓝藻毒素的研究概况[J]. 武汉植物学研究, 2009, 27(1): 90-97. doi: 10.3969/j.issn.2095-0837.2009.01.014 [3] 王欣伊, 阚振荣, 王梅梅. 淡水藻类产毒研究进展[J]. 生物学杂志, 2005, 22(2): 5-9. doi: 10.3969/j.issn.2095-1736.2005.02.002 [4] 查广才, 麦雄伟, 周昌清, 等. 凡纳滨对虾低盐度养殖池浮游藻类群落研究[J]. 海洋水产研究, 2006, 27(1): 1-7. doi: 10.3969/j.issn.1000-7075.2006.01.001 [5] 彭聪聪, 李卓佳, 曹煜成, 等. 凡纳滨对虾半集约化养殖池塘浮游微藻优势种变动规律及其对养殖环境的影响[J]. 海洋环境科学, 2011, 30(2): 193-198. doi: 10.3969/j.issn.1007-6336.2011.02.010 [6] BRITTAIN S, MOHAMED Z A, WANG J, et al. Isolation and characterization of microcystins from a River Nile strain of Oscillatoria tenuis Agardh ex Gomont[J]. Toxicon, 2000, 38(12): 1759-1771. doi: 10.1016/S0041-0101(00)00105-7
[7] 金星. 藻类代谢产物中典型异味物质及其变化规律研究[D]. 南京: 南京理工大学, 2009. [8] 曹平, 黄翔鹄, 李长玲, 等. 颤藻对凡纳滨对虾生长和免疫相关酶活力的影响[J]. 渔业现代化, 2011, 38(5): 25-30. doi: 10.3969/j.issn.1007-9580.2011.05.006 [9] 梁伟峰, 陈素文, 李卓佳, 等. 虾池常见微藻种群温度、盐度和氮、磷含量生态[J]. 应用生态学报, 2009, 20(1): 223-227. [10] 王颜萍, 何鹰, 郑晓玲, 等. 铁限制条件下东海原甲藻分泌铁载体[J]. 生态学报, 2005, 25(10): 2788-2791. doi: 10.3321/j.issn:1000-0933.2005.10.047 [11] 蒲新明. 长江口区浮游植物营养限制因子的研究[D]. 青岛: 中国科学院海洋研究所, 2000. [12] SANO T, KAYA K. A 2-amino-2-butenoic acid (Dhb)-containing microcystin isolated from Oscillatoria agardhii[J]. Tetrahedron Lett, 1995, 36(47): 8603-8606. doi: 10.1016/0040-4039(95)01824-22095-1736.2005.02.002
[13] FUJⅡ K, SIVONEN K, NAGANAWA E, et al. Non-toxic peptides from toxic cyanobacteria, Oscillatoria agardhii[J]. Tetrahedron, 2000, 56(5): 725-733. doi: 10.1016/S0040-4020(99)01017-0
[14] JIA W, HUANG X H, LI C L. A preliminary study of the algicidal mechanism of bioactive metabolites of Brevibacillus laterosporus on Oscillatoria in prawn ponds[J]. Sci World J, 2014, doi: 10.1155/2014/869149.
[15] 贾雯, 黄翔鹄, 李长玲, 等. 侧孢短芽孢杆菌溶藻活性代谢产物对虾池颤藻溶藻效果研究[J]. 水产学报, 2013, 27(3): 465-472. https://www.cqvip.com/QK/90183X/201303/45244554.html [16] 贺春花, 黄翔鹄, 李长玲, 等. 温度、光照度、盐度和pH对颤藻生长的限制条件研究[J]. 渔业现代化, 2011, 38(6): 20-25. doi: 10.3969/j.issn.1007-9580.2011.06.005 [17] 寻涛. 高锰酸钾预氧化混凝去除水中颤藻的试验研究[J]. 安全与环境工程, 2009, 16(4): 45-48. doi: 10.3969/j.issn.1671-1556.2009.04.012 [18] MILLIE D F, GREENE D A, JOHNSEN P B. Effects of the carotenoid-inhihiting herbicide, flufidone on Oscillatoria agardhii Gomont(cyanobacteria)[J]. Aquat Toxicol, 1990, 16(1): 41-52. doi: 10.1016/0166-445X(90)90076-2
[19] 梁伟峰, 李卓佳, 陈素文, 等. 对虾养殖池塘微藻群落结构的调查与分析[J]. 南方水产, 2007, 3(5): 33-39. doi: 10.3969/j.issn.2095-0780.2007.05.006 [20] 刘孝竹, 李卓佳, 蓸煜成, 等. 低盐度养殖池塘浮游微藻的种类组成、数量及优势种群变动[J]. 南方水产, 2009, 5(1): 9-16. doi: 10.3969/j.issn.1673-2227.2009.01.002 [21] 曹煜成, 王少沛, 李卓佳, 等. 微绿球藻、隐藻和颤藻竞争氮磷营养的通径分析[J]. 渔业科学进展, 2012, 33(4): 99-106. doi: 10.3969/j.issn.1000-7075.2012.04.013 [22] WILBUR K M, ANDERSON N G. Electrometric and colorimetric determination of carbonic Anhydrase[J]. Biol Chem, 1948, 176(1): 147-154. doi: 10.1016/S0021-9258(18)51011-5
[23] 国家环保总局, 《水和废水检测分析方法》编委会. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002: 670-671. [24] 石岩峻. 赤潮藻对营养盐的吸收及生长和相关特性研究[D]. 北京: 北京化工大学, 2004. [25] 李志伟, 崔力拓, 齐凤生, 等. 铜绿微囊藻生长特征及营养盐对其生长的影响[J]. 水利渔业, 2006, 26(1): 65-68. doi: 10.3969/j.issn.1003-1278.2006.01.031 [26] 江燕, 甘旭华, 唐欣昀, 等. 氮、磷营养因子对赤潮异弯藻生长的影响[J]. 应用生态学报, 2006, 17(3): 557-559. doi: 10.3321/j.issn:1001-9332.2006.03.040 [27] 黄翔鹄. 对虾高位池水环境养殖污染和浮游微藻生态调控机制研究[D]. 上海: 东华大学, 2013. [28] YUSOFF F M, ZUBAIDAH M S, MATIAS H B, et al. Phytoplankton succession in intensive marine shrimp culture ponds treated with a commercial bacterial product[J]. Aquac Res, 2002, 33(4): 269-278. doi: 10.1046/j.1355-557x.2002.00671.x
[29] 陆珠润, 蒋霞敏, 陆艳晶. 氮、磷、铁对原绿球藻生长的影响[J]. 宁波大学学报: 理工版, 2009, 22(3): 326-331. doi: 10.3969/j.issn.1001-5132.2009.03.006 [30] KRUSKOPF M, DU P S. Growth and filament length of the bloom forming Oscillatoria simplicissima (Oscillatoriales, Cyanophyta) in varying N and P concentrations[J]. Hydrobiologia, 2006, 556(1): 357-362. doi: 10.1007/s10750-005-1061-0
[31] 徐景亮. 东海原甲藻的氮、磷、铁、锰营养生态位研究[D]. 广州: 暨南大学, 2005. [32] MARTIN J H, FITZWATER S E. Iron deficiency limits phytoplankton growth in the northeast Pacific subartic[J]. Nature, 1988, 331(6154): 341-343. doi: 10.1038/331341a0
[33] 孙颖颖. 环境因子对球等鞭金藻生长的影响[D]. 大连: 大连理工大学, 2007. [34] 王扬才. 氮、磷、铁营养盐浓度对牟氏角毛藻生长的影响[J]. 海洋渔业, 2006, 28(2): 173-176. doi: 10.3969/j.issn.1004-2490.2006.02.016 [35] 吕秀平, 胡晗华, 张栩, 等. Fe3+对浮游颤藻生长和光合作用的影响[J]. 水生生物学报, 2005, 29(3): 318-322. doi: 10.3321/j.issn:1000-3207.2005.03.014 [36] 刘静. Fe3+对富营养化水体中三种常见淡水藻类生长的影响[D]. 扬州: 扬州大学, 2008. -
期刊类型引用(1)
1. 旷泽行,汪慧娟,谷阳光,齐占会,黄洪辉. 海南岛昌化江河口海域生物体重金属富集特征与概率健康风险评价. 海洋环境科学. 2021(05): 699-706 .  百度学术
百度学术
其他类型引用(2)
计量
- 文章访问数: 3466
- HTML全文浏览量: 125
- PDF下载量: 1669
- 被引次数: 3



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
