Genetic diversity analysis of six cultured populations of Macrobrachium rosenbergii using microsatellite markers
-
摘要:
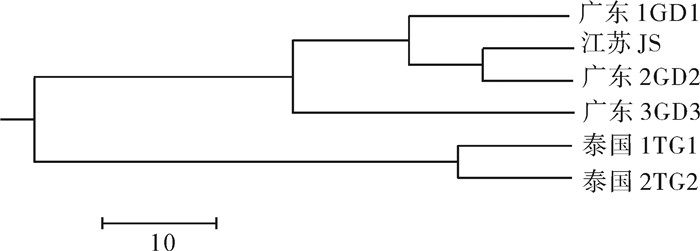
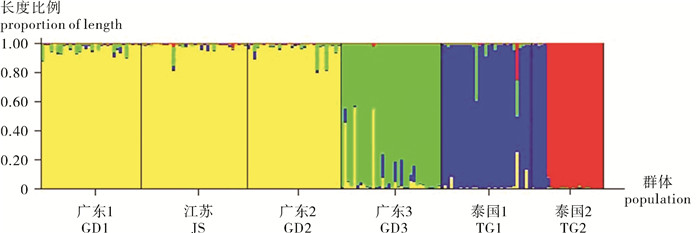
采用微卫星分子标记技术比较了中国和泰国罗氏沼虾(Macrobrachium rosenbergii)养殖群体的遗传多样性及遗传结构。使用12对荧光标记微卫星引物扩增3个广东罗氏沼虾养殖群体、1个江苏养殖群体以及2个泰国养殖群体,结果显示所检测的12个微卫星位点均具有较高的多态性[多态信息含量(PIC)=0.853~0.941]。各群体均具有较高的遗传多样性水平[期望杂合度(He)=0.848~0.896]。群体间遗传分化指数(Fst)及AMOVA分析显示,群体间遗传分化属于中低水平(Fst<0.15),遗传变异有5.27%来自群体之间,94.73%来自于群体内部。遗传距离分析显示江苏群体和广东群体2的遗传距离(Da)最近(0.160 8);而广东群体1和泰国群体2之间的遗传距离最远(0.695 8)。基于遗传距离构建的UPGMA系统进化树显示,6个群体聚为2个大支,广东3个群体与江苏群体聚为一支,泰国的2个群体聚为另一支。研究结果显示所分析的中国和泰国罗氏沼虾养殖群体均具有较高的遗传多样性,但彼此亲缘关系较远。
Abstract:We compared the genetic diversity and structure of cultivated population of Macrobrachium rosenbergii collected from different areas in China and Thailand by microsatellite analysis. Twelve fluorescently labeled primers were used to amplify microsatellite DNA from three Guangdong cultivated populations (GD1, GD2 and GD3), one Jiangsu cultivated population (JS) in China and two cultivated populations in Thailand (TG1 and TG2). The results show that the detected microsatellite loci possessed high polymorphism (PIC=0.853~0.941). All the populations analyzed displayed high genetic diversity (He=0.848~0.896). Genetic differentiation index (Fst) and AMOVA analysis reveal that the genetic differentiation within populations was relatively low (Fst < 0.15). About 5.27% genetic variation was derived from inter-populations, while 94.73% variation was derived from intra-population. Nei′s genetic distance indicates that the genetic distance between JS and GD2 population was the lowest (0.160 8), while that between the GD1 population and TG2 population was the highest (0.695 8). Phylogenetic analysis displays that these six M.rosenbergii populations could be divided into two groups. GD1, GD2, GD3 and JS populations were clustered together as one group and TG1 population was clustered with the TG2 population as another group. The results demonstrate that the analyzed cultivated M.rosenbergii populations maintained relatively high genetic diversity, and there was low kinship between China and Thailand populations.
-
东南太平洋地区蕴含着极为丰富的生物种类资源[1],且在生物群落分布上呈现出一定的地理与生态特点[2]。在智利、秘鲁等近海海域,已发现的生物种类多达10 000余种,其中鱼类和甲壳类占据总数的2/5,且生物多样性呈自海域北部向南部递减的趋势[3]。然而,在东南太平洋公海海域,由于受到多种复杂因素的制约,生物多样性的监测以及深入研究工作面临挑战,可获取的海洋生物生态信息相对有限。这阻碍了对东南太平洋生态系统稳定性的深入研究和全面认知,也不利于制定合理的渔业资源保护和管理方法。一直以来,长期监测是研究海洋生物多样性和生态系统的重要方法,通过长期持续性地监测可以掌握海洋生物现状以及正在变化的过程[4]。但是,长期监测考验时间、人力及资金成本,其数据可靠性与监测时间成正比。尤其在深远海地区,由于科考活动较少以及受到恶劣环境限制,往往导致监测数据缺失或者不完整,影响了科学观察数据的准确性[5]。近年来,人们发现海洋捕食者的食物组成也可以反映海洋生态系统的种间关系和生物群落结构,能够揭示研究海域的生物多样性[6]。这是因为捕食者具有与气候变化、人为干扰等因素协同影响生态系统稳定的特性,是食物网、食物链结构稳定的重要调控者[7]。作为评估生物多样性的重要指标,捕食者的种群动态变化可以更有效地评估生态系统健康状况,揭示生物多样性稳定性的潜在风险[8]。同时,利用捕食者研究生物多样性有利于学者通过单一生境的研究,全面监测生态系统的动态变化,有效地反映群落结构和种间关系[9]。比如,Link等[10] 以不同的鱼作为生物采集器,评估了西苏格兰大陆架、芬迪湾和加拿大部分乔治海岸东北大陆架生态系统的底栖生物多样性以及空间分布。Faring等[11] 也通过大西洋鳕 (Gadus morhua) 的胃含物组成研究了毛鳞鱼 (Mallotus villosus) 的空间分布及其丰度。因此,利用海洋捕食者作为生物采集器是研究海洋生物多样性的有效补充方法。
茎柔鱼 (Dosidicus gigas) 广泛分布于东南太平洋,承担着连接生态系统营养物质循环与能量传递的关键生态职能[12]。该物种生长速度快、生命周期短[13],具有贪婪且随机的食性,能够捕食体型大于自身的生物,是一种凶猛的“机会主义”捕食者[13]。在栖息海域内,茎柔鱼大量捕食甲壳类、头足类和鱼类以满足其生长发育需求[13-14]。此外,茎柔鱼也是许多大型海洋生物的重要饵料,其主要捕食者包括大型鱼类、哺乳动物和海鸟等[15-16]。而且茎柔鱼资源丰度的变化会影响其饵料生物和捕食者的种群规模与分布[17]。由此可见,茎柔鱼具备监测海域生物多样性的重要特征和潜力。相较于传统的长期定点监测或者大范围稀疏的采样方法,以茎柔鱼为生物采集器,能够在相对较短的时间跨度内获取多个时间节点和空间位置的生物多样性数据,捕捉生物多样性的动态变化以及空间异质性,为生物多样性研究提供一种新的思路。基于此,本研究采用茎柔鱼作为生物采集器,通过Alpha多样性 (Alpha diversity) 和多变量分析法,研究了东南太平洋赤道、厄瓜多尔南部和秘鲁北部等鱿钓渔场海域在不同季节的茎柔鱼饵料生物组成差异。同时,基于广义加性混合模型 (Generalized Additive Mixed-Effects Models, GAMMs) 解析了生物多样性指数与海域环境因子的相关关系。旨在阐明东南太平洋鱿钓渔场饵料生物多样性的时空分布特征及其影响因素,为深入研究东南太平洋生物多样性提供基础数据,并为东南太平洋鱿钓渔场的渔业资源管理与养护提供科学依据。
1. 材料与方法
1.1 样本来源
茎柔鱼样本是中国远洋鱿钓作业渔船于2020年7—9月及2022年1—10月采集的渔获物。采集站点分布在东南太平洋的赤道作业海域、厄瓜多尔外海南部和秘鲁外海北部,采集范围分别为100°W—112°W、1°N—7°S,91°W—97°W、2°S—6°S以及85°W—88°W、3°S—8°S (图1)。考虑到远洋鱿钓作业渔船在作业过程中具有相对流动性的特点,在每个采样站点均采用随机抽取的方式进行样本采集。采集工作完成后,所获取的样本即刻放置于 −20 ℃的冰箱内保藏,以确保样本的完整性与可用性,为后续研究工作提供可靠的基础材料。
1.2 胃含物分析
在实验室常温解冻之后,测定每尾茎柔鱼样本的生物学数据,记录胴长、体质量以及胃饱满度。胴长测定精确到1 mm,体质量精确至1 g。以Zuev等[18] 的胃饱满等级划分为标准,将样本胃饱满度划分为5个等级。本研究选取120尾胃饱满度等级 ≥2的茎柔鱼胃样本进行胃含物分析。其中,赤道海域39尾,厄瓜多尔外海南部48尾,秘鲁外海北部33尾 (表1)。将每尾鱼完整的胃摘取后,置于密封袋中,保存于−40 ℃冰箱,用于后续胃含物分析。
表 1 东南太平洋不同采样海域和采样季节的茎柔鱼样本数Table 1 Number of samples of D. gigas by different sampling sea areas and sampling seasons in Southeast Pacific尾 采样海域
Sampling area春季
Spring夏季
Summer秋季
Autumn冬季
Winter总数
Total赤道海域 Equatorial waters — 19 20 — 39 厄瓜多尔外海南部 Offshore of South Ecuador — — — 48 48 秘鲁外海北部 Offshore of North Peru 17 — — 16 33 总数 Total 17 19 20 64 120 每尾茎柔鱼的胃于实验室常温解冻后,用无纺布吸干表面水分,用剪刀纵向剪开胃壁,取出胃含物并称质量。称质量后的胃含物中加入超纯水充分混匀,先后经20、40、60、80和100目的筛网过滤,将残留在筛网上的耳石、角质颚、可辨认的浮游动物以及未消化的食物残渣逐一取出并保存。共获得可辨认的耳石样本9 952个、角质颚样本107个、浮游动物8种。在显微镜 (SMZ745T, Nikon) 成像系统下,对所有胃含物进行拍照,同时用数字卡尺测量耳石、角质颚等硬组织的长度和宽度等,精确至0.01 mm。对照耳石鉴定指南[19]、头足类与角质颚鉴定指南[20] 及浮游生物图片集[21] 等,对所有胃含物鉴定至最低分类阶元,最后将收集的耳石、角质颚、浮游生物等样品置于95% (φ) 的乙醇溶液中保存。
1.3 饵料生物多样性分析
根据胃含物鉴定结果统计每种饵料生物的数量,其中鱼类数量以左矢耳石或右矢耳石的最大计数值为准,头足类数量以角质颚上颚或下颚最大计数值为准,其他饵料生物则直接计数。根据每种饵料生物数量,计算其出现频次。饵料生物的出现频率 (F%)、相对丰度 (R%) 计算公式分别为:
$$ F {\text{%}}{\mathrm{=}}\frac{O_{{i}}}{S_{\text {total}}} \times 100 {\text{%}}$$ (1) $$ R {\text{%}}{\mathrm{=}}\frac{N_{{i}}}{N_{\text {total}}} \times 100 {\text{%}} $$ (2) 式中:Oi为第i个饵料生物出现的次数;Stotal为胃含物分析的胃样本总数;Ni为第i个饵料生物的个体数;Ntotal为所有饵料生物的个体总数。
根据胃含物统计结果,计算饵料生物的Margalef指数[22] 和Shannon-Wiener指数[23]。两指数从不同维度对生物群落特征进行量化描述。Margalef指数作为衡量物种丰富度的重要指标,具有独特的生态学意义。基于对胃含物中的饵料生物种类和数量的综合考量,Margalef指数越高,表示饵料生物种类越丰富[24]。Shannon-Wiener指数专注于描述生物群落结构的复杂度,它不仅考虑物种的数量,还兼顾各个物种的相对丰度。该指数值越高,表明生物群落中各个物种的分布更为均匀,种间关系更为复杂多样,即生物多样性更加丰富,反之则越低[25]。两指数的计算公式分别为:
$$D{\mathrm{=}}(S{\text{−}}1) / \ln N$$ (3) $$ {{H}}{{\text{'}}}{{\mathrm{=}}{\text{−}}}\sum {{P}}_{{i}}{\text{log}}_{\text{2}}{{P}}_{{i}} $$ (4) 式中:D为Margalef指数;H'为Shannon-Wiener指数;S为指茎柔鱼饵料生物的种类数;N为胃样本中出现的饵料生物个体总数;$ {{P}}_{{i}} $为第i个饵料生物个体数的占比。
1.4 统计分析
通过置换多元方差分析 (Parametric multivariate analysis of variance, PERMANOVA) 研究东南太平洋鱿钓渔场不同海域、不同季节的饵料生物组成差异。并通过相似性百分比 (Similarity percentages, SIMPER) 计算不同饵料生物对物种组成时空差异的贡献率。
针对生物多样性指数,采用Shapiro-Wilk检验分析其是否符合正态性分布,若符合正态分布,利用单因素方差分析 (One-way, ANOVA) 检验Margalef和Shannon-Wiener指数在采样海域间和采样季节间的差异性;若Shapir-Wilk 检验结果显示数据不符合正态分布,则利用Kruskal-Wallis 检验分析各多样性指数的差异性。显著差异水平设为p<0.05。
采用GAMMs[26] 分析东南太平洋鱿钓渔场饵料生物的时空分布。由于茎柔鱼消化速度极快,本研究以茎柔鱼的采样站点作为其饵料生物的栖息位置。因此,利用GAMMs分别拟合分析Margalef和Shannon-Wiener指数随采样经纬度的变化趋势,以研究饵料生物多样性的空间分布格局,模型中以采样海域为随机因子。此外,利用GAMMs依次拟合Margalef和Shannon-Wiener指数与海表温度 (Sea surface temperature, SST)、海平面高度 (Sea surface height, SSH)、叶绿素a浓度 (Chlorophyll a concentration, Chl-a)、净初级生产力 (Net primary productivity per unit volume, NPPV) 等环境因子的关系,模型中以采样海域、采样季节为随机因子。SST、SSH、Chl-a和NPPV从哥白尼海洋服务网站下载 (SST and SSH, doi: 10.48670/moi-00016; Chl-a and NPPV, doi: 10.48670/moi-00148)。为了减少日变化的偏差,环境因子的时间分辨率为月,SST空间分辨率为0.083°×0.083°,SSH、Chl-a、NPPV空间分辨率为0.25°×0.25°。
所有统计分析均利用R平台进行。其中PERMANOVA、SIMPER分析可通过“vegan”包实现;GAMMs通过“mgcv”包实现。
2. 结果
2.1 饵料生物组成
在东南太平洋赤道海域、厄瓜多尔外海南部和秘鲁外海北部的鱿钓渔场,在茎柔鱼的胃含物中共发现43种生物种类,来自于4纲9目20科32属。以辐鳍鱼纲种类最多,共有27种;头足纲和腹足纲分别有8和7种,软甲纲种类仅1种,为端足类。其中,荧串光鱼 (Vinciguerra lucetia) 的出现频率和相对丰度均最高 (F%=87.50%, R%=43.99%);钝吻缘光鱼(Margrethia obtusirostra) 次之 (F%=70.83%, R%=30.45%);诺贝珍灯鱼 (Lampanycyus nobilis)、长翅龟螺 (Diacavolinia longirostris) 的出现频率均低于1.00%,相对丰度均为0.01% (附录A,详见http://dx.doi.org/10.12131/20240293 的资源附件)。
2.2 生物多样性的空间分布
分析显示,赤道海域、厄瓜多尔外海南部和秘鲁外海北部等采样海域间的饵料生物组成存在显著性差异 (PERMANOVA, F=0.04, p<0.05);而且,任意两海域间饵料生物组成均存在显著差异 (赤道海域和厄瓜多尔外海南部:F=0.03,p<0.05;赤道海域和秘鲁外海北部:F=0.06,p<0.05;厄瓜多尔外海南部和秘鲁外海北部:F=0.05,p<0.05)。根据SIMPER分析结果可知,饵料生物组成的海域间差异贡献率最高的是荧串光鱼,贡献率为25.74%;其次是钝吻缘光鱼,贡献率为20.99%;贡献率高于5%的物种还包括明灯鱼属 (9.16%)、朗明灯鱼 (7.85%);其余物种的贡献率均低于3.10% (图2)。
生物多样性指数结果显示,东南太平洋鱿钓渔场生物种类的Margalef指数存在显著的海域间差异(
 $ \chi $2=9.01, p=0.01)。然而,不同采样海域之间,Shannon-Wiener指数无显著差异(F=2.47, p=0.08)。在秘鲁外海北部,Margalef和Shannon-Wiener指数最大,分别为$ \text{1.48±}\text{0.70} $ (范围0.31~2.26)和$ \text{1.13±0.48} $ (0.14~2.08);厄瓜多尔外海南部次之,分别为$ \text{1.24±0.}\text{66} $ (0.40~3.46) 和$ \text{1.12±0.}\text{34} $ (0.50~1.95);赤道海域最低,分别为$ \text{1.02±}\text{0.46} $ (0.36~2.15)和$ \text{0.96±}\text{0.37} $ (0.20~1.76) (图3-a—3-b)。GAMMs显示,Margalef和Shannon-Wiener指数与经度、纬度显著相关 (表2)。Margalef指数在110°W—−100°W海域范围内最小,低于1.25;在85°W—88°W,0°S—2°S范围内,Margalef指数最大,均大于1.5。Shannon-Wiener指数在110°W—95°W海域范围内小于1.0;在90°W—93°W,0°S—2°S范围内最大,大于1.4。此外两个指数均从大洋海域向近海海域呈增大趋势(图4-a—4-b)。
表 2 东南太平洋鱿钓渔场生物多样性指数与经度、纬度的广义加性混合效应模型结果Table 2 Results of GAMMs fitted biodiversity indexes with longitude and latitude in squid jigging fishery ground of Southeast Pacific
$ \chi $2=9.01, p=0.01)。然而,不同采样海域之间,Shannon-Wiener指数无显著差异(F=2.47, p=0.08)。在秘鲁外海北部,Margalef和Shannon-Wiener指数最大,分别为$ \text{1.48±}\text{0.70} $ (范围0.31~2.26)和$ \text{1.13±0.48} $ (0.14~2.08);厄瓜多尔外海南部次之,分别为$ \text{1.24±0.}\text{66} $ (0.40~3.46) 和$ \text{1.12±0.}\text{34} $ (0.50~1.95);赤道海域最低,分别为$ \text{1.02±}\text{0.46} $ (0.36~2.15)和$ \text{0.96±}\text{0.37} $ (0.20~1.76) (图3-a—3-b)。GAMMs显示,Margalef和Shannon-Wiener指数与经度、纬度显著相关 (表2)。Margalef指数在110°W—−100°W海域范围内最小,低于1.25;在85°W—88°W,0°S—2°S范围内,Margalef指数最大,均大于1.5。Shannon-Wiener指数在110°W—95°W海域范围内小于1.0;在90°W—93°W,0°S—2°S范围内最大,大于1.4。此外两个指数均从大洋海域向近海海域呈增大趋势(图4-a—4-b)。
表 2 东南太平洋鱿钓渔场生物多样性指数与经度、纬度的广义加性混合效应模型结果Table 2 Results of GAMMs fitted biodiversity indexes with longitude and latitude in squid jigging fishery ground of Southeast Pacific效应
Effect模型参数因子
Model parameter估计
Estimated标准偏差
Standard deviance自由度
Degree of freedomt F p Margalef 指数Margalef index 随机效应
Random effect采样海域 Sampling sea area 1.05×10–5 残差Residual 0.47 固定效应
Fixed effect截距Intercept 1.16 0.07 16.75 <2×10–16 经度-纬度 (Longitude-Latitude) 24 0.40 0.01 Shannon-Wiener 指数Shannon-Wiener index 随机效应
Random effect采样海域 Sampling sea area 5.81×10–6 残差Residual 0.30 固定效应
Fixed effect截距Intercept 1.03 0.04 23.00 <2×10–16 经度-纬度 (Longitude- Latitude) 3 0.48 0.009 注:GAMMs中多样性指数作z-score标准分数转化。 Note: The biodiversity indexes are standardized by z-score transformation for GAMMs. 2.3 生物多样性的季节性分布
本研究结果显示,东南太平洋鱿钓渔场不同季节间的饵料生物组成存在显著性差异 (PERMANOVA, F=0.03, p<0.05);且任意两个季节间的饵料生物组成也存在显著性差异 (春季和夏季:F=0.08,p<0.05;春季和秋季:F=0.10,p<0.05;春季和冬季:F=0.03,p<0.05;夏季和秋季;F=0.09,p<0.05;夏季和冬季:F=0.09,p<0.05;秋季和冬季:F=0.02,p<0.05)。SIMPER分析可知,饵料生物组成季节间差异贡献率最大的是荧串光鱼,贡献率为25.17%;其次是钝吻缘光鱼,贡献率为21.38% ;贡献率高于5%的物种还包括明灯鱼属 (9.15%)、朗明灯鱼 (6.19%);其余物种对于饵料生物组成季节性差异的贡献率均≤3.00% (图5)。
在东南太平洋鱿钓渔场,Margalef和Shannon-Wiener指数均不存在显著季节性差异 (Margalef指数:χ2=6.25,p=0.10;Shannon-Wiener指数:F=0.83,p=0.48)。在春季,Margalef和Shannon-Wiener指数较大,分别为$ \text{1.43±}\text{0.75} $ (范围0.31~3.18) 和$ \text{1.11±}\text{0.52} $ (0.20~2.08);冬季次之,分别为$ \text{1.29±0.66} $ (0.31~2.65) 和$ \text{1.10±0.37} $ (0.14~1.95);秋季较低,分别为$ \text{0.96±}\text{0.45} $ (0.36~1.92) 和$ \text{0.98±}\text{0.33} $ (0.51~1.57);夏季分别为$ \text{1.13±0.53} $ (0.46~2.15) 和$ \text{0.99±0.41} $ (0.45~1.76) (图6-a—6-b)。
2.4 生物多样性与海域环境因子的关系
在东南太平洋鱿钓渔场,海表温度为18.55~26.87 ℃,平均 (22.94±1.82) ℃;海平面高度为 −1.52~−0.28 m,平均 (−1.37±0.18) m;叶绿素a 质量浓度为0.22~1.31 mg·m−3,平均 (0.33±0.16) mg·m−3;净初级生产力为11.81~23.11 mg·m−3·d−1 ,平均 (16.77±2.64) mg·m−3 ·d−1。4个环境因子在不同采样海域和采样季节的数据如表3 所示。差异性检验结果显示,4个环境因子均存在显著的采样海域间差异和采样季节间差异 (海域间:SST,χ2=27.27,p<0.01;SSH, χ2=14.56,p<0.01;Chl-a, χ2=24.98,p<0.01。季节间:SST, χ2=34.14,p<0.01;SSH,χ2=7.82,p=0.04;Chl-a,χ2=19.81,p<0.01);然而,净初级生产力在采样海域和采样季节间的差异性均不显著 (海域间:χ2=0.41,p=0.82;季节间:χ2=7.23, p=0.06)。
表 3 东南太平洋鱿钓渔场不同采样海域和采样季节间的环境因子数据Table 3 Summary of environmental variables by different sampling sea areas and sampling seasons in squid jigging fishery ground of Southeast Pacific海表温度
Sea surface
temperature/℃海平面高度
Sea surface
height/m叶绿素a浓度
Chlorophyll a concentration/
(mg·m−3)净初级生产力
Net primary productivity/
(mg·m−3·d−1)采样海域 Sampling sea area 赤道 Equator 21.10~26.87 −1.52~−1.37 0.22~0.43 11.81~22.80 厄瓜多尔 Ecuador 20.87~24.63 −1.48~−1.29 0.28~0.45 13.72~23.11 秘鲁 Peru 18.55~22.22 −1.37~−0.29 0.30~1.31 14.53~18.99 采样季节 Sampling season 春季 Spring 18.55~22.21 −1.51~−0.28 0.35~1.30 15.53~22.80 夏季 Summer 23.20~24.26 −1.44~−1.37 0.25~0.30 11.81~19.22 秋季 Autumn 22.51~26.87 −1.46~−1.41 0.22~0.42 13.39~23.11 冬季 Winter 19.74~24.33 −1.48~−1.28 0.28~0.45 13.96~21.83 GAMMs分析结果显示,东南太平洋鱿钓渔场饵料生物种类的Margalef指数、Shannon-Wiener指数均与海平面高度、叶绿素a浓度以及净初级生产力存在显著的效应关系,而与海表温度关系不显著 (表4)。两指数均与叶绿素a 浓度呈负效应关系,随着叶绿素a浓度升高而降低;相反,海平面高度以及净初级生产力对两指数具有正效应的影响关系,两指数随着海平面高度升高、净初级生产力增加而增大 (图7)。
表 4 东南太平洋鱿钓渔场多样性指数与环境因子的广义加性混合效应模型拟合结果Table 4 Results of GAMMs fitted biodiversity indexes with environmental variables in squid jigging fishery ground of Southeast Pacific效应
Effect模型参考因子
Model parameter估计
Estimated标准偏差
Standard deviance自由度
Degree of freedomt F p Margalef指数 Margalef index 随机效应
Random effect采样季节 Sampling season 0.22 采样海域 Sampling sea area 残差Residual 0.78 固定效应Fixed effect 截距Intercept −0.05 4.92×10−11 −0.23 0.81 海表温度SST 1.00 3.55 0.07 海平面高度SSH 1.00 13.99 0.05×10−2 叶绿素a浓度Chl-a 1.00 9.26 0.04×10−1 净初级生产力NPPV 1.00 6.61 0.13×10−1 Shannon-Wiener指数 Shannon-Wiener index 随机效应
Random effect采样季节Sampling season 0.24 采样海域Sampling sea area 残差Residual 0.81 固定效应
Fixed effect截距Intercept −0.05 1.84×10−7 −0.20 0.85 海表温度SST 1.00 0.06 0.80 海平面高度SSH 1.00 9.74 0.003 叶绿素a浓度Chl-a 1.00 6.67 0.01 净初级生产力NPPV 1.00 4.14 0.05 注:GAMMs中多样性指数、环境因子均作z-score标准分数转化。 Note: The diversity indexes and environmental variables are standardized by z-score transformation for GAMMs. ![]() 图 7 东南太平洋鱿钓渔场生物多样性指数与环境因子的关系注:蓝色实线和灰色阴影分别表示GAMMs拟合曲线及其95%置信区间。Fig. 7 Relationship between biodiversity indexes and environmental variables in squid jigging fishery ground of Southeast PacificNote: Blue solid lines represents model fits of Generalized Additive Mixed-Effects Models, with 95% confidence intervals in grey shading.
图 7 东南太平洋鱿钓渔场生物多样性指数与环境因子的关系注:蓝色实线和灰色阴影分别表示GAMMs拟合曲线及其95%置信区间。Fig. 7 Relationship between biodiversity indexes and environmental variables in squid jigging fishery ground of Southeast PacificNote: Blue solid lines represents model fits of Generalized Additive Mixed-Effects Models, with 95% confidence intervals in grey shading.3. 讨论
3.1 物种组成
生物多样性是维持生态系统稳定与健康的重要基础,通过物种之间捕食与被捕食的关系维系着系统中能量流动平衡[30]。因而,海洋捕食者,尤其是食性贪婪的捕食者被认为是揭示海洋生态系统生物多样性的重要媒介[6],可有效弥补当前难以开展长期监测生物多样性的短板[9]。茎柔鱼是凶猛、贪婪的随机主义捕食者,摄食生态位宽,摄食的饵料生物种类多样[13-14]。比如,在加利福利亚湾,茎柔鱼主要摄食巴拿马底灯鱼 (Benthosema panamense)、胡瓜鱼 (Osmerus mordax)、鳀 (Engraulis japonicus) 等98种生物种类[31],与加利福利亚洋流系统的主要物种数相当[32]。在智利中部近海和外海,茎柔鱼的胃含物发现了24种饵料生物,包括鱼类、甲壳类、头足类等,与洪堡洋流系统中已记录在库的生物种类组成相似[33]。可见,茎柔鱼的食物组成可以反映其栖息海域的主要生物种类组成及群落结构。本研究在茎柔鱼的胃含物中共发现东南太平洋赤道海域、厄瓜多尔外海南部和秘鲁外海北部等海域43种不同生物种类,包括鱼类、头足类、腹足类、软甲类等,以鱼类的出现频率最高,这与李云凯等[34] 和Bruno等[35] 的研究结果相近。该结果进一步佐证了在东南太平洋赤道海域至秘鲁外海的生物组成以鱼类为主的观点[28,36]。
此外,本研究还发现茎柔鱼胃含物中荧串光鱼的出现频率最高,其次是明灯鱼属、灯笼鱼属等。这些小型鱼类是东南太平洋温热带水域最丰富的中上层鱼类之一,富含多不饱和脂肪酸,可满足捕食者日常代谢、生长发育等能量需求[37]。在秘鲁外海,茎柔鱼的栖息水层及昼夜垂直迁徙习性与荧串光鱼的高度重合[38],这可能是后者在茎柔鱼胃含物分析中出现频率高的原因。然而,本研究SIMPER分析发现荧串光鱼是东南太平洋鱿钓渔场不同海域以及不同季节饵料生物组成差异贡献率最大的物种,说明荧串光鱼资源分布存在海域及季节性差异[39-40]。可见,茎柔鱼的饵料生物组成与海域的饵料生物资源可获得性紧密相关,也进一步佐证了以茎柔鱼为生物采集器监测东南太平洋生物多样性是可行的。
3.2 生物多样性时空分布
生物多样性分布通常会随着时间推移、地理位置以及环境气候差异而变化[41]。1995年,Rosenzweig[42] 认为生物多样性自赤道向两极呈下降趋势,这是全球公认的生物多样性分布格局。然而,Chaudhary等[43] 在研究全球变暖趋势下的生物多样性分布变化时,发现随着温度的升高,生物多样性呈“双峰形”变化趋势,即生物多样性随着纬度升高而降低,但在赤道海域附近出现明显的下降趋势。本研究中,赤道海域、厄瓜多尔外海南部和秘鲁外海北部的生物多样性存在显著性差异,秘鲁外海北部的多样性指数最高,厄瓜多尔外海南部次之,赤道海域多样性指数最低。GAMMs拟合生物多样性指数的空间分布图证实了这一结果,即生物多样性指数从赤道海域到秘鲁公海呈递增的趋势。这与Miloslavich等[28] 研究结果相一致,后者发现洪堡洋流系统对秘鲁海域的生态环境产生了显著影响,使其生物种类更为丰富。在东南太平洋,秘鲁处于沿海上升流带,丰富的营养盐促进了浮游植物光合作用,提高了秘鲁外海的初级生产力,为浮游动物及海洋捕食者提供了更为丰富的饵料生物资源[40,44]。可见,海域生态环境对生物多样性分布至关重要。
本研究还发现东南太平洋近海海域多样性指数显著高于大洋海域,高度异质性的生物栖息地极有可能是导致这一现象产生的关键因素。通常,近海海域具备复杂且多样的生态系统,如珊瑚礁生态系统、海草床生态系统、红树林生态系统以及河口生态系统等[45],这些多样化的生态环境可为各类海洋生物提供多元化的生存条件,既能为生物个体早期生长阶段提供适宜温度、盐度及营养物质等,也能满足其成长发育过程中对栖息空间、食物资源种类多样化的需求,乃至繁殖阶段对特定繁殖场所及环境因子的严格要求[46]。相较而言,大洋海域生境类型呈现出较为单一的特征,主要以深海平原、深海热液区等为主,在很大程度上限制了大洋海域生物的种类丰富度和数量分布规模[28]。因此,生境异质性是生物多样性空间分布差异的重要影响因素,并且生物多样性指数自深海海域至近海增大的变化趋势可能是一种全球性的海洋生物分布特征。
此外,海洋生物多样性的季节性变化是海洋生态系统的重要特征之一。张浩博等[47] 通过环境DNA分析评估鱼类多样性的时空分布,发现夏季生物多样性指数显著高于秋季和冬季;而张敬怀等[48] 利用2004—2015大亚湾底拖网数据分析大亚湾生物多样性时,发现夏季生物多样性指数略高于春季,但无明显的季节性差异。本研究中生物多样性指数不存在季节间差异,春季生物多样性指数相对较高,表明东南太平洋生物多样性的季节性分布相对稳定,这可能与荧串光鱼、明灯鱼等优势种资源有关。Sasaki和Lauenroth[49] 研究揭示了优势种对生态系统稳定性的影响,其结果表明:生态系统稳定性与优势种的相对丰度呈显著正相关,即优势种丰度增加可明显增强生态系统恢复力并维持生物多样性稳定。因此,东南太平洋海域生物多样性在季节间的稳定性可能主要归因于优势种的生态补偿作用。
3.3 生物多样性时空分布与环境的关系
全球多达40%的海洋生态系统正受到多重环境压力的影响,这些压力源主要包括气候变化、过度捕捞及人类活动等[50]。已有研究表明,极端事件频发、气候变异以及海平面上升等环境变化均可能对生物多样性产生负面影响,进而威胁生态系统稳定性[51]。本研究发现东南太平洋鱿钓渔场的生物多样性指数与海平面高度呈正相关关系,这可能源于海平面变化通过调控营养物质分布格局而影响了海洋生物的营养获取[52]。
通常海平面高度与冷水团分布存在紧密关联。当冷暖水团交汇或者上升流区域与周边海水存在显著性差异时,会在海平面高度场形成特定的高值区[53]。这些高值区通常具有低温的环境特点,且富含高浓度的营养盐和叶绿素a,为海洋生物提供了营养丰富的栖息地,从而显著促进了其繁殖和种群发展[54]。
在海洋生态系统中,浮游植物是海洋初级生产力的关键组成部分,为海洋生物的生长发育、繁殖等提供了重要的物质基础[55]。本研究结果显示,东南太平洋鱿钓渔场的生物多样性指数与净初级生产力呈正相关,这与Wilsey等[56]、Costanza等[57] 的研究结果一致,他们都发现生物多样性随着净初级生产力的提升而增加的现象。然而,本研究同时发现,东南太平洋鱿钓渔场的生物多样性指数与叶绿素a浓度呈负相关关系,这与Witman等[58] 关于北半球表层动物群落的研究结果一致,后者的研究显示,在高叶绿素a浓度的海域,某些优势种可以获得竞争优势,其过度繁殖反而导致整体物种多样性下降[58]。生物多样性的时空分布差异是多种环境因素协同作用的结果。尽管初级生产力变化对生物多样性分布具有直接影响,但其具体作用机制和影响因素仍需通过后续深入研究来进一步验证。
4. 结论
本研究基于胃含物分析法,以茎柔鱼为生物采集器,初步阐明了东南太平洋鱿钓渔场生物多样性的时空分布及其与海域环境因子的关系。东南太平洋鱿钓渔场生物多样性存在显著的空间变化,生物多样性指数由大洋至近海海域呈增大趋势,这与海域生境异质性相关;优势种的补偿作用维持了东南太平洋不同季节生物多样性的稳定。海平面高度、净初级生产力、叶绿素a浓度与生物多样性指数显著相关,证明了海域初级生产力是生物多样性时空分布的主要影响因素。这些结果可为开展该海域生态系统稳定性研究奠定基础,并为后续开展海洋生物资源的养护管理,以及经济种类的可持续开发利用提供重要的资料参考。
-
表 1 用于罗氏沼虾微卫星扩增的引物序列及其退火温度
Table 1 Primer sequence and annealing temperature for microsatellite marker amplification
序号No. 位点loci 重复序列repeat sequence 引物序列primer sequence 片段大小production size 复性温度/℃ annealing 1 EMR-31B (CA)7 F: FAM-GCTGTGCTCCAAAATCTCTCTC
R: CTCACCCATACTTGACAACGAC210 58 2 EMR-55 (TTA)13 F: FAM-GAAGTCATCCGACAAACTTCAC
R: AGTAATCATGTGGCCTAGCCTAG200 58 3 EMR81 (CT)15 F: TAMRA-GGAACCAGTGAAAAAGCAATGA
R: GGGGTGCATTCAAAAATAGGT240 58 4 EMR85 (AG)12 F: FAM-GACGGACAGACATTCATTAGCC
R: ATTCACCCCACACTTTGACATT220 58 5 Mbr1 (GA)24 F: HEX-CCCACCATCAATTCTCACTTACC
R: TCCTTTTCACATCGTTTCCAGTC272~320 60 6 Mbr-2 (GT)22 F: HEX-TTCCCGACCAATTTCTCTTTCTC
R: GGCAAAAATGATCTTGGATTCAC298~336 60 7 Mbr-3 (AG)14 F: TAMRA-CAACTCTATGTTTCGGCATTTGG
R: GGGGAATTTTACCGATGTTTCTG232~284 62 8 Mbr-4 (GT)29 F: HEX-CCACCTACCGTACATTCCCAAAC
R: CGGGGCGACTTTTAGTATCGAC288~326 62 9 Mbr-5 (AG)25 F: HEX-CAAGGCTCGTGTCTCTTGTTTC
R: GCTTGTACTTGTTCAGCTTTTGC286~328 62 10 Mbr-9 (TG)5(AG)17 F: TAMRA-TTGTTTGCTTGTTTAGTGTCAAGG
R: CTCCAAAACCGAAAAATCCTCAC240~284 60 11 Mbr11 (AG)31 F: TAMRA-GTATTGAGAACAAAGGCGCACAG
R: ATCTCTTTCCAAAACAGGGCACA263~291 60 12 MRMB25 (CT)17 F: FAM-CCGGTCCAAAGGAATACAGA
R: GTGGGTGGTGTCCCTATGTT194~216 46 表 2 罗氏沼虾12个微卫星位点的等位基因数、杂合度及多态信息含量
Table 2 Number of alleles, heterozygosity and polymorphic information content of 12 microsatellite loci of M.rosenbergii
位点locus 等位基因数Na 有效等位基因数Ne Shannon指数I 观测杂合度Ho 期望杂合度He 多态信息含量PIC EMR-31B 22 12.71 2.766 0.673 0.924 0.915 EMR-55 14 10.79 2.506 0.906 0.910 0.908 EMR81 23 13.72 2.853 0.980 0.930 0.919 EMR85 21 14.70 2.840 0.853 0.935 0.933 Mbr1 19 12.96 2.725 0.671 0.926 0.897 Mbr-2 13 6.61 2.124 0.691 0.852 0.853 Mbr-3 16 8.68 2.449 0.590 0.888 0.887 Mbr-4 24 18.33 3.024 0.723 0.948 0.941 Mbr-5 19 11.40 2.666 0.891 0.915 0.914 Mbr-9 28 16.57 3.045 0.713 0.943 0.939 Mbr11 17 8.41 2.439 0.488 0.884 0.886 MRMB25 14 7.88 2.321 0.994 0.876 0.876 均值mean 19.17 11.90 2.646 0.765 0.911 0.906 表 3 6个罗氏沼虾养殖群体的遗传多样性
Table 3 Genetic diversity of six populations of M.rosenbergii
参数index 广东1 GD1 江苏JS 广东2 GD2 广东3 GD3 泰国1 TG1 泰国2 TG2 等位基因数Na 13.000 12.750 12.000 13.833 12.500 10.917 有效等位基因数Ne 7.409 7.204 6.791 8.947 8.274 6.558 Shannon指数I 2.207 2.159 2.135 2.348 2.239 2.046 观测杂合度Ho 0.821 0.751 0.720 0.761 0.808 0.683 期望杂合度He 0.871 0.858 0.861 0.896 0.881 0.848 多态信息含量PIC 0.850 0.846 0.845 0.880 0.857 0.806 表 4 6个罗氏沼虾养殖群体的遗传分化指数
Table 4 Fixation index (Fst) of six populations of M.rosenbergii
广东1 GD1 江苏JS 广东2 GD2 广东3 GD3 泰国1 TG1 泰国2 TG2 广东1 GD1 江苏JS 0.023 0 广东2 GD2 0.024 5 0.006 3 广东3 GD3 0.031 0 0.046 9 0.041 0 泰国1 TG1 0.071 3 0.073 4 0.074 9 0.058 4 泰国2 TG2 0.093 1 0.077 8 0.082 5 0.072 9 0.006 1 表 5 6个罗氏沼虾养殖群体的AMOVA分析
Table 5 AMOVA analysis among six populations of M.rosenbergii
变异来源source of variation 自由度df 平方和sum of squares 方差组分variance component 百分率/% percentage 群体间among populations 5 108.518 0.296 76 5.273 51 群体内within populations 312 1663.064 5.330 52 94.726 49** 总变异total 317 1771.582 5.627 28 注:* *. 1 023次模拟检验后显示为极显著(P<0.01)
Note:* *. very significance (P<0.01) after 1 023 permutation tests表 6 6个罗氏沼虾养殖群体的遗传距离(对角线下)和遗传相似度(对角线上)
Table 6 Nei′s genetic distance (below diagonal)and genetic similarity (above diagonal)of six populations of M.rosenbergii
广东1 GD1 江苏JS 广东2 GD2 广东3 GD3 泰国1 TG1 泰国2 TG2 广东1 GD1 - 0.760 4 0.737 4 0.664 0 0.393 9 0.311 7 江苏JS 0.273 9 - 0.851 5 0.572 2 0.407 7 0.432 5 广东2 GD2 0.304 6 0.160 8 - 0.597 4 0.382 2 0.390 0 广东3 GD3 0.409 4 0.458 2 0.415 2 - 0.423 5 0.379 7 泰国1 TG1 0.611 7 0.597 1 0.661 8 0.559 3 - 0.814 2 泰国2 TG2 0.695 8 0.568 1 0.611 7 0.628 4 0.205 5 - -
[1] NEW M B, SINGHOLKA S. Freshwater prawn farming. A manual for the culture of Macrobrachium rosenbergii[M]. FAO Fish Tech, 1985, 225: 1-118. doi: 10.1016/0044-8486(84)90320-X
[2] 杨国梁, 陈雪峰, 王军毅, 等. 罗氏沼虾产业在中国持续增长的经济与社会原因分析[J]. 浙江海洋学院学报, 2011, 30(5): 450-457. doi: 10.3969/j.issn.1008-830X.2011.05.015 [3] 张海琪, 何中央, 徐晓林, 等. 罗氏沼虾缅甸野生群体和浙江养殖群体的遗传多样性比较[J]. 中国水产科学, 2004, 11(6): 506-512. doi: 10.3321/j.issn:1005-8737.2004.06.004 [4] 蒋钦杨, 杨学明, 郭亚芬, 等. 3个不同群体罗氏沼虾线粒体16S rRNA基因序列分析及遗传差异[J]. 水产科学, 2005, 24(10): 28-31. doi: 10.3969/j.issn.1003-1111.2005.10.009 [5] 杨学明, 郭亚芬, 陈福艳, 等. 罗氏沼虾3个群体线粒体COI基因的序列差异和遗传标记研究[J]. 遗传, 2006, 28(5): 540-544. doi: 10.3321/j.issn:0253-9772.2006.05.008 [6] 姚茜, 杨频, 陈立侨, 等. 罗氏沼虾三群体线粒体D-loop基因序列差异的初步研究[J]. 水产学报, 2007, 31(1): 18-22. https://cstj.cqvip.com/Qikan/Article/Detail?id=25387846&from=Qikan_Article_Detail [7] 陈雪峰, 杨国梁, 孔杰, 等. 人工养殖与选育对罗氏沼虾遗传多样性的影响[J]. 水生生物学报, 2012, 36(5): 866-873. doi: 10.3724/SP.J.1035.2012.00866 [8] CHAREONTAWEE K, POOMPUANG S, NA-NAKORN U, et al. Genetic diversity of hatchery stocks of giant freshwater prawn (Macrobrachium rosenbergii) in Thailand[J]. Aquaculture, 2007, 271(1): 121-129. doi: 10.1016/j.aquaculture.2007.07.001
[9] 朱其建, 戴习林, 邹卫丽, 等. 罗氏沼虾抗病选育群体的抗病性能及其遗传多样性分析[J]. 水产学报, 2013, 30(10): 1468-1478. doi: 10.3724/SP.J.1231.2013.38664 [10] 农业部渔业局. 中国渔业年鉴[M]. 北京: 中国农业出版社, 2012: 1-134. https://xueshu.baidu.com/usercenter/paper/show?paperid=2ecf4ddeeaa147fe5b8746aee49c1506 [11] CHAREONTAWEE K, POOMPUANG S, NA-NAKORN U, et al. Isolation and characterization of microsatellites in giant freshwater prawn Macrobrachium rosenbergii[J]. Mol Ecol Notes, 2006, 6(3): 823-825. doi: 10.1111/j.1471-8286.2006.01358.x
[12] DIVU D, KARUNASAGAR I, KARUNASAGAR I. Microsatellite DNA markers in the giant freshwater prawn, Macrobrachium rosenbergii: a tool for genetic analysis[J]. Mol Ecol Resour, 2008, 8(5): 1040-1042. doi: 10.1111/j.1755-0998.2008.02148.x
[13] MOHANTY P, SAHOO L, PARIDA K, et al. Development of polymorphic EST-SSR markers in Macrobrachium rosenbergii by data mining[J]. Cons Genet Resour, 2013, 5(1): 133-136. doi: 10.1007/s12686-012-9751-1
[14] TAMURA K, PETERSON D, PETERSON N, et al. MEGA5: molecular evolutionary genetics analysis using maximum likelihood, evolutionary distance, and maximum parsimony methods[J]. Mol Biol Evol, 2011, 28(10): 2731-2739. doi: 10.1093/molbev/msr121
[15] KALINOWSKI S T, TAPER M L, MARSHALL T C. Revising how the computer program CERVUS accommodates genotyping error increases success in paternity assignment[J]. Mol Ecol, 2007, 16(5): 1099-1106. doi: 10.1111/j.1365-294X.2007.03089.x
[16] EXCOFFIER L, LISCHER H L. Arlequin suite ver 3.5 : a new series of programs to perform population genetics analyses under Linux and Windows[J]. Mol Ecol Resour, 2010, 10(3): 564-567. doi: 10.1111/j.1755-0998.2010.02847.x
[17] EVANNO G, REGNAUT S, GOUDET J. Detecting the number of clusters of individuals using the software STRUCTURE: a simulation study[J]. Mol Ecol, 2005, 14(8): 2611-2620. doi: 10.1111/j.1365-294X.2005.02553.x
[18] CHAUHAN T, RAJIV K. Molecular markers and their applications in fisheries and aquaculture[J]. Adv Biosci Biotechnol, 2010, 1(4): 281-291. doi: 10.4236/abb.2010.14037
[19] LIU Z J, CORDES, J F. DNA marker technologies and their applications in aquaculture genetics[J]. Aquaculture, 2004, 242(1): 1-37. doi: 10.1016/j.aquaculture.2004.05.027
[20] ZANE L, BARGELLONI L, PATARNELLO T. Strategies for microsatellite isolation: a review[J]. Mol Ecol, 2002, 11(1): 1-16. doi: 10.1046/j.0962-1083.2001.01418.x
[21] BORNMAN D M, HESTER M E, SCHUETTER J M, et al. Short-read, high-throughput sequencing technology for STR genotyping[J]. Biotechniques, 2012, 4(1): 1-6. https://pubmed.ncbi.nlm.nih.gov/25621315/
[22] SHETE S, TIWARI H, ELSTON R C. On estimating the eterozygosity and polymorphism information content value[J]. Theor Popul Biol, 2000, 57(3): 265-271. doi: 10.1006/tpbi.2000.1452
[23] BOTSTEIN D, WHITE R L, SKOLNICK M. Construction of genetic linkage map in man using restriction fragment length polymorphisms[J]. Am J Hum Genet, 1980, 32(3): 314-331. https://pubmed.ncbi.nlm.nih.gov/6247908/
[24] 包文斌, 束婧婷, 许盛海, 等. 样本量和性比对微卫星分析中群体遗传多样性指标的影响[J]. 中国畜牧杂志, 2007, 43(1): 6-9. doi: 10.3969/j.issn.0258-7033.2007.01.002 [25] QIN Y, SHI G, SUN Y. Evaluation of genetic diversity in Pampus argenteus using SSR markers[J]. Genet Mol Res, 2013, 12(4): 5833-5841. doi: 10.4238/2013.November.22.10
[26] 傅建军, 李家乐, 沈玉帮, 等. 草鱼野生群体遗传变异的微卫星分析[J]. 遗传, 2013, 35(2): 192-201. doi: 10.3724/SP.J.1005.2013.00192 [27] 崔蕾, 谢从新, 李艳和, 等. 斑点叉尾 
[28] 孙立元, 郭华阳, 朱彩艳, 等. 卵形鲳鲹育种群体遗传多样性分析[J]. 南方水产科学, 2014, 10(2): 67-71. doi: 10.3969/j.issn.2095-0780.2014.02.010 -
期刊类型引用(11)
1. 周胜杰,胡静,杨蕊,杨其彬,马振华. 三斑海马早期发育观察. 南方农业学报. 2021(08): 2302-2310 .  百度学术
百度学术
2. 周胜杰,胡静,马振华,陈旭,杨其彬,杨蕊,刘亚娟,孟祥君. 尖吻鲈尾部骨骼胚后发育研究. 水产科学. 2018(03): 342-347 .  百度学术
百度学术
3. 周胜杰,马婷,胡静,马振华,杨其彬,陈旭,杨蕊,刘亚娟,孟祥君. 尖吻鲈仔鱼骨骼发育观察. 南方农业学报. 2018(03): 592-598 .  百度学术
百度学术
4. 刘亚娟,程大川,周胜杰,马振华,胡静,杨蕊. 尖吻鲈仔、稚鱼异速生长研究. 海洋渔业. 2018(02): 179-188 .  百度学术
百度学术
5. 江民天,周胜杰,胡静,杨蕊,马振华,孟祥君,苏胜齐. 军曹鱼仔鱼异速生长研究. 南方农业学报. 2018(11): 2320-2326 .  百度学术
百度学术
6. 区又君,谢木娇,李加儿,温久福,周慧,刘奇奇. 广东池塘培育四指马鲅亲鱼初次性成熟和苗种规模化繁育技术研究. 南方水产科学. 2017(04): 97-104 .  本站查看
本站查看
7. 区又君,李加儿,柳琪,周慧. 斜带髭鲷和紫红笛鲷早期发育阶段的行为选择. 水生态学杂志. 2017(01): 86-93 .  百度学术
百度学术
8. 聂广锋,李加儿,区又君,吴水清,王鹏飞,温久福. 梭鱼早期发育阶段体色形成与鳍的分化. 动物学杂志. 2016(03): 395-403 .  百度学术
百度学术
9. 谢木娇,区又君,李加儿,温久福,王鹏飞,王雯,陈世喜. 不同发育阶段的四指马鲅消化道组织学比较研究. 南方水产科学. 2016(02): 51-58 .  本站查看
本站查看
10. 区又君,李加儿,艾丽,王雯,李刘冬. 条石鲷早期鳞被的形成和初生鳞的发育. 南方水产科学. 2016(05): 112-117 .  本站查看
本站查看
11. 区又君,李加儿,柳琪. 褐毛鲿早期发育阶段行为选择和游泳能力的研究. 生态科学. 2016(04): 1-11 .  百度学术
百度学术
其他类型引用(2)




 下载:
下载:






 粤公网安备 44010502001741号
粤公网安备 44010502001741号
