Effect of different copper salts on acute toxicity and histomorphology of juvenile sea cucumbers
-
摘要:
采用急性毒性试验方法研究异源铜盐对仿刺参(Apostichopus japonicus)幼参的毒性影响,通过24 h、48 h、72 h和96 h的致死数量统计分析硫酸铜(CuSO4)/氯化铜(CuCl2)对幼参的半致死质量浓度(LC50)和安全质量浓度(SC);利用石蜡切片显微定性观察不同铜盐对刺参幼参后肠的毒性情况。结果表明,CuSO4来源的Cu2+对幼参24 h、48 h和72 h的LC50均大于CuCl2来源的Cu2+对幼参24 h、48 h和72 h的LC50,而CuCl2对幼参96 h LC50大于CuSO4对幼参96 h LC50;异源铜盐在暴露前48 h内对刺参的毒性影响极其显著,随着暴露时间的延长其对刺参的毒性影响不显著;2种铜盐(以铜离子质量浓度为0.06 mg · L-1计)对幼参的消化道均有不同程度的腐蚀作用,导致结缔层与上皮层分离,CuCl2对刺参肠道的毒性(类似腐蚀作用)大于CuSO4的毒性;不同的阴离子对Cu2+的毒性有拮抗作用。
Abstract:The toxic effect of different copper salts on juvenile sea cucumbers was studied by acute toxicity test. LC50 and safety concentration of two copper ions (CuSO4 and CuCl2) were determined by statistical analysis of dead numbers of juvenile sea cucumbers (Apostichopus japonicus) after treatments of 24 h, 48 h, 72 h and 96 h, respectively. The toxic effect of different copper salts on foregut of juvenile sea cucumbers were observed on paraffin section with microscope. The results show that LC50s of CuSO4 on juvenile sea cucumbers after treatment of 24 h, 48 h and 72 h were higher than that of CuCl2, while LC50 of CuCl2 was higher than that of CuSO4 after 96 h treatment. The difference of toxic effect of juvenile sea cucumbers exposed to the two copper ions within 48 h was very significant, but was not significant as the exposure time. Corrosive actions were observed in digestive tracts of juveniles treated with two kinds of salts (with concentration of 0.06 mg · L-1 as copper ion), which resulted in connective tissue layer separating from the epithelial layer. The toxicity (corrosive action) of CuCl2 on digestive tracts of sea cucumbers was greater than that of CuSO4. Different anions of copper salts had antagonistic effect to copper toxicity.
-
Keywords:
- CuSO4 /
- CuCl2 /
- juvenile sea cucumber /
- LC50 /
- digestive tract histomorphology
-
珠江河口是南海北部最重要的河口型生态系统,是许多经济鱼类产卵、索饵和避难的场所,也是多种经济鱼类入海或溯河洄游的通道,渔业资源丰富且种类繁多[1-2]。近年来,随着粤港澳大湾区经济的不断发展,人类活动频繁,渔业资源被过度开发,鱼类资源量和种类多样性呈下降趋势[3]。为保护珠江河口鱼类资源,确保其可持续利用,亟需开展鱼类多样性的评估和监测。长期以来,鱼类多样性的研究主要是通过对传统的形态学特征进行比较作为分类依据,但由于鱼类的生长具有阶段性,传统的形态学方法对于鱼卵、幼鱼或形态特征被破坏的鱼类鉴定难度较大,即使有完整的成年标本,但遇到形态极其相似的物种,即便经验丰富的分类学家也很难识别[4]。因此,快速、准确的可模式化操作用于物种鉴定的方法显得尤为重要。
DNA条形码技术是一种利用生物体DNA中一段保守片段对物种进行区分的分子鉴定手段,经过近20年的实践和发展,已形成了一套完善的研究体系,能够快速准确地识别鉴定鱼类。而在DNA条形码技术中,DNA条形码的选择十分关键[5]。2005年,Ward[6]提出使用线粒体细胞色素氧化酶I(Cytochrome oxidase subunit I, COI) 基因5'端约652 bp的序列用于鉴定澳大利亚的207种鱼类,表明COI基因能够有效区分不同物种。随后该片段由于大小适宜、进化速度适中、相对保守且检测简单高效等特点,已成为鱼类鉴定的经典条形码。
近年来,DNA条形码技术不断发展并且与环境DNA (Environmental DNA) 结合产生了新型的环境DNA宏条形码 (Meta-barcoding) 技术,该技术由于非侵入性、无污染、检测范围广以及敏感性高等特点,在鱼类多样性研究中得到广泛使用[7-9]。环境DNA宏条形码技术就是从环境样本提取DNA、选取特定序列扩增并进行高通量测序,通过测序分析获得大量OTU序列 (Operational taxonomic units, OTUs),然后通过序列检索比对来鉴定环境中存在的目标生物类群物种组成[10]。该技术最重要的两个条件是选取一段合理的序列扩增,以及一个全面的检索数据库。但由于环境样本中DNA片段小,以及高通量测序长度的限定,就需要比较短的微型条形码。Miya等[11]开发了一套12S rDNA基因的环境DNA通用PCR引物,针对880种鱼类线粒体中具有的163~185 bp超可变区域。该微型条形码即使在只获得少量DNA的情况时也可以很容易地扩增,而且它在物种之间也有很高的差异,现广泛应用于鱼类多样性研究[12-13]。然而12S rDNA序列也并不是完美的,其长度相对于国际上通用的DNA条形码长度 (552~652 bp) 仍太短,可能在某些近缘物种间无法识别或者识别错误[14]。例如Wang等[15]根据12S rDNA序列将中华瞻星鱼 (Uranoscopus chinensis) 鉴定为日本瞻星鱼 (U. japonicus)。
不管是DNA条形码技术还是环境DNA宏条形码技术都十分依赖对比数据库的准确性和全面性[6,13]。目前,鱼类条形码数据库有NCBI (National Center for Biotechnology Information) 和BOLD (Barcode of Life Data),但由于上传门槛低,数据量冗余庞大,经常出现比对错误,制约了条形码技术的应用。因此,本研究选取南海典型河口珠江河口的鱼类作为研究对象,基于线粒体COI和12S rDNA基因构建珠江河口鱼类条形码数据库,并初步探讨其系统发育关系以及两种DNA条形码在珠江河口鱼类物种鉴定中的适用性,以期为珠江河口鱼类的群落动态监测以及物种多样性保护提供技术支持。
1. 材料与方法
1.1 样品采集及形态鉴定
在珠江河口设置采样断面,设置依据是尽可能覆盖整个珠江河口水域以及盐度范围,但由于珠江河口航道繁忙,工程建设多,以及部分海域存在建筑垃圾,所以拖网站位的选取受到一定限制。本研究共设置9个采样站位 (图1),其站位覆盖地区盐度范围为9~32.17,此外在盐度低于9的地区设置过站位,但这些地区基本处于航道,禁止底拖网。样本采集通过底拖网方式进行,采集时间为2020年4月、2020年9月以及2021年4月。样本冷冻运至实验室后,根据《中国鱼类系统检索》[16]进行形态学分类鉴定。随后取背部肌肉保存于95%乙醇中,于−20 ℃保存备用。
1.2 DNA提取与目的片段的扩增
剪取20~30 mg保存的鱼类肌肉,晾干酒精,用海洋动物组织基因组DNA提取试剂盒 (天根,中国) 提取基因组DNA。采用Ward等[6]设计的引物对COI基因片段进行扩增,引物序列为:Fish-F1:5'-TCAACCAACCACAAAGACATTGGCAC-3'和Fish-R1:5'-TAGACTT CTGGGTGGCCAAAGAATCA-3'。采用Miya等[11]设计的引物对12S rDNA基因片段进行扩增,引物序列为:MiFish-F:5'-GTCGGTAAAACTCGTGCCAGC-3'和MiFish-R:5'-CATAGTG GGGTATCTAATCCCAGTT-TG-3'。使用擎科生物Golden Star T6 Super PCR Mix (1.1×) 试剂盒,扩增体系 (总体积25 μL) 为:Mix预混液22 μL,正反向引物各1 μL,DNA模板1 μL。COI序列扩增反应程序:98 ℃预变性2 min;98 ℃变性10 s,56 ℃复性30 s,72 ℃延伸40 s,35个循环;72 ℃延伸5 min。12S rDNA序列扩增反应程序:98 ℃预变性2 min;98 ℃变性10 s,56 ℃复性30 s,72 ℃延伸20 s,35个循环;72 ℃延伸5 min。
PCR产物用2% TBE琼脂糖凝胶电泳检测,将条带清晰PCR产物送往北京六合华大基因科技有限公司进行测序。
1.3 数据库的构建
对照往年珠江河口鱼类资源调查文献[1,17-21],整理得到珠江河口鱼类名录,物种的有效学名以Fishbase数据库 (www.fishbase.org) 为准。为全面构建珠江河口鱼类DNA条形码数据库,未通过拖网采集到的鱼类种类从GenBank (http://www.ncbi.nlm.nih.gov/genbank/) 筛选并下载COI序列和12S rDNA序列,下载标准是优先下载具有全基因组的序列。
1.4 数据分析
通过DNAStar软件包中的SeqMan软件对测得的COI与12S rDNA序列进行人工校对和拼接[22]。校正后的序列经MitoFish、BOLD、GenBank数据库验证,当序列相似度大于99%时,才能定为同种,确保序列的准确性。运用MEGA-X软件将本研究所得序列与GenBank下载序列合并,分析序列特征,计算碱基组成[23];基于Kimura2-parameter (K2P) 双参数模型对种间遗传距离 (Interspecific genetic distance) 和种内遗传距离 (Intraspecific genetic distance) 进行计算,同时使用COI序列和12S rDNA序列根据种内遗传距离与种间遗传距离绘制遗传距离频数分布直方图[24]。采用ABGD (Automatic Barcode Gap Discovery) 软件将全部序列自动分组,相对间隙宽度值取X=0.8,其余参数全部默认[25]。使用PhyloSuit软件中的ModelFinder程序进行核苷酸序列的模型选择,选出最佳模型GTR+F+I+G4,然后使用PhyloSuit软件中的MrBayes进行贝叶斯系统发育树构建[26]。最后使用itol软件对系统树进行展示和标记[27]。站位图的底图来源于广东省标准地图服务子系统 (http://nr.gd.gov.cn/map/bzdt/),地图数据下载于全国地理信息资源目录服务系统 (http://www.webmap.cn/main.do?method=index),采用ArcGis10.6软件绘制后叠加而成。
2. 结果
2.1 序列库概况
通过底拖网采集珠江河口鱼类标本251尾,经过实验获得219条COI序列和247条12S rDNA序列,共鉴定出99种鱼,隶属于6目10科41属。然后从GenBank数据库下载鱼类165条COI序列和128条12S rDNA序列,共得到384条COI序列和375条12S rDNA序列,隶属于17目66科125属172种 [图2,附录A (详见http://dx.doi.org/10.12131/20210210 的资源附件)]。根据往年珠江河口鱼类资源调查文献初步统计出珠江河口鱼类188种,本研究鱼类占比91%。其中一半种类为鲈形目,占绝对优势,其次是鲽形目和鲱形目,共占比20%。其中包括棘头梅童鱼 (Collichthys lucidus)、风鲚 (Coilia mystus)、杜氏棱鳀 (Thryssa dussumieri) 等咸淡水鱼类优势种以及丽叶鲹 (Alepes djedaba)、带鱼 (Trichiurus lepturus)、银鲳 (Pampus argenteus) 等海水鱼类优势种,常见经济种如龙头鱼 (Harpadon nehereus)、花鰶 (Clupanodon thrissa)、皮氏叫姑鱼 (Johnius belangerii) 等也已全部包括[27]。此外在野外收集了软骨鱼纲的2个物种,条纹斑竹鲨 (Chiloscyllium plagiosum) 和日本燕魟 (Gymnura japonica),从GenBank数据库下载了软骨鱼纲1个物种,尖头斜齿鲨 (Scoliodon laticaudus)。
2.2 线粒体COI和12S rDNA序列的序列特征
172种鱼类384条COI序列经比对对齐,获得一致序列长度为614 bp,平均碱基交换/颠换值为1.29,碱基T、C、A、G的平均含量分别为29.17%、28.60%、24.03%、18.20%,A+T (53.20%) 含量均高于G+C (46.80%),表现出明显的碱基组成偏向性,该结果与海洋鱼类COI基因碱基组成特征一致[6]。172种鱼类375条12S rDNA序列经比对对齐后,长度为163~182 bp,平均碱基交换/颠换值为1.09,碱基T、C、A、G的平均含量分别为19.61%、23.97%、33.90%、22.52%,与COI序列一样,存在A+T (53.51%) 含量显著高于G+C (46.49%) 的现象。
2.3 种间与种内遗传距离
根据K2P遗传距离模型计算384条COI序列结果显示 (表1),172个种类COI序列的种内遗传距离为0~1.66%,平均为0.20%;种间遗传距离为2.16%~40.87%,平均为25.54%,种间平均遗传距离是种内的127.7倍。这一结果符合Hebert等[5]提出的“10倍规则”,即满足种间平均遗传距离值大于种内平均遗传距离10倍的标准可用于区分物种。基于375条12S rDNA序列,172种鱼类种内遗传距离为0~1.79%,平均为0.12%;种间遗传距离为0.59%~72.32%,平均为34.39%;种间平均遗传距离是种内的286.6倍。基于COI序列的遗传距离频数分布直方图能形成明显的条形码间隙,而基于12S rDNA序列的遗传距离频数分布直方图不能形成明显的条形码间隙,说明COI序列能对珠江河口鱼类物种进行区分鉴定,而12S rDNA序列在有些物种间存在区分困难的情况 (图3)。
表 1 基于COI和12S rDNA序列的种内与种间遗传距离Table 1. Genetic distance of intraspecies and interspecies based on mitochondrial COI and 12S rDNA sequences% 遗传距离
Genetic distanceCOI序列 COI sequence 12S rDNA序列 12S rDNA sequence 最小值
Minmum最大值
Maxium平均值
Mean最小值
Minmum最大值
Maxium平均值
Mean种内 Intraspecies 0 1.66 0.2 0 1.79 0.12 种间 Interspecies 2.16 40.87 25.54 0.59 72.32 34.39 2.4 系统发育关系
基于COI序列构建的贝叶斯系统发育树见图4,在物种较多的科中,石首鱼科、鲾科、舌鳎科、带鱼科、鲹科、鲻科可各自形成科的单系支,但在鲀科、鳀科、鰕虎鱼科、鲱科、狗母鱼科中个别物种存在互相交叉的现象,与传统分类存在一些分歧。在属水平上,绝大多数同属物种都能各自聚在一起,仅有小公鱼属 (Stolephorus),䱨属 (Terapon) 和细棘鰕虎鱼属 (Acentrogobius) 3个属的物种未能聚成独立的小分支。软骨鱼纲的3种物种可以形成一个单系支。当种内先验最大遗传距离P为1.29%时,384条DNA序列根据ABGD分析显示有172个分类单元,与本研究物种数量一致。
基于12S rDNA序列构建的贝叶斯系统发育树见图5,在物种较多的科中,带鱼科、舌鳎科、鳀科、鲾科、鲻科、鲀科可各自形成单系支,但在狗母鱼科、鰕虎鱼科、石首鱼科、鲱科、鲹科中聚类效果不明显;软骨鱼纲3种物种可形成一个单系支。在属的水平上,绝大多数同属的物种都能各自聚在一起,仅有细棘鰕虎鱼属、舌鳎属 (Cynoglossus)、蛇鲻属 (Saurida) 和兔头鲀属 (Lagocephalus) 4个属未聚成小分支。软骨鱼纲的3种物种可以形成一个单系支。当种内先验最大遗传距离P为1.29%时,375条DNA序列根据ABGD分析显示有166个分类单元,将带鱼和南海带鱼 (T. nanhaiensis) 聚为一个分类单元,大甲鲹 (Megalaspis cordyla) 和六带鲹 (Caranx sexfasciatus) 聚为一个分类单元,弓斑东方鲀 (Takifugu ocellatus)、星点东方鲀 (T. niphobles) 和黄鳍东方鲀 (T. xanthopterus) 聚为一个分类单元,翼红娘鱼 (Lepidotrigla alata) 和绿鳍鱼 (Chelidonichthys kumu) 聚为一个分类单元,乌鲹 (Parastromateus niger) 和马拉巴若鲹 (Carangoides malabaricus) 聚为一个分类单元,剩余161个由单个物种组成,占比93.6%。这些结果说明COI序列能很好地划分鱼类物种,而12S rDNA序列对于少数近缘物种无法有效划分。
3. 讨论
为了使DNA条形码技术和环境DNA宏条码技术在珠江河口鱼类多样性的研究中得到充分和有效的应用,本研究建立了珠江河口本地鱼类的COI和12S rDNA宏条形码数据库。而本地数据库的有效构建需到达到2个条件[27]:1) 数据库所含物种基本覆盖本地已出现的物种;2) 足够的核苷酸序列特异性来区分密切相关的物种[28]。
3.1 数据库的物种覆盖度
本研究获得172种鱼类物种序列,占珠江河口统计鱼类的91%。李因强[29]研究发现珠江河口鱼类优势种主要为棘头梅童鱼、凤鲚等,以及皮氏叫姑鱼、丽叶鲹等一些常见经济种,本研究已全部包括。剩余16种鱼类未在野外采集到样本,可能是由于本研究的采集方式为底拖网,该方式主要采集底栖鱼类,例如斑点马鲛 (Scomberomorus guttatus) 和革似鲹 (Scomberoides tol) 这种上层鱼类很难捕获[30]。另一方面,GenBank数据库和Bold数据库没有详细的数据可供下载,所以没有进行收集。此外这些鱼类在该地区基本属于偶见种、非经济种,对本研究影响不大。在今后的研究中将持续不断地完善数据库。
3.2 COI条形码在珠江河口鱼类物种鉴定中的适用性
目前已经有多项关于COI条形码在鱼类鉴定的报道。2021年罗纯等[31]使用COI序列研究中日沿海部分鱼类DNA条形码时,其种间与种内平均遗传距离比值为14.81,符合“10×”的阈值规则,可实现物种的高效鉴定;郜星晨和姜伟[32]在2020年使用COI序列建立三峡鱼类DNA条形码数据库时,其种间平均遗传距离为种内的9.38倍,表示COI基因可以作为三峡库区常见鱼类鉴定的有效条形码基因。
本研究中,COI序列种间平均遗传距离是种内的127.7倍,也十分符合“10×”的阈值规则。与上述研究相比,远大于其他研究中的遗传距离比值,这可能由于不同地区鱼类活动范围不同,基因交流不同,所以遗传距离有所差异[33-34]。还有可能就是本实验每种鱼类采样量不足,部分种类COI仅1条,未收集到物种内所有序列差异,导致种内平均遗传距离偏小。此外根据遗传距离频数分布直方图显示COI序列已形成明显的条形码间隙,同时根据ABGD正好将172种鱼类分成172个分类单元,所以COI序列在本研究中具有较好的物种鉴别率,可以满足珠江河口鱼类精准识别的需求。
3.3 12S rDNA条形码在珠江河口鱼类物种鉴定中的适用性
虽然12S rDNA序列种间平均遗传距离是种内的286.6倍,也十分符合“10×”的阈值规则。但是遗传距离直方图显示,种间遗传距离与种内遗传距离发生了重叠,未形成明显的条形码间隙。此外ABGD将一些近缘物种划分到了同一个分类单元,例如,本研究东方鲀属的3个物种根据ABGD划分为一个分类单元,且黄鳍东方鲀、星点东方鲀与弓斑东方鲀之间的遗传距离介于0.59%~1.2%,在GenBank上相似度高达99%以上,只有2个碱基的差别。因为基因会发生交换和重组,所以即使同一个物种间,12S rDNA序列有时也会存在几个碱基的差异,将导致该类型物种无法区分开来[35]。在Zou等[8]使用12S rDNA序列对南沙湿地的环境DNA研究中,出现了双斑东方鲀 (T. bimaculatus) 和铅点东方鲀 (T. alboplumbeus),与本研究东方鲀属的3个物种也仅有1~3个碱基的差异,所以很有可能会出现低估鱼类多样性的情况。此外在带鱼与南海带鱼两个亚种的区分上,ABGD也将两者划分为一个物种,且两者遗传距离为1.8%,仅有3个碱基的差别,说明12S rDNA序列可能无法对亚种进行区分。在本研究172个鱼类物种中,11个物种存在以上情况,占6.4%,说明12S rDNA序列还是可以用于大部分珠江河口鱼类的种类鉴定。但是在今后的研究中,区分一些近缘种类需特别注意,应当使用COI序列加以验证,并参考当地鱼类名录,调查是否出现过该物种而后加以确认。
综上所述,根据COI序列和12S rDNA序列建立的珠江河口鱼类DNA条形码数据库已经达到数据库建立的两个条件。同时,证明了COI条形码能很好地适用于珠江河口鱼类鉴定,并且论证了线粒体12S rDNA条形码适用于大部分珠江河口鱼类的种类鉴定,但是对少数亲缘关系近的物种可能难以区分,这可能会导致鱼类多样性的低估,在今后的研究中应特别注意此类物种。
-
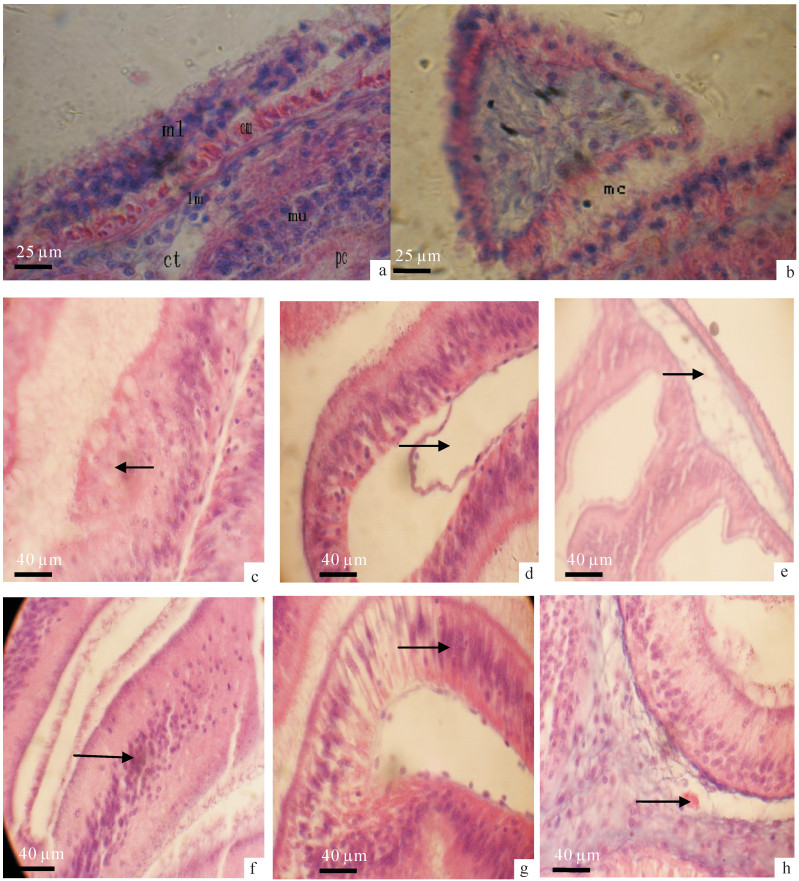
图 1 对照组与硫酸铜/氯化铜攻毒组刺参后肠组织切片图
a. 对照组刺参后肠(×1 000);b. 对照组血小窦(×1 000);c~e. CuCl2攻毒刺参后肠(×400);f~h. CuSO4攻毒刺参后肠(×400);ml. 黏膜层;cm. 环肌;lm. 纵肌;ct. 结缔组织;mu. 粘膜上皮层;pce. 假复层纤毛柱状上皮;mc. 间皮细胞
Figure 1. Intestinal tissue slices of sea cucumber of control group and CuSO4/CuCl2 toxic group
a. hindgut 1 000 times micro-amplification; b. blood sinus 1 000 times micro-amplification of control group; c~e. hindgut 400 times micro-amplification of CuCl2 toxic group; f~h. hindgut 400 times micro-amplification of CuSO4 toxic group; ml. mucous layer; cm. circular muscle; lm. longitudinal muscle; ct. connective tissue; mu. Mucosa; pc. pseudostratified ciliated columnar epithelium; mc. mesothelial cells
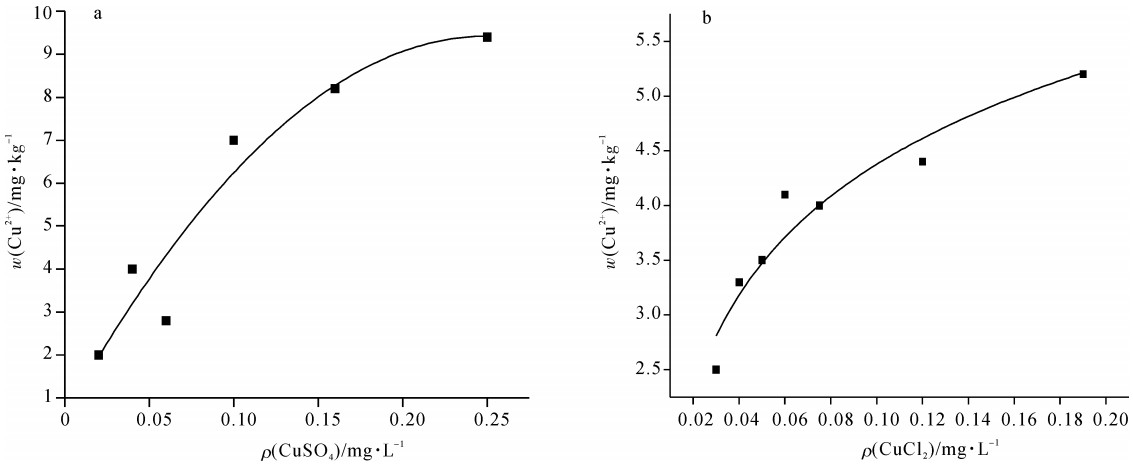
表 1 CuSO4/CuCl2来源的Cu2+对幼参急性毒性试验浓度设计与死亡结果(n=3)
Table 1 Analysis of concentrations of different copper ions on juvenile sea cucumber
mg · L-1 暴露时间/hexposure time ρ(CuSO4)(Cu2+) ρ(CuCl2)(Cu2+) 0.25 0.16 0.10 0.06 0.04 0.19 0.12 0.075 0.05 0.03 24 9 6 3 0 0 9 6 3 0 0 48 10 9 6 2 0 10 9 9 2 1 72 10 10 8 7 4 10 10 10 4 3 96 10 10 10 8 7 10 10 10 6 5 表 2 CuSO4/CuCl2来源的Cu2+对幼参急性毒性试验统计结果(n=3)
Table 2 Result of different copper ions on juvenile sea cucumber in acute toxicity test
时间/h time 硫酸铜/氯化铜CuSO4/CuCl2 浓度对数-概率回归方程regression equation 半致死质量浓度/mg·L-1 LC50 相对标准偏差RSDLC50 95%置信区间/mg·L-1 95%confidence interval P 24 CuSO4 P=5.29x+4.53 0.140 0.005 0 0.110~0.180 0.001 CuCl2 p=5.58x+5.52 0.100 0.005 0 0.097~0.130 48 CuSO4 p=5.72x+5.97 0.090 0.008 0 0.072~0.110 0.003 CuCl2 p=4.19x+5.01 0.064 0.008 0 0.053~0.076 72 CuSO4 p=3.62x+4.81 0.047 0.008 0 0.023~0.063 0.966 CuCl2 p=4.14x+5.74 0.041 0.009 0 0.028~0.053 96 CuSO4 p=4.18x+6.24 0.032 0.003 0 1.2×10-23~0.045 0.933 CuCl2 p=5.37x+7.75 0.036 0.004 0 0.029~0.042 表 3 CuSO4/CuCl2对幼参的暴露时间和半致死浓度回归参数一览表
Table 3 Expose time and LC50 of juvenile with different copper ions
铜来源source 回归方程regression equation R2 t 硫酸铜CuSO4 y=-0.08 ln(x)+0.1411 0.99 0.053 氯化铜CuCl2 y=0.110 3x-0.836 0.99 0.034 Table 4 Table of different standards of copper maximum limit in seawater in China
标准名称standard name 标准类型type 最高限量/mg·L-1maximum limit NY 5052-2001 强制性 第一类≤0.005 ≤0.010 第三类、第四类≤0.050 GB 3097-1997 强制性 第二类 ≤0.010 GB 11607-1989 强制性 ≤0.010 表 5 刺参幼参对异源铜离子96 h富集系数
Table 5 96 h bioconcentration factor of juvenile with different copper ions toxicity
铜来源source of copper ion 暴露质量浓度/mg·L-1 exposure concentration 96 h富集系数96 h bioconcentration factor 硫酸铜CuSO4 0.020~0.25 27.37~100 氯化铜CuCl2 0.030~0.19 37.60~132.50 表 6 关于铜限量的食品安全标准
Table 6 Food safety standards maximum limit of copper
标准名称standard name 标准类型type 最高限量/mg·L-1maximum limit GB 2733-2005《鲜冻动物性水产品卫生标准》 强制性 / GB 2762-2005《食品中污染物限量》 强制性 / GB 15199-1994《食品中铜限量卫生标准》* 强制性 ≤50 注:*.根据2011年第3号中国国家标准公告,已废止
Note:*.According to announcement of No.3 National Standard of P.R.China of 2011 which was abolished.表 7 有毒物质对水产类的毒性标准
Table 7 Toxicity criteria of toxicants for fish
等级scale 剧毒extremely toxic 高毒highly toxic 中毒toxic 低毒low toxic 半数耐受限/mg·L-1 TLm <0.10 0.10~1 1~10 >10 -
[1] 朱文嘉, 王联珠. 优劣干海参的鉴别[J]. 科学养鱼, 2011(5): 68-69. https://www.zhangqiaokeyan.com/academic-journal-cn_scientific-fish-farming_thesis/0201261500619.html [2] TAIYEB T B, ZAINUDDIN S L, SWAMINATHAN D, et al. Efficacy of gamadent to othpaste on the healing of gingival tissues: a preliminary report[J]. J Oral Sci, 2003, 45(3): 153-159. doi: 10.2334/josnusd.45.153
[3] 王淑娴, 叶海斌, 于晓清, 等. 海参的免疫机制研究[J]. 安徽农业科学, 2012, 40(25): 12553-12555. https://doc.taixueshu.com/journal/20123445ahnykx.html [4] SUN W H, LENG K L, LIN H. et al. Analysis and evaluation of chief nutrient composition in different parts of Stichopus japonicus[J]. Chin J Animal Nutr, 2010, 22(1): 212-220. https://www.semanticscholar.org/paper/Analysis-and-Evaluation-of-Chief-Nutrient-in-Parts-Weihong-Kai-liang/2a80ad000a3b18668775e7c3de2a4b3a4b7d94f0#:~:text=Nutritive%20and%20functional%20composition%20in%20different%20parts%20%28body,of%20high%20nutrition%20value%20and%20some%20officinal%20value.
[5] 谷阳光, 林钦, 王增焕, 等. 柘林湾及邻近海域沉积物重金属分布与潜在生态风险[J]. 南方水产科学, 2013, 9(2): 32-37. doi: 10.3969/j.issn.2095-0780.2013.02.006 [6] WANG H, DONG Y H, YANG Y Y, et al. Changes in heavy metal contents in animal feeds and manures in an intensive animal production region of China[J]. J Environ Sci, 2013(12): 2435-2442. https://pubmed.ncbi.nlm.nih.gov/24649675/
[7] 张伟, 阎海, 吴之丽. 铜抑制单细胞绿藻生长的毒性效应[J]. 中国环境科学, 2001, 21(1): 4-7. https://qikan.cqvip.com/Qikan/Article/Detail?id=4904212 [8] ROSA G C, LUCIA L V, ALEXANDRA P, et al. Sublethal zinc and copper exposure affect acetylcholinesterase activity and accumulation in different dissues of leporinus obtusidens[J]. Bull Environ Contam Toxicol, 2013, 90(1): 12-6. doi: 10.1007/s00128-012-0896-0
[9] 朱国霞, 季延滨, 孙学亮. Cu2+、Fe2+及铜铁合剂对血鹦鹉幼鱼的急性毒性试验[J]. 中国水产, 2013(8): 56-58. https://d.wanfangdata.com.cn/periodical/ChlQZXJpb2RpY2FsQ0hJTmV3UzIwMjQwNzA0EhN6aG9uZ2d1b3NjMjAxMzA4MDIyGghwMmJxcG92OA%3D%3D [10] 李华, 李磊. 铜离子对栉孔扇贝幼贝几种免疫因子的影响[J]. 生命科学仪器, 2009, 7(8): 31-34. https://lib.cqvip.com/Qikan/Article/Detail?id=32283483&from=Qikan_Article_Detail [11] KARAYAKAR F, CICIK B, CIFTCI N. Accumulation of copper in liver, gill and muscle tissues of Anguilla Anguilla (Linnaeus, 1758)[J]. J Anim Vet Adv, 2010, 9(17): 2271-2274. doi: 10.3923/javaa.2010.2271.2274
[12] GASPAR M C D M, FERNANDA B I, JAIME D M E, et al. Acute toxicity, accumulation and tissue distribution of copper in the blue crab Callinectes sapidus acclimated to different salinities: in vivo and in vitro studies[J]. Aquat Toxicol, 2010, 101(1): 88-99. https://www.semanticscholar.org/paper/Acute-toxicity%2C-accumulation-and-tissue-of-copper-Martins-Barcarolli/4dd0ed246c6812123f3fa2585f594a076fcf04ff
[13] BUNDRIGE J. A comparison of bioaccumulation and digestive enzyme solubilization of copper in two species of sea cucumbers with different feeding habits[D]. East Tennessee State, US: East Tennessee State University, 2003: 49. https://dc.etsu.edu/etd/832/
[14] 马莉芳, 蒋晨, 高春生. 水体铜对水生动物毒性的研究进展[J]. 江西农业学报, 2013, 25(8): 73-76. https://www.doc88.com/p-7983700313732.html [15] GUDRUN D B, WOUTER M, WIM D C, et al. Tissue-specific Cu bioaccumulation patterns and differences in sensitivity to waterborne Cu in three freshwater fish: rainbow trout (Oncorhynchus mykiss), common carp (Cyprinus carpio), and gibel carp (Carassius auratus gibelio)[J]. Aquat Toxicol, 2004, 70(3): 179-88. https://www.infona.pl/resource/bwmeta1.element.elsevier-0a8750ee-c7d0-3686-a814-0ef392695c6f/tab/summary
[16] 周永欣, 王士达, 夏宜琤. 水生生物与环境保护[M]. 北京: 科学出版社, 1983. https://book.sciencereading.cn/shop/book/Booksimple/show.do?id=BC72D6A2ECB3C4E32B499B3418CF88DB8000 [17] 张丽岩, 宋欣, 高玮玮, 等. Cd2+对青蛤(Cyclina sinensis)的毒性[J]. 海洋与湖沼, 2010, 41(3): 418-421. https://cstj.cqvip.com/Qikan/Article/Detail?id=34464526&from=Qikan_Article_Detail [18] 刘天红, 孙福新, 王颖, 等. 无机镉对栉孔扇贝(Chlamys farreri)急性毒性研究及其安全评价[J]. 食品研究与开发, 2010, 31(4): 161-165. https://med.wanfangdata.com.cn/Paper/Detail/PeriodicalPaper_spyjykf201004050 [19] 肖培华, 唐永新, 于乐河, 等. 刺参病害细菌感染试验[J]. 齐鲁渔业, 2005, 22(6): 26-27. https://qikan.cqvip.com/Qikan/Article/Detail?id=15778593 [20] 刘国光, 王莉霞, 徐海娟, 等. 水生生物毒性试验研究进展[J]. 环境与健康杂志, 2004(6): 67-69. https://xueshu.baidu.com/usercenter/paper/show?paperid=e40cbe5b145dffcdac09e3f668a70d75 [21] 孙福新, 李晓, 王颖, 等. 栉孔扇贝对无机砷的富集与排出特征研究[J]. 海洋科学, 2011, 35(4): 85-90. http://qdhys.ijournal.cn/hykx/ch/reader/view_abstract.aspx?file_no=20110415&st=alljournals [22] 孙元芹, 吴志宏, 孙福新, 等. 文蛤对重金属Cu的富集与排出特征[J]. 渔业科学进展, 2013, 34(1): 128-134. http://www.aquaticjournal.com/article/id/784b1873-4c2b-4cc8-81ab-e5c573255e92 [23] 李霞, 王斌, 刘静, 等. 虾夷马粪海胆体腔细胞的类型及功能[J]. 中国水产科学, 2003, 11(5): 30-34. http://www.fishscichina.com/zgsckx/article/abstract/4437?st=article_issue [24] 孙永欣. 黄芪多糖促进刺参免疫力和生长性能的研究[D]. 大连: 大连理工大学, 2008. https://med.wanfangdata.com.cn/Paper/Detail?id=DegreePaper_Y1419262&dbid=WF_XW [25] NRJAGU J O. Zincin environment partⅡ[M]. New York: Wiley, 1980: 415-438. doi: 10.1002/9780470960707.ch16
[26] 刘天红, 孙福新, 王颖, 等. 硫酸铜对栉孔扇贝急性毒性胁迫研究[J]. 水产科学, 2011, 30(6): 11-14. https://d.wanfangdata.com.cn/periodical/Ch9QZXJpb2RpY2FsQ0hJTmV3UzIwMjQxMTA1MTcxMzA0Eg1zY2t4MjAxMTA2MDAyGghkYXlrczVxdQ%3D%3D [27] 程波, 刘鹰, 杨红生. Cu2+在凡纳滨对虾组织中的积累及其对蜕皮率、死亡率的影响[J]. 农业环境科学学报, 2008(5): 403-407. https://www.aes.org.cn/nyhjkxxb/ch/reader/view_abstract.aspx?file_no=6487&flag=1 [28] 孙云明, 刘会峦. 海洋中的主要化学污染物及其危害[J]. 化学教育, 2001(7/8): 2-5. https://www.hxjy.chemsoc.org.cn/CN/abstract/abstract8947.shtml [29] FUNES V, ALHAMA J, NAVAS J I, et al. Ecotoxicological effects of metal pollution in two mollusc species from the Spanish south Atlantic littoral[J]. Environ Pollut, 2005, 139(2): 214-223. https://pubmed.ncbi.nlm.nih.gov/16054738/
[30] 张志杰, 张维平. 环境污染生物监测与评价[M]. 北京: 中国环境科学出版社, 1991: 78-102. https://xueshu.baidu.com/usercenter/paper/show?paperid=308b5dde6cba4788c928c739dc9f2526 [31] 刘存歧, 安通伟, 张亚娟, 等. Cu2+对日本沼虾的毒性研究[J]. 安徽农业科学, 2008, 36(28): 227-228. https://www.doc88.com/p-4334547118044.html [32] 李国基, 刘明星, 张首临, 等. Zn等金属离子对栉孔稚贝成活的毒性影响[J]. 海洋环境科学, 1994, 13(2): 13-16. https://xueshu.baidu.com/usercenter/paper/show?paperid=320aa99ba6e08c1d969beff090ca5b87 [33] 刘亚杰, 王笑月. 锌、铜、铅、镉金属离子对海湾扇贝稚贝的急性毒性试验[J]. 水产科学, 1995, 14(1): 10-12. https://xueshu.baidu.com/usercenter/paper/show?paperid=7f01559403956766080630325e7fb8c5&sc_from=pingtai4&cmd=paper_forward&wise=0 -
期刊类型引用(11)
1. 王大伟,邢盈,蒋成宇,胡淼,赵金良. 放养密度对鳜幼鱼HPI轴激素、应激酶活力及呼吸频率的影响. 淡水渔业. 2025(02): 26-32 .  百度学术
百度学术
2. 何静怡,魏涯,岑剑伟,郝淑贤,陈胜军,黄卉,赵永强,王悦齐,杨少玲,林织. 基于梯度降温的草鱼暂养及有水保活运输技术. 食品科学. 2024(04): 271-278 .  百度学术
百度学术
3. 何静怡,郑伟,黄卉,岑剑伟,赵永强,王田,魏涯,郝淑贤,杨少玲,陈琛. 不同温度、盐度条件对草鱼暂养及应激保活的影响. 大连海洋大学学报. 2024(04): 597-605 .  百度学术
百度学术
4. 梁雪莹,郑晓婷,陈秋羽,谢静怡,董宏标,李勇,杨金龙,陈成勋,张家松. 模拟运输胁迫对牛蛙幼蛙生理机能的影响. 广东海洋大学学报. 2024(06): 118-126 .  百度学术
百度学术
5. 刘浩,李洁,李亚军,康鹏天,张国维,邵东宏,王建福. 水体中泥沙含量对虹鳟生存、生理和体表微生物的影响. 中国水产科学. 2024(11): 1365-1374 .  百度学术
百度学术
6. 唐忠林,张佳佳,周国勤,陈树桥,徐钢春,徐跑,强俊,王佩佩. 丁香酚对“优鲈3号”幼鱼运输水质及其血液、肌肉生理指标的影响. 水产科技情报. 2023(01): 44-52 .  百度学术
百度学术
7. 王文雯,杨静茹,付正祎,于刚,马振华. 运输时间对高体鰤幼鱼应激、代谢、抗氧化和免疫的影响. 中国渔业质量与标准. 2023(02): 25-36 .  百度学术
百度学术
8. 李哲,周珊珊,王好学,王嘉浩,陈璐,徐开达. 运输振荡对条石鲷幼鱼生理应激和水体总氨氮含量的影响. 水产科技情报. 2023(05): 327-332 .  百度学术
百度学术
9. 范宏博,胡丁月,徐莉,孙浩,刘峰,刘春娥,张小栓. 运输密度和时间对单环刺螠保活运输品质的影响. 农业工程. 2023(10): 72-77 .  百度学术
百度学术
10. 虞为,陈雪晴,杨育凯,张燕娃,黄小林,黄忠,李涛,马振华,吴洽儿,于刚,周传朋,林黑着. 饲料中添加雨生红球藻对尖吻鲈生长性能、抗氧化能力及免疫状态的影响. 南方水产科学. 2022(05): 46-54 .  本站查看
本站查看
11. 陈旭,赵旺,陈明强,谭春明,于刚. 盐度胁迫对红娇凤凰螺耗氧率、排氨率以及免疫相关酶活性的影响. 南方水产科学. 2022(05): 160-165 .  本站查看
本站查看
其他类型引用(4)




 下载:
下载:




 粤公网安备 44010502001741号
粤公网安备 44010502001741号
