Influence of boron stress on growth and physiological characteristics of Gracilaria lemaneiformis
-
摘要:
该研究以龙须菜(Gracilaria lemaneiformis)为试验材料,探讨不同硼(B)浓度对龙须菜的生长及生理指标的影响。结果表明,与对照组(0.375 mmol·L-1)相比,缺B组(0 mmol·L-1)和高B组(3.75 mmol·L-1)龙须菜呈红褐色,日特定生长速率无显著差异;缺B组龙须菜第6天的叶绿素a与第9天的别藻蓝蛋白显著下降;高B组的藻红蛋白、藻蓝蛋白、叶绿素a和可溶性糖显著下降,多酚氧化酶(PPO)和过氧化氢酶(CAT)活力显著上升。B过量组(37.5 mmol·L-1)的龙须菜在第6天完全变绿,日特定生长速率出现负增长,光合色素(藻胆蛋白、叶绿素a)、可溶性糖、PPO和CAT酶活力均显著下降。因此,龙须菜养殖中要确保海水中的B浓度适宜,缺乏或过高都会造成龙须菜的减产。
Abstract:We explored the influence of different concentrations of boron on the growth and physiological characteristics of Gracilaria lemaneiformis. Compared to the control, G.lemaneiformis were reddish brown and special growth rate (SGR) showed no significant difference between deficient boron group (0 mg·L-1) and high boron group (40 mg·L-1). The contents of Chl-a on the 6th day and allophycocyanin (APC) on the 9th day significantly decreased in deficient boron group. The contents of phycoerythrin (PE), phycocyanin (PC) and Chl-a remarkably decreased in high boron group; while the activities of polyphenol oxidase (PPO) and catalase (CAT) significantly increased. In excess boron group (37.5 mmol·L-1), G.lemaneiformis all turned green on the 6th day with negative growth of SGR; the contents of Chl-a, phycobiliprotein and soluble sugar as well as the activities of PPO and CAT dramatically decreased. Therefore, in order to ensure G.lemaneiformis′ production, concentration of boron in seawater must be appropriate.
-
硼(B)是植物生长所必需的微量元素,与铁(Fe)、锰(Mn)、锌(Zn)等不同,B并不是酶的组成部分[1],而与甘露醇、甘露聚糖、多聚糖醛酸等其他多糖形成硼糖复合体,成为细胞壁的重要组成成分,在碳水化合物运输与稳定细胞膜等方面发挥重要作用[2-3]。不同的生物对B的需求量不同,适合某种生物生长的B浓度对另外一种生物可能会产生毒性[4]。大量研究表明,缺B会给植物带来严重危害,造成作物减产,而B浓度较高也会对植物造成B生理毒害[5]。2012年LANDI等[6]研究了紫叶和绿叶的罗勒属(Ocimum basilicum)植物在高B胁迫下抗氧化物和光合作用的响应,发现高B对2种植物的生长和光合作用均产生负面影响。B在海洋藻类中也是一个重要的元素,相对于陆地的缺B环境,海洋环境中的B浓度较高,因此不会出现缺B影响海洋初级生产力的问题,但是高B浓度会带来潜在的B毒性问题[7]。目前研究B元素对陆地植物的影响比较广泛,而其对海洋藻类的影响报道较少。
龙须菜(Gracilaria lemaneiformis)隶属红藻门,杉藻目,是江蓠属(Gracilaria)中一种重要的产琼胶红藻,以生长快、经济价值高、琼胶含量高和能适应较高温度等特点在中国东南沿海大规模养殖[8]。2011年汕头市南澳岛部分海域养殖的龙须菜出现腐烂现象,将该批龙须菜样品送入汕头市质检局检测后发现藻体B元素的质量分数过高(24.168 mg·kg-1)[9],由此推测这可能是B中毒引起的腐烂。因此,明确B元素对龙须菜生长的影响对于正确辨认龙须菜养殖中由B元素导致的生理性病害具有重要的指导意义。文章对龙须菜进行B胁迫处理,探讨B胁迫对龙须菜的生长状况、光合色素质量分数、可溶性糖质量分数和抗氧化酶活力的影响,并分析了龙须菜养殖过程中B引起的毒害机理,以期为龙须菜的养殖生产提供理论支持。
1. 材料与方法
1.1 材料和处理
试验材料为龙须菜981品系,由汕头大学南澳实验站提供,在3 h内运回实验室。洗净,去除杂藻后将其放入光照培养箱中用天然海水培养一段时间以适应环境,培养箱的条件设置为温度(20±1)℃和光照强度1 440 lx[光周期L(光) : D(暗)为12 h : 12 h]。
试验之前取汕头市南澳岛不同地点的海水,通过电感耦合等离子质谱仪(ICP-MS)检测海水中B浓度范围为0.093 4~0.375 0 mmol·L-1。试验分为预培养阶段和试验阶段。预培养需称取8 g左右的健康藻体于规格为28 cm×27 cm×18 cm的塑料培养箱中培养1周,每个培养箱中盛有4 L人工海水(B的浓度为0.375 mmol·L-1),B以硼酸的形式加入培养液。预培养结束后,设置4个水平的B浓度处理,分别为缺B组(0 mmol·L-1)、对照组(0.375 mmol·L-1)、高B组(3.75 mmol·L-1)和B过量组(37.5 mmol·L-1),4个处理组的海水pH分别为8.79、8.76、7.98和7.06,每个处理组设置3个重复,培养条件同上。试验周期为12 d,每隔2 d测定藻体的日特定生长速率、藻胆蛋白质量分数、叶绿素a(Chl-a)质量分数、可溶性糖质量分数和抗氧化酶活力等生理生化指标。
1.2 测定方法
1.2.1 特定生长率
龙须菜特定生长率(SGR)按照YU和YANG [10]的计算公式:
SGR(%·d-1)=[(Wt/W0)1/t-1]×100。其中,W0为初始龙须菜鲜质量(g);Wt为t时刻龙须菜鲜质量(g);t为2次时间间隔(d)。
1.2.2 藻胆蛋白
提取和质量浓度测定参考徐永健等和张学成等[11-13]方法,计算公式:
藻蓝蛋白(PC, μg·g-1)=(151.1A618-99.1A651)·Ve/W;别藻蓝蛋白(APC, μg·g-1)=(181.3A651-22.3A618)·Ve/W;藻红蛋白(PE, μg·g-1)=(155.8A498-40.0A618-10.5A651)·Ve/W;其中Ve为提取液PBS的体积(mL);W为所取藻体的鲜质量(g)。
1.2.3 叶绿素a
Chl-a的计算公式为:Chl-a(mg·g-1)= [12. 65 (A664-A750)-2. 99 (A647-A750)-0.04 (A625-A750)]·Ve / (I·W×1 000)。其中A750、A664、A647和A625分别为波长750 nm、664 nm、647 nm和625 nm处的吸光值;Ve为萃取液二甲基甲酰胺(DMF)的体积(5 mL);I为比色皿的光径(cm);W为所取藻体的鲜质量(g)。
1.2.4 可溶性糖
取0.2 g新鲜龙须菜于预冷的研钵中,在液氮下充分研磨3次至细粉状后加入9 mL蒸馏水,转移至10 mL离心管80 ℃水浴2 h,提取液在6 000 r·min-1下离心10 min,即为粗糖溶液。粗糖的质量分数测定采用蒽酮法[14]。
1.2.5 过氧化氢酶(CAT) 粗酶液的提取
取0.2 g新鲜龙须菜于预冷的研钵中,在液氮下充分研磨3次至细粉状。加入1.5 mL PBS(pH 7.8)研磨成匀浆,转入离心管中在4 ℃、12 000 r·min-1下离心20 min,上清液即为粗酶液。酶活测定方法为以每分钟A240吸光值减少0.01定义为1个酶活力单位[15]。
1.2.6 超氧化物歧化酶(SOD)
SOD粗酶液的提取同1.2.5。酶活测定用南京建成SOD测定试剂盒。
1.2.7 多酚氧化酶(PPO)
PPO粗酶液的提取。取0.3 g新鲜龙须菜于预冷的研钵中,在液氮下充分研磨3次至细粉状。加入1.2 mL PBS(pH 6.5,含4%PVP)研磨成匀浆,转入离心管中在4 ℃、12 000 r·min-1下离心20 min,上清液即为粗酶液。酶活测定参照梁建荣[16]的方法,以每分钟A408吸光值增加0.01定义为1个酶活力单位。
1.3 数据整理与分析
试验数据采用SPSS 19.0软件进行统计分析,设置显著水平为α=0.05。
2. 结果与分析
2.1 不同pH处理对龙须菜光合色素的影响
相关文献显示pH在7.9~9.0之间对龙须菜的生长无显著影响[17-18],而该试验pH在7.06~8.79范围内,因此预试验设置了pH 7.0[2.5 mol·L-1盐酸(HCl)调节海水的pH]与自然海水(pH 8.0)2个组,每隔2 d更换海水,培养12 d之后检测指标。不同pH处理的龙须菜光合色素质量分数无显著差异(P>0.05), 因此该试验中硼酸的添加导致海水pH的改变对龙须菜的生长无显著影响(表 1)。
表 1 不同pH处理对龙须菜光合色素的影响Table 1. Effect of different pH on photosynthetic pigments of G.lemaneiformis光合色素
photosynthetic pigment自然海水(pH 8.0)
natural seawaterpH 7.0 t-检验
t-testw(藻红蛋白)/μg·g-1 phycoerythrin 397.810 500±41.973 390 426.818 800±22.078 650 P>0.05 w(藻蓝蛋白)/μg·g-1 phycocyanin 85.224 800±6.361 275 94.359 880±6.845 448 P>0.05 w(别藻蓝蛋白)/μg·g-1 allophycocyanin 72.676 100±9.629 774 79.661 630±5.232 312 P>0.05 w(叶绿素a)/mg·g-1 chlorophyll a 0.181 957±0.049 480 0.128 701±0.023 890 P>0.05 2.2 不同浓度B处理对龙须菜的形态和特定生长率的影响
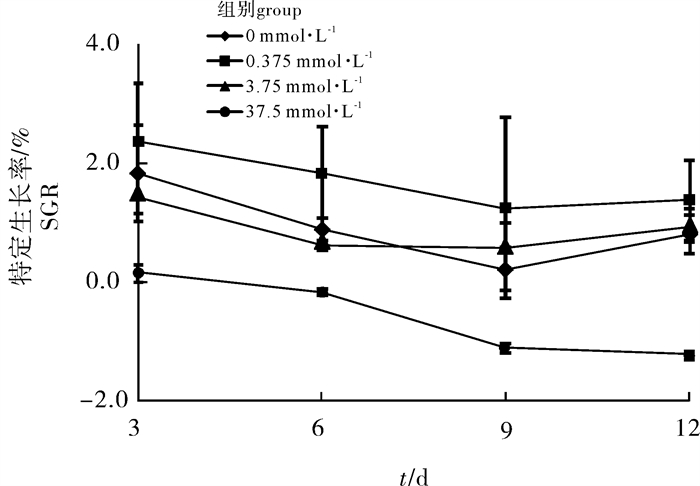
整个试验过程中,缺B组(0 mmol·L-1)、对照组(0.375 mmol·L-1)和高B组(3.75 mmol·L-1)的龙须菜生长良好,藻体红润。B过量组(37.5 mmol·L-1)的龙须菜第3天主支就开始出现偏褐色的不良症状,试验第6天龙须菜主枝和分支稍显微绿,随着培养时间延长,绿色越来越深,呈透明状,但是藻体并未断裂(图 1)。
![]() 图 1 不同硼浓度对龙须菜形态的影响a.缺B组(0 mmol·L-1); b.对照组(0.375 mmol·L-1); c.高B组(3.75 mmol·L-1); d.B过量组(37.5 mmol·L-1)Figure 1. Effect of different concentrations of boron on morphology of G.lemaneiformisa.deficient boron group (0 mmol·L-1); b.control (0.375 mmol·L-1); c.high boron group (3.75 mmol·L-1); d.excess boron group (37.5 mmol·L-1)
图 1 不同硼浓度对龙须菜形态的影响a.缺B组(0 mmol·L-1); b.对照组(0.375 mmol·L-1); c.高B组(3.75 mmol·L-1); d.B过量组(37.5 mmol·L-1)Figure 1. Effect of different concentrations of boron on morphology of G.lemaneiformisa.deficient boron group (0 mmol·L-1); b.control (0.375 mmol·L-1); c.high boron group (3.75 mmol·L-1); d.excess boron group (37.5 mmol·L-1)不同B浓度培养的龙须菜表现出不同的生长速率(图 2)。在整个B胁迫试验过程中,缺B组和高B组培养的龙须菜生长速率均维持正增长,与对照组相比无显著性差异。B过量组培养的龙须菜在第6天出现负增长,生长速率显著低于对照组(P < 0.05),之后持续下降。
2.3 不同浓度B处理对龙须菜光合色素质量分数的影响
2.3.1 不同B浓度处理对龙须菜藻红蛋白质量分数的影响
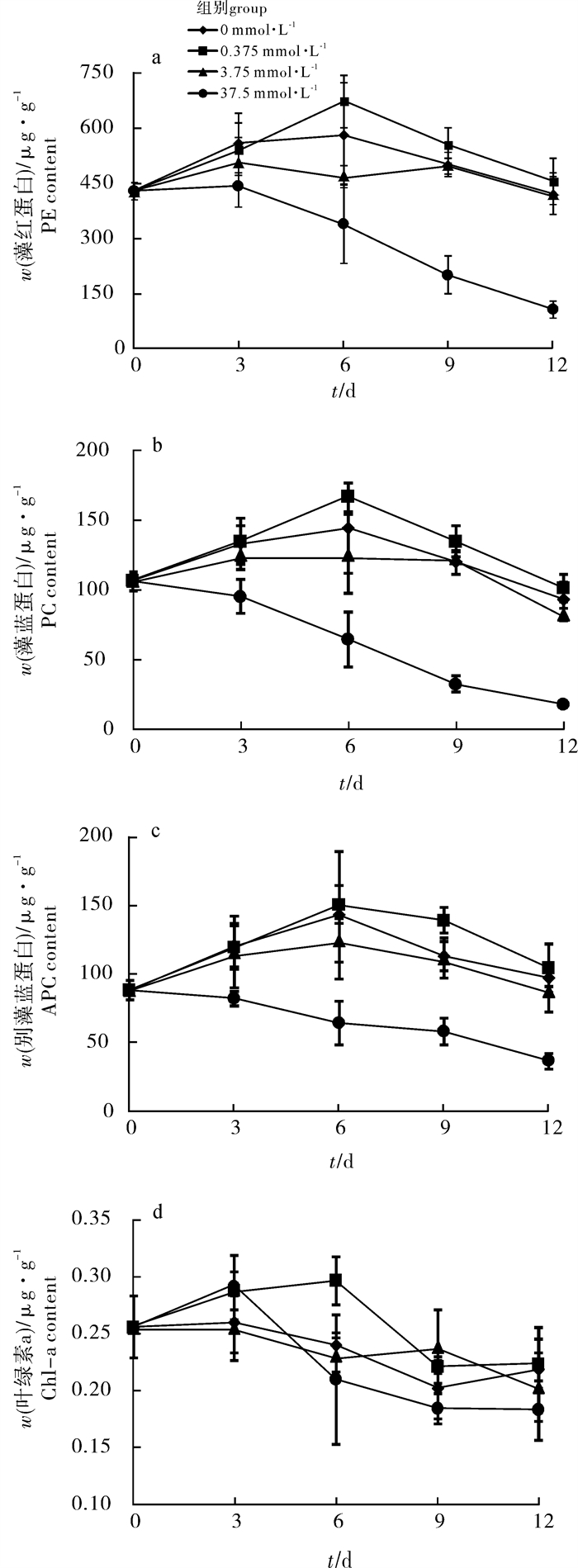
缺B组培养的龙须菜藻红蛋白质量分数在整个试验周期中与对照组相比无显著性差异。试验第6天,高B组和B过量组的藻红蛋白质量分数与对照组相比显著下降(P < 0.05)。之后随着天数的增加,高B试验组的藻红蛋白质量分数基本保持稳定,而B过量试验组的藻红蛋白质量分数持续下降,到试验第12天B过量试验组的藻红蛋白质量分数与对照组相比下降了约76.7%(图 3-a)。
2.3.2 不同浓度B处理对龙须菜藻蓝蛋白质量分数的影响
在整个B胁迫试验中缺B组培养的龙须菜藻蓝蛋白质量分数与对照组相比无显著性差异。高B组的龙须菜藻蓝蛋白质量分数在试验前9 d与对照相比无显著差异,试验第12天显著下降,与对照组相比下降了18.8%。B过量组处理的龙须菜藻蓝蛋白质量分数在第3天就开始下降,之后一直保持下降,试验第12天藻蓝蛋白质量分数与对照组相比下降了约82.3%(图 3-b)。
2.3.3 不同浓度B处理对龙须菜别藻蓝蛋白质量分数的影响
缺B组培养的龙须菜别藻蓝蛋白质量分数在第9天显著低于对照组。在整个试验过程中,高B组培养的龙须菜别藻蓝蛋白质量分数与对照组相比无显著性差异(P>0.05),B过量处理组别藻蓝蛋白质量分数明显下降。测定结果发现,试验第12天B过量组的龙须菜别藻蓝蛋白质量分数与对照组相比下降了63.1%(图 3-c)。
2.3.4 不同浓度B处理对龙须菜叶绿素a质量分数的影响
试验前3 d不同浓度的B处理对龙须菜叶绿素a质量分数均无显著影响。试验第6天,与对照组相比缺B、高B和B过量组的龙须菜叶绿素a质量分数都有明显的下降,与当天的对照组相比分别下降了约19.3%、40.0%和29.2%。试验第9天对照组的叶绿素a质量分数出现下降,可能是因为人工海水培养的时间过长对藻体有一定的伤害。第9天,B过量组的叶绿素a仍显著低于对照组(P < 0.05)。试验第12天,各组叶绿素a质量分数与第9天的相比无明显变化,且与对照组相比均无显著性差异(P>0.05)(图 3-d)。
2.4 不同浓度B处理对龙须菜可溶性糖质量分数的影响
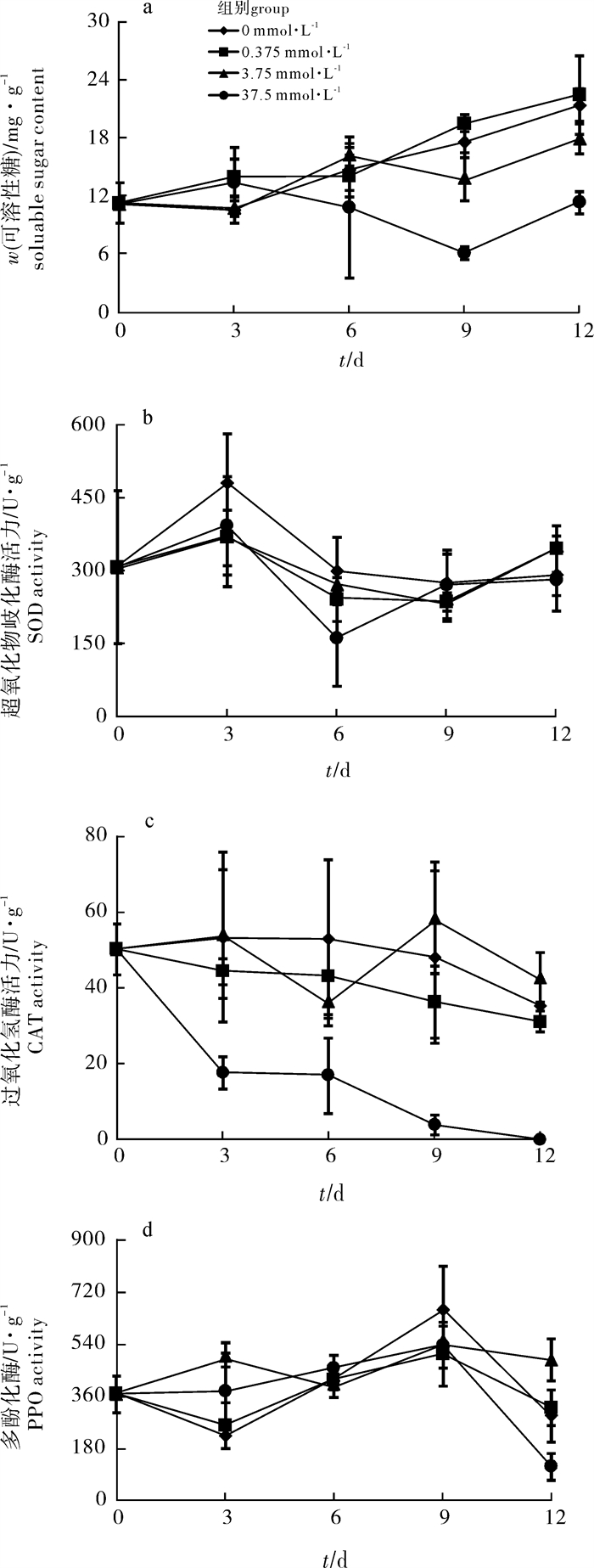
在整个试验过程中,缺B和高B条件下培养的龙须菜的可溶性糖质量分数有所积累,与对照组相比无显著性差异。而B过量组的龙须菜可溶性糖质量分数没有积累反而下降,到试验第9天与对照组相比下降了约62.3%。第12天B过量组的可溶性糖质量分数略有升高,但仍显著低于对照组(P < 0.05)(图 4-a)。
2.5 不同浓度B处理对龙须菜SOD活性的影响
SOD在第0、第3、第6、第9和第12天酶活在各组都有较大浮动,但是各试验组的酶活与对照组均无显著性差异(P>0.05)(图 4-b)。
2.6 不同浓度B处理对龙须菜CAT活力的影响
整个试验过程中缺B组CAT活力与对照组(4 mg·L-1)相比均无显著性差异(P < 0.05)。高B组的CAT活力在试验过程中上下波动,试验第12天显著高于对照组。B过量组的龙须菜CAT活力则在试验过程中呈下降趋势,在培养第3天就开始下降,与当天对照组相比下降了约60.3%,培养至第12天时下降到几乎为零(图 4-c)。
2.7 不同浓度B处理对PPO活力的影响
缺B组龙须菜的PPO活力在不同的天数与对照组的变化趋势一致,与对照组相比无显著差异。高B组的PPO活力在试验过程中上下波动,试验第12天与对照组相比显著上升了52.5%(P < 0.05)。而B过量组的PPO活力在第12天显著下降了64.2%(P < 0.05)(图 4-d)。
3. 讨论
3.1 B对龙须菜光合色素及可溶性糖质量分数的影响
B是植物正常生长的必需微量元素,但不同植物对B的需求量、缺B敏感程度以及B毒害的承受能力差异很大[19]。该试验中龙须菜经缺B处理,藻体的叶绿素a和别藻蓝蛋白质量分数质量分数下降,日特定生长速率与其他各项生理指标与对照组相比差别不显著,表明在短时期内龙须菜对缺B不敏感。龙须菜经高B处理12 d,藻体的日特定生长速率仍呈正增长,试验过程中叶绿素a、藻红蛋白与藻蓝蛋白以及可溶性糖质量分数出现下降,抗氧化酶活力上升。说明龙须菜对3.75 mmol·L-1的高B浓度有较强的耐受能力。该试验中B过量处理后龙须菜出现了明显的B中毒症状,主要表现为藻体变褐色再变绿色最后出现白化,症状首先出现在主枝。红藻的光合色素是叶绿素a和藻胆蛋白,藻胆蛋白能高效地捕获光能并传递给光合系统Ⅱ,光能传递方向为藻红蛋白→藻蓝蛋白→别藻蓝蛋白→叶绿素a[20]。该试验中过高浓度的B造成龙须菜的藻胆蛋白质量分数下降,朱喜锋等[21]研究铜(Cu)胁迫对龙须菜的影响时发现过量铜离子(Cu2+)对龙须菜藻胆蛋白的质量分数有类似影响,Cu2+与藻胆蛋白有较强的结合力,使藻胆蛋白遭到破坏,从而导致吸收光能的减少,最终影响藻体的光合作用。
缺B和高B条件还会使植物的可溶性糖质量分数受到影响。HAN等[22]在对葡萄柚的研究中发现,缺B和高B能影响糖的转运,导致葡萄糖和果糖的质量分数上升。张卫华等[23]研究结果表明过量的糖较长时间停留在叶片叶绿体中,可能会对光合系统造成阻碍和破坏,因此过量的B处理会导致光合产物减少,使总糖质量分数维持在一个很低的水平。该试验中高B组的可溶性糖质量分数在第9天显著低于对照组,第12天与对照组相比无显著差异;B过量组处理的龙须菜第9天可溶性糖质量分数与对照组相比显著下降,第12天仍显著低于对照组。可能是因为B过量处理使龙须菜的藻胆蛋白遭到了严重破坏,影响了藻体的光合作用,导致可溶性糖质量分数显著下降。研究发现其他微量元素如硒(Se)也具有促进植物生长的作用,适量Se可提高叶片的叶绿素质量分数,增强植物的光合作用[24]。
3.2 B对龙须菜体内保护酶的影响
在正常的生理生化过程中产生的活性氧自由基如O2、O2-和H2O2等,如果未解毒,O2-和H2O2发生反应产生OH-,OH-的活性比其他几种都强,对植物体产生严重的毒害[25]。刘鹏等[26]研究结果发现适量的B和钼都有利于大豆抗脂质过氧化胁迫,B通过糖蛋白和糖脂的相互作用使生物膜维持最有效构型,微量元素钼(Mo)通过对氮(N)和磷(P)代谢的作用而间接影响生物膜的稳定性。SOD是催化O2-的歧化作用将其变成H2O2和O2,有毒性的H2O2可通过CAT分解[27-28]。该试验中各组的SOD活性在不同天数的差异性不大。而CAT活力在不同组明显不同,缺B组和高B组的CAT活力分别在第3和第9天出现上升,比正常组的酶活略高。可能是因为在缺B和高B下龙须菜大量产生的超氧阴离子增加诱导酶活上升的结果。B过量处理的龙须菜CAT活力在第3天就明显下降,到第12天几乎降到零。说明B过量处理的龙须菜中CAT活力完全受到抑制,藻体的活性氧无法清除,从而导致龙须菜死亡。
过低或过高的B浓度都会影响植物中酚类物质的积累,导致抗氧化酶活性降低[29]。PPO虽然不属于抗氧化系统,但是在植物的氧化代谢中起着重要作用。PANDEY [30]对芸苔属植物芥菜在B胁迫下的PPO活力做了研究,发现PPO可以氧化酚类物质,保护机体免受氧化损伤。该试验中高B处理的龙须菜能诱导PPO的活性上升,B过量培养的龙须菜PPO活性显著下降(图 4-d)。可见龙须菜对高B浓度有一定耐受能力,只有B浓度过高时,机体无法清除大量有毒性的酚类物质,才会导致藻体死亡。
4. 小结
该试验结果表明,缺B和高B胁迫处理的龙须菜在12 d内仍可正常生长,说明龙须菜在短时期内可耐受的海水B浓度范围较大。B浓度达到37.5 mmol·L-1时会导致藻体的生长停滞,光合色素减少、可溶性糖质量分数降低,抗氧化酶活性显著下降。缺B和B中毒都会对龙须菜的光合色素造成负面影响,且B中毒对龙须菜的影响程度更大。因此,龙须菜养殖中要确保养殖环境的海水中的B浓度适宜,缺乏或过高都会造成龙须菜的减产。
-
图 1 不同硼浓度对龙须菜形态的影响
a.缺B组(0 mmol·L-1); b.对照组(0.375 mmol·L-1); c.高B组(3.75 mmol·L-1); d.B过量组(37.5 mmol·L-1)
Figure 1. Effect of different concentrations of boron on morphology of G.lemaneiformis
a.deficient boron group (0 mmol·L-1); b.control (0.375 mmol·L-1); c.high boron group (3.75 mmol·L-1); d.excess boron group (37.5 mmol·L-1)
表 1 不同pH处理对龙须菜光合色素的影响
Table 1 Effect of different pH on photosynthetic pigments of G.lemaneiformis
光合色素
photosynthetic pigment自然海水(pH 8.0)
natural seawaterpH 7.0 t-检验
t-testw(藻红蛋白)/μg·g-1 phycoerythrin 397.810 500±41.973 390 426.818 800±22.078 650 P>0.05 w(藻蓝蛋白)/μg·g-1 phycocyanin 85.224 800±6.361 275 94.359 880±6.845 448 P>0.05 w(别藻蓝蛋白)/μg·g-1 allophycocyanin 72.676 100±9.629 774 79.661 630±5.232 312 P>0.05 w(叶绿素a)/mg·g-1 chlorophyll a 0.181 957±0.049 480 0.128 701±0.023 890 P>0.05 -
[1] 施益华, 刘鹏. 硼在植物体内生理功能研究进展[J]. 亚热带植物科学, 2002, 31(2): 64-69. doi: 10.3969/j.issn.1009-7791.2002.02.015 [2] MATOH T. Boron in plant cell walls [J]. Plant Soil, 1997, 193(1/2): 59-70. doi: 10.1023/A:1004207824251
[3] KASAJIMA I, IDE Y, HIRAI M Y, et al. WRKY6 is involved in the response to boron deficiency in Arabidopsis thaliana[J]. Physiol Plantarum, 2010, 139(1): 80-92. doi: 10.1111/j.1399-3054.2010.01349.x
[4] KELES Y, NCEL I, YENICE N. Relationship between boron content and antioxidant compounds in Citrus leaves taken from fields with different water source [J]. Plant Soil, 2004, 265(1/2): 345-353. doi: 10.1007/s11104-005-0646-8
[5] 段九菊, 曹冬梅, 康黎芳, 等. 高硼胁迫对观赏凤梨植株生长和元素含量的影响[J]. 中国农学通报, 2011, 27(2): 137-143. https://d.wanfangdata.com.cn/periodical/Ch9QZXJpb2RpY2FsQ0hJTmV3UzIwMjQxMTA1MTcxMzA0Eg96Z254dGIyMDExMDIwMjkaCDJteWE0YzZ4 [6] LANDI M, PARDOSSI A, REMORINI D, et al. Antioxidant and photosynthetic response of a purple-leaved and a green-leaved cultivar of sweet basil (Ocimum basilicum) to boron excess [J]. Environ Exp Bot, 2013, 85: 64-75. doi: 10.1016/j.envexpbot.2012.08.008
[7] CARRANO C J, SCHELLENBERG S, AMIN S A, et al. Boron and marine life: a new look at an enigmatic bioelement [J]. Mar Biotechnol, 2009, 11(4): 431-440. doi: 10.1007/s10126-009-9191-4
[8] 郭翠, 陈伟洲, 曹会彬, 等. 不同龙须菜品系在高温胁迫下的生理响应比较[J]. 南方水产科学, 2011, 7(3): 14-19. doi: 10.3969/j.issn.2095-0780.2011.03.003 [9] 韩飞, 姚庆伟, 赵质创, 等. 广东省南澳岛水产品中硼元素本底值测定研究[J]. 化学分析计量, 2013, 22 (4): 24-26. doi: 10.3969/j.issn.1008-6145.2013.04.007 [10] YU J, YANG Y F. Physiological and biochemical response of seaweed Gracilaria lemaneiformis to concentration changes of N and P [J]. J Exp Mar Biol Ecol, 2008, 367(2): 142-148. doi: 10.1016/j.jembe.2008.09.009
[11] 徐永健, 钱鲁闽, 王永胜. 氮素营养对龙须菜生长及色素组成的影响[J]. 台湾海峡, 2006, 25(2): 222-228. doi: 10.3969/j.issn.1000-8160.2006.02.011 [12] 张学成, 王永旭, 仵小南, 等. 不同产地龙须菜光合色素的比较研究[J]. 海洋湖沼通报, 1993(1): 52-59. https://d.wanfangdata.com.cn/periodical/Ch9QZXJpb2RpY2FsQ0hJTmV3UzIwMjQxMTA1MTcxMzA0Eg5RSzAwMDAwMTUzMjAxORoINHI0dDlxbXU%3D [13] SAMPATH-WILEY P, NEEFUS C D. An improved method for estimating R-phycoerythrin and R-phycocyanin contents from crude aqueous extracts of Porphyra (Bangiales, Rhodophyta) [J]. J Appl Phycol, 2007, 19(2): 123-129. doi: 10.1007/s10811-006-9118-7
[14] 张志良, 瞿伟菁. 植物生理学实验指导[M]. 北京: 高等教育出版社, 2003: 127-128. https://xueshu.baidu.com/usercenter/paper/show?paperid=dcd70cfa892389e9cb68d3d0083118d1&site=xueshu_se [15] SCHVTZENDVBEL A, POLLE A. Plant responses to abiotic stresses: heavy metal-induced oxidative stress and protection by mycorrhization [J]. J Exp Bot, 2002, 53(372): 1351-1365. doi: 10.1093/jexbot/53.372.1351
[16] 梁建荣. 甘薯叶多酚氧化酶的分离纯化及部分性质与功能基团研究[D]. 重庆: 西南大学, 2011. 10.7666/d.y1881484 [17] 胡凡光, 郭萍萍, 王娟, 等. 水温, 盐度, pH和光照度对龙须菜生长的影响[J]. 渔业现代化, 2013, 40(4): 23-27. doi: 10.3969/j.issn.1007-9580.2013.04.005 [18] 钱鲁闽, 徐永健, 焦念志, 等. 环境因子对龙须菜和菊花心江蓠N、P吸收速率的影响[J]. 中国水产科学, 2006, 13(2): 257-262. doi: 10.3321/j.issn:1005-8737.2006.02.015 [19] SIMÓN I, DÍAZ-LÓPEZ L, GIMENO V, et al. Effects of boron excess in nutrient solution on growth, mineral nutrition, and physiological parameters of Jatropha curcas seedlings [J]. J Plant Nutr Soil Sci, 2013, 176(2): 165-174. doi: 10.1002/jpln.201100394
[20] 张学成, 秦松, 马家海, 等. 海藻遗传学[M]. 北京: 中国农业出版社, 2004: 286-289. https://xueshu.baidu.com/usercenter/paper/show?paperid=71118ef7e27253cb43fa243228499c75&site=xueshu_se [21] 朱喜锋, 邹定辉, 简建波, 等. 龙须菜对重金属铜胁迫的生理响应[J]. 应用生态学报, 2009, 20(6): 1438-1444. http://qikan.cqvip.com/Qikan/Article/Detail?id=30687343&from=Qikan_Search_Index [22] HAN S, TANG N, JIANG H X, et al. CO2 assimilation, photosystem Ⅱ photochemistry, carbohydrate metabolism and antioxidant system of citrus leaves in response to boron stress [J]. Plant Sci, 2009, 176(1): 143-153. doi: 10.1016/j.plantsci.2008.10.004
[23] 张卫华, 曹齐卫, 张帆洋, 等. 硼对黄瓜幼苗的生长及部分生理指标影响的研究[J]. 西南农业学报, 2011, 24(6): 2147-2151. doi: 10.3969/j.issn.1001-4829.2011.06.025 [24] 翁伯琦, 黄东风. 我国红壤区土壤钼, 硼, 硒元素特征及其对牧草生长影响研究进展[J]. 应用生态学报, 2004, 15(6): 1088-1094. http://qikan.cqvip.com/Qikan/Article/Detail?id=9825061&from=Qikan_Search_Index [25] AFTAB T, KHAN M M A, IDREES M, et al. Boron induced oxidative stress, antioxidant defense response and changes in artemisinin content in Artemisia annua L. [J]. J Agron Crop Sci, 2010, 196(6): 423-430. doi: 10.1111/j.1439-037X.2010.00427.x#:~:text=The%20increased%20activities%20of%20antioxidant%20enzymes%20like%20CAT%2C,applying%20higher%20doses%2C%20further%20reduced%20contents%20were%20obtained.
[26] 刘鹏, 杨玉爱. 钼, 硼对大豆叶片膜脂过氧化及体内保护系统的影响[J]. 植物学报, 2000, 42(5): 461-466. doi: 10.3321/j.issn:1672-9072.2000.05.004 [27] PISANI T, MUNZI S, PAOLI L, et al. Physiological effects of a geothermal element: boron excess in the epiphytc lichen Xanthoria parietina (L. ) TH. FR [J]. Chemosphere, 2009, 76(7): 921-926. doi: 10.1016/j.chemosphere.2009.04.058
[28] 吕成群, 黄宝灵. 低温下硼对巨尾桉叶片膜脂过氧化及体内保护系统的影响[J]. 热带亚热带植物学报, 2003, 11(3): 217-222. doi: 10.3969/j.issn.1005-3395.2003.3.004 [29] CERVILLA L M, BLASCO B, RÍOS J J, et al. Oxidative stress and antioxidants in tomato (Solanum lycopersicum) plants subjected to boron toxicity [J]. Ann Bot, 2007, 100(4): 747-756. doi: 10.1093/aob/mcm156
[30] PANDEY N. Antioxidant responses and water status in Brassica seedlings subjected to boron stress [J]. Acta Physiol Plant, 2013, 35(3): 697-706. doi: 10.1007/s11738-012-1110-z
-
期刊类型引用(4)
1. 吴胜,任兰英,高旭,刘岩,宫庆礼. 柴油水溶性组分对鼠尾藻和孔石莼生长及抗氧化酶的影响. 中国海洋大学学报(自然科学版). 2023(07): 31-41 .  百度学术
百度学术
2. 龚芳芳,李勇勇,王晔,陈淑敏,张玉琦,刘英丹,孟天宇,娄永江. 龙须菜中硼的化学形态分析. 宁波大学学报(理工版). 2021(01): 15-20 .  百度学术
百度学术
3. 于娇,胡晓,杨贤庆,陈胜军. 海洋藻类藻胆蛋白的提取、纯化与应用研究进展. 食品工业科技. 2018(11): 314-318+326 .  百度学术
百度学术
4. 王云祥,李正,秦传新,陈丕茂,袁华荣,周文礼. 不同季节江蓠脱落物对大型海藻场上覆水的影响. 南方水产科学. 2016(02): 13-20 .  本站查看
本站查看
其他类型引用(3)



 下载:
下载:

 粤公网安备 44010502001741号
粤公网安备 44010502001741号
