Preparation and research of collagen polypeptide chelated calcium from fishbone of silver carp
-
摘要:
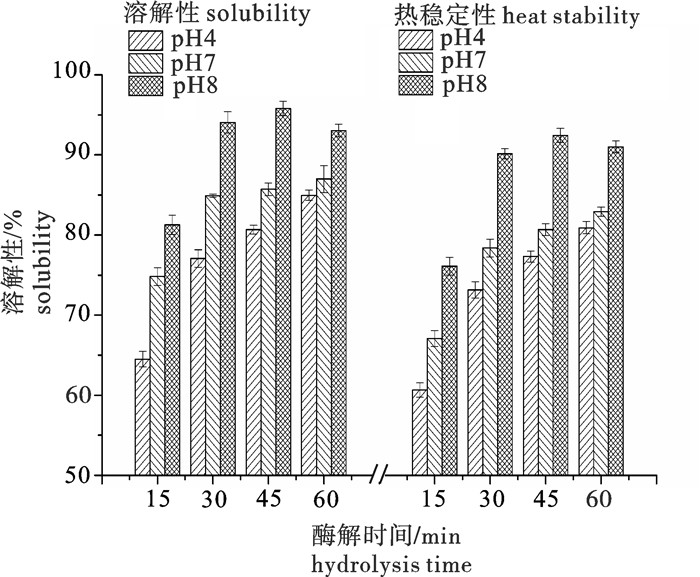
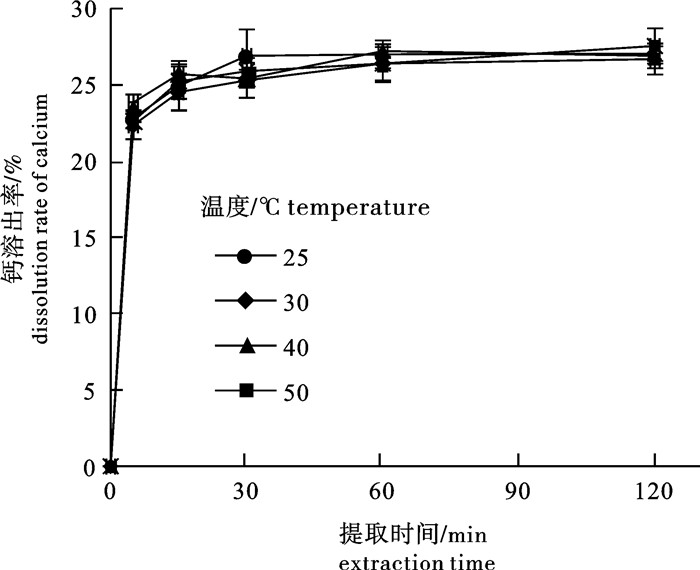
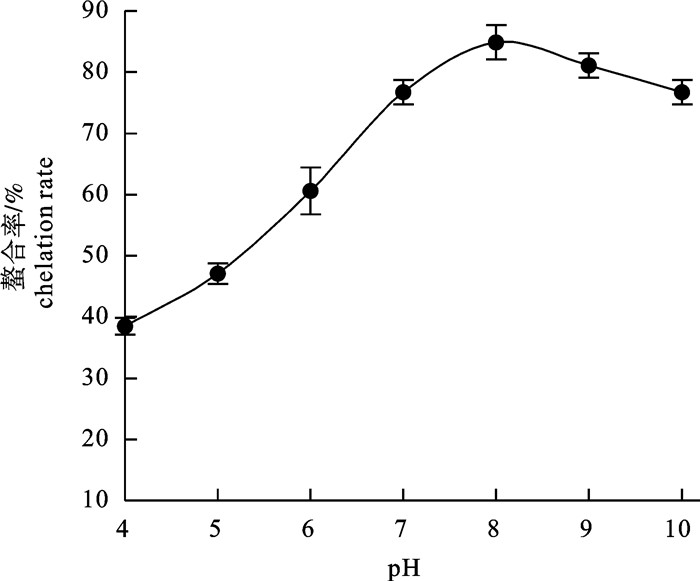
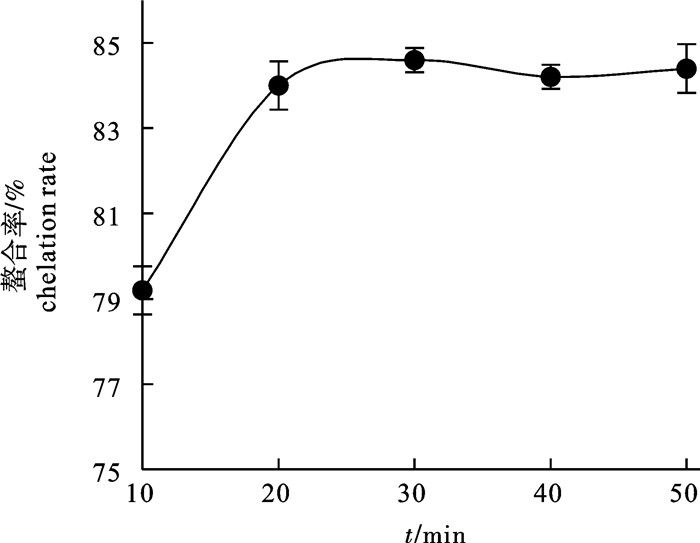
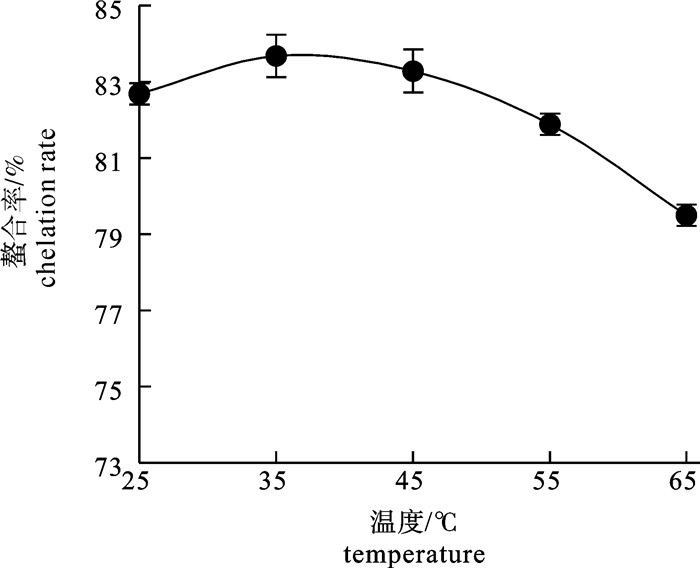
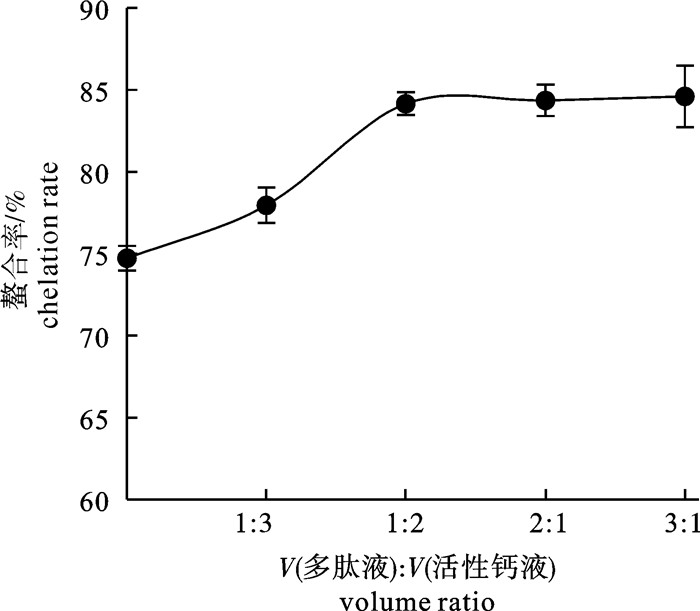
文章探讨了以鲢(Hypophthalmichthys molitrix)鱼骨为原料,采用风味蛋白酶酶解制备骨胶原多肽水解液,剩余骨渣经乳酸提取制备骨粉酸解液(钙液),研究其通过螯合制备鲢鱼骨胶原多肽螯合钙的工艺条件。分析了酶解时间对鲢鱼骨蛋白酶解产物产品品质和功能特性(溶解性和热稳定性)的影响以及采用乳酸提取鲢鱼骨中钙时提取温度对钙溶出率的影响,并以螯合率为指标,考察pH、时间、温度和多肽液与钙液体积比对螯合反应的影响。结果表明,在温度50 ℃,按原料鱼排质量0.09%加入风味蛋白酶酶解30 min制备出的鲢鱼骨胶原多肽具有良好的产品品质和功能特性;乳酸提钙时提取温度对钙溶出率没有显著性影响(P>0.05);在pH 8、温度25 ℃条件下,多肽液与钙液体积比1∶1反应40 min得到的鲢鱼骨胶原蛋白螯合钙螯合率最高(85.24%)。
Abstract:We investigated the technological parameters in preparation of collagen polypeptide chelated calcium (CPCC) from fishbone of silver carp (Hypophthalmichthys molitrix) which were chelated by collagen polypeptide hydrolysates (CPH), hydrolyzed by flavourzyme and calcium extract (CE), and extracted with lactic acid from fishbone to explore the effect of hydrolysis time on the quality and functional properties (solubility and heat stability) of CPH and effect of extraction temperature on the concentration of calcium of CE, as well as influence of chelation parameters (pH, time, temperature and volume ratio of CPH to CE) on the chelate rate of CPCC. The optimal quality and functional properties for preparation of CPH were obtained when the fish was hydrolyzed at 50 ℃ for 30 min by flavourzyme with an addition of 0.09% of the weight of fishbone. Extraction temperature of lactic acid had no significant effect on the concentration of calcium of CE (P > 0.05). The optimal parameters for chelation of CPCC were determined as: pH 8, 25 ℃, 40 min and the volume ratio of CPH to CE 1∶1, under which the chelation rate reached 85.24%.
-
Keywords:
- silver carp /
- fishbone /
- polypeptide hydrolysate /
- calcium extract /
- chelate /
- polypeptide chelated calcium
-
任何形式的捕捞均有选择性, 其选择性主要取决于渔具选择性,它强烈影响着捕捞群体结构。为了实现渔业资源的可持续利用,开展生态渔业、负责任渔业的研究有重要的意义,渔具选择性和选择性渔具是生态渔业的核心内容之一。而在我国开展的渔具选择性研究尤其是定置渔具选择性能的研究并不多见。
日本沿海主要以小型底拖网、笼、筒捕捞星康吉鳗Conger myriaster(以下简称星鳗)。在我国星鳗也是重要的群众渔业捕捞对象,青岛近海渔民用筒、山东日照渔民利用延绳钓捕捞这种鱼。山东沿海渔民在利用地笼诱捕许氏平鲉、欧氏六线鱼时, 往往同时捕获大量星鳗。本文以东京湾星鳗笼为例,利用套网法研究了其网目选择性,以期为定置渔业的科学管理提供科学依据。
1. 材料和方法
1.1 海上实验
1995~2000年,每年的10~11月在东京湾进行实验。实验笼和生产的相同,不锈钢骨架,展开为640 mm×470 mm×150 mm。每个笼有2个椭圆形开口200 mm×90 mm, 和东京湾渔获对象星鳗(全长190~600 mm, 最大体周长28~104 mm)相比, 开口非常大。因此在研究笼的选择性时, 可以仅考虑网目的选择性。
笼的底部网目尺寸(内径)为10.8 mm,远小于其他部位的网目尺寸(表 1), 星鳗从笼中逃逸的部位是底部以外的其他部分。实验时,笼的底部以外结覆网目内径为10.8 mm的套网, 套网和笼之间有足够大的空间, 且所有套网的规格相同。套网、笼均为锦纶制造,有结节菱形网片。实验时的作业方法和生产相同, 采用延绳钓作业方式。
表 1 实验笼的数量以及网目尺寸(MC)Table 1. The number and mesh size of test net pot(MC)网目尺寸/mm mesh size 1995年 1996年 1997年 1998年 1999年 2000年 21.0±0.68 4 4 4 4 4 4 18.1±0.82 3 3 4 4 4 4 15.5±0.63 3 3 4 4 4 4 13.6±0.44 3 3 4 4 4 4 11.6±0.38 3 3 4 4 4 4 将笼网、套网捕获的星鳗分别装入化纤袋,回实验室测量全长、最大体周长,体重。最大体周长是胸鳍稍后鱼体最粗部位的周长。
1.2 解析方法
如果1尾鱼被捕获的概率是p, 那么Ni尾行为独立有相同特征的鱼遭遇笼,ni尾鱼被捕获的概率$p=C_{N_i}^{n_i} p^{n_i}(1-\$p)^{N_i-n_i}$。
假设1群鱼遭遇渔具, 该鱼群依据全长可以划分为k组,组中值为li,每组鱼Ni,每组被捕的数量mi,那么$\sum_\limits{i=1}^k$尾鱼被捕获的概率$F=\prod_\limits{i=i}^k C_{N_i}^{n_i} p^{n_i}(1-p)^{N_i-n_i}$。
如果套网和笼捕获的鱼的数量为nli, mli(i=1,2,3,…,k), 那么笼捕获的全长li鱼的占该类鱼总渔获量的比例为
$$ \phi_{l_i}=\frac{n_{l_i}}{n_{l_i}+m_{l_i}} $$ (1) 依据概率的统计学定义, F可用$\phi_{l_i}$估计, 而p是渔具的选择率SL[1], 可用Logistic方程表示[2],
$$ S_L=\frac{\exp (s+b L)}{1+\exp (s+b L)} $$ (2) a,b为待估参数,L为鱼类的特征变量(全长l,相对体周长$\frac{G}{M_e}$等)。由F和$\phi_{l_i}$, p和SL的关系, 利用极大似然估计法可以得到待估参数a,b的值。
由不同网目尺寸得到的不同的网目选择性曲线, 利用不同的处理方式可以得到不同的主选择性曲线。为比较这些曲线, 引入AIC(akayike information criterion),AIC=-2 max {ln F}+2K作为判断标准,为待估参数的数目,AIC较小的模型更合适[3]。
2. 结果与讨论
2.1 星鳗的体重、全长,最大体周长间的关系
捕获的星鳗的全长l(cm)与体重w(g)、体周长G(cm)的关系分别为,
w=0.1998l2-7.9106l+93.5290(R2=0.9610, n=2 102),
G=0.1906l-0.6786(R2=0.8488, n=2 102)。
2.2 全长选择性曲线
笼的选择性由2部分组成,网目选择性、出入口的选择性。在东京湾可仅考虑网目的选择性[4]。以全长为方程2的变量,由算式1, 2得到的网目选择性曲线的各个参数(表 2)。
表 2 全长选择性曲线的各参数Table 2. Parameters of whole body length selectivity curve网目尺寸/mm mesh size a b MLL AIC l0.5 S.R. 21.0 -17.26 0.58 -22.01 48.02 29.80 3.80 18.1 -13.83 0.52 -37.65 79.30 26.80 4.30 15.5 -14.44 0.63 -56.77 117.54 23.00 3.50 13.6 -16.11 0.73 -53.71 111.42 22.00 3.00 11.6 -14.65 0.73 -173.71 351.41 20.00 3.00 注: l0.5, 50%选择全长; S.R., 选择域; MLL=Max{lnF}
Notes:l0.5, 50% selective whole body length; S.R., selective range; MLL=Max{lnF}由上述的各参数可知,网目尺寸21.0、18.1、15.5、13.6、11.6 mm笼的全长选择性能,全长0 < l < 25.50 cm、0 < l < 22.50 cm、0 < l < 18.50 cm、0 < l < 18.50 cm、0 < l < 16.50 cm时,全长选择率几乎为0;全长25.50 < l < 35.50 cm、22.50 < l < 32.50 cm、18.50 < l < 27.50 cm、18.50 < l < 26.50 cm、16.50 < l < 24.00 cm时,全长选择率随全长不断增长而逐渐增大;全长在l>35.50 cm、l>32.50 cm、l>27.50 cm、l>26.50 cm、l>24.00 cm时,全长选择率几乎接近于1.00,50%选择全长l0.5分别为29.8、26.8、23.0、22.0、20.0 cm;全长选择域为3.80、4.30、3.50、3.00、3.00 cm。因此,全长选择性曲线沿全长增加方向,随网目增大而向右移,并且网目越小,选择越尖锐。
笼的网目尺寸分别为21.0、18.1、15.5、13.6、11.6 mm,和套网的网目尺寸的比值依次为1.07、1.26、1.44、1.68、1.94。所对应的AIC逐渐减少(表 2)。由于实验中,除笼的网目尺寸有差别外,其他条件尽可能相同,因此造成这种趋势的原因很可能来自套网对实验笼的影响(例如局部流场的改变程度),即可能是在一定范围内,实验网和套网的网目尺寸差别越大,套网对实验网的影响越小;而当两者相当时,套网的影响相当显著。是否是这种原因,有待于更多关于鱼类行为以及渔具和捕捞对象相互作用的实验检验。
2.3 主选择性曲线
鱼能否穿过网目,主要取决于鱼沿体高方向的截面形状以及相对于网目内径的大小[4]。由或为方程1的变量,所得到的方程为主选择性方程,它描绘的曲线为主选择性曲线(master selectivity curve)。有2种方法,each curve model和single curve model可得到主选择性曲线。前者是求得每一网目尺寸所对的主选择性曲线。后者将所有的网目尺寸所对应的相对体周长$\frac{G}{M_c}$或相对全长$\frac{l}{M_c}$值合并,看作一组数值,求得一条反映渔具选择性的曲线。
以$\frac{G}{M_c}$为方程2的变量,由single curve model和each curve model,利用极大似然估计法,得到待估参数(表 3)。因∑ (AICeach curve model)=250.18,而AICsingle curve model=244.32,其差值│244.32-250.18│>1,所以可以认为single curve model与each curve model之间的差异并非偶然,single curve model得到的主选择性曲线可更好地反映网目选择性。
表 3 主选择性曲线的各参数Table 3. Parameters of master selectivity curve模式models a b $\frac{G}{M_{e0.5}}$ S.R. MLL AIC single curve model -4.71 4.25 1.11 0.52 -120.16 244.32 each curve model- 115.09 250.18 21.0 mm -10.47 8.68 1.21 0.25 -16.96 37.92 18.1 mm -8.92 7.70 1.16 2.87 -24.45 52.90 15.5 mm -1.58 2.87 0.55 0.77 -24.54 53.07 13.6 mm -4.87 4.62 1.06 0.48 -16.95 37.91 11.6 mm -0.01×10-2 1.08 9.20×10-5 2.03 -32.19 68.38 50%选择相对体周长1.11,相对体周长的选择域为0.52。$0<\frac{G}{M_c}<0.55$,相对体周长选择率几乎为0;$0.55< \frac{G}{M_c}<1.60$,选择率随相对体周长增加而增加;$\frac{G}{M_c}>1.60$,选择率趋向于1.00。一般认为当$\frac{G}{M_c}=1$时,选择率就应当趋向于1.0,而本实验当$\frac{G}{M_c}>1.60$,选择率才趋向1.00。这种结果和星鳗底拖网的网目选择性中的类似[5]。其最可能的原因是星鳗体表鳞片退化,凸起减少,且分泌大量粘液,使之容易穿过网目。另外,网线对星鳗的刺激,也有促进星鳗积极逃逸的可能。
3. 小结
比较显示,套网和实验网的网目尺寸差别较大时,套网的影响较小。而在两者接近时,套网的影响极为显著。
此外,本文中给出了利用套网法得到的星鳗笼的网目选择性能, 但套网对入笼的星鳗行为存在影响, 这种影响到底有多大, 以及入网的星鳗如何从笼中逃逸, 逃逸后的残存率有多大, 都是将来要研究的重点所在。
-
表 1 鲢鱼骨基本成分组成(X±SD)
Table 1 Basic components in fishbone of silver carp
成分
component质量分数/%
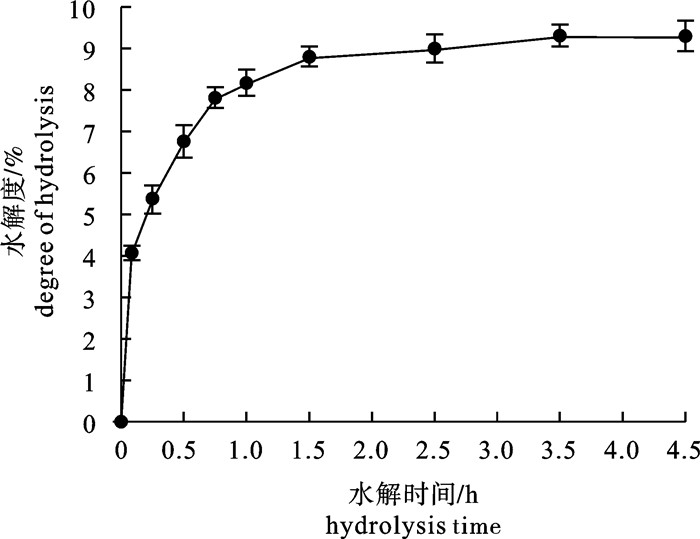
content水分water 64.91±1.23 灰分ash 9.92±0.90 粗脂肪fat 4.40±1.32 粗蛋白protein 14.76±0.28 钙calcium 4.15±0.23 表 2 酶解时间对酶解产物品质的影响
Table 2 Effect of hydrolysis time on quality of hydrolysates
酶解时间/min
hydrolysis time水解度/%
degree of hydrolysis色泽
color苦味
bitterness0 0 白色 无 5 4.07 白色 轻 15 5.36 微黄 较轻 30 6.76 微黄 较轻 45 7.81 微黄 稍苦 60 8.17 微黄 稍苦 90 8.81 微黄 苦 150 9 较黄 苦 210 9.31 较黄 苦 270 9.3 较黄 苦 表 3 酶解产物的氨基酸组成
Table 3 Amino acid composition of hydrolysates
氨基酸amino acid 质量分数/% content 氨基酸amino acid 质量分数/% content 天门冬氨酸Asp 7.78 亮氨酸Leu 4.92 苏氨酸Thr 3.58 酪氨酸Tyr 2.33 丝氨酸Ser 3.70 苯丙氨酸Phe 2.56 谷氨酸Glu 12.64 赖氨酸Lys 5.52 甘氨酸Gly 13.26 组氨酸His 1.36 丙氨酸Ala 7.30 精氨酸Arg 6.34 缬氨酸Val 3.35 脯氨酸Pro 8.08 蛋氨酸Met 2.41 色氨酸Trp 0.75 异亮氨酸Ile 2.30 胱氨酸Cys 0.51 表 4 螯合反应正交试验设计与结果分析
Table 4 Experimental design and result of orthogonal test of chelation reaction
试验号
test No.因素factor 螯合率/%
chelation ratepH
(A)时间/min
time (B)温度/℃
temperature (C)体积比*
volume ratio* (D)1 1(7) 1(20) 1(25) 1(1∶2) 75.41 2 1 2(30) 2(35) 2(1∶1) 77.11 3 1 3(40) 3(45) 3(2∶1) 77.38 4 2(8) 1 2 3 84.95 5 2 2 3 1 79.17 6 2 3 1 2 85.24 7 3(9) 1 3 2 82.15 8 3 2 1 3 81.39 9 3 3 2 1 77.80 均值1
mean 176.63 80.84 80.68 77.46 均值2
mean 283.12 79.22 79.95 81.50 均值3
mean 380.45 80.14 79.57 81.24 极差
range6.49 1.61 1.11 4.04 注:*.多肽液与钙液体积比;括号内为实际值
Note:*.volume ratio of CPH to CE;value in brackets are the actual value of each factor.表 5 鲢鱼骨多肽螯合钙粉基本成分组成(X±+SD)
Table 5 Nutritional components of collagen polypeptide chelate calcium powder from fishbone of silver carp
营养成分
nutritional component质量分数/%
content蛋白质protein 86.15±1.14 脂肪lipid 1.48±0.37 水分moisture 1.72±0.11 灰分ash 9.96±0.52 钙calcium 8.89±0.46 -
[1] 农业部渔业局. 中国渔业统计年鉴2013 [M]. 北京: 中国农业出版社, 2013: 23. [2] TOPPE J, ALBREKTSEN S, HOPE B, et al. Chemical composition, mineral content and amino acid and lipid profiles in bones from various fish species [J]. Comp Biochem Phys B, 2007, 146(3): 395-401. doi: 10.1016/j.cbpb.2006.11.020
[3] 赵玉红. 骨的综合利用[J]. 肉类工业, 2001 (3): 23-24. doi: 10.3969/j.issn.1005-9989.2003.04.032 [4] GILDBERG A, ARNESEN J A, CARLEHOG M. Utilisation of cod backbone by biochemical fractionation [J]. Process Biochem, 2002, 38(4): 475-480. doi: 10.1016/S0032-9592(02)00103-6
[5] 甄润英, 李晓雁, 高巍. 鲶鱼骨酶解物的抗氧化活性研究[J]. 天津农学院学报, 2011, 18(4): 13-15, 19. doi: 10.3969/j.issn.1008-5394.2011.04.005 [6] 杨露, 丁利君, 蓝德安. 马面鱼骨胶原多肽的理化特性及其抗氧化活性[J]. 食品科学, 2013, 34(11): 109-112. doi: 10.7506/spkx1002-6630-201311024 [7] 吴燕燕, 李来好, 林洪, 等. 罗非鱼骨制备CMC活性钙的工艺及生物利用的研究[J]. 食品科学, 2005, 26(2): 114-117. https://www.spkx.net.cn/CN/Y2005/V26/I2/114 [8] 洪惠, 沈慧星, 罗永康. 鱼骨多肽钙粉的研究与开发[J]. 肉类研究, 2010(8): 78-82. doi: 10.3969/j.issn.1001-8123.2010.08.022 [9] 陆剑锋, 孟昌伟, 李进, 等. 斑点叉尾鱼骨胶原多肽螯合钙的制备及其特征[J]. 水产学报, 2012, 36(2): 314-320. doi: 10.3724/SP.J.1231.2012.27739 [10] 洪惠, 罗永康, 吕元萌, 等. 酶法制备鱼骨胶原多肽螯合钙的研究[J]. 中国农业大学学报, 2012, 17(1): 149-155. https://xueshu.baidu.com/usercenter/paper/show?paperid=00959eb002b067475c67e0bfe56669b6&site=xueshu_se [11] 梁春辉, 菅景颖, 张志胜. 胶原多肽螯合钙壮骨作用研究[J]. 河北农业大学学报, 2010, 33(5): 94-97. doi: 10.3969/j.issn.1000-1573.2010.05.021 [12] 张晓霞, 刘盛取, 李国英. 碱法水解黑鱼鱼鳞及制备多肽螯合钙工艺的研究[J]. 食品科技, 2010, 35(12): 130-134. [13] ADLER-NISSEN J. Determination of the degree of hydrolysis of food protein hydrolysates by trinitrobenzenesulfonic acid [J]. J Agric Food Chem, 1979, 27(6): 1256-1262. doi: 10.1021/jf60226a042
[14] SPELLMAN D, MCEVOY E, O′CUINN G, et al. Proteinase and exopeptidase hydrolysis of whey protein: comparison of the TNBS, OPA and pH stat methods for quantification of degree of hydrolysis [J]. Int Dairy J, 2003, 13(6): 447-453. doi: 10.1016/S0958-6946(03)00053-0
[15] 李雪, 罗永康, 吕元萌, 等. 鲽鱼下脚料酶解产物的功能特性[J]. 肉类研究, 2011, 25(7): 5-7. doi: 10.3969/j.issn.1001-8123.2011.07.003 [16] 赵瑞香, 连喜军, 王欣, 等. 利用酶法促使骨粉中钙转化的研究[J]. 食品科学, 2000, 21(3): 34-36. doi: 10.3321/j.issn:1002-6630.2000.03.012 [17] 王东, 蒲训, 陈明凯, 等. 鲑鳟鱼骨提取胶原肽工艺与产品生物活性研究[J]. 中兽医医药杂志, 2010(4): 15-19. doi: 10.3969/j.issn.1000-6354.2010.04.004 [18] 张俊杰, 段蕊. 浅谈淡水鱼的综合加工[J]. 渔业现代化, 2004(1): 36-38. doi: 10.3969/j.issn.1007-9580.2004.01.017 [19] YUST M D, PEDROCHE J, MILLAN-LINARES M D, et al. Improvement of functional properties of chickpea proteins by hydrolysis with immobilised alcalase [J]. Food Chem, 2010, 122(4): 1212-1217. doi: 10.1016/j.foodchem.2010.03.121
[20] QUAGLIA G B, ORBAN E. Influence of the degree of hydrolysis on the solubility of the protein hydrolysates from sardine (Sardina pilchardus) [J]. J Sci Food Agric, 1987, 38(3): 271-276. doi: 10.1002/jsfa.2740380311
[21] 范鸿冰, 陈孙福, 洪惠, 等. 鳄鱼骨双酶酶解产物的功能特性及其抗氧化活性[J]. 食品与发酵工业, 2012, 38(12): 78-82. [22] BAE I, OSATOMI K, YOSHIDA A, et al. Biochemical properties of acid-soluble collagens extracted from the skins of underutilised fishes [J]. Food Chem, 2008, 108(1): 49-54. doi: 10.1016/j.foodchem.2007.10.039
[23] 罗凯. 由鲮鱼排制备活性钙的研究[J]. 广东化工, 2007, 34(6): 60-63. doi: 10.3969/j.issn.1007-1865.2007.06.020 [24] 薛长湖, 李兆杰, 孙成, 等. 由鳕鱼排制备活性钙[J]. 青岛海洋大学学报, 1995, 25(2): 173-179. https://xueshu.baidu.com/usercenter/paper/show?paperid=0671a68d35eefa79090b65f3852b7262&site=xueshu_se&hitarticle=1 [25] 赫美, 许鑫, 杨春瑜. 食醋对鱼骨中钙溶出的影响[J]. 现代食品科技, 2011(1): 87-89. doi: 10.3969/j.issn.1673-9078.2011.01.021 [26] 白艳, 谈小登, 黄晓, 等. 鳗鱼骨钙酸法提取工艺的研究[J]. 食品科技, 2010(8): 274-277. [27] WEDEKIND K, HORTIN A, BAKER D. Methodology for assessing zinc bioavailability: efficacy estimates for zinc-methionine, zinc sulfate, and zinc oxide [J]. J Anim Sci, 1992, 70(1): 178-187. doi: 10.2527/1992.701178x
[28] 吴玥霖, 王俊. 鱼骨粉制备复合氨基酸螯合钙工艺研究[J]. 食品与发酵科技, 2009, 45(1): 51-54. doi: 10.3969/j.issn.1674-506X.2009.01.014 -
期刊类型引用(1)
1. 张静,胡长圣,刘前,戴佳玥,王学锋,汤保贵. 流速对卵形鲳鲹游泳行为及运动生理的影响. 中国水产科学. 2024(04): 381-390 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
