Structure and phylogenetic analysis of mitochondrial DNA control region of genus Trachurus
-
摘要:
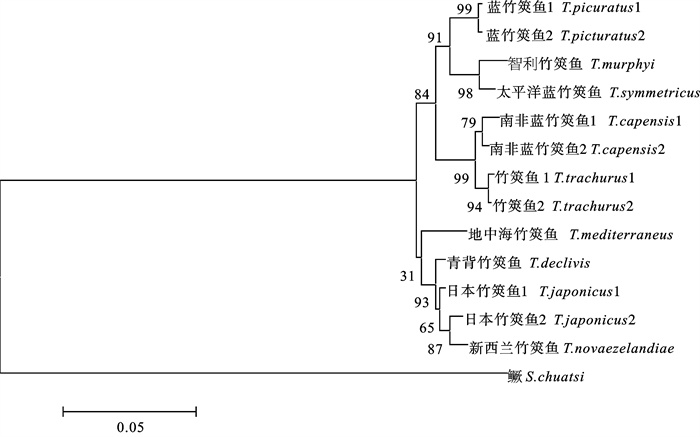
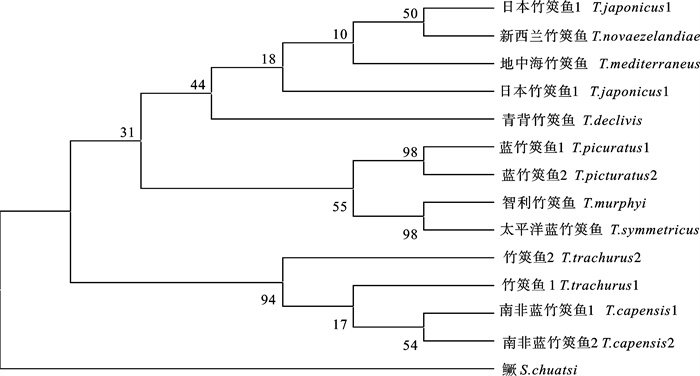
采用PCR产物直接测序法测定了2尾来自中国南海的日本竹筴鱼(Trachurus japonicus)线粒体DNA控制区基因全序列,并结合从GenBank中下载的8种竹筴鱼属相应序列,对竹筴鱼属控制区序列进行了结构分析,识别出终止序列区、中央区和保守序列区3个区域,并找到了2个与DNA复制终止相关的序列TAS和中央保守区的保守序列CSB-F、CSB-E和CSB-D,以及保守序列区的保守序列CSB1、CSB2和CSB3。以鳜(Siniperca chuatsi)作为外群,使用邻接法和最大简约法构建了9种竹筴鱼属的系统发育树。竹筴鱼属鱼类为单系类群,蓝竹筴鱼(T.picturatus)、智利竹筴鱼(T.murphyi)、太平洋竹筴鱼(T.symmetricus)、南非竹筴鱼(T.capensis)和竹筴鱼(T.Trachurus)构成一支,地中海竹筴鱼(T.mediterraneus)、青背竹筴鱼(T.declivis)、日本竹筴鱼(T.japonicus)和新西兰竹筴鱼(T.novaezelandiae)为另一支;日本竹筴鱼未单独成一支,而是聚入青背竹筴鱼和新西兰竹筴鱼之间,初步猜测日本竹筴鱼和新西兰竹筴鱼为同种异名。
Abstract:We used PCR to amplify the complete sequences of mitochondrial DNA (mtDNA) control region of 2 Trachurus japonicus from South China Sea, and then aligned them by Clustal X with 8 other species of the genus Trachurus from GenBank. According to the alignment and structure comparison, the mtDNA control region of the genus Trachurus can be divided into 3 domains: termination associated sequence domain (TAS), central conserved domain (CD) and conserved sequence block domain (CSB).We identified 2 termination-associated sequences (TAS) and 3 conserved blocks (CSB-F, CSB-E and CSB-D) in CD domain as well as 3 conserved sequence blocks (CSB-1, CSB-2 and CSB-3) in CSB domain. Taking Siniperca chuatsi as outgroup, the molecular phylogenetic relationship among 9 Carangidae was analyzed using neighbor-joining (NJ) method and maximum parsimony method in MEGA 4.0. Results show that the genus Trachurus fishes belong to a monophyletic group: T.picturatus, T.murphyi, T.symmetricus, T.capensis and T.Trachurus gather into one cluster; T.mediterraneus, T.declivis, T.japonicus and T.novaezelandiae gather another. T.japonicus does not form into an independent group but is merged into T.declivis and T.novaezelandiae. Thus, it is suggested that T.japonicus and T.novaezelandiae may be 2 synonyms.
-
Keywords:
- genus Trachurus /
- mtDNA control region /
- structure /
- phylogenetic relationship
-
雷州湾是南海北部许多经济海洋生物的关键栖息地之一。该海湾底形平坦,底质以泥沙为主[1]; 潮汐属非正规半日潮,最大水深不超过20 m。该海域不仅是南海北部主要虾产区之一[2],而且是仅次于珠江口的第二大中华白海豚(Sousa chinensis)种群栖息地[3]。海湾在游泳生物的生长、补充、繁殖等关键生活史阶段扮演着重要角色[4]。游泳生物特别是鱼类、甲壳类、头足类是渔业捕捞的重要组成部分[5]。解析海湾游泳生物群落结构特征及其影响因子是渔业生态学研究的重要内容[4, 6-7],也是渔业资源科学管理和合理利用的参考依据。20世纪70、80年代[2]及2005年[8-9]分别采用虾拖网调查了雷州湾的硇洲岛一侧海域、湛江港邻近海域的渔业资源。近年来,粤西地区社会经济的迅速发展过程中,人类活动(捕捞、污染、涉海工程建设)对该海域生态环境的干扰日益加剧,而近10年来该海域的渔业资源的相关研究尚未见报道。雷州湾内沿岸有湛江红树林自然保护区(国家级),且湾内多处存在养殖牡蛎用的筏架、栅架等限制了拖网渔业资源的调查范围。因此,文章采用三重流刺网调查雷州湾海域的渔业资源,分析其游泳生物群落的结构特征及其影响因子,为该海域的中华白海豚保护与渔业资源持续利用提供参考依据。
1. 材料与方法
1.1 站点布设与样品采集
分别于2014年11月(秋季)、2015年1月(冬季)、2015年4月(春季)和2015年8月(夏季)在雷州湾海域采用单船表层三重流刺网共完成了4航次的游泳生物调查(每航次调查站位一致),在湾内、湾中和湾口3个断面共布设6个站点(图 1),调查范围基本覆盖中华白海豚在雷州湾内的主要活动区域[3],并避开航道和筏式牡蛎养殖区。调查所用渔具为三重刺网,两侧两片大网目网衣和中间小网目网衣的网目尺寸分别为150 mm、150 mm和50 mm,装配完成后的刺网高度为1.50 m。每站点分别采用200 m和400 m 2种网具长度各下网1次。捕捞作业时间取渔民实际作业时间近似值(1 h),准确记录起放网的位置、时间。同步监测捕捞作业水层的水温、盐度、pH、溶解氧(DO)、水深等环境因子,水体表层叶绿素a(Chl-a)质量浓度(mg·m-3)自凯撒渔业遥感系统(CATSAT)中按捕捞作业时间匹配进行提取。
1.2 渔获物鉴定
依据《海洋调查规范》[10]GB/T12763.6—2007的操作要求,渔获物的种类鉴定、分类标准主要参照董正之[11]、戴爱云等[12]、NELSON[13]及刘瑞玉[14]等,将渔获物分种类后分别计数和称质量。
刺网的渔获率用刺网单位捕捞努力量渔获量(catch per unit effort,CPUE)[15]表示,考虑到渔获质量与渔获尾数的差异,分别采用每小时每米长度刺网的渔获尾数[number per unit effort,NPUE,尾·(m·h)-1]和渔获质量[biomass per unit effort, BPUE,kg·(m·h)-1] 2个参数表征。
1.3 数据处理
1.3.1 多样性指数
采用分类学多样性指数(Δ)表征雷州湾游泳生物种类组成分类阶元的多样性。分类多样性指数不仅反映了站位间、物种间丰度的结构特征,亦反映了站位间样品的种类分类阶元的关联程度[16-17],在评价群落多样性、比较生物多样性的区域变化、时间序列变化等方面均提供了重要信息[17-18]。各指数的计算公式为:
基于丰度的分类多样性指数:
$ \mathit{\Delta }=\text{ }\left[\sum {{\sum }_{i\text{ } < \text{ }j~}}{{w}_{ij~}}{{x}_{i~}}{{x}_{j~}} \right]/\left[n\left( n-1 \right)/2 \right] $
(1) 平均分类差异指数:
$ {{\mathit{\Delta }}^{*}}=\left[\sum {{\sum }_{i\text{ } < \text{ }j}}{{w}_{ij}}{{x}_{i}}{{x}_{j}} \right]/\left[\sum {{\sum }_{i\text{ } < \text{ }j}}{{x}_{i}}{{x}_{j}} \right] $
(2) 分类差异变异指数:
$ {{\mathit{\Lambda }}^{+}}=\left[\sum {{\sum }_{i\text{ } < \text{ }j}}{{\left( {{w}_{ij}}-\mathit{\Delta } \right)}^{2}} \right]/\left[s\left( s-1 \right)/2 \right] $
(3) 此外,运用皮尔逊相关性检验分类多样性指数与Shannon-Wiener多样性指数(H′)和Pielou均匀度指数(J′)[19]的相关性。
$ H\prime =-\sum\limits_{i=1}^{s}{{{P}_{i}}\text{ln}{{P}_{i}}} $
(4) $ J\prime =H\prime /\text{ln}s $
(5) 式(1)~(5)中xi、xj分别表示第i、j个物种的丰度,n为一个样品中的个体数总和,s为渔获物的总种数,wij是第i种鱼类与第j种鱼类在系统分类树中的路径长度,采用默认值(即最长的分类路径长度为100,且在不同分类水平之间的路径长度相等),Pi为第i种鱼的质量占总渔获质量的比例。
1.3.2 物种重要性排序
游泳生物群落的物种重要性排序运用RAD模型(rank abundance dominance)分析[20-21],运用最大似然估计估算下述4个模型的参数,各模型的拟合程度采用赤池信息准则(Akaike′s information criterion,AIC)判别。
$ \text{Preemption 方程}:{{\widehat{a}}_{r}}=N\alpha {{\left( 1-\alpha \right)}^{r-1}} $
(6) $ \text{Log-normal 方程}:{{\widehat{a}}_{r}}=\text{exp}[\text{log}\left( \mu \right)+log\left( \sigma \right)\mathit{\Phi }] $
(7) $ \text{Zipf 方程}:{{\widehat{a}}_{r}}=Np_{^{1}}^{\mu }{{r}^{\gamma }} $
(8) $ \text{Mandelbrot 方程}:{{\widehat{a}}_{r}}=Nc{{\left( r+\beta \right)}^{\gamma }} $
(9) 式(6)~(9)中âr是种类在排序r序列中的相对丰度,N是所有种类的频数和,Φ是标准正态分布函数,p1μ是丰度最高的物种占全部物种丰度的比例估值; α, μ, σ, γ, β, c是各模型的待估参数。
1.3.3 广义线性模型建模
运用广义线性模型(general linear modeling,GLM)分析CPUE与季节、网具长度、站点和环境数据的关系[21]。分别将NPUE、BPUE取lg(x+1)转换后作为因变量Y1和Y2。关联函数选用类泊松quasi-poisson方法,建立了11个变量的广义线性模型,其中9个独立变量(X1~X9)依次为站位、季节、网具长度、pH、DO、盐度、水温、水深和叶绿素a,同时将季节与水温(X10),站位与网具长度(X11)的交互作用作为另外2个自变量。统计分析用R语言[22]和Excel 2013完成[23]。
2. 结果
2.1 种类组成
雷州湾海域进行的流刺网调查共鉴定游泳动物113种,隶属于5纲16目49科86属(表 1)。鱼类种类数最多,共10目39科65属82种,约占出现总种类数的72.5%;其中软骨鱼纲仅尖头斜齿鲨(Scoliodon laticaudus)1种; 辐鳍鱼纲为9目38科64属81种,约占出现总种类数的71.7%,种类以鲈形目最多,计45种。头足纲为3目3种3属3种,如短蛸(Octopus fangsiao), 中国枪乌贼(Uroteuthis chinensis)等。软甲纲(甲壳类)为6科17属27种,约占出现总种类数的23.9%;其中口足目8种,如长叉口虾蛄(Miyakella nepa)、口虾蛄(Oratosquilla oratoria); 虾类8种,如中国对虾(Penaeus chinensis)、日本囊对虾(P.japonicus)、鹰爪虾(Trachysalambria curvirostris)等; 蟹类10种,如矛形梭子蟹(Portunus hastatoides)、红星梭子蟹(Macropipus tuberculatus)、红线黎明蟹(Matuta planipes)等。而海胆纲仅1种,为马粪海胆(Hemicentrotus pulcherrimus)。
表 1 雷州湾研究海域游泳生物种类数分类及其所占比例Table 1. Species composition of nekton and proportion in survey area of Leizhou Bay纲class 目order 科family 属genus 种species 软骨鱼纲Chondrichthyes 真鲨目Carcharhiniformes 1(2.0) 1(1.2) 1(0.9) 辐鳍鱼纲Actinopterygii 鲽形目Pleuronectiformes 3(6.1) 7(8.1) 7(6.2) 鲱形目Clupeiformes 3(6.1) 9(10.5) 14(12.4) 鲈形目Perciformes 22(44.9) 34(39.5) 45(39.8) 鲶形目Siluriformes 1(2.0) 1(1.2) 1(0.9) 鲀形目Tetraodontiformes 2(4.1) 3(3.5) 3(2.7) 仙女鱼目Aulopiformes 2(4.1) 2(2.3) 2(1.8) 银汉鱼目Atheriniformes 1(2.0) 1(1.2) 2(1.8) 鲉形目Scorpaeniformes 3(6.1) 6(7.0) 6(5.3) 鲻形目Mugiliformes 1(2.0) 1(1.2) 1(0.9) 头足纲Cephalopoda 八腕目Octopoda 1(2.0) 1(1.2) 1(0.9) 乌贼目Sepioidea 1(2.0) 1(1.2) 1(0.9) 枪形目Teuthoidea 1(2.0) 1(1.2) 1(0.9) 软甲纲Malacostraca 口足目Stomatopoda 1(2.0) 7(8.1) 8(7.1) 十足目Decapoda 5(10.2) 10(11.6) 19(16.8) 海胆纲Echinoidea 拱齿目Camarodonta 1(2.0) 1(1.2) 1(0.9) 合计total 16 49 86 113 注:括号中数字为分类单元所占比例(%)。
Note:Values in the brackets are the percentage of taxa.雷州湾游泳生物的分类多样性指数(Δ)与J′和H′的空间变化趋势一致,均呈湾内 < 湾中 < 湾口的变化特征(表 2)。该海域游泳生物Δ为72.72,平均分类差异指数(Δ*)为80.25,分类差异变异指数(Λ+)为455.37。整个雷州湾渔业资源种类的J′平均为0.79,H′均值为3.12。
表 2 基于流刺网调查的雷州湾游泳生物群落多样性特征Table 2. Diversity of nekton communities in Leizhou Bay using gillnetting站位site 种数species 分类多样性指数(Δ)taxonomic diversity 平均分类差异指数(Δ*)average TD 分类差异变异指数(Λ+)variation in TD 均匀度指数(J′)Pielou′s evenness index 香农-威纳多样性指数(H′)Shannon′s diversity index G1 34 67.32 78.46 431.35 0.75 2.63 G2 44 63.98 83.55 517.56 0.58 2.21 G3 50 74.01 77.94 419.28 0.85 3.32 G4 61 76.17 79.78 419.17 0.84 3.44 G5 61 77.66 81.20 494.96 0.86 3.55 G6 66 77.20 80.62 449.91 0.85 3.54 均值mean 53 72.72 80.25 455.37 0.79 3.12 注:G1和G2代表湾内,G3和G4代表湾中,G5和G6代表湾口。
Note:Site of G1 and G2,G3 and G4,G5 and G6 represented three groups of the inner,middle and mouth of the bay,respectively.Δ与Λ+无显著相关性且能够较全面地反映群落多样性特征。表 3中5个多样性指数的相关性存在较大波动,Δ与J′、H′均显著相关,且J′与H′显著相关; 3个分类多样指数中,仅Δ*和Λ+显著相关(P < 0.05),其他两两相关性均不显著。与J′、H′相比,Δ不仅考虑到种类数、丰度,也包含了系统发生、种类丰度沿环境因子的梯度变化等信息。
表 3 多样性指数皮尔逊相关性检验Table 3. Pearson′s correlations among five biodiversity indices变量
variable分类多样性指数(Δ)
taxonomic diversity平均分类差异指数(Δ*)
average taxonomic diversity分类差异变异指数(Λ+)
variation in taxonomic diversity均匀度指数(J′)
Pielou′s evenness index香农-威纳多样性指数(H′)
Shannon′s diversity indexΔ 1 Δ* 0.299 1 Λ+ -0.348 0.907 9* 1 J′ 0.928** -0.622 0.597 1 H′ 0.996** -0.381 6 -0.419 0.955** 1 注:*.差异显著P < 0.05;**.差异极显著P < 0.01;后表同此。
Note:* indicates significant difference (P < 0.05);** indicates very significant difference (P < 0.01). The same case in the following table.2.2 物种的重要性
基于RAD的雷州湾海域游泳生物种类-丰度建模分析表明(图 2),种丰度分布基于丰度排序而形成单调递减的曲线; Mandelbrot模型âr=N×1.01×105(r-3.91)33.36的拟合优度最佳(AIC=485)。
![]() 图 2 雷州湾游泳生物群落的RAD模型拟合优度J.bel.皮氏叫姑鱼; P.xi.矛形梭子蟹; S.ova.卵鳎; M.nep.长叉口虾蛄; P.chi.中国对虾; T.set.长颌棱鳀; T.dus.杜氏棱鳀; O.ora.口虾蛄; P.xi.红星梭子蟹; M.pla. 红线黎明蟹;
图 2 雷州湾游泳生物群落的RAD模型拟合优度J.bel.皮氏叫姑鱼; P.xi.矛形梭子蟹; S.ova.卵鳎; M.nep.长叉口虾蛄; P.chi.中国对虾; T.set.长颌棱鳀; T.dus.杜氏棱鳀; O.ora.口虾蛄; P.xi.红星梭子蟹; M.pla. 红线黎明蟹;
Lognormal,Preemption,Zipf,Mandelbrot为基于RAD理论的4个模型。Figure 2. Rank-Abundance Dominance Modeling on nekton community from Leizhou Bay watersJ.bel. Johnius belangerii; P.xi. Portunus (Xiphonectes) hastatoides; S.ova. Solea ovata; M.nep. Miyakella nepa; P.chi. Penaeus chinensis; T.set. Thryssa setirostris; T.dus. Thryssa dussumieri; O.ora. Oratosquilla oratoria; P.xi. Portunus triberculatus; M.pla. Matuta planipes;
Lognormal, Preemption, Zipf and Mandelbrot were the fitted RAD models.4个季度雷州湾流刺网捕捞的113种游泳生物中,重要性居前10的种类中有鱼类4种,甲壳类6种(图 2)。4种鱼类中包括2种底层、近底层鱼类,皮氏叫姑鱼(Johnius belangerii)和卵鳎(Solea ovata),NPUE分别为45.5×10-2尾·(m·h)-1和21.3×10-2尾·(m·h)-1; 2种中上层小型鱼类长颌棱鳀(Thryssa setirostris)和杜氏棱鳀(T.dussumieri),NPUE分别为15.8×10-2尾·(m·h)-1和18.9×10-2尾·(m·h)-1。6种甲壳类依次为矛形梭子蟹、长叉口虾蛄、中国对虾、口虾蛄、红星梭子蟹和红线黎明蟹,NPUE依次为22.1×10-2尾·(m·h)-1、36.8×10-2尾·(m·h)-1、17.2×10-2尾·(m·h)-1、14.3×10-2尾·(m·h)-1、14.7×10-2尾·(m·h)-1和16.4×10-2尾·(m·h)-1。
2.3 CPUE与环境因子的相关性
基于GLM的BPUE和NPUE与11个环境因子的分析表明(表 4),各环境因子对BPUE与NPUE的影响程度存在差异。显著影响BPUE的因子为水体溶解氧含量(P < 0.01);而显著影响NPUE的除DO外(P < 0.05),还包括水温(P < 0.01)及因季节变动所导致的季节间水温差异(P < 0.05)。导致BPUE和NPUE受环境因子影响差异的原因主要是游泳生物的平均体质量(即BPUE/NPUE)变化太大,以皮氏叫姑鱼为例,平均体质量为25.38~93.5 g·尾-1。
表 4 雷州湾流刺网渔业资源量与环境因子的广义线性模型Table 4. GLM modeling of stock of gillnetting fishery with ecological variables in Leizhou Bay自变量
independent variable因变量Y1:BPUEa
dependent variable Y1,BPUEa因变量Y2:NPUEa
dependent variable Y2,NPUEa截距intercept -19.57±29.12 -7.51±11.11 X1:站位sites -0.57±0.56 -0.03±0.23 X2:季节season -5.72±4.18 -3.44±1.58* X3:网具net-size -0.08±0.24 -0.08±0.11 X4:pH 0.35±2.12 1.13±0.73 X5:DO 4.25±1.72** 1.62±0.77* X6:S -0.13±0.43 -0.15±0.14 X7:T -0.48±0.50 -0.39±0.17** X8:depth 0.01±0.28 0.02±0.09 X9:Chl-a -1.25±1.36 0.32±0.53 X10:season-T 0.22±0.17 0.14±0.06* X11:sites-net-size 0.02±0.11 0.01±0.05 注:a.取常用对数转换
Note:a indicates that both the variables are log10 transformed.此外,调查站位空间差异、季节变动及流刺网的不同网具长度对该海域CPUE(以BPUE、NPUE表征)未产生显著影响(P>0.05)。综上,基于流刺网调查的雷州湾海域游泳生物总体分布较均匀,初步分析可能与2个因素相关,1)调查所用的流刺网的作业水层仅限于1.5 m,主要捕捞栖息于该水深的游泳生物; 2)整个调查海域的水深均在20 m以浅,湾内、湾中、湾口不同调查站位之间游泳生物的群落结构变化较小。
3. 讨论
3.1 多样性指数的比较
多样性指数的本质是信息熵,综合考虑了物种的种类数和其相对丰度[24],群落多样性表示从一个群落中随机抽取的一个物种的不确定性[20],一个群落中的物种数越多表示这种不确定性越大,从而群落的多样性水平越高[24]。文章以雷州湾海域的游泳生物为例,对比分析表征群落多样性特征的多样性指数适用情况,建议选用Δ,且Δ*和Λ+二选一即可。1)Δ与H′、J′显著相关(表 3),所表达的信息熵存在重复; 2)Δ包含了系统发生、群落种个体的数量与物种分类地位信息等较H′、J′更加综合地反映群落多样性水平[17-18, 25]。3)Δ*和Λ+显著相关且均反映分类差异的指标,选其一即可。雷州湾海域游泳生物群落的Δ与H′、J′的空间变化趋势相一致,其主要原因在于参数间的皮尔逊相关(表 3),在长江口近岸海域浮游桡足类[18]、鱼类[26]等研究方面均有类似结论。
雷州湾海域游泳生物种类的Δ高于许多近岸海域。主要原因是文章的研究对象包括鱼类、头足类、甲壳类的种类多样性,而不仅仅是鱼类。雷州湾海域Δ*(80.25)、Λ+ (455.37)均高于山东近海[26]、福建台山列岛[27]、大亚湾[28]和东沙群岛[29]海域鱼类群落的各对应参数值。此外,由于雷州湾及附近海域的游泳生物研究文献较少[8-9, 30],有关雷州海域的游泳生物种类总名录尚未能系统整理; 种类总目录的缺少影响了Δ漏斗曲线(funnel plots)的绘制和所研究海域的游泳生物种类的时间序列、区域变化等研究的深入。由于种类总名录在分类多样性研究中主要影响总体的理论均值与置信区间,而对Δ*及置信范围影响极小[18, 25],因此,文章关于游泳生物种类Δ的各参数值均可信。
3.2 种类的重要性排序
物种在群落结构中的作用决定了其重要性,PINKAS等[31]的相对重要性指数(index of relative importance, IRI)在研究游泳生物优势种中应用广泛,它反映了物种的出现频率、质量、丰度三方面信息,在优势种的划分标准选取方面无明确的标准。RAD模型则综合物种的上述三方面信息,定量分析群落中物种的相对重要性。
基于RAD模型的雷州湾游泳生物种类重要性排序表明,Mandelbrot模型的拟合程度最优(AIC值最小)。Mandelbrot方程中β和γ的生态学意义尚未完全证实[32],分形论(fractal theory)认为β与观测的尺度相关,而γ则描述分形的基本属性,与分形的维度相关[20],因为在不同的研究尺度下研究对象的特征会有所不同,而在给定的观测尺度内,其属性则相对稳定。RAD模型中,Preemption模型基于资源利用分化(生态位)假设理论[23],假设群落中竞争力强的种类(如入侵种)在资源利用方面具有较大优势,与其进入该群落的时相无关; 而Lognormal、Zipf和Mandelbrot则是统计类模型,Mandelbrot模型假设一个物种在群落中的丰度取决于其先前条件(即环境和现存物种),这些先前条件决定了一个物种在该群落中生存所要付出或平衡的“成本”。首先到达该群落中的先锋种所需“成本”较低,而随群落演替出现的后续物种则需要付出更多的成本(能量、时间、竞争等)以在群落中获取或扩大自己的生态位。
4个季度的雷州湾游泳生物群落结构表明(图 2),丰度上皮氏叫姑鱼和矛形梭子蟹等占优势(排序分别居第一和第二),而种类组成上甲壳类(虾、蟹)占优势(排序前10种中6种为甲壳类)。需要指出的是,生态模型以简化的方式便于人们理解生态系统的复杂性[23],其可靠程度及其所含理论假设需要长时间的实测数据检测方能验证。初步结论为雷州湾研究流刺网捕捞的游泳生物总体分布较均匀,季节间波动较小,群落中重要种类之间的竞争所需付出的“成本”较大,渔业资源群落结构较稳定。
3.3 CPUE及其影响因子
CPUE是反映游泳生物相对资源量变化和渔业资源评估的重要指标,可从NPUE和BPUE两方面进行分析[33]。1)文章的GLM建模研究发现影响流刺网CPUE的主要环境因子是DO和水温,而调查站位的位置差异、季节变化及网具长度则无显著影响。今后类似研究中,应考虑增加海流作为环境因子,因为海流对刺网在水中捕捞作业时的冲刷会影响水平张开程度。海洋流向与网具长度方向垂直会增加刺网的网具张开程度,而两者方向平行时则相反。2)从渔具材料本身来看,流刺网的CPUE与其网具材料、高度、网目尺寸[34]密切相关。网具材料的可视性如光、扰动及网线颜色会影响刺网的捕捞效果,文章调查中所用的流刺网材料均为锦纶单丝,是当前刺网的主流渔具材料。而刺网的网目尺寸[35]、刺网长度[36]对CPUE的影响会因鱼的种类不同而有所差异,如黄鲈(Perca flavescens)的CPUE不受刺网的网片长度的影响,而白鲈(Morone americana)、灰西鲱(Alosa pseudoharengus)和玻璃梭鲈(Sander vitreus)的CPUE则随网片长度的增加而降低[36]。刺网捕捞的白斑狗鱼(Esox lucius)以春季最多,而冬季最低[37]。此外,流刺网的作业水层、作业时间、渔场水深也会影响CPUE,一些水母、大型藻类或漂浮垃圾若刺挂在刺网网片上[7]会影响刺网网目的捕捞能力。由于刺网的被动式捕捞特点和较高的选择性,在种类区系调查、资源量评估等方面应尽可能与笼壶类渔具[16]或其他渔具渔法(如影像记录调查[38-40]、电渔[6]等)相结合,以提高渔业资源量评估和群落生态学数据的准确性。
致谢: 文章承中国科学院水生生物研究所刘焕章研究员指导,谨此谢忱! -
图 1 9种竹筴鱼属鱼类线粒体DNA控制区序列比较
T.cp1. 南非竹筴英鱼1; Tcp2. 南非竹筴鱼2; T.t1. 竹筴鱼1; Tr2. 竹筴鱼2; Tmp. 智利竹筴鱼; TSy. 太平洋竹筴鱼; Tpc1. 蓝竹筴鱼1; T.pc2. 蓝竹筴鱼2; Tnv. 新西兰竹筴築鱼; Tjp2. 日本竹筴鱼2; Tdc. 青背竹筴鱼; Tjp1. 日本竹筴鱼1; T.md. 地中海竹筴鱼
Figure 1. Sequences of mtDNA control region of 9 species of genus Trachurus fishes
T.cp1.T.capensis1: T.cp2.T.capensis2; T.tr1.T.trachurus1; T.tr2.T.trachurrus2; T.mp.T.murphyi; T.sy.T.symmetricus: T.pc1.T.picturatus1; T.pc2.T.picturatus2; T.nv.T.novaezelandiae; T.jp2.T.japonicus2; T.dc.T.declivis; T.jp1.T.japonicus1; T.md.T.mediterraneus
表 1 竹筴鱼属鱼类数据来源
Table 1 GenBank accession No. of genus Trachurus fishes
种类 species GenBank登录号
GenBank accession No.日本竹筴鱼1(T.japonicus 1) FJ914951 日本竹筴鱼2(T.japonicus 2) FJ914952 竹筴鱼1(T.trachurus 1) AY533482 竹筴鱼2(T.trachurus 2) AY534483 蓝竹筴鱼1(T.picturatus 1) AY533477 蓝竹筴鱼2(T.picturatus 2) EU246459 智利竹筴鱼(T.murphyi) AY532713 南非竹筴鱼1(T.capensis 1) AY533480 南非竹筴鱼2(T.capensis 2) AY533481 青背竹筴鱼(T.declivis) AY533476 新西兰竹筴鱼(T.novaezelandiae) AY533475 太平洋竹筴鱼(T.symmetricus) AY532701 表 2 竹筴鱼属鱼类控制区序列碱基组成
Table 2 Nucleotide composition of sequence of mtDNA control region in genus Trachurus fishes
种
species终止序列区
termination associated sequence domain中央保守区
central conserved domainT C A G length T C A G length 南非竹筴鱼1(T.capensis 1) 30.5 20.5 37.0 12.0 292 31.6 20.6 26.4 21.4 364 南非竹筴鱼2(T.capensis 2) 30.5 20.9 36.6 12.0 292 31.6 20.9 26.1 21.4 364 竹筴鱼1(T.trachurus 1) 30.8 20.2 36.6 12.3 292 31.3 20.9 26.4 21.4 364 竹筴鱼2(T.trachurus 2) 31.2 19.9 36.6 12.3 292 31.0 21.2 26.4 21.4 364 智利竹筴鱼(T.murphyi) 31.2 19.5 37.3 12.0 292 30.5 21.2 26.6 21.7 364 太平洋竹筴鱼(T.symmetricus) 30.5 20.2 37.7 11.6 292 29.9 21.7 26.6 21.7 364 蓝竹筴鱼1(T.picturatus 1) 30.5 19.5 38.4 11.6 292 30.8 20.9 26.1 22.3 364 蓝竹筴鱼2(T.picturatus 2) 32.9 18.8 37.7 10.6 292 30.8 20.9 26.1 22.3 364 新西兰竹筴鱼(T.novaezelandiae) 29.8 21.2 37.3 11.6 292 31.0 21.2 26.6 21.2 364 日本竹筴鱼2(T.japonicus 2) 31.5 20.2 36.0 12.3 292 31.3 21.2 26.1 21.4 364 青背竹筴鱼(T.declivis) 32.2 19.9 37.3 10.6 292 31.0 21.2 25.8 22.0 364 日本竹筴鱼1(T. japonicus 1) 32.2 19.9 37.0 11.0 292 30.8 21.4 25.8 22.0 364 地中海竹筴鱼(T.mediterraneus) 31.3 20.3 38.1 10.3 292 30.8 21.2 26.4 21.7 364 平均 average 31.1 20.1 37.2 11.6 291.9 31.0 21.1 26.3 21.7 364 种
species终止序列区
termination associated sequence domain整个控制区
whole control regionT C A G length T C A G length 南非竹筴鱼1(T.capensis 1) 31.4 28.1 29.7 10.8 185 31.0 21.9 31.2 15.9 862 南非竹筴鱼2(T.capensis 2) 31.4 28.1 29.7 10.8 185 31.0 22.2 31.0 15.9 862 竹筴鱼1(T.trachurus 1) 31.4 28.1 29.7 10.8 185 31.0 21.9 31.1 16.0 862 竹筴鱼2(T.trachurus 2) 31.4 28.1 29.7 10.8 185 31.0 21.9 31.1 16.0 862 智利竹筴鱼(T.murphyi) 30.3 28.6 29.7 11.4 185 30.7 21.7 31.4 16.1 862 太平洋竹筴鱼(T.symmetricus) 31.4 27.6 29.7 11.4 185 30.1 22.1 31.6 16.2 857 蓝竹筴鱼1(T.picturatus 1) 31.4 27.6 29.7 11.4 185 30.6 21.8 31.3 16.2 862 蓝竹筴鱼2(T.picturatus 2) 31.4 27.6 30.3 10.8 185 30.4 22.2 31.3 16.1 862 新西兰竹筴鱼(T.novaezelandiae) 31.4 27.6 30.3 10.8 180 31.2 21.9 31.4 15.4 862 日本竹筴鱼2(T.japonicus 2) 30.8 28.1 29.7 11.4 186 31.1 22.0 31.3 15.5 862 青背竹筴鱼(T.declivis) 30.6 28.4 29.0 12.0 185 31.3 21.7 31.2 15.8 862 日本竹筴鱼1(T.japonicus 1) 30.6 28.3 28.9 12.2 183 31.0 22.1 30.8 16.0 860 地中海竹筴鱼(T.mediterraneus) 31.2 28.0 29.0 11.8 185 31.0 21.9 31.0 16.1 862 平均 average 31.1 28.0 29.6 11.3 184.5 30.9 21.9 31.2 16.0 861.5 -
[1] 伍汉霖, 邵广昭, 赖春福. 拉汉世界鱼类名典[M]. 基隆: 水产出版社, 1999. https://xueshu.baidu.com/usercenter/paper/show?paperid=d1a399a58f751d887b00f7e32bc1d765&site=xueshu_se WU Hanlin, SHAO Guangzhao, LAI Chunfu. Latin-Chinese dictionary of fishes names[M]. Keelung : The Suei Chan Press, 1999. (in Chinese) https://xueshu.baidu.com/usercenter/paper/show?paperid=d1a399a58f751d887b00f7e32bc1d765&site=xueshu_se
[2] 中国科学院动物研究所, 中国科学学院海洋研究所, 上海水产学院. 南海鱼类志[M]. 北京: 科学出版社, 1962: 213-421. Institute of Zoology, Chinese Academy of Science, Institute of Oceanology, Chinese Academy of Sciences, Shanghai Fisheries University. Fish fauna of the South China Sea[M]. Beijing: Science Press, 1962: 213-421. (in Chinese)
[3] 郭新红, 刘少军, 刘巧, 等. 鱼类线粒体研究新进展[J]. 遗传学报, 2004, 31(9): 983-1000. https://xueshu.baidu.com/usercenter/paper/show?paperid=25713e1ff4e884760e4e4364b31966b8&site=xueshu_se&hitarticle=1 GUO Xinhong, LIU Shaojun, LIU Qiao, et al. New progresses on mitochondrial DNA in fish[J]. Acta Genetica Sinica, 2004, 31(9): 983-1000. (in Chinese) https://xueshu.baidu.com/usercenter/paper/show?paperid=25713e1ff4e884760e4e4364b31966b8&site=xueshu_se&hitarticle=1
[4] 刘焕章. 鱼类线粒体DNA控制区的结构与进化: 以鳑鲏鱼类为例[J]. 自然科学进展, 2002, 12(3): 266-270. doi: 10.3321/j.issn:1002-008X.2002.03.008 LIU Huanzhang. Structure and evolution of mitochondrial DNA control region in fish: Take Rhodeus ocellatus as an example[J]. Progr Nat Sci, 2002, 12(3): 266-270. (in Chinese) doi: 10.3321/j.issn:1002-008X.2002.03.008
[5] 曾青兰, 刘焕章. 大口胭脂鱼线粒体DNA控制区序列的研究[J]. 湖北大学学报: 自然科学版, 2001, 23(3): 261-264. doi: 10.3969/j.issn.1000-2375.2001.03.021 ZENG Qinglan, LIU Huanzhang. Study on mitochondrial DNA control region of the Ictiobus cyprinellus[J]. J Hubei Univ: Natural Science, 2001, 23(3): 261-264. (in Chinese) doi: 10.3969/j.issn.1000-2375.2001.03.021
[6] 郑冰蓉, 张亚平, 肖蘅, 等. 鲤属鱼类mtDNA控制区序列的变异性分析[J]. 水产学报, 2002, 26(4): 289-294. ZHENG Bingrong, ZHANG Yaping, XIAO Heng, et al. The sequence variation feature of mtDNA D-loop region of Cyprinus[J]. J Fish China, 2002, 26(4): 289-294. (in Chinese)
[7] 张燕, 张鹗, 何舜平. 中国鲿科鱼类线粒体DNA控制区结构及其系统发育分析[J]. 水生生物学报, 2003, 27(5): 463-467. doi: 10.3321/j.issn:1000-3207.2003.05.004 ZHANG Yan, ZHANG E, HE Shunping. Studies on the structure of the control region of the Bagridae in China and its phylogenetic significance[J]. Acta Hydrobiological Sinica, 2003, 27(5): 463-467. (in Chinese) doi: 10.3321/j.issn:1000-3207.2003.05.004
[8] 赫崇波, 高祥刚, 王效敏, 等. 圆斑星鲽线粒体基因组全序列结构及其进化[J]. 中国水产科学, 2007, 14(4): 584-592. doi: 10.3321/j.issn:1005-8737.2007.04.009 HE Chongbo, GAO Xianggang, WANG Xiaomin, et al. Structure and evolution of complete mitochondrial genome of spotted halibut Verasper variegatus[J]. J Fish Sci China, 2007, 14(4): 584-592. (in Chinese) doi: 10.3321/j.issn:1005-8737.2007.04.009
[9] 诸廷俊, 杨金权, 唐文乔. 长江口鲚属鱼类线粒体DNA控制区结构分析[J]. 上海水产大学学报, 2008, 17(2): 152-157. https://xueshu.baidu.com/usercenter/paper/show?paperid=b55fe9a1202052c0c326f8d6a472e79b&site=xueshu_se&hitarticle=1 ZHU Tingjun, YANG Jinquan, TANG Wenqiao. MtDNA control region sequence structure of the genus Coilia in Yangtze River estuary[J]. J Shanghai Fish Univ, 2008, 17(2): 152-157. (in Chinese) https://xueshu.baidu.com/usercenter/paper/show?paperid=b55fe9a1202052c0c326f8d6a472e79b&site=xueshu_se&hitarticle=1
[10] 邵爱华, 朱江, 史全良. 暗纹东方鲀线粒体DNA控制区结构和系统发育分析[J]. 中国水产科学, 2007, 14(3): 352-360. doi: 10.3321/j.issn:1005-8737.2007.03.002 SHAO Aihua, ZHU Jiang, SHI Quanliang, et al. Characterization and phylogenetic analysis of control region of mitochondrial genome from Takifugu fasciatus[J]. J Fish Sci China, 2007, 14(3): 352-360. (in Chinese) doi: 10.3321/j.issn:1005-8737.2007.03.002
[11] 赵金良, 王伟伟, 李思发, 等. 鳜类鱼类的线粒体DNA控制区结构及其系统发育分析[J]. 遗传学报, 2006, 33(9): 793-799. https://xueshu.baidu.com/usercenter/paper/show?paperid=73ea5ac23d7b1bfa03e86298d133066b&site=xueshu_se&hitarticle=1 ZHAO Jinliang, WANG Weiwei, LI Sifa, et al. Structure of the mitochondrial DNA control region of the Sinipercine fishes and their phylogenetic relationship[J]. Acta Genetica Sinica, 2006, 33(9): 793-799. (in Chinese) https://xueshu.baidu.com/usercenter/paper/show?paperid=73ea5ac23d7b1bfa03e86298d133066b&site=xueshu_se&hitarticle=1
[12] 朱世华, 郑文娟, 邹记兴, 等. 鲹科鱼类线粒体DNA控制区结构及系统发育关系[J]. 动物学研究, 2007, 28(6): 606-614. doi: 10.3321/j.issn:0254-5853.2007.06.005 ZHU Shihua, ZHENG Wenjuan, ZOU Jixing, et al. Mitochondrial DNA control region structure and molecular phylogenetic relationship of Carangidae[J]. Zool Res, 2007, 28(6): 606-614. (in Chinese) doi: 10.3321/j.issn:0254-5853.2007.06.005
[13] CÁRDENAS L, HERNÁNDEZ C E, POULIN E, et al. Origin, diversification, and historical biogeography of the genus Trachurus (Perciformes: Carangidae)[J]. Mol Phylogenet Evol, 2005, 35(2): 496-507. doi: 10.1016/j.ympev.2005.01.011
[14] THOMPSON J D, GIBSON T J, PLEWNIAK F, et al. The CLUSTAL_X windows interface: flexible strategies for multiple sequence alignment aided by quality analysis tools[J]. Nucleic Acids Res, 1997, 25(24): 4876-82. doi: 10.1093/nar/25.24.4876
[15] TAMURA K, DUDLEY J, NEI M, et al. MEGA 4: Molecular Evolutionary Genetics Analysis (MEGA) software version 4.0[J]. Mol Biol Evol, 2007, 24(8): 1596-1599. doi: 10.1093/molbev/msm092
[16] ROZAS J, SANCHEZ-DELBARRIO J C, MESSEGUER X, et al. DnaSP, DNA polymorphism analyses by the coalescent and other methods[J]. Bioinformatics, 2003, 19(18): 2496-2497. doi: 10.1093/bioinformatics/btg359
[17] 杨路存, 陈桂琛, 刘荣堂, 等. 3种鼢鼠线粒体DNA控制区结构及其系统发育分析[J]. 草业科学, 2009, 26(2): 100-106. https://xueshu.baidu.com/usercenter/paper/show?paperid=dbc3653adead7c5b73f9317d39025d66&site=xueshu_se YANG Lucun, CHEN Guichen, LIU Rongtang, et al. Studies on the structure of the mitochondrial DNA control region and phylogenetic relationships of 3 zokor species[J]. Pratac Sci, 2009, 26(2): 100-106. (in Chinese) https://xueshu.baidu.com/usercenter/paper/show?paperid=dbc3653adead7c5b73f9317d39025d66&site=xueshu_se
[18] WOLSTENHOLME D R. Animal mitochondrial DNA: structure and evolution[M]//WOLSTENHOLME D R, JEON K W. Mitochondrial Genomes. San Diego: Academic Press, 2006: 173-372.
[19] LEE W J, CONROY J, HOWELL W H. Structure and evolution of teleost mitochondrial control regions[J]. J Mol Evol, 1995, 41(1): 54-66. doi: 10.1007/BF00174041
[20] SBISA E, TANZARIELLO F, REYES A, et al. Mammalian mitochondrial D-loop region structural analysis: identification of new conserved sequences and their functional and evolutionary implications[J]. Gene, 1997, 205(1/2): 125-140. doi: 10.1016/S0378-1119(97)00404-6
-
期刊类型引用(1)
1. 陈晓婷,吴雨璇,刘淑集,潘南,许旻,苏永昌,张玉苍,刘智禹. 空气炸鲨鱼皮工艺条件的优化. 渔业研究. 2024(03): 260-270 .  百度学术
百度学术
其他类型引用(2)




 下载:
下载:


 粤公网安备 44010502001741号
粤公网安备 44010502001741号
