Study on annual development of hermaphroditic gland of Onchidium struma
-
摘要:
研究了江、浙、沪地区瘤背石磺(Onchidium struma)两性腺周年发育规律。结果显示,瘤背石磺雌雄同体,雄性先熟,生物学最小型为体长2.81 cm,体质量1.81 g。其两性腺发育为1年1个周期,发育经历增殖期、精子发生期、精卵同步发生期、排放期和休止期。其中排放期又分精子排放、精卵排放和卵子排放,体现了精卵发生的异时性。精子的发生包括精原细胞、初级精母细胞、次级精母细胞、精子细胞和精子;卵子的发生包括卵原细胞期、无卵黄期、卵黄形成期、卵黄形成后期和成熟期。成熟系数周年呈明显单峰分布,峰值出现在7~9月间;蛋白腺系数、卵黄腺系数与成熟系数具有一定的相关性,蛋白腺系数基本随着成熟系数变化而变化,卵黄腺系数随着成熟系数变化的过程中出现3个峰值,分别在6、8和12月。
Abstract:We investigated the annual developmental rule of hermaphroditic gland of Onchidium struma from Jiangsu, Zhejiang and Shanghai. The results indicate that O.struma is a hermaphrodite, which often becomes a functional male before its female organs develop. The smallest individual is 2.81 cm in length and 1.81 g in weight. The development of hermaphroditic gland has a cycle per year, which is divided into proliferation, spermatogenesis, synchronous occurence of ova and sperm, exporting and resting stages. Specifically, exporting stage is divided into sperm exporting, simultaneous exporting of ova and sperm, and ova exporting, indicating a heterochrony of spermatogenesis and oogenesis. The male reproductive cells have spermatogonia, primary spermatocyte, secondary spermatocyte, spermatid and sperm. The female ones have oogonium, previtellogenic oocyte, vitellogenic oocyte, postvitellogenic oocyte and maturation. The annual change of gonadosomatic index (GSI) shows a unimodal distribution whose peak value occurs during July and September. The albumin gland index (AI) and vitelline gland index (VI) are correlated with GSI. AI changes along with GSI and has three peak values during GSI′s change, which occur in June, August and December, respectively.
-
Keywords:
- Onchidium struma /
- hermaphroditic gland /
- annual development /
- GSI
-
瘤背石磺(Onchidium struma)系软体动物门(Mollusca)、腹足纲(Gastropoda)、肺螺亚纲(Pulmonata)、柄眼目(Stylommatophora)、石磺科(Onchidiidae),分布于中国江苏、上海和浙江沿海滩涂,与福建以南产石磺在形态上存在着明显差异[1]。有关瘤背石磺性腺发育规律及周年变化的研究尚未见报道,国内王金庆等[2]仅局限于对6~7月的性腺情况做过描述。国外工作集中在O.verruculatum,DESHPANDE和NAGABHUSHANAM[3]对其滤泡组织发育进行了分期。目前,对瘤背石磺的生物学特性及增养殖前景[4]、饲料[5]、生理生态[6-9]和胚胎发育[10-12]已有较为深入的研究,但缺乏周年发育规律的研究报道,迄今国内外也未见瘤背石磺生殖细胞发生过程各阶段的基础数据研究。文章通过室内、室外仿生态饲养试验,运用组织学切片技术,结合每月实地调查、采样、观察江、浙、沪地区瘤背石磺群体的繁殖行为等方法,研究了瘤背石磺周年发育变化规律,初步分析了两性腺发育过程中两性腺成熟系数的变化情况,弥补了瘤背石磺繁殖生物学基础资料的不足,以期为人工繁育工作的开展及其资源的可持续利用提供参考依据。
1. 材料与方法
1.1 取材、试验地点及饲养方法
试验用瘤背石磺分别采自上海崇明(121°51′E,31°35′N)、浙江慈溪(121°23′E,30°18′N)。基于便于及时取样观察性腺发育的考虑,仿照野外生境,用上口长62 cm,宽44 cm,下口长58 cm,宽38 cm,高36 cm蓝色塑料箱设置生态箱在室内暂养部分样品;箱底铺5 cm厚泥土,箱内适量栽种大米草(Spartina anglica)等植物,箱壁搭建瓦片,供瘤背石磺遮阴躲藏,上扎纱网防逃。采用沈和定等[5]的试验结果,每天傍晚定时定点在瘤背石磺集中处附近直接喷洒玉米粉。由于水分蒸发,须定期检查并及时添加淡水,始终保持箱内的湿度。
1.2 野外观察及成体越冬试验
分别于2006~2009年越冬后及时做野外调查,发现有瘤背石磺出没即采样至实验室生态箱内,并取部分样品用Bouin′s液固定。同时,在瘤背石磺越冬之前,野外采样以保证实验室有一定数量的瘤背石磺进行越冬试验。
1.3 性腺发育过程中相关指标的测定
取周年发育各阶段瘤背石磺,在实验室内解剖,用滤纸吸水、称质量。成熟系数(GSI)=两性腺质量/去内脏体质量,蛋白腺系数(AI)=蛋白腺质量/去内脏体质量,卵黄腺系数(VI)=卵黄腺质量/去内脏体质量。
1.4 各发育阶段样品制备及观察
每月从野外采回的样品中随机选取30只瘤背石磺,解剖观察其性腺发育情况;同时随时从室内生态箱中取样解剖观察。解剖观察后均迅速分离出性腺,根据性腺大小将其切成小段,用Bouin′s液固定,按照常规程序脱水、透明和石蜡包埋(56~58 ℃)、切片(厚度5~7 μm)、用苏木精和体积分数是0.5%的伊红酒精溶液染色(H.E.);用Olympus BH-12显微镜作显微摄影并测量生殖细胞直径(精确到0.01 μm)。
1.5 数据处理
试验数据用SPSS 16.0统计软件处理。
2. 结果与分析
2.1 两性腺的形态、发育及精卵发生
瘤背石磺为雌雄同体、异体受精种类。雌、雄生殖腺着生在一起,且无明显区分,同一滤泡内既能产生卵子,又能产生精子,故称为两性腺(图 1)。两性腺位于瘤背石磺腹腔后部,靠近肛门腺,与卵黄腺、蛋白腺包绕在一起。越冬及越冬结束时两性腺萎缩暗淡,与周围的卵黄腺和蛋白腺混在一起不可辨;发育初期的两性腺呈淡黄色,无光泽;成熟时黄色发亮,除去外面包被,可见饱满粉状颗粒,此即是滤泡。解剖观察,瘤背石磺的两性腺基部向外伸出1个两性管,此管向两性腺内,则分成3个分支,各自连接1个性腺区域。每个分支在它连接区域的基部又分成更细的分支,以此类推,直至两性管分布到滤泡周围,整个两性腺结构组成似葡萄串状。
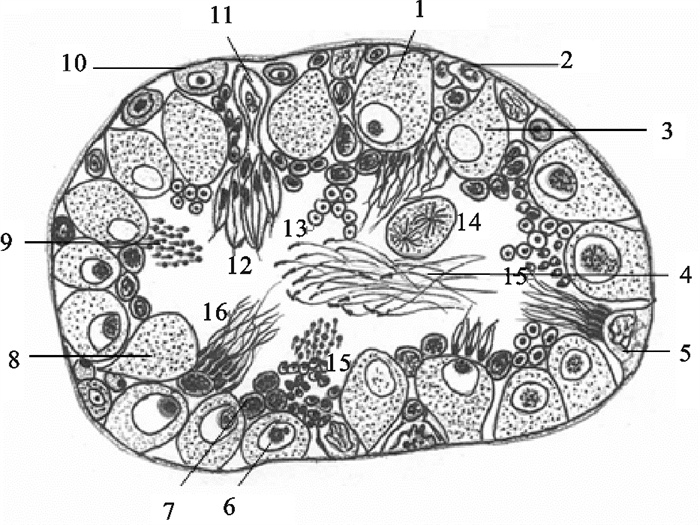
![]() 图 1 瘤背石磺生殖细胞发生模式图1. 卵黄合成卵母细胞;2. 精原细胞;3. 卵黄合成后卵母细胞中期;4. 精子;5. 支持细胞;6. 无卵黄卵母细胞,双质核仁;7. 初级精母细胞;8. 卵黄合成后卵母细胞后期;9. 精子细胞;10. 卵原细胞;11. 支持细胞;12. 变形精子;13. 次级精母细胞;14. 减数分裂;15. 精子细胞早期;16. 精子细胞后期Figure 1. Miniature diagram of cytogenesis in hermaphroditic gland of O.struma1. vitellogenic oocyte; 2. spermatogonium; 3. metaphase of postvitellogenic oocyte; 4. spermatozoon; 5. supporting cell; 6. previtellogenic oocyte, amphinucleous; 7. primary spermatocyte; 8. anaphase of postvitellogenic oocyte; 9. spermatid; 10. oogonium; 11. supporting cell; 12. forming spermatozoon; 13. secondary spermatocyte; 14. miosis; 15. prophase of spermatid; 16. anaphase of spermatid
图 1 瘤背石磺生殖细胞发生模式图1. 卵黄合成卵母细胞;2. 精原细胞;3. 卵黄合成后卵母细胞中期;4. 精子;5. 支持细胞;6. 无卵黄卵母细胞,双质核仁;7. 初级精母细胞;8. 卵黄合成后卵母细胞后期;9. 精子细胞;10. 卵原细胞;11. 支持细胞;12. 变形精子;13. 次级精母细胞;14. 减数分裂;15. 精子细胞早期;16. 精子细胞后期Figure 1. Miniature diagram of cytogenesis in hermaphroditic gland of O.struma1. vitellogenic oocyte; 2. spermatogonium; 3. metaphase of postvitellogenic oocyte; 4. spermatozoon; 5. supporting cell; 6. previtellogenic oocyte, amphinucleous; 7. primary spermatocyte; 8. anaphase of postvitellogenic oocyte; 9. spermatid; 10. oogonium; 11. supporting cell; 12. forming spermatozoon; 13. secondary spermatocyte; 14. miosis; 15. prophase of spermatid; 16. anaphase of spermatid2.1.1 两性腺发育分期
根据瘤背石磺两性腺发育的特殊情况,可将其分为增殖期、精子发生期、精卵同步发生期、排放期和休止期。
增殖期。两性腺随着气温的上升开始发育,气温超过20 ℃瘤背石磺即钻出越冬的洞穴,恢复正常身体机能。至3月中下旬,两性腺已含有丰富的结缔组织,生殖上皮随结缔组织内伸。滤泡开始沿着发达的结缔组织逐渐形成,滤泡大小不等,数量由少到多,形状不规则(图版-1)。
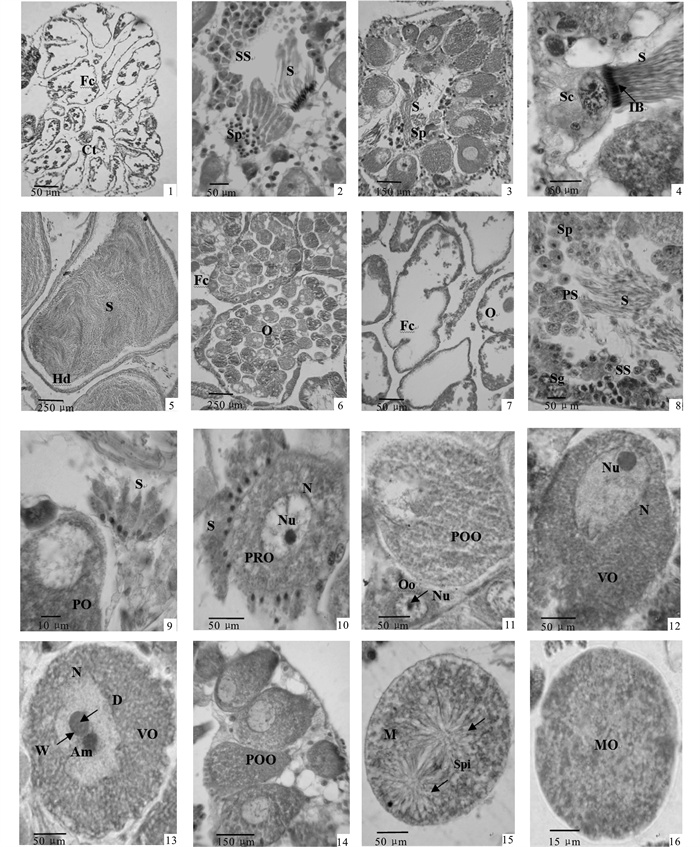
![]() 图版I 瘤背石磺两性腺周年发育的组织学观察1. 增值期×90,示大小不一滤泡,结缔组织;2. 精子发生期×360,示次级精母细胞,精子细胞;3. 精卵同步发生期×180,示各级生殖细胞;4. 滤泡×900,示支持细胞,变形晚期精子,间桥;5. 两性管×90,示成熟精子;6. 排放期×90,示滤泡中成熟卵子的集中排放,滤泡壁上卵母细胞;7. 排空滤泡×90,示残留的精卵细胞;8. 精子发生期×360,示各级生殖细胞;9. 滤泡×360,示变形中期精子,卵黄合成后期卵母细胞;10. 滤泡×360,示变形中期精子,无卵黄合成卵母细胞;11. 卵原细胞和卵黄合成后期卵母细胞×360;12. 卵黄合成期×360,示核偏位、变形精子;13. 双质核仁×360,示浅色↗,深色↙;14. 卵黄合成后期×180,示本期早期、晚期卵母细胞;15. 卵黄合成后期×360,示本期晚期有丝分裂卵母细胞,纺锤体;16. 成熟卵子×360;Sg. 精原细胞;PS. 初级精母细胞;SS. 次级精母细胞;Sp. 精子细胞;S. 精子;Oo. 卵原细胞;PRO. 无卵黄生成卵母细胞;VO. 卵黄生成卵母细胞;POO. 卵黄生成后卵母细胞;MO. 成熟卵子;N. 细胞核;Nu. 核仁;Am. 双质核仁;M. 减数分裂;Spi. 纺锤体图版I. Histological observation of annual development of hermaphroditic gland of O. struma1.proliferation×90, showing follicle cell (Fc), connective tissue(Ct); 2.spermatogenesis×360, showing secondary spermatocyte, spermatid; 3.ova and sperm in phase×180, showing germ cells at different stage of development; 4.follicle cell×900, showing supporting cell (Sc), spermatozoon at forming telophase, intercellular bridges(IB); 5.hermaphroditic duct (Hd)×90, showing mature spermatozoon; 6.exporting stage×90, showing follicle filled with exporting mature ova, oocyte on follicle wall; 7.resting follicle×90, showing rudimental germ cells; 8.spermatogenesis×360, showing germ cells at different stage of development; 9.follicle cell×360, showing spermatozoon at forming metaphase, postvitellogenic oocyte; 10.follicle cell×360, showing spermatozoon at forming metaphase, previtellogenic oocyte; 11.oogonium and postvitellogenic oocyte×360;12.vitellogenic stage×360, showing migrated nucleus, forming spermatozoon; 13.amphinucleous×360, showing weakly dyed part (W)↗, deeply dyed part(D)↙; 14.postvitellogenic stage×180, showing prophase and anaphase of oocyte at the stage; 15.postvitellogenic stage×360, showing mitosis at telophaseof oocyte, spindle; 16.mature ova×360;Sg.spermatogonium; PS.primary spermatocyte; SS.secondary spermatocyte; Sp.spermatid; S.spermatozoon; Oo.oogonium, PRO.previtellogenic oocyte; VO.vitellogenic oocyte; POO.postvitellogenic oocyte; MO.mature ova; N.nucleus; Nu.nucleolus; Am.amphinucleous; M.miosis; Spi.spindle
图版I 瘤背石磺两性腺周年发育的组织学观察1. 增值期×90,示大小不一滤泡,结缔组织;2. 精子发生期×360,示次级精母细胞,精子细胞;3. 精卵同步发生期×180,示各级生殖细胞;4. 滤泡×900,示支持细胞,变形晚期精子,间桥;5. 两性管×90,示成熟精子;6. 排放期×90,示滤泡中成熟卵子的集中排放,滤泡壁上卵母细胞;7. 排空滤泡×90,示残留的精卵细胞;8. 精子发生期×360,示各级生殖细胞;9. 滤泡×360,示变形中期精子,卵黄合成后期卵母细胞;10. 滤泡×360,示变形中期精子,无卵黄合成卵母细胞;11. 卵原细胞和卵黄合成后期卵母细胞×360;12. 卵黄合成期×360,示核偏位、变形精子;13. 双质核仁×360,示浅色↗,深色↙;14. 卵黄合成后期×180,示本期早期、晚期卵母细胞;15. 卵黄合成后期×360,示本期晚期有丝分裂卵母细胞,纺锤体;16. 成熟卵子×360;Sg. 精原细胞;PS. 初级精母细胞;SS. 次级精母细胞;Sp. 精子细胞;S. 精子;Oo. 卵原细胞;PRO. 无卵黄生成卵母细胞;VO. 卵黄生成卵母细胞;POO. 卵黄生成后卵母细胞;MO. 成熟卵子;N. 细胞核;Nu. 核仁;Am. 双质核仁;M. 减数分裂;Spi. 纺锤体图版I. Histological observation of annual development of hermaphroditic gland of O. struma1.proliferation×90, showing follicle cell (Fc), connective tissue(Ct); 2.spermatogenesis×360, showing secondary spermatocyte, spermatid; 3.ova and sperm in phase×180, showing germ cells at different stage of development; 4.follicle cell×900, showing supporting cell (Sc), spermatozoon at forming telophase, intercellular bridges(IB); 5.hermaphroditic duct (Hd)×90, showing mature spermatozoon; 6.exporting stage×90, showing follicle filled with exporting mature ova, oocyte on follicle wall; 7.resting follicle×90, showing rudimental germ cells; 8.spermatogenesis×360, showing germ cells at different stage of development; 9.follicle cell×360, showing spermatozoon at forming metaphase, postvitellogenic oocyte; 10.follicle cell×360, showing spermatozoon at forming metaphase, previtellogenic oocyte; 11.oogonium and postvitellogenic oocyte×360;12.vitellogenic stage×360, showing migrated nucleus, forming spermatozoon; 13.amphinucleous×360, showing weakly dyed part (W)↗, deeply dyed part(D)↙; 14.postvitellogenic stage×180, showing prophase and anaphase of oocyte at the stage; 15.postvitellogenic stage×360, showing mitosis at telophaseof oocyte, spindle; 16.mature ova×360;Sg.spermatogonium; PS.primary spermatocyte; SS.secondary spermatocyte; Sp.spermatid; S.spermatozoon; Oo.oogonium, PRO.previtellogenic oocyte; VO.vitellogenic oocyte; POO.postvitellogenic oocyte; MO.mature ova; N.nucleus; Nu.nucleolus; Am.amphinucleous; M.miosis; Spi.spindle精子发生期。瘤背石磺的两性腺为雄性先熟,滤泡中精原细胞不断分裂增殖,使滤泡壁上精原细胞排列密集,较早掉入滤泡腔内的精原细胞发育成精母细胞,很快又分裂产生精细胞。4月中旬前后,可见从滤泡壁向滤泡腔内分布有发育不同步的各期精细胞(图版-2),同时滤泡内的生殖细胞已从原来的单层成为多层排列呈漩涡状或放射状。
精卵同步发生期。大约在4月下旬至6月初,此期滤泡为全周期最丰满,滤泡壁和滤泡腔内充满各种生殖细胞,因此,腔内很少有空隙。沿着滤泡壁大量分布着卵原细胞和卵黄形成期细胞(图版-3),各级精子细胞夹杂其间。由于分裂过快,可以看到很多精细胞粘联在一起,成细胞团,彼此间以细胞间桥相连(图版-2,4)。
排放期。此期根据两性腺发育的特点又可分为精子排放、精卵排放和卵子排放。在精子发生期即有精子排放,此时不仅表现在滤泡腔充满成熟精子,而且邻近的两性管内亦充盈精子,H.E.染色,精子头部着色很深,尾部相互缠绕,成精子束状,后组成精子流,由两性管向外输送(图版-5)。精卵同步发生期时,成熟的精卵各自排放入腔内,但此期主要是精子排放。研究发现,成熟卵子有个集中排放期,滤泡内充满成熟卵子。由于成熟卵数量多,在腔内相互挤压,致使卵子的形态成不规则状,有梨形、椭圆形和多边形等多种形态(图版-6)。该期主要发生在6月中下旬至9月。
休止期。是紧接着排放期后的一个时期。滤泡由于成熟生殖细胞的相继排放而变成大空腔,滤泡稀疏,形状不规则,滤泡腔或空虚,或残留少量精卵细胞(图版-7)。接着滤泡数减少并萎缩,消失的滤泡被网状结缔组织替代,生殖腺处于一个相对静止时期,一般在10月之后至翌年2月。
2.1.2 精子发生
精子细胞发生的全过程在滤泡腔内进行,从原始生殖细胞到成熟精子,要经过滤泡的增殖期生长期,精细胞的成熟期变态期,一般可以分为5期。
精原细胞。精原细胞与滤泡壁紧密相连,细胞接近圆形,染色较浅,细胞直径(27.27±5.33)×(25.33±5.17)μm,核径(22.45±3.59)×(19.88±2.57)μm(图版-8,表 1)。
表 1 瘤背石磺精子细胞各期情况Table 1. Data of O.struma spermatozoa at different stages雄性生殖细胞的发育阶段spermatogenesis stages 细胞直径/μm cell diameter 核径/μm nucleus diameter 长径long diameter 短径short diameter 长径long diameter 短径short diameter 精原细胞spermatogonium 27.27±5.33 25.33±5.17 22.45±3.59 19.88±2.57 初级精母细胞primary spermatocyte 47.62±4.52 40.39±3.51 30.89±1.45 27.42±2.61 次级精母细胞secondary spermatocyte 31.43±2.33 29.09±2.20 17.53±2.02 15.35±2.28 精子细胞spermatid 10.59±3.13 8.76±2.59 - - 精子spermatozoon 全长450 μm 初级精母细胞。初级精母细胞位于精原细胞靠近滤泡腔的一方,染色加深,直径(47.62±4.52)×(40.39±3.51)μm,核径(30.89±1.45)×(27.42±2.61)μm(图版-8,表 1)。
次级精母细胞。该期的精细胞与初级精母细胞临近,直径(31.43±2.33)×(29.09±2.20)μm,核径(17.53±2.02)×(15.35±2.28)μm,细胞核染色较深,细胞质呈透明状(图版-2,8;表 1)。次级精母细胞一般分裂较快,存在的时间很短。
精子细胞。精子细胞早期染色较深,核渐趋浓缩,细胞直径(27.18±4.88)×(25.02±4.49)μm,核直径(8.11±0.92)×(6.66±1.12)μm。后期核质不清,染色进一步加深,整个精子细胞直径(10.59±3.13)×(8.76±2.59)μm,此期可在滤泡中看到处于变形的精子细胞,把多余的细胞质舍弃,已可见精子尾部雏形(图版-9,表 1)。石蜡切片还发现,此期细胞还有环绕在卵母细胞、把头部埋于卵母细胞的正在变形的精子细胞(图版-10)。
精子。精子全长450 μm左右,在滤泡腔中或两性管腔中聚集成束,头部朝向滤泡壁,尾部朝向游离面(图版-4,表 1)。
2.1.3 卵子发生
瘤背石磺卵细胞的发生可以分为以下5期。
卵原细胞期。卵原细胞多为圆形,少数为椭圆形,紧贴滤泡上皮,直径(99.25±17.12)×(73.56±14.04)μm,细胞内位于中央有一透亮的核,核径(54.75±7.95)×(42.79±7.40)μm,核内有核仁1个,直径(19.60±2.87)×(17.47±2.69)μm(图版-11,表 2)。
表 2 瘤背石磺卵子发生中卵母细胞情况Table 2. Data of O.struma oocyte in oogenesis卵子发生分期oogenesis stages 核仁/μm nucleolus 核/μm nucleus 卵径/μm ovum diameter 核质比* nucleocytoplasmic ratio 长径long diameter 短径short diameter 长径long diameter 短径short diameter 长径long diameter 短径short diameter 卵原细胞oogonium 19.60±2.87 17.47±2.69 54.75±7.95 42.79±7.40 99.25±17.12 73.56±14.04 0.24±0.07 无卵黄形成previtellogenic oocyte 28.65±2.94 25.47±2.64 85.80±10.40 65.11±10.97 174.36±20.32 131.08±16.51 0.15±0.05 卵黄形成期vitellogenic oocyte 31.63±5.20 26.31±3.56 117.29±11.34 89.47±7.86 274.19±18.12 191.28±14.21 0.10±0.02 卵黄形成后期postvitellogenic oocyte - - 96.03±17.30 73.87±9.07 290.07±32.81 192.72±35.31 < 0.06±0.03 成熟卵子maturation - - - - 236.53±20.47 175.80±11.26 - 注:*. 核质比=细胞核体积/ (细胞体积-细胞核体积);体积=0.523长径2×短径[13]
Note:*. nucleocytoplasmic ratio = nucleus volume/(cell volume nucleus volume); volume=0.523 long diameter 2×short diameter[13]无卵黄期。此期主要特点表现为细胞大小较卵原细胞期显著增长,直径(174.36±20.32)×(131.08±16.51)μm,核径(85.80±10.40)×(65.11±10.97)μm,核内有核仁1个,直径(28.65±2.94)×(25.47±2.64)μm(图版-10,表 2)。
卵黄形成期。卵母细胞进一步向滤泡腔中突出,其游离端变得较宽,而与滤泡壁相连的那端变得较窄,形成不很明显的卵柄,有脱离滤泡壁的趋势,其核内有核仁1个。在靠近滤泡壁的一端,卵母细胞的细胞质开始出现卵黄,但分布不均匀,此时卵母细胞大小(274.19±18.12)×(191.28±14.21)μm,核径(117.29±11.34)×(89.47±7.86)μm,核仁(31.63±5.20)×(26.31±3.56)μm(图版-12)。研究还发现双质核仁现象(图版-13)。
卵黄形成后期。与滤泡壁连接的卵柄愈加明显,有不少卵母细胞与滤泡壁之间已出现间隙,随时掉入腔中(图版-14)。此时随着卵黄物质的积累,细胞核的界限变得模糊(图版-11),染色质呈细丝状松散分布与发泡内,核内核仁消逝。瘤背石蜡切片发现,在本期的最后,掉入滤泡腔内的卵母细胞已看不到细胞核,在其细胞两极各形成1组纺锤丝,行细胞分裂,此为有丝分裂(图版-15)。
成熟期。成熟的卵母细胞脱离滤泡壁掉入滤泡腔内,细胞形状不规则,有圆形、椭圆形、梨形和多角形等(图版-6,16)。瘤背石磺的成熟卵含有丰富的卵黄物质,细胞质内充满大而明显卵黄颗粒,细胞核和核仁已被卵黄颗粒覆盖而不可见。
2.2 两性腺周年变化及发育指标
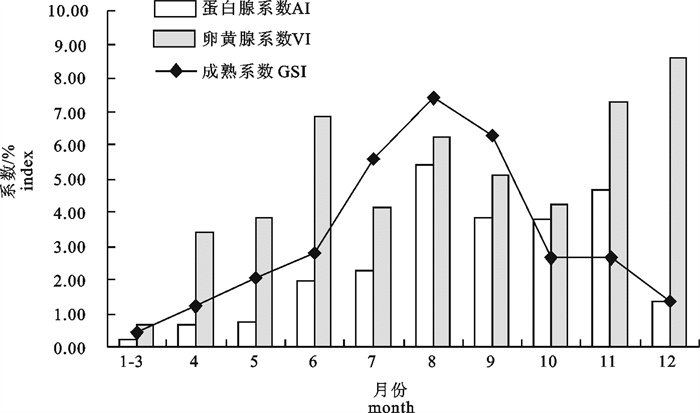
瘤背石磺两性腺的研究发现,其发育有着明显的周年变化规律(图 2),1至3月的瘤背石磺成熟系数为全年最低,平均为0.40%;4月以后成熟系数显著上升;7、8月出现1个明显的成熟高峰,具体表现为在这个阶段,瘤背石磺的繁育旺盛。此时恰逢长江流域的梅雨季节,终日阴雨绵绵,很适合瘤背石磺的繁殖,实验室昼夜观察也证明此时瘤背石磺交配频繁,可以认为瘤背石磺的繁殖盛季为7~9月;10月以后两性腺开始衰退;根据GSI曲线也可以推断出12月至翌年3月是瘤背石磺的越冬期。从图 2可以看出,成熟系数的周年变化规律与蛋白腺系数、卵黄腺系数具有一定的规律性。蛋白腺系数基本随着成熟系数变化而变化,卵黄腺系数随着成熟系数变化的过程中出现3个峰值,分别在6、8和12月。
2.3 性成熟年龄和生物学最小型
野外采样发现翌年春天的滩涂可见很多1~3 g左右的小瘤背石磺,偶有0.1~0.4 g的更小个体集中躲藏在凹陷的淤泥表面。移入实验室的小瘤背石磺养殖到6月,观察发现3.71 g个体即已充当雄性与较大个体进行交配。通过对瘤背石磺周年样本的切片观察认为,瘤背石磺的性成熟年龄为近1龄。前一年夏、秋季繁殖发育的瘤背石磺到次年5月性腺已趋成熟。从切片上可以看到两性腺内已有发育成熟的精子,且滤泡壁上有待发育的卵原细胞。生物学最小型为体长2.81 cm,体质量1.81 g。
3. 讨论
3.1 瘤背石磺两性腺发育分期与其他贝类的比较
CHIPPERFIELD[14]对贝类性腺发育分期方法多见于双壳类中。沈决奋等[15]将海湾扇贝(Argopecten irradians)性腺发育分为增殖期、生长期、成熟期、排放期和休止期。廖承义等[16]即提出用此5期统一双壳类性腺发育分期,但众多学者的意见并不完全一致。吴洪流等[17]根据波纹巴非蛤(Paphia undulate)性腺发育的特点,在这5期基础上增加了滞留退化期。在腹足纲贝类研究中,学者们亦参照CHIPPERFIELD[14]方法分期,但相对较混乱。聂宗庆和王素平[18]将鲍(Haliotis)的性腺发育分成休止期、恢复期、成熟前期、成熟期和排精(卵)末期。瘤背石磺两性腺的发育存在有别于其他贝类的特殊性。已有的贝类性腺研究中,性腺尚可分成独立的卵巢和精巢,雌雄同体者基本上也有各自的产卵区域和产精区域,或是出现雌、雄生殖细胞产生于1个滤泡腔中的间性发育阶段[17],最终还是趋向雌、雄单独存在。瘤背石磺与泥螺(Bullacta exarata)较相近,雌、雄生殖细胞产生于同1个滤泡中,但与原来认识不一样,吕来清等[19]指出泥螺两性腺还有明显的精卵分区,即精巢一般位于两性腺的中间部位,卵巢包围在四周,精巢中间为两性管,也有雌、雄两性生殖细胞共处1个滤泡,雌、雄滤泡混杂分布。而瘤背石磺两性腺不存在这种分区,从休止期恢复的两性腺最初均成产生精子的滤泡,之后相继转变成精卵同步发育的滤泡,此种滤泡在其整个发育周期里占绝大多数时间。瘤背石磺两性腺的发育中没有单独存在的卵子期,王金庆等[2]认为滤泡发育经历卵子期是不妥的,故瘤背石磺性腺的分期不能简单划分为增殖期、生长期、成熟期、排放期和休止期这种模式,应根据滤泡发生中精卵发生特点划分为宜。
3.2 雌雄同体问题
贝类多为雌雄异体,但雌雄同体种类也相当普遍。根据研究报道,ATZ[20]提出雌雄同体的定义,现在这个定义已被多数学者采纳,所谓雌雄同体(hermaphroditism)是指雌、雄两性腺在同1个体中出现的现象,可将其区分为3类:1)由雌性功能转变雄性功能的雌性先熟的雌雄同体(protogynous hermaphroditism);2)由雄性功能转变为雌性功能的雄性先熟的雌雄同体(protandrous hermaphroditism);3)雌、雄两性功能同体存在的同步性雌雄同体(synchronous hermaphroditism)。光镜下观察表明,瘤背石磺每个发育周期的早期为雄性生殖细胞先发育,后迅速转变为雌、雄同步发育滤泡,且终年是此种滤泡类型,直至两性腺衰退进入越冬状态止,待到翌年重新以此规律开始新一轮周期。初次迎来性腺周期的瘤背石磺也是雄性先熟,但较其他进入周期的瘤背石磺停留在雄性滤泡的时间稍长,最终也进入雌雄同步发育滤泡阶段,因此认为瘤背石磺属于雄性先熟,雌雄同体存在的雌雄同体类型。
3.3 精子发生同步性及卵细胞的双核现象
瘤背石磺滤泡细胞中普遍发现精细胞呈团状分布,这与精子细胞发生具有同步性有关,分裂增殖很快的精原细胞之间存在细胞间桥,致使精细胞联成一团。秦鹏春等[21]认为这种结构上的联系可使物质、能量和信息彼此传递,使精子细胞发育、成熟和分化同步化,确保大量精子同时成熟。曲漱惠等[22]亦有同样认识,且认为此种间桥普遍见于各类动物。杨增明等[23]认为精子细胞有细胞间桥可能是精子同步分化的基础。观察证明存在细胞间桥的瘤背石磺精细胞同时变态形成精子,也正是这种同步性才导致滤泡内精细胞的爆发性增殖,常观察到精子充盈滤泡腔。
瘤背石蜡切片发现,在雌性生殖细胞发生的过程中,核仁发生了一系列变化,在大小上,随卵原细胞经无卵黄卵母细胞发育到卵黄形成初期卵母细胞时,核仁由小变大,随后又不易在切片上观察到,而进入到卵黄形成后期尤其是发育到成熟期的卵母细胞在核的边缘一侧常能观察到一较大的核仁,并为双质核仁。杨耀聪和李复雪[24]在尖紫蛤(Hiatula acuta)的研究中认为,双质核仁的出现反映了在卵细胞不同发育时期核仁功能的活动状况及卵母细胞代谢强度。研究中同样发现杨耀聪和李复雪[24]描述的c型双质核仁的位置关系,但是否还存在其他类型的位置关系仍有待进一步的研究。
3.4 成熟系数和蛋白质系数、卵黄腺系数的关系
两性腺、蛋白腺和卵黄腺在生殖系统中互生着,三者在瘤背石磺完成生理功能中密切相关。卵黄是瘤背石磺生长发育的主要物质能量来源。3月末瘤背石磺完成越冬之后,卵黄腺由越冬阶段的衰弱几乎不可见开始恢复,并迅速积累,到6月达到第一个积累高峰,之后由于两性腺发育旺盛,绝大部分营养物质用于其发育,这种需求大于积累造成卵黄腺系数一度下降。相反,在两性腺成熟系数峰值处,卵黄腺系数反而又上升了,这是因为这一阶段滤泡内的生殖细胞已经完成发育,较前一阶段对卵黄腺提供的营养物质需求相对降低,积累增多。9月之后由之前主要是性腺发育转变成生殖和长个体并行阶段,故成熟系数下降,瘤背石磺个体大小此时开始有明显增长,这是导致卵黄系数再次下降的原因。10月以后准备过冬是卵黄腺系数第3次增长的原因,直至12月达到越冬前卵黄积累的又1个峰值。蛋白腺的作用是形成卵膜,蛋白腺系数的增减与产卵密切相关。沈和定等[25]研究发现瘤背石磺从6月末至10月初有6个集中的产卵高峰,此研究发现蛋白腺系数保持在一个高水平,与其报道结果相一致。10月之后由于不产卵,蛋白腺不生产卵膜,造成蛋白腺系数一时的增加,随着越冬的来临,蛋白腺衰退。
-
图 1 瘤背石磺生殖细胞发生模式图
1. 卵黄合成卵母细胞;2. 精原细胞;3. 卵黄合成后卵母细胞中期;4. 精子;5. 支持细胞;6. 无卵黄卵母细胞,双质核仁;7. 初级精母细胞;8. 卵黄合成后卵母细胞后期;9. 精子细胞;10. 卵原细胞;11. 支持细胞;12. 变形精子;13. 次级精母细胞;14. 减数分裂;15. 精子细胞早期;16. 精子细胞后期
Figure 1. Miniature diagram of cytogenesis in hermaphroditic gland of O.struma
1. vitellogenic oocyte; 2. spermatogonium; 3. metaphase of postvitellogenic oocyte; 4. spermatozoon; 5. supporting cell; 6. previtellogenic oocyte, amphinucleous; 7. primary spermatocyte; 8. anaphase of postvitellogenic oocyte; 9. spermatid; 10. oogonium; 11. supporting cell; 12. forming spermatozoon; 13. secondary spermatocyte; 14. miosis; 15. prophase of spermatid; 16. anaphase of spermatid
图版I 瘤背石磺两性腺周年发育的组织学观察
1. 增值期×90,示大小不一滤泡,结缔组织;2. 精子发生期×360,示次级精母细胞,精子细胞;3. 精卵同步发生期×180,示各级生殖细胞;4. 滤泡×900,示支持细胞,变形晚期精子,间桥;5. 两性管×90,示成熟精子;6. 排放期×90,示滤泡中成熟卵子的集中排放,滤泡壁上卵母细胞;7. 排空滤泡×90,示残留的精卵细胞;8. 精子发生期×360,示各级生殖细胞;9. 滤泡×360,示变形中期精子,卵黄合成后期卵母细胞;10. 滤泡×360,示变形中期精子,无卵黄合成卵母细胞;11. 卵原细胞和卵黄合成后期卵母细胞×360;12. 卵黄合成期×360,示核偏位、变形精子;13. 双质核仁×360,示浅色↗,深色↙;14. 卵黄合成后期×180,示本期早期、晚期卵母细胞;15. 卵黄合成后期×360,示本期晚期有丝分裂卵母细胞,纺锤体;16. 成熟卵子×360;Sg. 精原细胞;PS. 初级精母细胞;SS. 次级精母细胞;Sp. 精子细胞;S. 精子;Oo. 卵原细胞;PRO. 无卵黄生成卵母细胞;VO. 卵黄生成卵母细胞;POO. 卵黄生成后卵母细胞;MO. 成熟卵子;N. 细胞核;Nu. 核仁;Am. 双质核仁;M. 减数分裂;Spi. 纺锤体
图版I. Histological observation of annual development of hermaphroditic gland of O. struma
1.proliferation×90, showing follicle cell (Fc), connective tissue(Ct); 2.spermatogenesis×360, showing secondary spermatocyte, spermatid; 3.ova and sperm in phase×180, showing germ cells at different stage of development; 4.follicle cell×900, showing supporting cell (Sc), spermatozoon at forming telophase, intercellular bridges(IB); 5.hermaphroditic duct (Hd)×90, showing mature spermatozoon; 6.exporting stage×90, showing follicle filled with exporting mature ova, oocyte on follicle wall; 7.resting follicle×90, showing rudimental germ cells; 8.spermatogenesis×360, showing germ cells at different stage of development; 9.follicle cell×360, showing spermatozoon at forming metaphase, postvitellogenic oocyte; 10.follicle cell×360, showing spermatozoon at forming metaphase, previtellogenic oocyte; 11.oogonium and postvitellogenic oocyte×360;12.vitellogenic stage×360, showing migrated nucleus, forming spermatozoon; 13.amphinucleous×360, showing weakly dyed part (W)↗, deeply dyed part(D)↙; 14.postvitellogenic stage×180, showing prophase and anaphase of oocyte at the stage; 15.postvitellogenic stage×360, showing mitosis at telophaseof oocyte, spindle; 16.mature ova×360;Sg.spermatogonium; PS.primary spermatocyte; SS.secondary spermatocyte; Sp.spermatid; S.spermatozoon; Oo.oogonium, PRO.previtellogenic oocyte; VO.vitellogenic oocyte; POO.postvitellogenic oocyte; MO.mature ova; N.nucleus; Nu.nucleolus; Am.amphinucleous; M.miosis; Spi.spindle
表 1 瘤背石磺精子细胞各期情况
Table 1 Data of O.struma spermatozoa at different stages
雄性生殖细胞的发育阶段spermatogenesis stages 细胞直径/μm cell diameter 核径/μm nucleus diameter 长径long diameter 短径short diameter 长径long diameter 短径short diameter 精原细胞spermatogonium 27.27±5.33 25.33±5.17 22.45±3.59 19.88±2.57 初级精母细胞primary spermatocyte 47.62±4.52 40.39±3.51 30.89±1.45 27.42±2.61 次级精母细胞secondary spermatocyte 31.43±2.33 29.09±2.20 17.53±2.02 15.35±2.28 精子细胞spermatid 10.59±3.13 8.76±2.59 - - 精子spermatozoon 全长450 μm 表 2 瘤背石磺卵子发生中卵母细胞情况
Table 2 Data of O.struma oocyte in oogenesis
卵子发生分期oogenesis stages 核仁/μm nucleolus 核/μm nucleus 卵径/μm ovum diameter 核质比* nucleocytoplasmic ratio 长径long diameter 短径short diameter 长径long diameter 短径short diameter 长径long diameter 短径short diameter 卵原细胞oogonium 19.60±2.87 17.47±2.69 54.75±7.95 42.79±7.40 99.25±17.12 73.56±14.04 0.24±0.07 无卵黄形成previtellogenic oocyte 28.65±2.94 25.47±2.64 85.80±10.40 65.11±10.97 174.36±20.32 131.08±16.51 0.15±0.05 卵黄形成期vitellogenic oocyte 31.63±5.20 26.31±3.56 117.29±11.34 89.47±7.86 274.19±18.12 191.28±14.21 0.10±0.02 卵黄形成后期postvitellogenic oocyte - - 96.03±17.30 73.87±9.07 290.07±32.81 192.72±35.31 < 0.06±0.03 成熟卵子maturation - - - - 236.53±20.47 175.80±11.26 - 注:*. 核质比=细胞核体积/ (细胞体积-细胞核体积);体积=0.523长径2×短径[13]
Note:*. nucleocytoplasmic ratio = nucleus volume/(cell volume nucleus volume); volume=0.523 long diameter 2×short diameter[13] -
[1] 沈和定. 中国大陆沿海石磺生物学实验研究及系统分类[D]. 上海: 上海海洋大学, 2009. [2] 王金庆, 成永旭, 吴旭干, 等. 瘤背石磺的生殖系统和性腺发育[J]. 动物学杂志, 2006, 41(1): 19-26. doi: 10.3969/j.issn.0250-3263.2006.01.004 [3] DESHPANDE U D, NAGABHUSHANAM R. Annual reproductive cycle of the marine pulmonate, Onchidium verruculatum (Cuvier) and its control by environmental factors[J]. Indian J Mar Sci, 1983, 12(2): 122-124.
[4] 沈和定, 李家乐, 张缓溶. 石磺的生物学特性及其增养殖前景分析[J]. 中国水产, 2004(1): 60-64. doi: 10.3969/j.issn.1002-6681.2004.01.045 [5] 沈和定, 陈汉春, 陈贤龙, 等. 几种饲料对石磺的暂养效果及其消化率的初步研究[J]. 上海水产大学学报, 2004, 13(4): 293-297. doi: 10.3969/j.issn.1004-7271.2004.04.002 [6] MCFARLANE I D. Ecology and behaviour of the intertidal pulmonate mollusk Onchidium peronii in Kuwait[J]. J Univ Kuwait, 1979, 6: 16-180.
[7] MCFARLANE I D. Trail-following and trail-searching behaviour in homing of the intertidal gastropod mollusk, Onchidium verruculatum[J]. Mar Behav Physiol, 1980, 7(1): 95-108. doi: 10.1080/10236248009386974
[8] SMITH A, KENNY R. Reproduction and development of Onchidium damelii Semper, 1882[J]. J Malac Soc Aust, 1987, 8: 37-39. doi: 10.1080/00852988.1987.10673989
[9] DESHPANDE U D, NAGABHUSHANAM R, HANUMANTE M M. Reproductive ecology of the marine pulmonate, Onchidium verruculatum[J]. Hydrobiologia, 1980, 71(2): 83-85. doi: 10.1007/BF00005830
[10] 沈和定, 陈贤龙, 陈汉春, 等. 水温对石磺胚胎发育的影响[J]. 水产学报, 2005, 29(6): 776-782. doi: 10.3321/j.issn:1000-0615.2005.06.008 [11] 王金庆, 成永旭, 吴旭干. 瘤背石磺的胚胎和幼虫发育[J]. 上海水产大学学报, 2005, 14(2): 108-115. doi: 10.3969/j.issn.1004-7271.2005.02.003 [12] 沈和定, 陈汉春, 陈贤龙, 等. 盐度对石磺胚胎发育的影响[J]. 上海水产大学学报, 2006, 15(3): 297-302. doi: 10.3969/j.issn.1004-7271.2006.03.008 [13] 尤仲杰, 王一农, 董任彭, 等. 浙江沿海泥螺繁殖生物学初步观察[J]. 浙江水产学院学报, 1993, 12(4): 233-239. [14] CHIPPERFIELD P N J. Observation on the breeding and settlement of Mytilns edulis (L. ) in British water[J]. J Mar Biol Ass, 1953, 32(2): 449-470. doi: 10.1017/S002531540001465X
[15] 沈决奋, 杨爱国, 燕敬平. 海湾扇贝性腺发育的初步研究[J]. 海洋与湖沼, 1996, 27(6): 632-637. https://d.wanfangdata.com.cn/periodical/Ch9QZXJpb2RpY2FsQ0hJTmV3UzIwMjQxMTA1MTcxMzA0EhVDQVMyMDEzMDMwNDAwMDAwMjcwNDgaCGFhdWZqc2Fu [16] 廖承义, 徐应馥, 王远隆. 栉孔扇贝的生殖周期[J]. 水产学报, 1983, 7(1): 1-13. https://d.wanfangdata.com.cn/periodical/Ch9QZXJpb2RpY2FsQ0hJTmV3UzIwMjQxMTA1MTcxMzA0Eg5RSzAwMDAwMjU1NTk0ORoIeWZqbndzd2U%3D [17] 吴洪流, 王红勇, 王珺. 波纹巴非蛤性腺发育分期的研究[J]. 海南大学学报: 自然科学版, 2002, 20(1): 41-47. [18] 聂宗庆, 王素平. 鲍鱼养殖实用技术[M]. 北京: 中国农业出版社, 2000: 74-75. [19] 吕来清, 林志强, 王达飞. 泥螺养殖技术[M]. 杭州: 浙江科学技术出版社, 1998: 28-29. [20] ATZ J W. Intersexuality in fishes[M] //MARSHALL A J, ARMATRONG C N. Intersexuality in vertebrates including man. New York: Academic Press, 1964: 145-232.
[21] 秦鹏春, 李云龙, 谭景和, 等. 哺乳动物胚胎学[M]. 北京: 科学出版社, 2001: 70-73. https://book.sciencereading.cn/shop/book/Booksimple/show.do?id=B76B75A12B25645A48675B224D66ACC07000 [22] 曲漱惠, 李嘉泳, 黄浙, 等. 动物胚胎学[M]. 北京: 人民教育出版社, 1980: 8-15. [23] 杨增明, 孙青原, 夏国良. 生殖生物学[M]. 北京: 科学出版社, 2005: 31-33. https://book.sciencereading.cn/shop/book/Booksimple/show.do?id=B9137B918C895457797C3785EF363B188000 [24] 杨耀聪, 李复雪. 尖紫蛤生殖周期的研究[J]. 热带海洋, 1994, 13(2): 61-67. https://d.wanfangdata.com.cn/periodical/Ch9QZXJpb2RpY2FsQ0hJTmV3UzIwMjQxMTA1MTcxMzA0EhVDQVMyMDEzMDMwNDAwMDAyMDI1NDYaCDIxdWVkeWlx [25] 沈和定, 陈汉春, 陈贤龙, 等. 石磺繁殖生物学的实验研究[J]. 水产学报, 2006, 30(6): 753-760. doi: 10.3321/j.issn:1000-0615.2006.06.006 -
期刊类型引用(2)
1. 钱静, 沈和定, 管菊. 平疣桑椹石磺生殖系统结构及精子储存场所. 动物学杂志. 2015(04): 600-606 .  百度学术
百度学术
2. 钱静, 沈和定, 管菊, 王成暖. 两种石磺胚胎发育比较. 上海海洋大学学报. 2014(04): 498-504 .  百度学术
百度学术
其他类型引用(1)



 下载:
下载:
 粤公网安备 44010502001741号
粤公网安备 44010502001741号
